Тетрабромдивинил, гексахлорэтан, метилиодид.
винного (этилового) спирта как «соединение духа обычной соли с духом вина». Глаубер получил это вещество в 1648 г. взаимодействием этилового спирта с соляной кислотой: С2Н5ОН+HCl=C2H5Cl+Н2О. Другие галогенопроизводные были получены лишь в XIX в. Главной особенностью этих соединений считается их способность вступать в реакции замещения. Атом углерода, связанный с атомом галогена, несёт на себе частичный положительный заряд d+ и, следовательно, легко подвергается атаке частиц с повышенной электронной плотностью (нуклеофилов), например молекул воды, гидроксид-ионов, аммиака, аминов и т. д.
Происходящие при этом процессы называются реакциями нуклеофильного замещения. Продуктами таких превращений, в зависимости от количества и расположения атомов галогена в галогенопроизводном, могут быть спирты, карбонильные соединения, а также карбоновые кислоты, например:

Многие галогеноводороды широко используются в самых разнообразных целях: в качестве растворителей (хлороформ СHCl3, четырёххлористый углерод ССl4), как рабочее вещество в холодильных установках (CF2Cl2 и другие фреоны), при химической чистке одежды (трихлорэтилен СНСl=ССl2).
реакции образуются нитросоединения:
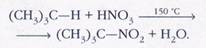
Эта реакция, открытая в 1893 г. русским химиком Михаилом Ивановичем Коноваловым (1858—1906), явилась, по образному выражению учёного, первой удачной попыткой оживить «химических мертвецов», которыми считались алканы.
Взаимодействие алканов со смесью хлора и сернистого газа (сульфохлорирование) приводит к образованию хлорангидридов сульфокислот (сульфохлоридов):
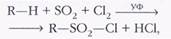
где R — радикал, например октил —С8Н17.
При обработке сульфохлоридов водным раствором NaOH образуются натриевые соли сульфокислот (алкилсульфонаты), которые используются в качестве синтетических моющих средств:
RSO2Cl+2NaOH=RSO2ONa+NaCl+H2O.
Для алканов характерны и реакции окисления, которые также протекают через образование свободных радика-