рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Высокие технологии
- /
- РАСЧЕТЫ РАСХОДНЫХ КОЭФФИЦИЕНТОВ
Реферат Курсовая Конспект
РАСЧЕТЫ РАСХОДНЫХ КОЭФФИЦИЕНТОВ
РАСЧЕТЫ РАСХОДНЫХ КОЭФФИЦИЕНТОВ - раздел Высокие технологии, ТЕХНОЛОГИЧЕСКИЕ РАСЧЕТЫ Расходные Коэффициенты - Величины, Характеризующие Расход Ра...
Расходные коэффициенты - величины, характеризующие расход различных видов сырья, воды, топлива, электроэнергии, пара на единицу вырабатываемой продукции. При конструировании аппаратов и определении параметров технологического режима задаются также условия, при которых рационально сочетаются высокая интенсивность и производительность процесса с высоким качеством продукции и возможно более низкой себестоимостью.
Пример 1. Определить теоретические расходные коэффициенты для следующих железных руд в процессе выплавки чугуна, содержащего 92% Fe, при условии, что руды не содержат пустой породы и примесей:
| Мольная масса | |
| Шпатовый железняк FeCO3 | 115,8 |
| Лимонит 2Fe2O3×3Н2О | |
| Гетит 2Fe2O3×2H2O | |
| Красный железняк Fe2O3 | 159,7 |
| Магнитный железняк Fe3O4 | 231,5 |
Решение
FeCO3
Из 1 кмоль FeCO3 можно получить 1 кмоль Fe или из 115,8 кг FeCO3 - 55,9 кг Fe. Отсюда для получения 1 т чугуна с содержанием Fe 92% (масс) необходимо:
 т
т
Аналогично находим значения теоретических расходных коэффициентов для других руд:
2Fe2O3×3H2O
 т
т
2Fe2O3-2H2O
 т
т
Fe2O3
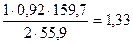 т
т
Fe3O4
 т
т
Пример 2. Рассчитать расходный коэффициент для природного газа, содержащего 97% (об.) метана в производстве уксусной кислоты (на 1 т) из ацетальдегида. Выход ацетилена из метана составляет 15% от теоретически возможного, ацетальдегида из ацетилена - 60%, а уксусной кислоты из ацетальдегида 90% (масс).
Решение
Уксусная кислота получается из метана многостадийным методом. Схематично процесс может быть описан следующими, последовательно протекающими реакциями:



Молекулярная масса: С2Н2 - 26; СН3СНО - 44; СН3СООН - 60; СН4- 16.
Теоретический расход метана на 1 т уксусной кислоты составит:
 кг
кг
с учетом выхода продукта по стадиям
 кг
кг
или
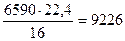 см3 СН4
см3 СН4
или
 м3 природного газа
м3 природного газа
Пример 3. Определить количество аммиака, требуемое для производства 100000 т/год азотной кислоты, и расход воздуха на окисление аммиака (в м3/ч), если цех работает 355 дней в году, выход окиси азота Х1 = 0,97%, степень абсорбции Х2 = 0,92, а содержание аммиака в сухой аммиачно-воздушной смеси - 7,13% (масс).
Решение
Окисление аммиака является первой стадией получения азотной кислоты из аммиака. По этому методу аммиак окисляется кислородом воздуха в присутствии платинового катализатора при 800-900°С до окислов азота. Затем, полученная окись азота окисляется до двуокиси, а последняя поглощается водой с образованием азотной кислоты. Схематично процесс
можно изобразить следующими уравнениями:
4NH3 + 5О2 = 4NO + 6Н2О
2NO + О2 = 2NO2
3NO2 + H2O = 2HNO3 + NO
Для материальных расчетов можно в первом приближение записать суммарное уравнение этих трех стадий в виде:
NH3 + 2О2 = HNO3 + Н2О
Молекулярная масса: NH3 -17; HNO3 -63.
Необходимое количество аммиака для получения 100000 т HNO3 с учетом степени окисления и степени абсорбции составит:
 т
т
Расход аммиака составит:
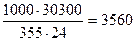 кг/ч
кг/ч
Объем аммиака составит:
 м3
м3
Расход воздуха (в м3/ч), требуемый для окисления (в составе аммиачно-воздушной смеси), будет равен
 м3
м3
где 11,5 - содержание NH3 в смеси в % (об), то есть

– Конец работы –
Эта тема принадлежит разделу:
ТЕХНОЛОГИЧЕСКИЕ РАСЧЕТЫ
Федеральное агентство по образованию... Саратовский государственный технический университет...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: РАСЧЕТЫ РАСХОДНЫХ КОЭФФИЦИЕНТОВ
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов