Постулаты Бора
 Неустойчивость планетарной модели атома по Резерфорду и закономерности атомных спектров, в частности их дискретность и дискретность спектральных термов привели Н.Бора в 1913г. к пониманию двух важнейших квантовых законов квантовой физики. Тем более, что ему была известна идея Планка и Эйнштейна о дискретном изменении энергии гармонического осциллятора и об излучении и поглощении света порциями (квантами).
Неустойчивость планетарной модели атома по Резерфорду и закономерности атомных спектров, в частности их дискретность и дискретность спектральных термов привели Н.Бора в 1913г. к пониманию двух важнейших квантовых законов квантовой физики. Тем более, что ему была известна идея Планка и Эйнштейна о дискретном изменении энергии гармонического осциллятора и об излучении и поглощении света порциями (квантами).
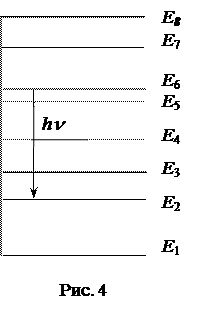
Первый закон, сформулированный Бором в виде постулата, утверждает: атом может находиться длительное время в стационарных состояниях, которые характеризуются дискретными значениями энергии 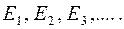 (рис. 4). В этих состояниях, вопреки классической электродинамике, атом не излучает. Возможные значения энергии стационарных состояний атома образуют энергетический спектр атома. Этот квантовый закон оказывается справедливым и для других систем микрочастиц (для ядер, молекул, кристаллов).
(рис. 4). В этих состояниях, вопреки классической электродинамике, атом не излучает. Возможные значения энергии стационарных состояний атома образуют энергетический спектр атома. Этот квантовый закон оказывается справедливым и для других систем микрочастиц (для ядер, молекул, кристаллов).
Второй постулат также является важнейшим законом квантовой физики. При переходе атома из состояния с большой энергией в состояние с меньшей энергией атом может испустить фотон (микрочастицу света) с энергией
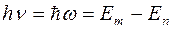 . (4)
. (4)
При обратном переходе из состояния с меньшей энергией в состояние с большей энергией может произойти поглощение фотона.
Изменение энергии состояния атома может происходить не только за счет излучения или поглощения фотона, но и при взаимодействии атома с другой микрочастицей (электроном, атомом и т.д.) или с колебаниями кристаллической решетки. Но во всех таких процессах выполняется соотношение (4).
Второй постулат Бора позволяет представить спектральный терм, как величину пропорциональную энергии состояния атома
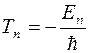 .
.
Отсюда следует, что энергия стационарных состояний в атоме водорода принимает отрицательные значения и в соответствии со спектральными закономерностями должна быть обратно пропорциональна квадрату номера состояния
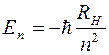 . (5)
. (5)