Другие посттрансляционные модификации белков
Многие белки и секретируемые пептиды претерпевают различные структурные изменения в результате котрансляционных и посттрансляционных модификаций, т.е. во время или после завершения их синтеза рибосомами. Подобные модификации существенно влияют на функциональную активность белков и пептидов, значительно расширяя возможности экспрессии генов, кодирующих эти молекулы, и их кодирующий потенциал. Одна из таких модификаций, а именно фосфорилирование факторов транскрипции протеинкиназами, рассмотрена выше. Кроме того, посттрансляционные модификации включают в себя гликозилирование остатков Asn в последовательностях Asn-X-[SerThr], N-концевое ацилирование, циклизацию N-концевого остатка Glu с образованием пироглутаминовой кислоты, C-концевое амидирование последовательностей освобождающихся пептидов, гидроксилирование остатков Lys и Pro, метилирование различных остатков аминокислот. Многие из перечисленных модификаций являются критическими для биологической активности пептидов. В частности, карбоксиамидирование C-концевого Gly активирует окситоцин и вазопрессин, а перенос сульфогруппы на остаток Tyr в холецистокинине-8 оказывается критическим для проявления его активности в поджелудочной железе. N-Ацетилирование b-эндорфина блокирует его опиоидную активность, тогда как ацетилирование меланоцитстимулирующего гормона усиливает его влияние на синтез меланинов. Поскольку большинство этих модификаций – тканеспецифические, пептиды, обладающие различной биологической активностью, должны быть доставлены к различным тканям в виде предшественников, где они претерпевают специфический процессинг.
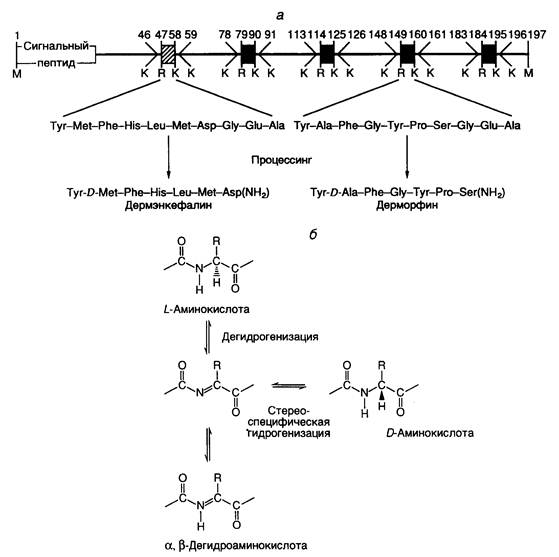
Среди ковалентных посттрансляционных модификаций пептидов, синтезируемых рибосомами, занимает особое место эпимеризация L-аминокислотных остатков с образованием D-энантиомеров, присутствие которых оказывает принципиальное влияние на биологическую активность пептидов. Известно, что только L-стереоизомеры аминокислот участвуют в синтезе белка рибосомами. В природных белках D-аминокислоты обнаруживаются редко, как правило, в составе антибиотиков пептидной природы, которые синтезируются ферментативными комплексами микроорганизмов без привлечения рибосом. Другим источником D-аминокислот в белках может быть спонтанная рацемизация их L-стереоизомеров в составе полипептидных цепей в результате старения. Недавно обнаружено, что у ряда природных пептидов, обладающих биологической активностью, D-аминокислоты образуются во время посттрансляционных модификаций. В частности, это явление характерно для опиоидных пептидов, секретируемых кожей некоторых амфибий. Структура наиболее известных из таких пептидов –дерморфина и дермэнкефалина представлена на рис. I.45,а. Активность этих пептидов как анальгетиков, по крайней мере, в 1000 раз превышает соответствующую активность морфина, и для ее проявления необходимо обязательное присутствие D-аминокислот в указанных положениях молекул. Дерморфиноподобные молекулы с теми же особенностями структуры были обнаружены в мозге крыс, а у амфибий найдена серия новых гексапептидов, делторфинов (Tyr-D-Ala-X-Val-Val-Gly, где X = Asp или Glu), которые являются агонистами d-опиоидных рецепторов и для активности которых также необходимы D-аминокислоты. К пептидам той же природы относятся полициклические пептидные антибиотики грамположительных бактерий, в частности низин, субтилин и эпидермин, а также некоторые нейропептиды высших беспозвоночных. Механизм образования D-аминокислот в составе пептидов до конца не понятен, однако предполагается, что имеют место ферментативные реакции, в результате которых происходят последовательные дегидрогенизация и гидрогенизация L-изомеров аминокислот (см. рис. I.45,б). Поскольку в последнее время появились высокочувствительные аналитические методы, позволяющие обнаруживать следовые количества D-аминокислот в природных белках, можно предполагать скорое подтверждение гипотезы о том, что эта группа явлений имеет гораздо большее биологическое значение, чем ей сегодня отводится в системе биохимических превращений макромолекул.