Контрольные задачи
1. В каком из растворов хлорида натрия: 2%, 0,86%, 0,2% жизнедеятельность эритроцитов не будет нарушена и почему? 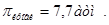 , T=37оС. Плотность растворов и степень диссоциации NaCI считать равными единице.
, T=37оС. Плотность растворов и степень диссоциации NaCI считать равными единице.
2. Изотоничны ли растворы мочевины и уксусной кислоты с массовой долей 0,6%, если степень диссоциации уксусной кислоты равна 0,01, ρ =1 г/мл?
3. Магния сульфат /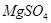 / в медицинской практике применяют как слабительное, желчегонное и успокаивающее действие на ЦНС. При концентрации препарата в крови 9-10 мг% наступает снотворный эффект, а при 15-18 мг% – наркотическое состояние. Большие концентрации могут вызвать угнетение дыхания. Определите осмотическое давление раствора сульфата магния концентрации 0,005 моль/л при 18оС, если кажущаяся степень диссоциации этой соли равна 66%.
/ в медицинской практике применяют как слабительное, желчегонное и успокаивающее действие на ЦНС. При концентрации препарата в крови 9-10 мг% наступает снотворный эффект, а при 15-18 мг% – наркотическое состояние. Большие концентрации могут вызвать угнетение дыхания. Определите осмотическое давление раствора сульфата магния концентрации 0,005 моль/л при 18оС, если кажущаяся степень диссоциации этой соли равна 66%.
4. Никотинамид (пиридин-3-карбоновой кислоты) в медицинской практике применяют как специфическое противоаллергическое средство. Осмотическое давление крови при 37оС равно 7.7 атм. Будет ли изотоничен крови 2% раствор никотинамида / (витамин РР), ρ=1,03 г/мл?
(витамин РР), ρ=1,03 г/мл?
5. Общая осмотическая концентрация в плазме крови в норме составляет 0,3 моль/л. Вычислите осмотическое давление плазмы крови при T=25oC.
6. Осмотическое давление раствора, содержащего 0,2 г белка в 10 мл, при 25оС равно 10-3 атм. Определить молярную массу белка.
7. Рассчитайте осмотическое давление 20%-ного водного раствора глюкозы (ρ = 1,08 г/мл) при 310 К, применяемого для внутривенного введения, например, при отеке легкого. Каким будет этот раствор (гипо-, гипер-, изотоническим) по отношению к крови, если учесть, что π крови равно 740-780 кПа?
8. Чему равно осмотическое давление раствора при 20оС, в 100 мл которого содержится 6,33 г красящего вещества крови – гематина (Mr (С34Н33N4O5Fe=633 г/моль))?.
9. Что произойдет с эритроцитами крови, если их поместить в 3 моль/л раствор глюкозы? 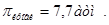 , при T=37оС.
, при T=37оС.
10. Что произойдет с эритроцитами при 310 К в 2%-ном растворе глюкозы (ρ=1,006 г/мл)
11. В каком из двух растворов глюкозы отклонение от закона Рауля будет больше: с С=0,1М или С=0,2М? Дайте пояснения.
12. В каком случае отклонение от закона Рауля будет больше: в растворе уксусной кислоты с моляльной концентрацией 0,05 моль/кг или в соляной кислоте с такой же моляльной концентрацией? Дайте пояснения.
13. Вычислите температуру кипения и температуру замерзания 4,6% раствора глицерина в воде.
14. Вычислите температуру кипения и температуру замерзания водного раствора сахарозы с массовой долей 2%.
15. Давление пара чисто го ацетона при 20°С 23940 Па. Давление пара раствора камфоры в ацетоне, содержащего 5 г камфоры на 200 г ацетона при той же температуре, равно 23 710 Па. Определить молекулярную массу камфоры, растворенной в ацетоне.
го ацетона при 20°С 23940 Па. Давление пара раствора камфоры в ацетоне, содержащего 5 г камфоры на 200 г ацетона при той же температуре, равно 23 710 Па. Определить молекулярную массу камфоры, растворенной в ацетоне.
16. Определите эбулиоскопическую постоянную ацетона, если раствор, содержащий 4,6 г глицерина /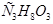 / в 200 г ацетона /
/ в 200 г ацетона /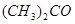 /, кипит при температуре 56,43оС. Ткип(
/, кипит при температуре 56,43оС. Ткип(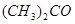 ) =56оС.
) =56оС.
17. Температура замерзания сыворотки крови равна -0,56оС. Рассчитайте моляльную концентрацию солей в крови, условно считая все соли бинарными и полностью распадающимися на ионы по схеме: 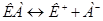 . Наличие в сыворотке неэлектролитов во внимание не принимать.
. Наличие в сыворотке неэлектролитов во внимание не принимать. 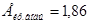 К∙кг/моль.
К∙кг/моль.