рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Охрана труда
- /
- Гидролиз солей слабых кислот и слабых оснований
Реферат Курсовая Конспект
Гидролиз солей слабых кислот и слабых оснований
Гидролиз солей слабых кислот и слабых оснований - раздел Охрана труда, Характеристики гидролиза Особенно Глубоко Протекает Гидролиз Солей, Образованных Слабо...
Особенно глубоко протекает гидролиз солей, образованных слабой кислотой и слабым основанием. Реакция гидролиза:
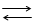 М+ + А - + Н2О МОН + НА. (22)
М+ + А - + Н2О МОН + НА. (22)
Продукты гидролиза все те же, хотя и слабо, диссоциированы на ионы, вследствие чего гидролиз не доходит до конца. Слабая щелочь диссоциирует следующим образом:
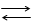 МОН М + +ОН-
МОН М + +ОН-
Косн. =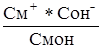 , Откуда
, Откуда 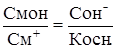 (23).
(23).
Слабая кислота диссоциирует так:
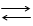 НА Н+ + А- ,
НА Н+ + А- ,
Ккисл. = 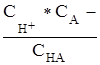 ,
,
Откуда 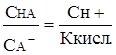 . (24)
. (24)
Подставляя выражения (24) и (23) в (22), получим
Кг = 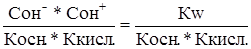 . (25)
. (25)
Если общая концентрация соли СМА, а степень гидролиза a, то концентрация негидролизованной соли См+ = СА - = Сма (1-a). Соответственно СНА= Смон= СМА* a.
Поэтому из выражения (22) можно получить
Кг=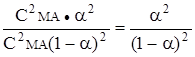 ,
,
или 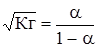
и a = 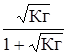 . (26)
. (26)
Из выражения (26) видно, что при гидролизе соли слабого основания и слабой кислоты степень гидролиза не зависит в первом приближении от общей концентрации соли. Если степень гидролиза a мала, т.е. a<< 1, то 1 - X »1 и выражение (26) упрощается
a » 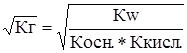
Из выражения (24) получим, принимая во внимание уравнения (25) и (26)
Сн+ = Ккисл. 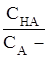 = Ккисл.
= Ккисл. 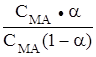 =
=
Ккисл 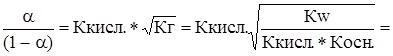
 .
.
После логарифмирования и перемены знаков
рН= ½рКw + ½рКкисл. - ½рКосн. (27)
Из выражения (27) видно, что если константы диссоциации слабой кислоты и слабого основания одинаковы (Ккисл. = Косн), то рН= ½ рКw. Это означает, что раствор имеет нейтральную реакцию, несмотря на гидролиз. Действительно, в этом случае рН=-lgСн+ = - ½ lgКw, или Сн+ =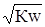 = (10-14) ½=10-7 Из выражения (27) далее видно, что если Ккисл. >Коснов., то рН< ½рКw, т.е. рН< 7 и раствор имеет кислую реакцию. Если Ккисл. < Коснов., то раствор имеет щелочную реакцию и рН > 7.
= (10-14) ½=10-7 Из выражения (27) далее видно, что если Ккисл. >Коснов., то рН< ½рКw, т.е. рН< 7 и раствор имеет кислую реакцию. Если Ккисл. < Коснов., то раствор имеет щелочную реакцию и рН > 7.
– Конец работы –
Эта тема принадлежит разделу:
Характеристики гидролиза
Введение... Гидролиз солей...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Гидролиз солей слабых кислот и слабых оснований
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов