Порядок выполнения работы
1. В стеклянный сосуд налить 150 мл исследуемой воды.
2. В пробу воды пипеткой добавить 1 мл хлорида марганца и 1 мл щелочного раствора йодида калия; конец пипетки должен касаться дна сосуда.
3. Добавить 2 мл концентрированной соляной кислоты. Хорошо перемешать, для того, чтобы растворился осадок гидроксида марганца, выпавший в щелочной среде. При этом йодистые соединения окислятся, выделившийся йод окрасит раствор в жёлтый цвет.
4. Для исследования отобрать из сосуда в коническую колбу 50 мл воды. Из бюретки оттитровать её 0,01 М раствором тиосульфата натрия следующим образом:
а) постоянно встряхивая коническую колбу, доливать в нее раствор тиосульфата до тех пор, пока желтый цвет не побледнеет;
б) добавить 3 капли раствора крахмала и продолжать титровать, постоянно встряхивая колбу до полного обесцвечивания.
Записать объем израсходованного тиосульфата натрия.
5. Дважды повторить операцию пункта 4 с 50 мл исследуемой воды и вычислить средний объем расходуемого тиосульфата (ā).
6. Рассчитать содержание кислорода в воде, мг/л, используя следующую формулу:
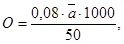
где а - объем тиосульфата, расходуемый на титрование 50 мл воды; 0,08 - 1 мл израсходованного 0,01 М тиосульфата соответствует 0,08 мл кислорода в условиях нормальной температуры и давления (НТД).