рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Образование
- /
- Химическое выветривание
Реферат Курсовая Конспект
Химическое выветривание
Химическое выветривание - раздел Образование, Шуя 2012 Главными Факторами Химического Выветривания Являются Вода, Кислород, Углекисл...
Главными факторами химического выветривания являются вода, кислород, углекислота и органические кислоты.
Под их влиянием существенно изменяются структура и вещественный состав горных пород и образуются новые минералы, которые оказываются устойчивыми в поверхностных или гипергенных условиях.
В химическом выветривании принимают участие и органические кислоты, выделяемые растительностью и микроорганизмами. И, следовательно, в данном типе выветривания принимают участие и биохимические процессы.
Важнейшим фактором химического и биохимического выветривания является вода, которая не только растворяет химические элементы и соединения, находящиеся в горной породе, но и обусловливает миграцию наиболее подвижных химических соединений.
Окисление

 H2O H+ + OH-
H2O H+ + OH-
Диссоциация воды
Ионы H+ способны извлекать и удалять из кристаллов различные ионы.
Скорость воздействия на горные породы во время химического выветривания возрастает в том случае, когда в растворе присутствуют углекислота и органические кислоты.
Химическое воздействие на минералы и горные породы оказывают находящиеся в растворенном в воде виде такие ионы, как НСО3-, SO2-, Ca2+, Mg2+, Na+, К+ и др. Они замещают заряженные атомы в кристаллах или взаимодействуют с ними, тем самым нарушая единство кристаллической решетки.
Процессы химического выветривания последовательно происходят в следующих основных химических реакциях: окислении, гидратации, растворении и гидролизе.
Этот процесс наиболее интенсивно протекает в горных породах, содержащих минералы, состоящие из соединений железа(III), марганца.
Например, при окислении магнетит переходит в более устойчивую форму — гематит:
 Fe3O4 Fe2O3
Fe3O4 Fe2O3
Сульфиды в кислой среде становятся неустойчивыми и постепенно замещаются сульфатами, оксидами и гидроксидами.

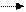
 FeS2 +nО2 + nН2О Fe3O4 Fe2(SO4)2 Fe2O3· nH2О
FeS2 +nО2 + nН2О Fe3O4 Fe2(SO4)2 Fe2O3· nH2О
пирит лимонит
Бурый железняк (лимонит) – это сложный полиминеральный агрегат, состоящий из гётита (FeO · ОН) и гидрогётита (FeO · ОН · nН2О).
Устойчивый в поверхностных условиях гематит возникает и при выветривании таких минералов, как оливин, пироксены, амфиболы под действием воды, кислорода и углекислоты.
Реакция такого преобразования может быть изображена следующим образом:

 (Mg,Fe)2(Si04) Fe2O3 + nMg(HCO3)2 + nH4Si04
(Mg,Fe)2(Si04) Fe2O3 + nMg(HCO3)2 + nH4Si04
оливин гематит растворимые соединения
В результате процесса преобразования железосодержащих минералов и их перехода в лимонит многие горные породы, в частности пески, песчаники, глины, мергели, окрашиваются в бурый или охристый цвет, что свидетельствует об окислении включений, содержащих железистые минералы.
Гидратация
Данный процесс заключается в присоединении воды к веществу. В результате этого осуществляется закрепление молекул воды на поверхности некоторых участков кристаллической решетки.
Примером гидратации является переход ангидрита в гипс:

 CaSO4 + 2Н2О CaSO4·2H2O
CaSO4 + 2Н2О CaSO4·2H2O
ангидрит гипс
При изменении условий реакция обратима и гидратация превращается в дегидратацию.
 Процесс гидратации происходит при переходе гематита в гидроксиды железа. Fe2O3 + H2O 2 FeO (OH)
Процесс гидратации происходит при переходе гематита в гидроксиды железа. Fe2O3 + H2O 2 FeO (OH)
гематит гётит
Далее гётит переходит в гидрогётит.
 FeO (OH) + nН2О FeO · nН2О
FeO (OH) + nН2О FeO · nН2О
гётит гидрогётит
Растворение
Горные породы растворяются водами, содержащими углекислоту или органические кислоты.
Особенно интенсивно этот процесс проявляется в осадочных горных породах, которые представлены хлоридами, сульфатами и карбонатами.
Наибольшей растворимостью обладают хлориды — соли натрия (галит или поваренная соль) и калия (сильвин).
Далее по степени растворимости следуют сульфаты — ангидрит и гипс, затем карбонаты — известняки и доломиты. В процессе растворения среди монолитных толщ осадочных пород возникают различные полости, создающие карстовые формы рельефа.
Гидролиз
Сущность этого процесса заключается в разложении минералов и выносе отдельных элементов и соединений и присоединении к оставшимся соединениям гидроксильных ионов и гидратации.
При этом существенным образом нарушается структура кристаллов, которая заменяется совершенно новой.
Различают несколько вариантов гидролиза солей:
1. Гидролиз соли слабой кислоты и сильного основания:
Na2CO3 + Н2О = NaHCO3 + NaOH



 2Na + + CO32 − + H+ + OH− = Na + + HCO3− + Na + + OH−
2Na + + CO32 − + H+ + OH− = Na + + HCO3− + Na + + OH−
CO32− + H2O = HCO3− + OH−
(раствор имеет щелочную реакцию, реакция протекает обратимо)
2. Гидролиз соли сильной кислоты и слабого основания:
CuCl2 + Н2О = CuOHCl + HCl
Cu2+ + Н2О = CuOH+ + Н+
(раствор имеет кислую реакцию, реакция протекает обратимо)
3. Гидролиз соли слабой кислоты и слабого основания:
Al2S3 + 6H2O = 2Al(OH)3 + 3H2S
2Al3+ + 3S2− + 6Н2О = 2Al(OH)3 + ЗН2S
(Гидролиз в этом случае протекает практически полностью, так как оба продукта гидролиза уходят из сферы реакции в виде осадка или газа).
4. Соль сильной кислоты и сильного основания не подвергается гидролизу, и раствор нейтрален.
В гипергенных условиях каркасная структура полевых шпатов превращается в слоевую, которая характерна для различных глинистых минералов.
Из кристаллической решетки полевых шпатов выносятся ионы калия, натрия и кальция (в виде К2СО3, Na2CO3, CaHCO3, СаСО3) в результате их взаимодействия с углекислотой.
Процесс идет в условиях влажного и жаркого климата.
Если климат сухой, то карбонаты остаются в глинах.
Стадии разложения полевых шпатов в условиях влажного теплого климата. В этих условиях полевые шпаты вначале переходят в гидрослюду, а затем в более устойчивый в гипергенных условиях глинистый минерал каолинит:




 K(AlSi3O8) (K,H2O)Al2(OH)2(AlSi4O10)·nН2О Al4(OH)8(Si4O10)
K(AlSi3O8) (K,H2O)Al2(OH)2(AlSi4O10)·nН2О Al4(OH)8(Si4O10)
ортоклаз гидрослюда каолинит
Судьба кремнезема в этом процессе:
SiO2 выносится в форме истинных растворов или комплексных кремнийорганических соединений (соединения, в которых Si связан с углеродом, как, например, в силанах: (CH3)4Si, CH3SiH2SiH2CH3, (CH3)3SiCl.

Структурная формула силана

Структурная формула силикона (кислородсодержащее кремнийорганическое соединение.
Значительная часть кремнезема в водах сравнительно быстро переходит в коллоидальное (от греч. «колла» — клей) состояние и выпадает из раствора в виде амофного гидратированного осадка SiO2·nН2О.
Это аморфный минерал при высыхании и частичной потере воды превращается в опал. Но часть кремнезема остается в связанном состоянии в каолинитовой молекуле.
[Опал – аморфный диоксид кремния SiO2·nH2O Формы выделения: гроздьевидные или почковидные агрегаты аморфного кремнезёма, выполнение трещин. По происхождению осадочный, гипергенный или низкотемпературно-гидротермальный. Встречается в виде прожилок, заполняя трещины вмещающих пород].
В условиях влажного тропического и экваториального климата при большом количестве атмосферных осадков, высоких среднегодовых температурах и большом растительном опаде выветривание горных пород на каолинитовой стадии не прекращается и происходит дальнейшее разложение каолинитовой молекулы до свободных оксидов и гидроксидов:
 Al4(OH)8(Si4O10) Аl(ОН)3 + SiO2·nН2О
Al4(OH)8(Si4O10) Аl(ОН)3 + SiO2·nН2О


 каолинит гидраргиллит опал
каолинит гидраргиллит опал
Гидраргиллит - Аl(ОН)3 - или гиббсит — один из главных рудоносных минералов, представляющих алюминиевую руду.
Непосредственно над материнскими выветрелыми породами располагаются латериты, главной составной частью которых являются полуторные оксиды алюминия и железа (А12О3 и Fe2O3) с небольшой примесью кремнезема (SiO2).
Переотложенные и преобразованные латериты называют бокситами.
[Латерит - своеобразная красноцветная горная порода, образуется в результате выветривания алюмосиликатов в условиях жаркого и влажного климата в зонах переменно влажных субэкваториальных, тропических и частично субтропических географических поясов. Латерит — сильнопористая твердая кора выветривания, состоящая из каолина, окислов железа, алюминия].
– Конец работы –
Эта тема принадлежит разделу:
Шуя 2012
Федеральное государственное бюджетное образовательное учреждение... Высшего профессионального образования... Шуйский государственный педагогический университет...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Химическое выветривание
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов