рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Образование
- /
- DP=f(v)·4πv2dv.
Реферат Курсовая Конспект
DP=f(v)·4πv2dv.
DP=f(v)·4πv2dv. - раздел Образование, Вывод давления идеального газа из молекулярно-кинетических представлений ...
 рис. 1
рис. 1 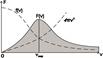 рис.2
рис.2
F(v)=dP/dv=4πv2f(v)→ F(v)= 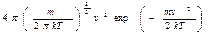
Это и есть закон распределения Максвелла по модулю скорости. Функция нормирована на единицу, т.е.:
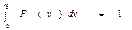
16.Распределение молекул в поле сил тяжести.
 Пусть имеется газ с массой молекул m0, T = const, на k-ю молекулу действует сила F =mg. Требуется найти концентрацию n на высоте h.
Пусть имеется газ с массой молекул m0, T = const, на k-ю молекулу действует сила F =mg. Требуется найти концентрацию n на высоте h.
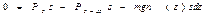 - условие равновесия системы.
- условие равновесия системы.
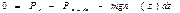
p = nkT; p(z+dz) - p(z)=dp=kTdn;
0 = - kTdn – gn(z)dz
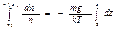 =>
=> 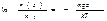 , где n0 – концентрация молекул на нулевом уровне (z = 0)
, где n0 – концентрация молекул на нулевом уровне (z = 0)
Т.о. получаем 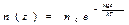 . Для того, чтобы вычислить количество молекул в слое толщиной z2 - z1, нужно посчитать интеграл
. Для того, чтобы вычислить количество молекул в слое толщиной z2 - z1, нужно посчитать интеграл 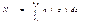
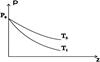
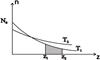
T1 < T2
17. Распределение Максвелла-Больцмана.
Распределения Максвелла и Больцмана являются составными частями единого распределения, называемого распределением Гиббса.
Оба разобранных нами распределения можно объединить в один закон распределения Максвелла-Больцмана, согласно которому число 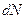 молекул, проекции скорости которых и их координаты лежат в интервалах
молекул, проекции скорости которых и их координаты лежат в интервалах
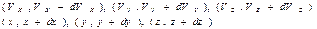
определяется выражением
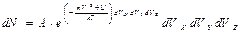
где нормировочный множитель 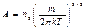 ,
, 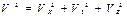 ,
,
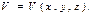
18.Барометрическая формула.
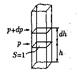
Известно, что атмосферное давление убывает с высотой. Попытаемся найти функцию p(h), описывающую зависимость давления от высоты.
Выделим мысленно в атмосфере вертикальный столб с площадью поперечного сечения S, равной единице . Атмосферное давление на высоте h обусловлено весом столба воздуха, простирающегося от сечения, расположенного на данной высоте, до внешней границы атмосферы. Поэтому на убыль давления -dp(dp означает приращение давления, которое отличается от убыли знаком) при переходе от высоты h к высоте h + dh, равна весу воздуха, заключенного в элементе столба высоты dh:
-dp = ρgdh (1),
где ρ — плотность воздуха на высоте h.
При условиях, близких к нормальным (т. е. при давлениях порядка 1 атм и температурах, близких к 0°С), воздух довольно хорошо подчиняется уравнению состояния идеального газа. Плотность идеального газа определяется выражением
ρ = Мр/(RТ). Подстановка этого выражения в формулу (1) приводит к уравнению
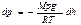
(мы перенесли знак минус в правую часть равенства). Здесь под М подразумевается молярная масса воздуха, определенная с учетом относительного содержания в воздухе азота, кислорода и других газов. Разделив переменные, придем к дифференциальному уравнению
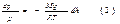
Чтобы проинтегрировать это уравнение, нужно знать, как изменяется с высотой температура, т. е. определить вид функции T(h) (зависимо стью g от h можно пренебречь). Для изотермической атмосферы, т. е. для случая, когда температура с высотой не изменяется, интегрирование уравнения (2) приводит к соотношению
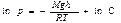
(имея в виду дальнейшие преобразования, мы обозначили постоянную интегрирования через lnC). Потенцируя это соотношение, придем к формуле
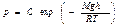
Положив h=0, получим, что С = р0, где р0 — атмосферное давление на высоте, принятой за начало отсчета.
Таким образом, для изотермической атмосферы зависимость давления от высоты описывается формулой
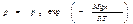
 которая называется барометрической формулой.
которая называется барометрической формулой.
19. Макро- и микросостояния. Статистический вес.
Макросостояние - это состояние тела, содержащего огромное число частиц (N ~ NA), заданное с помощью макроскоп.велич,характ.все тело в целом. Такими велич. могут быть давление p, объем V, температура T, внутренняя энергия U.
Задать микросостояние - это значит задать состояния всех частиц, из которых состоит макроскопическое тело.
В классической механике состояния материальной точки считается заданным, если задан ее радиус-вектор и вектор ее скорости . Величины и изменяются с течением времени непрерывно, поэтому в рамках классической механики нельзя ввести понятие "число состояний, в которых может находиться частица". Такая возможность появляется при описании микрочастиц на более глубоком, квантовом уровне, где величины, характеризующие состояние микрочастиц изменяются скачкообразно, дискретно.
Статистич.вес (статвес) - это число различн.микросост, соотв.данному макросостоянию.
Мы будем обозначать статвес греческой буквой Ω.
Энтропия S определяется как натуральный логарифм статистического веса макросостояния, умноженный на постоянную Больцмана
20. Энтропия и ее основные свойства.
В термодинамике энтропия определена как элементарное приращение 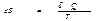 . При этом энтропия является именно функцией состояния.
. При этом энтропия является именно функцией состояния.
 Рассмотрим необратимый процесс расширения ид. газа в пустоту. V1 – первоначальный объем, V0 – полный объем. В данном случае газ не совершает работу, переданное газу тепло равно нулю, следовательно, по первому началу т/д приращение внутренней энергии тоже равно нулю, т.е. температура конечного и начального состояний одинакова. Т.к. энтропия – функция состояния, то вычислим ее работу по изотермическому процессу (т.к. он обратим). В изотермическом процессе Q=A=νRTln(V2/V1) и ΔS=Q/T=νRln(V2/V1)=kNln(V2/V1), N – число молекул в газе.
Рассмотрим необратимый процесс расширения ид. газа в пустоту. V1 – первоначальный объем, V0 – полный объем. В данном случае газ не совершает работу, переданное газу тепло равно нулю, следовательно, по первому началу т/д приращение внутренней энергии тоже равно нулю, т.е. температура конечного и начального состояний одинакова. Т.к. энтропия – функция состояния, то вычислим ее работу по изотермическому процессу (т.к. он обратим). В изотермическом процессе Q=A=νRTln(V2/V1) и ΔS=Q/T=νRln(V2/V1)=kNln(V2/V1), N – число молекул в газе.
Обозначим за P1 = (V1/V0)N вероятность попадания N молекул в объем V1, а за P2 = (V2/V0)N вероятность их попадания в V2. Тогда P2/P1 = (V2/V1)N и можно записать
ΔS=kNln(V2/V1)=kln(V2/V1)N =kln(P2/P1). А так как P~Ω, то получаем ΔS=kln(Ω2/Ω1) и приходим к формуле Больцмана
S = k lnΩ
– Конец работы –
Эта тема принадлежит разделу:
Вывод давления идеального газа из молекулярно-кинетических представлений
N кол во атомов в молекуле... Число степеней свободы N... Делятся на...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: DP=f(v)·4πv2dv.
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов