рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- З а д а н и е 1
Реферат Курсовая Конспект
З а д а н и е 1
З а д а н и е 1 - раздел Химия, Программа и контрольные задания по «Физической химии» А) Выразить Концентрацию Водного Раствора Через Молярность, М...
а) Выразить концентрацию водного раствора через молярность, моляльность, мольные доли и нормальность.
Таблица 4
| № варианта | Растворенное вещество | Масс.% | ρ, г/см3 | Т, К |
| AgNO3 | 1,668 | |||
| AlCl3 | 1,242 | |||
| Al2(SO4)3 | 1,226 | |||
| BaCl2 | 1,092 | |||
| BaCl2 | 1,096 | |||
| CaBr2 | 1,250 | |||
| CaCl2 | 1,282 | |||
| Cа(NO3)2 | 1,259 |
б) Выразить концентрацию водного раствора через массовые проценты, моляльность, нормальность, мольные доли.
Таблица 5
| № варианта | Растворенное вещество | С2, моль/дм3 | ρ, г/см3 | Т, К |
| AlCl3 | 1,185 | 1,129 | ||
| BaCl2 | 1,444 | 1,253 | ||
| CaCl2 | 1,190 | 1,101 | ||
| Cа(NO3)2 | 1,100 | 1,128 | ||
| CdSO4 | 1,034 | 1,198 |
в) Выразить концентрацию водного раствора через массовые проценты, молярность, нормальность и мольные доли.
Таблица 6
| № варианта | Растворенное вещество | m2 моль/1000 г | ρ, г/см3 | Т, К |
| FeCl3 | 2,055 | 1,234 | ||
| CaCl2 | 1,860 | 1,205 | ||
| FeCl2 | 1,970 | 1,200 | ||
| CdSO4 | 1,370 | 1,206 | ||
| FeSO4 | 1,650 | 1,213 |
г) выразить концентрацию водного раствора через массовые проценты, молярность, нормальность, моляльность.
Таблица 7
| № варианта | Растворенное вещество | N2, мольная доля | ρ, г/см3 | Т, К |
| HBr | 0,250 | 1,679 | ||
| AlCl3 | 0,083 | 1,341 | ||
| CaBr2 | 0,084 | 1,635 | ||
| CaCl2 | 0,100 | 1,396 |
д) Выразить концентрацию водного раствора через массовые проценты, молярность, моляльность, мольные доли.
Таблица 8
| № варианта | Растворенное вещество | Н, моль-экв/л | ρ, г-мл | Т, К |
| BaCl2 | 2,000 | 1,179 | ||
| CaCl2 | 2,380 | 1,101 | ||
| Cа(NO3)2 | 4,604 | 1,259 | ||
| CdSO4 | 2,068 | 1,198 |
З а д а н и е 2
1. Растворимость кислорода в воде при давлении 300 мм рт.ст. и температуре 25 °С равна 16 мг/л. Определите постоянную Генри (в атм.), если плотность раствора равна 1,05 г/см3.
2. При 291 К 1 литр воды растворяет 1 литр СО2, если давление двуокиси углерода над раствором равно 1 атм. Определите молярность раствора, над которым давление СО2 при той же температуре равно 155 мм рт.ст.
3. Определите температуру затвердевания сплава железа с кремнием, если сплав содержит 14,5 % масс. кремния. Температура затвердевания чистого железа равна 1530°С, а криоскопическая постоянная железа составляет 13,18 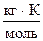 .
.
4. Вычислить температуру замерзания раствора 7,308 г хлорида натрия в 250 г воды, если при 18 °С осмотическое давление указанного раствора равно 2,1077×106 Па. Плотность раствора принять равной 1 г/см3.
5. При 18 °С осмотическое давление раствора глицерина в воде равно 3,039×105 Па. Определите осмотическое давление, если раствор разбавить в три раза, а температуру повысить до 37 °С.
6. Температура кипения чистого бензола равна 80,1°С. Его молярная теплота испарения при температуре кипения равна 7355 кал/моль. Найдите температуру кипения раствора нелетучего вещества в бензоле, если его моляльная концентрация равна 0,5 моль/кг.
7. Какую массу воды нужно взять, чтобы, растворив в ней 4,5 г глицерина при 27 °С, понизить давление пара на 379,7 Па? Давление пара воды при этой температуре равно 3565 Па.
8. Водный раствор содержит 0,5 % масс. мочевины и 1 % масс. глюкозы. Какова температура замерзания раствора, если криоскопическая постоянная воды равна 1,86 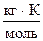 .
.
9. Определить атмосферное давление, если раствор 51,3 г сахара в 120 г воды закипает при 99,5°С. Давление пара чистой воды при данной температуре равно 99540 Па.
10. Чистый кадмий затвердевает при 321°С, а 10 % масс. раствор висмута в кадмии затвердевает при 312°С. Определите теплоту плавления чистого кадмия.
11. 1 л воды смешали с 400 мл амилового спирта, содержащего 2,5 г йода. Вычислите массу йода, перешедшего в водный слой, если коэффициент распределения йода между спиртом и водой равен 230.
12. Раствор, содержащий 0,05 моль сульфата алюминия в 100 г воды, замерзает при -4,19°С. Определите изотонический коэффициент, если криоскопическая постоянная воды равна 1,86 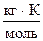 .
.
13. Сколько грамм глицерина надо растворить в 90 г воды при 30°С, чтобы понизить давление пара на 266,5 Па? Давление пара воды при данной температуре равно 4242,3 Па.
14. Коэффициент распределения бромида ртути (II) между водой и бензолом равен 0,89 при 298 К. Сколько бромида ртути можно извлечь из 100 мл 0,01 М водного раствора с помощью 300 мл бензола.
15. Некоторое количество сахара растворили в 1000 г воды. Давление пара полученного раствора при 100°С равно 100200 Па. Вычислите температуру кипения и осмотическое давление указанного раствора при 100 °С. Эбулиоскопическая постоянная воды равна 0,52 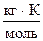 , плотность раствора принять равной 1 г/см3.
, плотность раствора принять равной 1 г/см3.
16. При давлении 1 атм. водный раствор хлорида калия, содержащий 7,5 % масс. соли, кипит при 101°С. Давление пара чистой воды при 374 К равно 104974 Па. Определите кажущуюся степень диссоциации соли в растворе.
17. Теплота испарения ртути при температуре кипения (357°С) равна 65 кал/г. Определите температуру кипения 10 % масс. раствора олова в ртути.
18. Коэффициент распределения молочной кислоты при 25°С между хлороформом и водой равен 0,0203. Какое количество молочной кислоты можно извлечь из 100 мл 0,8 М раствора молочной кислоты в хлороформе при помощи 100 см3 воды?
19. При растворении 0,6 г некоторого вещества в 25 г воды температура кипения раствора повысилась на 0,204 К. При растворении 0,3 г этого же вещества в 20 г бензола, температура кипения увеличилась на 0,67 К. Определите эбуллиоскопическую постоянную бензола, если эбулиоскопическая постоянная воды равна 0,51 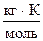 .
.
20. Нафталин и дифениламин образуют эвтектику с температурой затвердевания 32,45°С. Растворение 1,268 г эвтектики в 18,43 г нафталина понижает температуру затвердевания последнего на 1,89°С. Рассчитайте состав эвтектики в массовых долях.
21. Вычислите концентрацию йода в воде, если 250 см3 раствора амилового спирта, содержащего 10 г/л йода, взболтать с 1 л воды. Коэффициент распределения йода между спиртом и водой равен 230.
22. К 10 см3 бензола (плотность 0,879 г/мл) добавили 0,5548 г нафталина. Температура затвердевания полученного раствора 2,981°С. Определите молярную массу нафталина в бензоле, если температура замерзания чистого бензола 5,5 °С, а теплота плавления его 127,4 Дж/г.
23. Температура замерзания чистого нафталина 80,1°С. Определите молярную массу бензола, растворенного в нафталине, если при добавлении 0,4 см3 к 10 г нафталина температура замерзания раствора равна 77,01°С. Теплота плавления нафталина 148,7 Дж/г, плотность бензола 0,879 г/см3.
24. Температура затвердевания чистого бензола равна 5,5°С, а раствора 1,632 г трихлоруксусной кислоты в 100 г бензола 5,15°С. Подвергаются ли молекулы трихлоруксусной кислоты диссоциации или ассоциации в растворе.
25. Водный раствор, содержащий нелетучее растворенное вещество (неэлектролит), замерзает при -2,2°С. Определите температуру кипения раствора и давление пара раствора при 20°С, если давление пара чистой воды при указанной температуре равно 2337,8 Па.
– Конец работы –
Эта тема принадлежит разделу:
Программа и контрольные задания по «Физической химии»
На сайте allrefs.net читайте: "Программа и контрольные задания по «Физической химии»"
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: З а д а н и е 1
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов