рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- Szlig;………убрать после новых рисунков……..
Реферат Курсовая Конспект
Szlig;………убрать после новых рисунков……..
Szlig;………убрать после новых рисунков…….. - раздел Химия, КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ Использование Теории Кристаллического ПоляСовместно С Методо...
Использование Теории кристаллического полясовместно с методом ВС.
1.Лиганды располагаются вокруг комплексообразователя так, чтобы силы притяжения были максимальны, а силы отталкивания минимальны.
2. Лиганды влияют на энергетическое состояние d-электронов комплексообразователя.
В отсутствие внешнего поля все d-орбитали - вырожденные.
Под воздействием поля лигандов Þ расщепление d-подуровня на величину D, называемую энергией расщепления.
Величина D - зависит от координационного числа, природы лигандов и комплексообразователя и его заряда.
Если Еспаривания < Ерасщепления Þ спаривание электронов Þ низкоспиновые комплексы.
В противном случае комплекс- высокоспиновый.
плоский квадрат
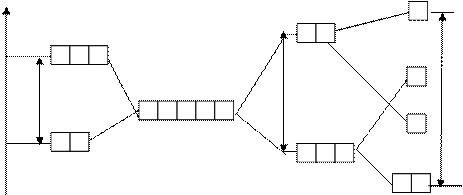 |
Е октаэдр
тетраэдр
de dg
Dтетр Dокт Dквадр.пл.
dg (n-1)d-орбитали de
комплексообразователя
в отсутствие лигандов
Ерасщепления(4d,5d АО) > Ерасщепления(3d) Þ для комплексообразователей 4d,5d-элементов Þ все лиганды сильного поля.
ПРИМЕР: Комплекс [Fe(Н2О)6]2+.
Комплексообразователь Fe2+: 3d64s0.
Координационное число 6 Þ октаэдрическое расщепление.
центральный ион – 3d-элемента Þсила поля лиганда по спектрохимическому ряду.
Н2О – лиганд среднего поля, а для Fe2+ (низшая степень окисления) он относится к слабым.
Энергетическая диаграмма расщепления d-подуровня
:н2о:н2о:н2о:н2:н2о:н2о



 Е
Е

3dg 4s 4p 4d
 |

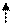
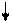
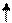
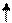
 3de
3de
– Конец работы –
Эта тема принадлежит разделу:
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ А m n В n mDm K Ag CN Fe H O Cl Cu NH SO комплексные... Так и в узлах кристаллической решетки... aelig анионы Ag CN...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Szlig;………убрать после новых рисунков……..
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов