рефераты конспекты курсовые дипломные лекции шпоры
Реферат Курсовая Конспект
Основные химические законы
Основные химические законы - Лекция, раздел Химия, Лекция № 1-2 Тема лекции: Введение. Основные понятия и законы химии Исходя Из Идеи О Несотворимости Атомов И Опираясь На Собствен...
Исходя из идеи о несотворимости атомов и опираясь на собственные наблюдения, в 1748 году М.В. Ломоносов впервые формулирует закон сохранения материи и движения:
“... все перемены, в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимется, столько присовокупится к другому... Сей всеобщий закон простирается и в самые правила движения: ибо тело, движущее своею силою другое, столько же оные у себя теряет, сколько сообщает другому, которое от него движение получает”.
Спустя 8 лет этот закон он подтвердил экспериментально. Прокаливая металлы в запаянных сосудах, М.В.Ломоносов нашел, что во всех случаях масса сосуда с содержимым до реакции равна его массе после реакции. Применительно к химическим процессам закон Ломоносова формулируется теперь как закон сохранения массы веществ: “Масса всех веществ, вступивших в реакцию, равна массе продуктов реакции".
В 1774 году французский химик Лавуазье повторил опыты Ломоносова и получил те же результаты. Работы этих ученых способствовали быстрому росту химических наук. Закон сохранения массы веществ является одним из основных законов природы. Он доказывает, что ничего не исчезает бесследно и не возникает из ничего, что материя всегда существовала и будет существовать, подвергаясь изменения, переходя из одной формы в другую. В СООТВЕТСТВИИ С ДОСТИЖЕНИЯМИ ФИЗИКИ XX ВЕКА, ЗАКОН СОХРАНЕНИЙ МАССЫ ВЕЩЕСТВ ДОЛЖЕН БЫТЬ ЗАМЕНЕН БОЛЕЕ ОБЩИМ ЗАКОНОМ СОХРАНЕНИЯ МАТЕРИИ. ТОЛЬКО МАТЕРИЯ ВО ВСЕХ ПРОЦЕССАХ СОХРАНЯЕТСЯ ПОСТОЯННОЙ, А МАССА, КАК ОДНА ИЗ ХАРАКТЕРИСТИК МАТЕРИИ, МОЖЕТ ПЕРЕХОДИТЬ В ДРУГУЮ ЕЕ ХАРАКТЕРИСТИКУ – ЭНЕРГИЮ, ЧТО ВЫРАЖАЕТСЯ УРАВНЕНИЕМ ЭНШТЕЙНА: Е = мс2, где Е - энергия;
м - масса;
с - скорость света.
Уравнение Е = мс2 нельзя трактовать так, что масса переходит в энергию или, наоборот, энергия в массу. Масса и энергия - свойства материи: масса - мера инертности, энергия - мера движения материи, и они не превращаются .друг в .друга. Приведенное уравнение показывает, что изменение массы данной системы обязательно сопровождается изменением энергии. Таким образом, масса и энергия - основные, неотъемлемые свойства движущейся материи - обнаруживают неразрывную связь.
Это значит, что существует глубокая взаимосвязь и между основными, фундаментальными законами всего современного естествознания - законов сохранения массы и законом сохранения и превращения энергии.
В конце ХVШ века французский химик Пруст на основании тщательных количественных исследований открыл закон постоянства состава:
"КАЖДОЕ ХИМИЧЕСКОЕ СОЕДИНЕНИЕ, НЕЗАВИСИМО ОТ СПОСОБА ЕГО ПОЛУЧЕНИЯ ИМЕЕТ ОДИН И ТОТ ЖЕ ПОСТОЯННЫЙ СОСТАВ".
Например: СаСО3 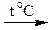 СаО + СО2
СаО + СО2
С + О2  СО2
СО2
Nа2СО3 + 2НС1  2NаС1 + СО2 + Н2О
2NаС1 + СО2 + Н2О
На основании этих уравнений можно сделать следующий вывод:
ЕСЛИ СОСТАВ ВЕЩЕСТВА НЕ ЗАВИСИТ ОТ СПОСОБА ЕГО ПОЛУЧЕНИИ, ТО, СЛЕДОВАТЕЛЬНО, ЭЛЕМЕНТЫ, ОБРАЗУЮЩИЕ ЭТО ВЕЩЕСТВО, СПОСОБНЫ СОЕДИНЯТЬСЯ МЕЖДУ СОБОЙ ТОЛЬКО В СТРОГО ОПРЕДЕЛЕННЫХ ВЕСОВЫХ КОЛИЧЕСТВАХ. ПОЭТОМУ И ОБРАЗУЮТСЯ ВЕЩЕСТВА ОПРЕДЕЛЕННОГО, А НЕ ПРОИЗВОЛЬНОГО СОСТАВА. Вторая Формулировка закона Пруста: "ХИМИЧЕСКИЕ ЭЛЕМЕНТЫ СОЕДИНЯЮТСЯ МЕЖДУ СОБОЙ В СТРОГО ОПРЕДЕЛЕННЫХ ВЕСОВЫХ КОЛИЧЕСТВАХ".
Закон постоянства состава дает возможность провести границу между химическим соединением и смесью, которая состоит из произвольных количеств, и не обладает постоянством состава: Например: Те и S.
– Конец работы –
Эта тема принадлежит разделу:
Лекция № 1-2 Тема лекции: Введение. Основные понятия и законы химии
Тема лекции Введение Основные понятия и законы химии... План лекции Предмет задачи и методы химии...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Основные химические законы
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов