рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Биология
- /
- Карбонильные соединения в биоорганической химии. Строение, химические свойства, медикобиологическое значение альдегидов и кетонов.
Реферат Курсовая Конспект
Карбонильные соединения в биоорганической химии. Строение, химические свойства, медикобиологическое значение альдегидов и кетонов.
Карбонильные соединения в биоорганической химии. Строение, химические свойства, медикобиологическое значение альдегидов и кетонов. - раздел Биология, Биологически активные вещества растительного происхождения Карбонильные Соединения Содержат Карбонильную Группу С=О. Од...
Карбонильные соединения содержат карбонильную группу С=О. Один из наиб. распространенных типов неорг. и орг. в-в. К ним относятся, напр., СО, СО2, карбонаты, мочевина. Однако под карбонильными соединениями в узком смысле понимают лишь альдегиды и кетоны, а также (в меньшей степени) карбоновые кислоты и их производные. Карбонильные соединения высоко реакционноспособны. Группа С=О способна восстанавливаться до спиртовой или метиленовой группы. Из-за наличия частичного положит. заряда на атоме С карбонильные соединения присоединяют разл. нуклеофилы, напр., амины, металлоорг. соед., вступают в р-ции электроф. замещения в ароматич. кольце. Р-ции с нуклеофилами часто сопровождаются дальнейшим отщеплением воды с образованием производных карбонильных соединений, напр., гидразонов, шиффовых оснований. Если группа С=О связана с гетероатомом, несущим неподеленную пару электронов, напр., в карбоновых к-тах и их производных, то р-ции по этой группе с нуклеофилами могут затрудняться, а с электрофилами (к-тами) облегчаться. Благодаря подвижности атомов Н у соседнего с карбонильной группой атома С (a-С-атома) карбонильные соединения сравнительно легко, в особенности при катализе к-тами или основаниями, переходят в енольную форму Енолизация или образованиеенолят-аниона первая стадия мн. важных р-ций карбонильных соединений, где они выступают в качестве С-нуклеофильных реагентов. К таким р-циям относятся галогенирование по a-С-атому, альдольная и кретоновая конденсации, присоединение к активир. кратным связям (реакция Михаэля ) и др.
У альдегидов карбонильный углерод соединен с атомом Н и органической группой R (общая формула RHC=O)
Применение альдегидов в медицине.
Формальдегид (формалин).Применяют как дезинфицирующее и дезодорирующее средство для мытья рук, обмывания кожи при повышенной потливости (0,5-1 %), для дезинфекции инструментов (0,5 %), для спринцеваний (1:2000 - 1:3000). Входит в состав лизоформа.
Формидрон - жидкость, содержащая раствора формальдегида 10 частей, спирта этилового 95 % 40 частей, воды 50 частей, одеколона 0,5 частей. Применяют для протирания кожи при повышенной потливости.
Мазь формальдегидная. Применяют при повышенной потливости, втирают в подмышечняю впадины один раз в сутки, в межпальцевые складки.
Лизоформ мыльный раствор формальдегида. Состав: формалина 40 частей, мыла калийного 40 частей, спирта 20 частей. Оказывает дезинфицирующее и дезодорирующее действие. Применяют для спринцевания в гинекологической практике, для дезинфекции рук (1-3 % растворы).
Уротропин (гексаметилентетрамин), бесцветные кристаллы без запаха, легко растворимы в воде. Водные растворы имеют щелочную реакцию. Применяют главным образом при инфекционных процессах мочевыводящих путей (циститах, пиелитах)
Кетоны — органические соединения общей формулы R—CO—R (где R — углеводородные радикалы, например СН3—, СН3 — СН2— и т. д.). Низшие кетоны — жидкости с характерным запахом, например ацетон (СН3)2CO, высшие — твердые вещества, например камфора. К классу кетонов относятся также стероидные гормоны (эстрон, кортизон и др.), многие из которых применяются в медицине в разных целях.
12. Карбоновые кислоты в биоорганической химии. Строение, химические свойства. Функциональные производные карбоновых кислот: ангидриды, амиды, сложные эфиры. Реакции декарбоксилирования.
Карбо́новые кисло́ты — класс органических соединений, молекулы которых содержат одну или несколько функциональных карбоксильных групп -COOH. Кислые свойства объясняются тем, что данная группа может сравнительно легко отщеплять протон. За редкими исключениями карбоновые кислоты являются слабыми. Например, у уксусной кислоты CH3COOH константа кислотности равна 1,75·10−5. Ди- и трикарбоновые кислоты более сильные, чем монокарбоновые
В зависимости от радикала, связанного с карбоксилом, различают следующие группы карбоновых кислот:
· ароматические
· алифатические (в том числе предельные и непредельные)
· алициклические
· гетероциклические.
По числу карбоксильных групп кислоты могут быть одно-, двух- и многоосновными. При введении в молекулы кислоты других функциональных групп (например, -ОН, =CO, -NH2 и др.) образуются окси-, кето-, аминокислоты и другие классы соединений. Эти соединения вступают в те же реакции, что и карбоновые кислоты, плюс ко всему протекают реакции и по замещенной группе.
Наиболее важные химические свойства, характерные для большинства карбоновых кислот:
1. Карбоновые кислоты при реакции с металлами, их оксидами или их осно́вными гидроксидами дают соли соответствующих металлов:
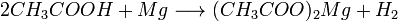
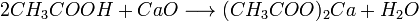
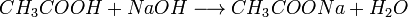
2. Карбоновые кислоты могут вытеснять более слабую кислоту из её соли, например:
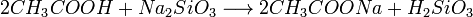

3. Карбоновые кислоты в присутствии кислого катализатора реагируют со спиртами, образуя сложные эфиры (реакция этерификации):
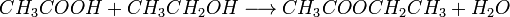
4. При нагревании аммонийных солей карбоновых кислот образуются их амиды:
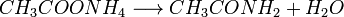
5. Под действием 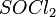 карбоновые кислоты превращаются в соответствующие хлорангидриды:
карбоновые кислоты превращаются в соответствующие хлорангидриды:
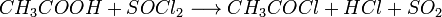
13. Строение и свойства дикарбоновых кислот.
Дикарбоновыекислоты, орг. соед., содержащие две карбоксильные группы СООН. Называют их аналогично карбоновым кислотам; многие дикарбоновые кислоты имеют тривиальные назв., которые, как правило, и используются (см. табл.). Дикарбоновые кислоты- кристаллич. в-ва. Т-ры плавления алифатич. дикарбоновых кислот с четным числом атомов С значительно выше, а р-римость в воде меньше, чем соответствующие показатели соседних нечетных гомологов. Первая константа диссоциации дикарбоновых кислот выше, чем соответствующих монокарбоновых к-т, что особенно заметно у низших гомологов.
Дикарбоновые кислоты проявляют все св-ва карбоновых к-т, образуя как моно-, так и дипроизводные. Взаимное влияние и взаимод. двух карбоксильных групп вызывает ряд р-ций, характерных только для дикарбоновых кислот. При нагр. низшие алифатич. дикарбоновые кислоты (щавелевая, малоновая) легко декарбоксилируются; к-ты, содержащие 2-3 атома С между карбоксилами, при нагр. или при действии дегидратирующих агентов образуют циклич. ангидриды, а высшие дикарбоновые кислоты - полимерные ангидриды. Образование циклич. продуктов характерно и для производных дикарбоновых кислот, напр., эфиров, дающих эфиры циклич. b-кетокислот (а)и восстанавливающихся в циклич. ацилоины (б):
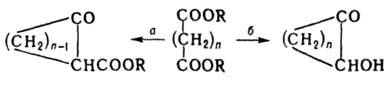
– Конец работы –
Эта тема принадлежит разделу:
Биологически активные вещества растительного происхождения
Биоорганическая химия наука которая изучает связь между строением органических веществ и их биологическими функциями Как самостоятельная наука... Методы Основной арсенал составляют методы органической химии для решения... Объекты изучения...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Карбонильные соединения в биоорганической химии. Строение, химические свойства, медикобиологическое значение альдегидов и кетонов.
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов