ПЕРЕГОНКА И РЕКТИФИКАЦИЯ
МОДУЛЬ № 5
МАСООБМЕННЫЕ ПРОЦЕССЫ
ЛЕКЦИЯ № 27
ПЕРЕГОНКА И РЕКТИФИКАЦИЯ
1. Г.Д. Кавецкий, В.П. Касьяненко «Процессы и аппараты пищевой технологии».- М., КолосС, 2008.-591 с.: ил. 2. Процессы и аппараты пищевых производств. Учебник для вузов в 2 книгах/…ВОПРОС №1. ОБЩИЕ СВЕДЕНИЯ
Перегонка и ректификация — наиболее распространенные методы разделения жидких однородных смесей, состоящих из двух или нескольких летучих… Процессы перегонки и ректификации широко применяют в пищевой промышленности… Процессы перегонки и ректификации основаны на разной летучести компонентов смеси при одной и той же температуре.…ВОПРОС 2. ПРОСТАЯ ПЕРЕГОНКА
Простую перегонку можно проводить с отбором фракций, дефлегмацией, водяным паром или под вакуумом (молекулярная перегонка). Фракционная перегонказаключается в постепенном испарении жидкости, находящейся…Рис. 3. Диаграмма для определения температуры кипения при перегонке с водяным паром

Рис. 4. Установка для перегонки с водяным паром:
1 — куб; 2— конденсатор; 3 — сепаратор
Отношение количества отогнанного компонента к количеству водяного пара
 (4)
(4)

Парциальное давление водяного пара рв = Р — φрк, где Р— общее давление; φ — степень насыщения. Тогда из уравнения (4):
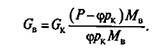 (5)
(5)
Молекулярная перегонкапредназначена для разделения компонентов, кипящих при высоких температурах и не обладающих необходимой термической стойкостью. Процесс проводят под глубоким вакуумом, соответствующим остаточному давлению 1,31...0,131Па.
Молекулярная перегонка происходит путем испарения жидкости с ее поверхности. Процесс осуществляется на близрасположенных поверхностях испарения и конденсации, причем расстояние между ними (обычно 20...30 мм) должно быть меньше длины свободного пробега молекул. В этом случае отрывающиеся от поверхности испарения молекулы летучего компонента попадают на поверхность конденсации и конденсируются на ней. Разность температур между поверхностями испарения и конденсации 100 'С.
На рис. 5 показана схема аппарата для молекулярной перегонки. Исходная смесь поступает в аппарат через трубу на дно ротора. Под действием центробежной силы поступившая жидкость поднимается в виде тонкой пленки по конусу, одновременно нагревается излучением от электронагревателя и испаряется. Оторвавшиеся с поверхности испарения молекулы уносятся к поверхностям конденсации. Пары менее летучего компонента конденсируются на поверхности конденсатора 4, а пары более летучих компонентов—на поверхности конденсатора 5. Первая фракция стекает с поверхности конденсатора 4 на поддон 8, а вторая конденсируется на змеевике и стекает на поддон 7. Неиспарившаяся часть жидкости под действием центробежной силы переливается через край ротора в отводной желоб и удаляется из аппарата.
Из поддона 8 дистиллят отводится через периферийную секцию кольцевого сборника, а из поддона 7—через центральную секцию.
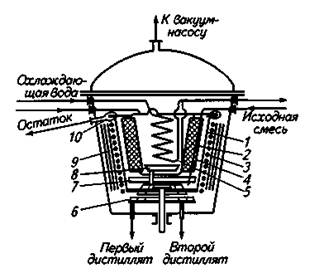
Рис. 5. Аппарат для молекулярной перегонки:
1 — ротор; 2—труба для подачи исходной смеси; 3— электронагреватель; 4,5— первый и второй конденсаторы; 6— кольцевой сборник; 7, 8— поддоны под первым и вторым конденсаторами; Р—концентрическая изоляционная плита; 10— отводной желоб
ВОПРОС 4. РЕКТИФИКАЦИЯ
При расчете процессов ректификации принимают, что: 1) при конденсации 1 кмоль пара испаряется 1 кмоль жидкости, следовательно,… 2) при конденсации пара в дефлегматоре его состав не изменяется, следовательно, состав пара, выходящего из…Рис.6. t—x, у-диаграмма
Процесс ректификации иллюстрируется t—x, у-диаграммой (рис. 6). При нагревании жидкой смеси состава х1 до температуры кипения t1 получают пар равновесного состава, после конденсации которого образуется жидкость состава х2, обогащенная легколетучим компонентом. В результате последующего нагревания этой жидкости до температуры кипения t2 и конденсации паров получают жидкость состава х3. Таким образом, проводя многократное испарение жидкости и конденсацию паров, можно разделить исходную смесь на чистые легколетучий и труднолетучий компоненты.
ВОПРОС 3. Расчет числа тарелок и рабочей высоты ректификационной колонны
Расчет числа тарелок и рабочей высоты ректификационной колоннычасто ведут по числу теоретических или действительных ступеней изменения концентраций (см. главу 16). При этом предполагается, что в теоретической ступени достигается равновесие между паром, уходящим на вышерасположенную ступень (тарелку), и жидкостью, стекающей со ступени (тарелки) на нижерасположенную.
Рассмотрим принцип работы барботажной тарелки (рис. 7, а). Пусть на n-ную тарелку поступает с вышерасположенной жидкость концентрацией хn + 1 а с нижерасположенной тарелки — пар концентрацией уn-1. В результате массообмена легколетучий компонент из жидкости переходит в пар, а труднолетучий — из пара в жидкость. Концентрация легколетучего компонента в паре возрастает до уп, а в жидкости уменьшается с хn + 1 до хn - 1.
При рассмотрении процесса примем следующие широко распространенные допущения: жидкость на тарелке идеально перемешана и имеет постоянную концентрацию хn, а концентрация пара в слое жидкости изменяется от уn-1 до уn в режиме идеального вытеснения (см. главу 2).
В случае достижения равновесия процесс изменения концентрации в паре от уn-1 до уn = упр изображается вертикальным отрезком АВ, а изменение концентрации в жидкости от хn + 1 до хn — горизонтальным отрезком BD (рис. 7, б). Таким образом, ступенька ABD изображает процесс, происходящий на одной теоретической тарелке.
Чтобы определить, сколько теоретических тарелок требуется установить в колонне для разделения исходной смеси в заданных

Рис. 7. К расчету числа ректификационных тарелок:
а — схема взаимодействия пара и жидкости на тарелке; б— изображение процесса в у-х -диаграмме в случае достижения равновесия между паром и жидкостью; в — изображение процесса в у—х-диаграмме в случае, когда равновесие между паром и жидкостью на тарелке не достигается
пределах от хf до xW. от хf до xd, вписывают между линией равновесия и рабочими линиями между точками А и С ступенчатую линию. Число полученных ступеней и определит число теоретических тарелок.
На реальной ступени (тарелке) изменения концентраций никогда не достигается равновесие, т. е. уn < упр (рис. 7, в).
Для определения числа действительных тарелок используют коэффициент полезного действия, значение которого находят опытным путем.
Методы расчета числа действительных ступеней изменения концентраций (тарелок), базирующиеся на коэффициентах массопередачи, изложены в главе 16.
Для расчета коэффициентов массоотдачи в фазах можно рекомендовать следующие уравнения:
в жидкой фазе
 (6)
(6)
в газовой фазе для ситчатых тарелок
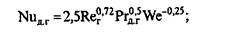 (7)
(7)
то же для колпачковых тарелок
 (8)
(8)
В уравнениях (7) и (8) линейным размером в критерии

Критерий Вебера 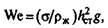 где σ— поверхностное натяжение, Н/м;
где σ— поверхностное натяжение, Н/м;
hст — высота статического слоя жидкости на тарелке, м.
ВОПРОС 5. СХЕМЫ РЕКТИФИКАЦИОННЫХ УСТАНОВОК
В пищевой промышленности используют главным образом тарельчатые и насадочные ректификационные колонны, конструкции которых описаны в главе 17. Ректификационная установка непрерывного действияпоказана на рис. 8. Исходная… В случае неполной конденсации паров в дефлегматоре они поступают в конденсатор-холодильник, где конденсируются и…Рис. 9. Ректификационная установка для разделения многокомпонентной смеси
Ректификационная установка периодического действия,используемая в малотоннажных производствах, показана на рис. 10. Исходная смесь загружается в кипятильник, который обогревается насыщенным водяным паром. После нагрева смеси до температуры кипения ее пары поступают в нижнюю часть ректификациионной колонны. Поднимаясь по колонне, пары обогащаются легколетучим компонентом и поступают в дефлегматор, в котором конденсируются. Как и при непрерывной ректификации, конденсат разделяется на флегму и продукт, который после охлаждения в холодильнике собирается в сборнике. После извлечения продукта кубовый остаток сливают и загружают в куб новую порцию исходной смеси.
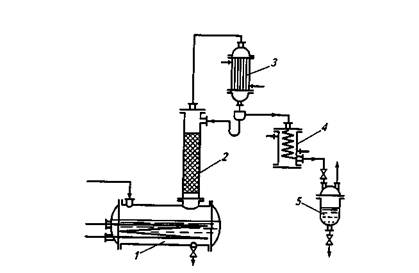
Рис. 10. Ректификационная установка периодического действия:
1— кипятильник; .2—колонна; 3—дефлегматор; 4—холодильник; 5—сборник