рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Политика
- /
- Атомный уровень организации вещества
Реферат Курсовая Конспект
Атомный уровень организации вещества
Атомный уровень организации вещества - раздел Политика, НИЖЕГОРОДСКИЙ ГОСУДАРСТВЕННЫЙ Атом–Это Микросистема, Состоящая Из Ядра И Электронов, Движущихся В Поле Я...
Атом–это микросистема, состоящая из ядра и электронов, движущихся в поле ядра. Размер любого атома имеет порядок 10-10 м, а размеры ядра 10-15 м. Ядро представляет собой сложную систему, состоящую из положительно заряженных протонов и электронейтральных нейтронов. Почему протоны в ядре удерживаются вместе и не разлетаются в результате электрических сил отталкивания? Ответ дает ядерная физика.
Протон состоит из двух верхних кварков с зарядом q= +2/3 и одного нижнего кварка с зарядом q= -1/3. Кварки связаны глюионным полем (сильным полем). В целом заряд протона q= 2×(+2/3) + (-1/3) = +1. Заряд нейтрона равен нулю, т.к. нейтрон состоит из двух нижних кварков и одного верхнего
q= 2×(-1/3) + (+2/3) = 0. В отличие от стабильного протона нейтрон имеет период полураспада, равный примерно 12 минутам. Периодом полураспада называется время, за которое распадется половина исходного вещества. Протоны и нейтроны на расстояниях порядка 10-15м (ядро) удерживаются вместе сильным полем. Силы взаимного притяжения протонов и нейтронов глюионным полем на таких небольших расстояниях превосходят силы электромагнитного отталкивания . При этом нейтроны в ядре существуют и не распадаются благодаря обменному взаимодействию.
Размеры атома по сравнению с размерами атомного ядра гигантские. Достаточно сравнить радиус ядра 10-15м и радиус атома 10-10м. Электронная оболочка, охватывающая ядро, обладает ничтожной массой по сравнению с массой ядра. И вновь возникает вопрос: почему отрицательно заряженные электроны не падают на положительно заряженное ядро? Чтобы ответить на этот вопрос, необходимо вернуться к истокам становления квантовой механики.
3. 2. 1. К о р п у с к у л я р н о – в о л н о в о й д у а л и з м
Во второй половине ХIХ века английский физик Д.К. Максвелл (1831-1879) разработал теорию электромагнитного поля, которую он сформулировал в виде системы уравнений, называемых уравнениями Максвелла. Они выражают основные закономерности электромагнитных явлений. В соответствии с теорией источником электрического поля могут быть электрические заряды или изменяющиеся во времени магнитные поля. Магнитные поля возбуждаются движущимися электрическими зарядами (электрическим током) или переменными электрическими полями. Это дало Максвеллу основание считать, что электрические и магнитные поля неразрывно связаны друг с другом в единое электромагнитное поле.
Распространение электромагнитных волн осуществляется со скоростью света, свет–это тоже электромагнитные волны. Электромагнитная теория Максвелла объясняла такие явления, как интерференция и дифракция света, зависимость скорости распространения света в среде от длины волны (дисперсия света). Однако с позиций электромагнитной теории невозможно было объяснить свечение тел, т.е. явление равновесного теплового излучения тел. Эксперименты показывали, что распределение энергии излучения по длинам волн при изменении температуры имеет вид, представленный на рис. 10.
Попытки немецкого физика М. Планка (1858-1947) согласовать электромагнитную теорию Максвелла с экспериментально наблюдаемым свечением нагретых тел привели к совершенно неожиданному результату. Противоречие преодолевалось, если постулировать: излучение света телами происходит не непрерывно, а дискретно, определенными порциями (квантами). «Ограничителем» соотношения между энергией и частотой излучения служит постоянная h, названная позже постоянной Планка:
h= E/n
где n=с/l;
с–скорость света;
l-длина волны электромагнитного излучения.
 |
| 
| ||||||||

| |||||||||
|
| ||||||||
| |||||||||

| |||||||||
| |||||||||

| |||||||||
  
|
| |
| |
| |
| |
Длина волны, l×10-6 м
Рис. 10. Распределение энергии излучения нагретого тела по длинам волн при различных температурах
Величина h, названная Планком квантом действия, казалась ему «либо фиктивной величиной, и тогда весь вывод закона излучения был в принципе ложным и представлял собой лишь игру в формулы, лишенными смысла», либо величина h имела фундаментальный смысл излучения квантами, порциями. Тогда дискретность излучения, по его мнению, «означает нечто совершенно новое и неслыханное, что должно произвести переворот в нашем физическом мышлении, основывающемся со времен Лейбница и Ньютона, открывших дифференциальное исчисление, на гипотезе непрерывности всех причинных соотношений» [7, с. 383].
Работа Планка в 1900 г. открыла путь к развитию квантовой физики. В ней говорилось, что тело излучает свет порциями, квантами. Но, как оказалось, это был лишь первый шаг. В 1905 г. А. Эйнштейн распространил идею Планка о дискретности излучения света телами на световой поток: не только нагретые тела излучают свет квантами (порциями), но само излучение представляет поток световых квантов–фотонов, энергия которых определяется формулой Планка
Е = hn = hc/l
и уравнением Эйнштейна
Е=mc2
Был подходящий случай задуматься о свойствах электромагнитного излучения.
Еще в 1887 г. немецкий физик Г. Герц (1857-1894) установил явление фотоэффекта. Под действием света вещество (например, цинковая пластина) испускает электроны. Количественные закономерности фотоэлектрического эффекта были установлены русским физиком А.Г. Столетовым (1839-1896). Электромагнитная теория не могла объяснить того факта, что энергия вылетающих с поверхности металла электронов не зависела от интенсивности светового излучения. Противоречие между экспериментально наблюдаемым явлением фотоэффекта и электромагнитной теорией Максвелла преодолевалось, по мнению Эйнштейна, следующим образом: «Мы должны предположить, что однородный свет состоит из зерен энергии….. «световых квантов», т.е. небольших порций энергии, несущихся в пустом пространстве со скоростью света» [7, с. 384]. Примечательно, что выдающиеся ученые чрезвычайно критически относились к собственным «безумным» идеям. Они старались задавать природе правильные вопросы и стремились правильно истолковывать ответы природы. Уместно еще раз напомнить слова Э. Резерфорда: «Мы делали больше, чем понимали». Это означало, что ученые по отношению к своим идеям были самыми первыми и самыми строгими критиками. Размышляя о гипотезе квантов, лауреат Нобелевской премии 1921 г. А. Эйнштейн писал в одном из своих писем в 1951 г.: «После 50 лет раздумий я так и не смог приблизится к ответу на вопрос, что же такое световой квант» [7, с. 386]. Выступая в 1947 г. перед студентами Боннского университета, лауреат Нобелевской премии 1918 г. М. Планк сказал: «Единственное, на что мы с уверенностью можем претендовать как на нашу собственность, высшее благо, которое у нас не может отнять никакая сила в мире и которое способно принести нам ни с чем не сравнимое счастье, это сознание честно выполненного долга. Тот, кто имел счастье принимать участие в создании точной науки, обретет высшее удовлетворение и внутреннее спокойствие в сознании, что он исследовал исследуемое и спокойно уважал неисследованное» [7, с. 383].
Квантовая теория света получила экспериментальное подтверждение лишь в 1922 г. когда американский физик А. Комптон (1892-1962) открыл явление изменения длины волны рентгеновского излучения вследствие рассеяния его электронами вещества (эффект Комптона). Опыты подтвердили дискретность, т.е. делимость света на частицы энергии-фотоны.
Рождение «безумных» идей в XX веке продолжалось. В 1909 г., через 4 года после выдвинутой Эйнштейном квантовой теории света, он указывает на необходимость поиска пути, объединяющей модели кванта с волновой моделью электромагнитного излучения. Но где этот путь? Пока было не ясно.
Если поле проявляет свойства непрерывности (волна) и дискретности (частица), то не проявляет ли вещество свойства не только дискретности (частица), но и непрерывности (волна)? Тридцатидвухлетнему французскому физику Луи де Бройлю (1892-1987) казалась весьма привлекательной идея о двойственной природе вещества. Для электромагнитного излучения, сочетающего в себе свойства дискретности и непрерывности, можно получить уравнение, отражающее свойства волны и частицы, если воспользоваться формулой Планка Е=hn и уравнением Эйнштейна Е=mс2:
mс2= hn,
или
mс2= hс/l
Отсюда следовало для фотона (foton):
(волновое свойство – длина волны) lf=h/mfc (корпускулярное свойство – масса)
Признавая за электромагнитным излучением (полем) волновые и корпускулярные свойства, де Бройль предполагал, что волновые и корпускулярные свойства присущи веществу, точнее любым частицам вещества. Например, для электрона (electron) уравнение волны имеет вид
lе=h/mеuе,
где mе–масса электрона, uе–скорость движения электрона, lе–длина волны электрона.
В конце 1923 г. де Бройль выполнил основные теоретические расчеты, а в конце 1924 г. появились первые публикации, в которых он высказал мысль о единстве природы (вещества и поля). Есть интересное замечание профессора Поля Ланжевена – учителя де Бройля, который в частной беседе с А.И. Иоффе (русским физиком) сказал о диссертационной работе де Бройля: «Идеи диссертанта, конечно, вздорны, но развиты с таким изяществом и блеском, что я принял диссертацию к защите». Конечно, идея казалась вздорной. Как частицы вещества могут быть волнами? Но она была не более безумной, чем идея Эйнштейна о том, что электромагнитные волны–это поток частичек энергии-фотонов. Позже за эти идеи де Бройль был удостоен Нобелевской премии.
По расчетам де Бройля стационарными электронными орбитами в модели атома Бора являются те, на которых укладывается целое число длин волн электрона lе. Только в этом случае волна не будет затухать. При круговых орбитах получаем соотношение
2pr=nlе,
где r – радиус круговой орбиты, n – целое число длин волн.
Подставляя в это уравнение значение длины волны де Бройля
lе=h/mеuе,
получаем
2pr=nh/ mеuе
Последнее уравнение позволяет рассчитать орбитали в водородоподобном атоме.
Гипотеза де Бройля о присущих частицам вещества волновых свойствах требовала экспериментального подтверждения. Нужен был экспериментальный способ доказательства верности или ложности гипотезы. Оказалось, что экспериментальное доказательство уже существовало. Еще в 1921 г. американский физик К. Дэвиссон (1881-1958) обнаружил, что поток электронов, отражаясь от поверхности металлической пластины, рассеивался под определенным углом. Картина рассеяния была необъяснимой, странной. После появления работ де Бройля стало понятно, какие свойства электронов следует искать, чтобы объяснить полученную картину рассеяния. В 1927 г. К. Дэвиссон совместно со своим сотрудником Л. Джермером провели дополнительные исследования отражения электронного пучка от поверхности металла и получили четкую дифракционную картину на атомной кристаллической решетке никеля. Независимо от них в этом же году английский физик Д. Томсон (1892-1975)–сын известного физика Дж.Дж. Томсона-открыл явление дифракции электронов (волновые свойства электронов) при рассеянии потока электронов через тонкую металлическую фольгу.
По поводу обнаружения волновых свойств микрочастиц вещества австрийский физик Э. Шредингер (1887-1961) писал, что «некоторые исследователи (Дэвиссон, Джермер и молодой Дж. П. Томсон) приступили к выполнению опыта, за который еще несколько лет назад поместили бы в психиатрическую больницу для наблюдения за их душевным состоянием. Но они добились полного успеха» [5, с. 23]. Добавим, что в 1937 г. за выдающиеся экспериментальные исследования волновых свойств вещества К. Дэвиссон и Дж.П. Томсон были удостоены Нобелевской премии.
Для микрочастиц вещества и поля характерны свойства непрерывности (волна) и дискретности (частица). Такое сочетание свойств названо корпускулярно-волновым дуализмом (лат. corpusculum-тельце, очень маленькая частица вещества; лат dualis-двойственный).
3. 2. 2. П р и н ц и п ы к в а н т о в о й м е х а н и к и
Постепенно сформировались взгляды на микромир, которые существенно отличаются от привычных представлений классической физики.
Можно ли одновременно точно определить положение и скорость снаряда, выпущенного из орудия? Классическая механика дает на это утвердительный ответ. То же самое относится к полету космического корабля, движущегося по орбите вокруг Земли со скоростью 8000 м/с (первая космическая скорость). Можно ли одновременно точно определить положение и скорость электрона, движущегося в поле ядра? Ответ будет отрицательный. Приемы вычислений классической механики имеют ограничения в механике микромира. Немецкий физик В. Гейзенберг (1901-1976) сформулировал в 1927 г. принцип (соотношение неопределенностей), который гласит: объект микромира невозможно одновременно с любой наперед заданной точностью характеризовать координатой и импульсом. Если неопределенность в определении координаты х составляет Dх, а неопределенность в определении импульса mu составляет D(mu), то неопределенности этих величин удовлетворяют условию
Dх×D(mu) ³ h
Произведение неопределенностей координаты и импульса не может быть меньше постоянной Планка.
Применительно к движению электрона в поле ядра атома соотношение неопределенностей Гейзенберга означает, что определенная с высокой точностью энергия движущегося электрона не позволяет с высокой степенью точности определить его координату. Мы можем лишь обозначить область пространства вблизи ядра, где чаще или реже встречается электрон. Поэтому не имеет никакого физического смысла говорить о траектории движения электрона по орбите. Орбиты в модели атома Бора отражают энергетические квантовые переходы, но не реальное движение электронов, как первоначально предполагал Бор. Поэтому можно сказать, что движение электронов в атоме–это «движение без траектории». Электронное облако атома называют не орбитой, а орбиталью. Сам Бор часто вспоминал, как в 1950-х годах к нему после лекции подошел студент и спросил: «Неужели действительно были такие идиоты, которые думали, что электрон вращается по орбите?» [5,
с. 27].
В тот же период Н. Бор сформулировал принцип квантовой механики, принцип дополнительности: получение экспериментальной информации об одних физических величинах, описывающих микрообъекты (элементарную частицу, атом, молекулу), неизбежно связано с потерей информации о некоторых других величинах, дополнительных к первым. Взаимно дополнительными величинами являются координата и импульс микрочастицы (в соотношении неопределенностей Гейзенберга). Состояния, в которых взаимно дополнительные величины имели бы точно определенные значения, принципиально невозможны. Если одна из таких величин точно определена, то значения другой полностью неопределенны.
Бору принадлежит также открытый им важный принцип–принцип соответствия: всякая новая более общая теория, являющаяся развитием классической, не отвергает её полностью, а включает в себя классическую теорию, указывая границы её применения, причем в определенных предельных случаях новая теория переходит в старую.
Классическая механика Ньютона не потеряла своего значения и роли со времени её создания потому, что она точно отражает явления и процессы макромира и не претендует на ту область, которую мы относим к микромиру, где действуют законы и принципы квантовой механики.
3. 2. 3. Д в и ж е н и е э л е к т р о н а в п о л е я д р а. В о л н о в о е у р а в н е н и е Ш р е д и н г е р а
Создание целостной теории квантовой механики связано с работами австрийского физика Э. Шредингера, немецкого физика В. Гейзенберга и английского физика П. Дирака (1902-1984). Движение микрочастицы в различных силовых полях должно учитывать её волновые свойства, если принимать во внимание идею де Бройля об универсальности корпускулярно-волнового дуализма материи. Опираясь на идею де Бройля о волнах материи, Шредингер в 1926 г. предложил уравнение, играющее такую же фундаментальную роль в микропроцессах, какую играют законы Ньютона в классической механике. В том же году он доказал эквивалентность волновой механики и матричной механики, разработанной Гейзенбергом в сотрудничестве с другими учеными. За эти работы в 1933 г. Шредингер вместе с П. Дираком были удостоены Нобелевской премии.
Воспитанный на традициях классической физики, основанной на полном детерминизме, Шредингер не принял квантовую механику как завершающую теорию. Это привело его к дискуссии с другими ведущими физиками того времени, в частности с Бором. «Если мы собираемся сохранить эти проклятые квантовые скачки, то я вообще жалею, что имел дело с атомной теорией»,-говорил Шредингер [13].
Но волновое уравнение Шредингера сделало свое дело. Оно является математическим выражением закона квантовой механики. Созданная Бором квантовая теория атома водорода, основанная на постулатах, обрела опору. В мире микросистем устойчивость объектов определяется волновым уравнением Шредингера. В уравнении фигурирует функция y (пси), квадрат модуля которой определяет положение электрона в данной точке в каждый момент времени. Для стационарных состояний электрона в атоме значения волновой функции соответствуют дискретным значениям энергии Е1 Е2,…Эти значения энергии соответствовали требованию, чтобы в области движения электрона уложилось целое число волн де Бройля.
Трудности перехода от описания состояния атома водорода, простейшей атомной системы, состоящей всего из одного протона и одного электрона, к многоэлектронным атомам были преодолены введением принципа запрета Паули: два электрона в атоме не могут находиться в одном и том же состоянии. Все электроны одинаковы, но в силу их неотличимости исключается вероятность того, что внутри одного атома одинаковые орбитали могут быть заняты одинаковыми электронами. Электроны не должны «мешать» друг другу двигаться по одной и той же орбитали с квантовыми числами n, l, m, подобно тому как не должны мешать друг другу двигаться в сцепленном состоянии две шестеренки. Если одна из них вращается по часовой стрелке, то другая-против часовой стрелки. Спин и есть то свойство, которое отличает электроны. В единицах постоянной Планка h спин электрона равен 1/2 и может иметь два значения: +1/2 и -1/2.
Принцип запрета Паули позволил дать физическое обоснование заполнению атомов электронами и раскрытию физического смысла периодического закона Д.И. Менделеева. Электроны заполняют орбитали атома от низшей, расположенной ближе всего к ядру, к высшим орбиталям. По мере увеличения заряда ядра электронные орбитали под действием электромагнитных сил все больше сжимаются. Поэтому размеры атомов имеют один и тот же порядок 10-10 м, несмотря на рост числа электронов в атоме.
Наиболее типичными для индивидуальных атомов являются следующие свойства:
обмениваться энергией;
обмениваться веществом (отдавать и присоединять электроны);
изменять геометрическую конфигурацию;
вступать в химические связи с другими атомами и молекулами.
Соударение атома с другими микрочастицами (например, атомом, молекулой, электроном, фотоном) сопровождается переходом его в возбужденное состояние. Один из электронов получает дополнительную энергию и переходит на более высокую орбиталь. В соответствии с законом сохранения энергии обратный процесс сопровождается выделением энергии в том же количестве в виде излученного фотона или соударения с микрочастицей. Соударение атома с другими микрочастицами может привести к отрыву или присоединению электрона.
Еи
 Li Li+ + е-
Li Li+ + е-
или
Еи







 + е-
+ е-
Есэ
 F + е- F-
F + е- F-
 или
или
 |
 Есэ
Есэ






 + е-
+ е-
 | |||
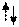 | |||
Рис. 11. Ионизация атомов лития и фтора. (В модели атома фтора изображены только внешние р- орбитали)
Энергия, необходимая для отрыва электрона от электронейтрального атома, называется энергией ионизации (Еи). Энергия, которая затрачивается или выделяется при присоединении электрона, называется сродством к электрону (Есэ).
Переход электронейтральных атомов в ионное состояние сопровождается изменением их размеров. Положительно заряженный ион лития примерно в два раза меньше электронейтрального атома, а отрицательно заряженный ион фтора увеличивает свои размеры примерно в два раза по сравнению с электронейтральным атомом. В последнем случае причиной увеличения размеров является возрастание отталкивания между одноименно заряженными р-орбиталями (рис.11).
– Конец работы –
Эта тема принадлежит разделу:
НИЖЕГОРОДСКИЙ ГОСУДАРСТВЕННЫЙ
НИЖЕГОРОДСКИЙ ГОСУДАРСТВЕННЫЙ... АРХИТЕКТУРНО СТРОИТЕЛЬНЫЙ УНИВЕРСИТЕТ...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Атомный уровень организации вещества
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов