рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Образование
- /
- Выведите формулу константы растворимости.
Реферат Курсовая Конспект
Выведите формулу константы растворимости.
Выведите формулу константы растворимости. - раздел Образование, Основные понятия Константа Равновесия Называется Произведением Растворимости Пр Или Констан...
Константа равновесия называется произведением растворимости ПР или константой растворимости KS. Как любая константа равновесия величина ПР зависит от температуры и не зависит от концентрации.
В общем виде, произведение растворимости для вещества с формулой AmBn, которое диссоциирует на m катионов An+ и n анионов Bm-, рассчитывается по уравнению:

где [An+] и [Bm-] — равновесные молярные концентрации ионов, образующихся при электролитической диссоциации.
Из произведений растворимости можно рассчитать концентрации катионов и анионов в растворе малорастворимого электролита. Значения произведений растворимости приведены в справочниках.
3. Как выражают константу растворимости для идеальных и реальных систем? От чего зависит величина константы растворимости для этих систем?
Константа равновесия для идеальных систем может быть выражена через равновесные парциальные давления компонентов pi по формуле:

где νi — стехиометрический коэффициент (для исходных веществ принимается отрицательным, для продуктов — положительным). Kp не зависит от общего давления, от исходных количеств веществ или от того, какие участники реакции были взяты в качестве исходных, но зависит от температуры .
Константа равновесия для реальных систем
вместо парциального давления и концентрации используют соответственно фугитивность fi и активность ai:
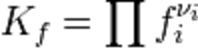

4. Как связаны термодинамическая, реальная и условная константы растворимости?
В системе, состоящей из раствора и осадка, идут два процесса - растворение осадка и осаждение. Равенство скоростей этих двух процессов является условием равновесия.
Насыщенныйраствор - это раствор, который находится в равновесии с осадком.
^Константа растворимости KS (или произведение растворимости ПР) - произведение концентраций ионов в насыщенном растворе малорастворимого электролита - есть величина постоянная и зависит лишь от температуры.
Способы выражения констант равновесия: термодинамическая и концентрационные (реальная, условная) константы.
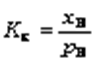
Кs – практическая константа. Такая константа называется константой растворимости
Условная константа - это константа какого-либо равновесия в вполне конкретных "отягчающих" условиях. По сути она может представлять собой, например, произведение реальной константы рассматриваемого равновесия на константу равновесия побочной реакции в случае, если они протекают последовательно. Либо эта зависимость может носить более сложный характер.
5. Как влияет одноименный ион на растворимость осадка?
Уменьшение растворимости. Абсолютно нерастворимых веществ нет. Все вещества растворимы в большей или меньшей степени. Добавление избытка осаждающего реактива при осаждении является одним из способов уменьшения растворимости осадков.
растворимость осадка при добавлении избытка осаждающего реактива уменьшается и зависит от избытка прибавленного иона, общего с одним из ионов, образующих осадок, а также от численного значения произведения растворимости данного малорастворимого электролита.
Аналогичным образом можно доказать, что (если малорастворимое вещество не растворяется с образованием комплексных соединений и не относится к амфотерным соединениям) растворимость малорастворимого электролита также понижается при добавлении не только осаждающего реактива, но и любого другого хорошо растворимого в данной среде электролита, имеющего общие ионы с малорастворимым веществом.
6. Почему при выделении осадка следует избегать большого избытка осадителя?
Иногда, если это необходимо, прибавляют значительно боль-шее (в 2-3 раза) количество осадителя. Однако слишком большой избыток осадителя вреден, т.к. он вызывает не понижение, а наоборот - повышение растворимости осадка. Причиной этого может быть образование растворимых комплексных соединений или кислых солей, амфотерность осаждаемого соединения (гидроксида), «солевой эффект» (вследствие возрастания ионной силы раствора) и т.д.
Необходимый объем осадителя рассчитывают по формуле:
 , (42)
, (42)
где ос.в. - осаждаемое вещество;
р.в. - реактив (реагент).
Этот расчет ориентировочный, поэтому полученное значение объема округляют до одной-двух значащих цифр.
7. Как влияют электролиты на растворимость осадка?
Применение слишком большого количества осадителя в ряде случаев оказывается недопустимым потому, что различные сильные электролиты, присутствующие в растворе, обычно повышают растворимость осадка.
Повышение растворимости осадков в присутствии электролитов называется солевым эффектом.
Это явление объясняется следующим образом.
Как известно из курса качественного анализа, произведение растворимости только в первом приближении можно рассматривать как произведение концентраций ионов в насыщенном растворе. В действительности же постоянным является произведение активностей (а не концентраций) ионов в насыщенном растворе.
Таким образом, активность ионов какого-либо электролита зависит не только от его концентрации в растворе, но и от концентраций и зарядов всех других присутствующих в растворе ионов.
в достаточно разбавленных растворах с одинаковой ионной силой коэффициенты активности большинства ионов, имеющих один и тот же заряд, приблизительно одинаковы.
8. Что называется растворимостью и молярной растворимостью?
РАСТВОРИМОСТЬ, способность в-ва образовывать с др. в-вом (или в-вами) гомог. смеси с дисперсным распределением компонентов. Обычно растворителем считают в-во, к-рое в чистом виде существует в том же агрегатном состоянии, что и образовавшийся р-р. Если до растворения оба в-ва находились в одном и том же агрегатном состоянии, р-рителем считается в-во, присутствующее в смеси в существенно большем кол-ве.
Молярная растворимость вещества (S, моль/л) - это количество растворенного вещества, содержащееся в одном литре его насыщенного раствора
– Конец работы –
Эта тема принадлежит разделу:
Основные понятия
Качественный химический анализ Основные понятия Предмет и средства Чувствительность специфичность селективность... Качественный анализ имеет своей целью обнаружение определенных веществ или их... В настоящее время к а выполняют инструментальными методами спектральными хроматографическими электрохимическими и...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Выведите формулу константы растворимости.
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов