рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Физика
- /
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
Реферат Курсовая Конспект
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ - раздел Физика, Образование молекул из возбужденного состояния атомов Реакции, Протекающие С Изменением Степени Окисления Элементов, Относятся К Ок...
Реакции, протекающие с изменением степени окисления элементов, относятся к окислительно-восстановительным (О В Р ) реакциям.
BaCl2 + Na2SO4 = BaSO4↓ + 2 NaCl - реакция обмена
SnCl2 + FeCl3 → FeCl2 + SnCl4 - ОВР
Sn2+ +2Cl‾ + Fe3+ + 3Cl‾ → Fe2+ + 2Cl‾ + Sn4+ + 4Cl‾
Fe3+ + ē = Fe2+ - процесс восстановления
окислитель
Sn2+ – 2ē = Sn4+ - процесс окисления
восстановитель
Окислитель (грабитель!) – принимает электроны и при этом восстанавливается (процесс восстановления – процесс присоединения электронов),
восстановитель – отдает электроны и при этом окисляется (процесс окисления – процесс отдачи электронов).
Степень окисления восстановителя повышается, а степень окисления окислителя при восстановлении понижается. Процессы восстановления и окисления сопряженные. Количество принятых и отданных ē должно быть одинаково.
Степень окисления и валентность.
Степень окисления - условный заряд атома, который мог бы возникнуть, если бы все связи в молекуле были ионными.
Водород в большинстве соединений (за исключением соединений с металлами) имеет степень окисления +1,
кислород –2 (за исключением соединения с фтором, и пероксидных соединений),
щелочные металлы +1, щелочноземельные +2,
степень окисления элементов в простых веществах равна 0.
Молекулы электронейтральны.
Например:
Na2S+4O3, Na2S+6O4, KMn+7O4, K2Cr+62O7, K2Mn+6O4, Cl20
Степень окисления и валентность могут не совпадать. Наиболее характерно это для органических соединений:
C–4H4 C–2H3OH HC0HO C+4O2 HC+2OOH,
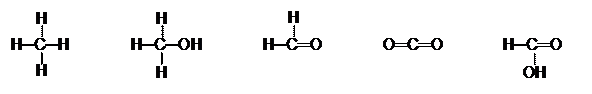 но углерод во всех этих соединениях четырехвалентен
но углерод во всех этих соединениях четырехвалентен
Восстановители. Мерой восстановительной способности является величина ионизационного потенциала.
Восстановителями могут быть:
а) металлы: Ме - nē = Меn+, например
Cu - ē = Cu+; Pb - 2ē = Pb2+.
б) неметаллы и отрицательно заряженные ионы неметаллов (S2‾, Se2‾, Te2‾, I‾, Br‾, Cl‾):
Н2–2ē = 2Н+; 2I‾ –2ē = I2
в) сложные ионы или молекулы, содержащие атомы в промежуточной степени окисления (SO32‾, CrO2‾, AsO33‾, NO2‾ - ионы, SO2, NO, MnO2 - молекулы).
Например, Fe2+ - ē = Fe3+ Pb2+ -2ē = Pb4+ Sn2+ - 2ē =Sn4+
Окислители. Мерой окислительной способности являются величины сродства к электрону и электроотрицательности.
Окислителями могут быть:
а) нейтральные атомы неметаллов:
Cl2 + 2ē =2Cl‾, S + 2ē = S2‾. Самым сильным окислителем является фтор F2
б) Ионы и молекулы, содержащие атомы металлов и неметаллов в высшейи промежуточной степенях окисления:
Pb4+, Sn4+, Cr3+, Fe3+, (ионы благородных металлов Ag+, Au+ )
CrO42‾, Cr2O72‾, MnO4‾, NO3‾, SO42‾, SeO42‾, ClO4‾.
В общем случае:Элементы в низшей степени окисления — только восстановители.
Элементы в высшей степени окисления — только окислители.
Элементы в промежуточной степени окисления — обладают окислительно-восстановительной двойственностью.
– Конец работы –
Эта тема принадлежит разделу:
Образование молекул из возбужденного состояния атомов
На сайте allrefs.net читайте: "Образование молекул из возбужденного состояния атомов"
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов