КОНТРОЛЬНАЯ РАБОТА по Химии
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ
ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
МОСКОВСКИЙ ГОСУДАРСТВЕННЫЙ СТРОИТЕЛЬНЫЙ УНИВЕРСИТЕТ
Кафедра общей химии
КОНТРОЛЬНЫЕ РАБОТЫ ПО ХИМИИ
Для студентов заочного отделения
Составители:
д.х.н., проф. Сидоров В.И., к.т.н., проф. Никифорова Т.П.,
К.х.н., доц. Платонова Е.Е., к.т.н., доц. Доможилова Ю.В.
МОСКВА 2007
Указания к выбору варианта контрольного задания и его оформления: 1. Номер варианта контрольного задания студент получает у преподавателя… 2. При выполнении контрольного задания студент должен:ПРИМЕРЫ РЕШЕНИЯ ЗАДАНИЙ
КОНТРОЛЬНАЯ РАБОТА № 1
1. Завершите уравнения реакций и уравняйте их:
Al2O3 + BaO → Ba(AlO2)2
3K2O + 2H3PO4 → 2K3PO4 + 3H2O
MgCO3 + H2CO3 → Mg(HCO3)2
Дайте структурную формулу сернистой кислоты.
Эмпирическая формула: H2SO3
Структурная формула:
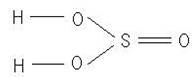
Найти массу серной кислоты, необходимую для полной нейтрализации 20 г гидроксида натрия.
Решение: Уравнение протекающей реакции: H2SO4 + 2NaOH = Na2SO4 + 2H2O Молекулярные массы H2SO4 и NaOH соответственно равны 98 и 40; следовательно, их мольные массы составляют 98 и 40…PCl5(г) Û PCl3 (г) + Cl2 + ΔH
Куда сместится равновесие при: а) повышении температуры; б) повышении давления; в) повышении концентрации Cl2?
Решение: Согласно закону действующих масс скорость прямой и обратной реакции равны: · скорость прямой реакции: v1 = k1×[PCl5] · скорость обратной реакции: v2 = k2×[PCl3]×[Cl2]При синтезе аммиака N2 + 3H2 Û 2NH3 равновесие установилось при следующих концентрациях реагирующих веществ (моль/л): [N2] = 2,5; [H2] = 1,8; [NH3] = 3,6. Рассчитайте исходные концентрации азота и водорода.
Решение: Введем обозначения: [N2] исх., [H2] исх. — исходные концентрации азота и водорода; [N2] равн., [H2] равн. — равновесные концентрации азота и водорода; [N2] изр., [H2] изр. — израсходованные концентрации азота и водорода.
Тогда запишем:
[N2] исх. = [N2] равн. + [N2] изр.
[H2] исх. = [H2] равн. + [H2] изр.
1 моль N2 расходуется на образование 2 моль NH3.
x моль/л N2 расходуется на образование 3,6 моль/л NH3.
x = 1,8 моль/л.
[N2] изр. = 1,8 моль/л.
[N2] исх. = 2,5 + 1,8 = 4,3 моль/л.
3 моль H2 расходуется на образование 2 моль NH3.
x моль/л H2 расходуется на образование 3,6 моль/л NH3.
x = 5,4 моль/л.
[H2] изр. = 5,4 моль/л.
[H2] исх. = 1,8 + 5,4 = 7,2 моль/л.
Исходные концентрации азота и водорода равны 4,3 моль/л и 7,2 моль/л.
Составьте электронную и электронно-графическую формулы элемента Si и иона Mg2+. Определите порядковый номер и название элемента, если структура валентного электронного слоя его атома соответствует формуле: 4f146s2.
Решение: В соответствии с порядком заполнения атомных орбиталей записываем электронную формулу кремния 1s22s22p63s23p2.
Электронно─графическая формула имеет следующий вид:
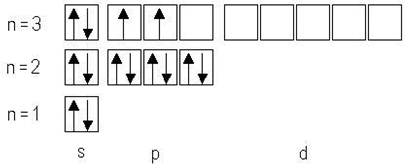
Mg0 ─ 2ē = Mg2+. Удаляются внешние электроны. Электронная конфигурация атома Mg0 — 1s22s22p63s2. Электронная конфигурация иона Mg2+ — 1s22s22p63s0.
Электронно─графическая формула имеет следующий вид:
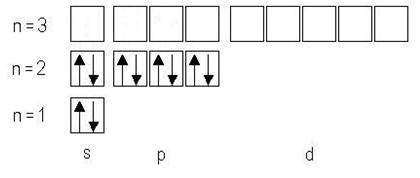
В соответствии с периодической системой элементов Д.И. Менделеева порядковый номер и название элемента со структурой валентного электронного слоя его атома 4f146s2 — № 70 иттербий (Yb).
КОНТРОЛЬНАЯ РАБОТА № 2
В лаборатории имеется раствор с массовой долей серной кислоты 5,5% (плотность 1,035 г/мл). Определите объем этого раствора, который потребуется для приготовления 0,25 М раствора H2SO4 объемом 300 мл.
Решение: Рассчитываем количество вещества серной кислоты (100%─ной), которое потребуется для приготовления 0,25 М раствора H2SO4 объемом 0,3 л:
CM(H2SO4) = n(H2SO4)/V, тогда
n(H2SO4) = CM(H2SO4)×V = 0,25×0,3 = 0,075 моль.
Масса H2SO4 составляет:
m(H2SO4) = n(H2SO4)×M(H2SO4) = 0,075 моль × 98 г/моль = 7,35 г.
Вычисляем массу раствора с массовой долей серной кислоты 5,5%, в котором содержится H2SO4 массой 7,35 г:
ω(H2SO4) = m(H2SO4)/mраствора, тогда
mраствора = m(H2SO4)/ω(H2SO4) = 7,35/0,055 = 133,6 г.
Определяем объем требуемого раствора:
V = m/ρ = 133,6 (г)/1,035 (г/мл) = 129,1 мл.
Написать уравнение в молекулярной, ионной и сокращенной ионной формах: хлорид цинка + гидроксид калия.
Решение:
ZnCl2 + 2KOH → Zn(OH)2↓ + 2KCl
Zn2+ + 2Cl─ + 2K+ + 2OH─ → Zn(OH)2↓ + 2K+ + 2Cl─
Zn2+ + 2OH─ → Zn(OH)2↓
Концентрация ионов водорода в растворе равна 2,5·10─5 моль/л. Вычислите pH раствора.
Решение: pH = ─lg[H+] = ─(2,5·10─5) = 4,6.
Вычислите pH 0,1 н. раствора синильной кислоты HCN, константа диссоциации которой равна 4,9×10─10.
Решение: Концентрация ионов водорода равна: [H+] = α×C(HCN). Степень электролитической диссоциации α можно вычислить, используя… КД = С× α2 Þ α = √(КД/С), где С — концентрация электролита, моль/л.Написать молекулярные и ионные формы уравнений гидролиза, протекающего в растворах солей: NaCN и Cu(NO3)2. Как можно усилить или ослабить их гидролиз?
Решение:
NaCN + HOH Û NaOH + HCN
Na+ + CN─ + HOH Û Na+ + OH─ + HCN
CN─ + HOH Û OH─ + HCN
pH>7
Для того чтобы усилить гидролиз надо повысить температуру, добавить воды или подкислить. Для того чтобы ослабить гидролиз надо понизить температуру, повысить концентрацию соли или подщелачить.
Cu(NO3)2 + HOH Û CuOHNO3 + HNO3
Cu2+ + 2NO3─ + HOH Û CuOH+ + NO3─ + H+ + NO3─
Cu2+ + HOH Û CuOH+ + H+
pH<7
CuOHNO3+ HOH Û Cu(OH)2↓ + HNO3
CuOH+ + NO3─ + HOH Û Cu(OH)2↓ + H+ + NO3─
CuOH+ + HOH Û Cu(OH)2↓ + H+
Для того чтобы усилить гидролиз надо повысить температуру, добавить воды или подщелачить. Для того чтобы ослабить гидролиз надо понизить температуру, повысить концентрацию соли или подкислить.
Дайте два примера солей железа (II), в водных растворах которых pH<7 и pH≈7.
Решение:
В водном растворе FeCl2 pH<7; в водном растворе FeS pH≈7.
КОНТРОЛЬНАЯ РАБОТА №3
В воде содержатся катионы и анионы в следующих концентрациях (мэкв/л): Ca2+ — 2,5; Na+ — 1,8; Mg2+ — 0,7; HCO3─ — 2,9; Cl─ — 1,5; SO42─ — 0,6. Рассчитайте величины общей, временной и постоянной жесткости воды.
Решение: Ионы натрия не обуславливают жесткость воды, тогда по определению жесткости общая жесткость равна:
Жо = [Ca2+] + [Mg2+] = 2,5 + 0,7 = 3,2 ммоль-экв/л.
Карбонатная жесткость — часть общей жесткости, эквивалентная содержанию HCO3─, т.е. Жк = 2,9 ммоль-экв/л.
Постоянную жесткость можно вычислить, зная общую и карбонатную жесткость:
Жп = Жо – Жк = 3,2 – 2,9 = 0,3 ммоль-экв/л.
Для умягчения 300 л воды потребовалось 15 г гашеной извести. Чему была равна временная жесткость воды?
Решение: Формула для расчета жесткости воды:
Ж = (m(Ca(OH)2), г ×1000)/(MЭ(Ca(OH)2)×Vводы, л), где
Мэ(Ca(OH)2) = М(Ca(OH)2)/2 = 74/2 = 37 г/экв, тогда
Ж = (15×1000)/(37×300) = 1,35 ммоль-экв/л.
Приведите формулы двух веществ, в одном из которых азот может быть только восстановителем, а в другом — только окислителем.
Решение: В соединении NH3 азот имеет минимальную степень окисления (─3) и не может ее больше понижать. Он может только отдавать электроны, а… В соединении HNO3 азот имеет максимальную степень окисления (+5) и не может ее…Технический цинк массой 1,32 г обработали избытком раствора разбавленной серной кислоты. Выделившийся водород занял при нормальных условиях объем 448 мл. Определите массовую долю цинка в техническом металле.
Решение: Запишем уравнение реакции:
Zn + H2SO4 (разб.) → ZnSO4 + H2↑
х г Zn расходуется на получение 0,448 л H2
65 г/моль Zn расходуется на получение 22,4 л/моль H2
m(Zn) = x = 65×0,448/22,4 = 1,30 г.
Определим массовую долю цинка:
ω(Zn) = (m(Zn)/mцинк техн.)×100% = 98,5%
КОНТРОЛЬНАЯ РАБОТА №4
Какой металл будет разрушаться при нарушении целостности покрытия оцинкованного железа? Дайте схему протекающих процессов в среде с pH=8.
Решение:
Оцинкованное железо:
Fe│Zn
Т.к. E0Fe2+/Fe = ─0,44 В; E0Zn2+/Zn = ─0,76 В и E0Fe2+/Fe > E0Zn2+/Zn, то
А: (Fe): Zn0 – 2ē → Zn2+
K: (Sn): O2 + 4ē + 2H2O → 4OH─
Приведите схему протекторной защиты. Какие материалы используются в качестве протекторов?
Решение:
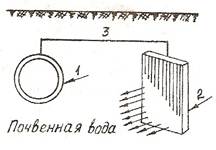
Рис. 1. Схема протекторной защиты:
1 – защищаемая конструкция; 2 – протектор; 3 – проводник
В качестве протекторов используют сплавы на основе магния, алюминия, цинка.
Какое количество строительного гипса можно получить при обжиге 15 кг природного гипса, содержащего 10 % примесей?
Решение: Реакция получения строительного гипса: 120…170 °CВ грунтовых водах содержатся соли магния. Напишите химические реакции, протекающие при контакте бетона с такой водой. Почему при этом происходит разрушение бетона?
Решение:
При действии морской воды на бетон происходят следующие реакции:
Ca(OH)2 + MgCl2 = CaCl2 + Mg(OH)2↓
Ca(OH)2 + MgSO4 = CaSO4·2H2O + Mg(OH)2↓
Mg(OH)2↓ — (рыхлая объемная масса) выпадает в осадок в виде пленки, проницаемой для воды; CaCl2 и CaSO4·2H2O вымываются.
Соли магния могут взаимодействовать с составными частями цементного камня:
2CaO·SiO2·nH2O + MgCl2 + 2H2O = 2CaCl2 + 2Mg(OH)2↓+ SiO2·nH2O
3CaO·Al2O3·6H2O + 3MgCl2 = 3CaCl2 + 3Mg(OH)2↓+ 2Al(OH)3↓
В результате цементный камень превращается в рыхлую массу.