рефераты конспекты курсовые дипломные лекции шпоры
Реферат Курсовая Конспект
- Физика
- /
- Лекции
- /
- КВАНТОВАЯ 3
Спин электрона
Спин электрона - Лекция, раздел Физика, КВАНТОВАЯ 3 Пространственное Квантование Атома Утверждает Дискретность Пр...
Пространственное квантование атома утверждает дискретность проекции магнитного момента атома на направление внешнего магнитного поля
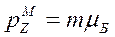 .
.
Продемонстрировать данное явление впервые удалось экспериментально Штерну и Герлахув 1922 г.
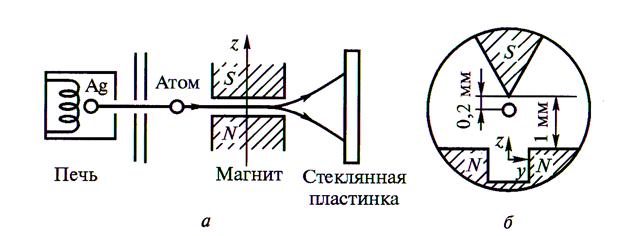
а – схема установки; б – форма межполюсного канала магнита
Узкий атомный пучок пропускают через неоднородное магнитное поле с существенным градиентом магнитной индукции 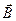 , которая в данном опыте достаточно велика и направлена вдоль оси Z .
, которая в данном опыте достаточно велика и направлена вдоль оси Z .
На пролетающие в зазоре магнита атомы вдоль направления магнитного поля действует сила
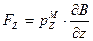 ,
,
обусловленная градиентом индукции неоднородного магнитного поля и зависящая от значения проекции магнитного момента атома на направление поля. Эта сила отклоняет движущийся атом в направлении оси Z , причём за время пролёта магнита движущийся атом отклоняется тем больше, чем больше сила FZ .
С позиций классической физики магнитный момент атомов вещества вследствие их хаотического теплового движения при влёте в магнитное поле может иметь любое направление в пространстве. В результате пролетевшие через магнит атомы серебра должны были образовать сплошную широкую зеркальную полосу на стеклянной пластинке.
В эксперименте была получена серия узких дискретных зеркальных полосок из напылённых атомов, что объясняется квантовой теорией о наличии пространственного квантования магнитных моментов атома.
Однако в этом же эксперименте был получен и результат, находящийся в противоречии с квантовой теорией.
Из квантовой теории следует, что вследствие симметрии электронного облака механический и магнитный моменты атома, находящегося в основном состоянии, равны нулю и для таких атомов на стеклянной подложке в опыте Штерна-Герлаха должна быть в центе одна узкая полоска. На самом деле поток расщепился на два пучка, которые напылили две узкие полоски, сдвинутые симметрично вверх и вниз. Измерение этих сдвигов позволило определить магнитный момент невозбуждённого атома серебра. Его проекция на ось Z оказалась равной +μБ и - μБ .
Противоречие с квантовой теорией наблюдалось и при изучении тонкой структуры оптических спектров щелочных металлов. Линии оказались двойными. Расщепление спектральных линий очевидно связано с расщиплением самих энергетических уровней, что никак не следует из решения уравнения Шрёдингера.
В экспериментах с ферромагнетиками было обнаружено аномальное значение гиромагнитного отношения, отличающееся от ожидаемого значения в два раза.
В 1925 г. Гаудсмит и Уленбек выдвинули гипотезу о наличии у электрона собственного магнитного момента, названного спином ( от англ. spin – кружение, верчение ).
Первоначально предполагалось, что спин обусловлен вращением электрона вокруг своей оси, подобно вращению Земли вокруг земной оси при движении по околосолнечной орбите.
Однако такая модель вращающегося заряженного шарика оказалась несостоятельной. Расчёт показал, что ни при каких допустимых скоростях меньших скорости света нельзя вращением электрона индуцировать магнитный момент, равный по величине магнетону Бора. Гиромагнитное отношение для вращающегося электрона оказалось в 2 раза меньше, чем то , что было получено в опытах.
Спин электрона не имеет классического аналога. Он характеризует внутреннее свойство квантовой частицы, связанное с наличием у неё дополнительной степени свободы. Это количественная характеристика и для электрона она равна s = ½ ( такая же важная как масса теи заряд -е ).
Спином обладают и некоторые другие частицы. У протона и нейтрона s = ½ , а у фотона s = 1.
11 - 3
По аналогии с орбитальными моментами можно определить значения собственных механического и магнитного моментов электрона
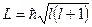
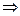
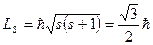
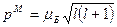
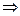
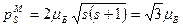
Гиромагнитное соотношение
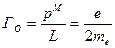
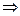
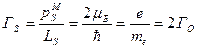
Проекции собственных моментов на выделенное направление Z определяется спиновым квантовым числом mS = 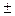 s =
s = 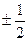 .
.
При этом
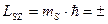
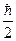
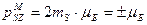
Из полученных соотношений следует, что значение спинового момента электрона постоянно, а с дополнительной степенью свободы электрона связана z-проекция этого момента, которая определяется спиновым квантовым числом mS и принимает два значения. О таких двух квантовых состояниях обычно говорят как о состояниях со спином, направленным вверх ( mS = + 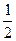 ) или вниз ( mS =
) или вниз ( mS = 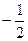 ) . Поэтому, определяя квантовое состояние электрона в любой системе, следует указать также и ориентацию спина.
) . Поэтому, определяя квантовое состояние электрона в любой системе, следует указать также и ориентацию спина.
Таким образом квантовое состояние электрона в атоме следует определять набором из четырёх квантовых чисел

– Конец работы –
Эта тема принадлежит разделу:
КВАНТОВАЯ 3
Лекция Ядерная модель атома частиц на атомах металлической фольги обосновал... Лекция Волновые функции и квантовые... Энергетический спектр электрона в атоме водорода...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Спин электрона
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов