рефераты конспекты курсовые дипломные лекции шпоры
Реферат Курсовая Конспект
- Физика
- /
- Лекции
- /
- КВАНТОВАЯ 3
Квантовая теория атома
Квантовая теория атома - Лекция, раздел Физика, КВАНТОВАЯ 3 Хотя Теория Бора Даёт Хорошие Результаты Для Водородоподобных...
Хотя теория Бора даёт хорошие результаты для водородоподобных атомов, она не может рассматриваться как законченная теория атомных явлений.
С позиций современной физики атом является физической системой, которая заведомо не может быть описана классической теорией, не учитывающей волновых свойств движущегося в атоме электрона, так как длина волны де Бройля такого электрона сравнима с размерами атома.
Потенциальная энергия взаимодействия электрона с ядром водородо- подобного атома
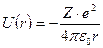 , где
, где
r – расстояние между электроном и ядром, которое в первом приближении
 будем считать точечным.
будем считать точечным.
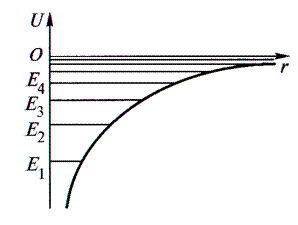
Движение электрона в таком поле можно рассматривать как движение в некоторой сферической потенциальной яме.
Спектр энергий электрона должен быть дискретным, т.е. состоять из отдельных энергетических уровней со
значениями полной энергии электрона Е1; Е2; Е3 и т.д.
Уравнение Шрёдингера 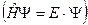 имеет вид
имеет вид
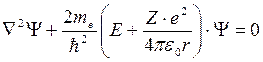
Решение этого уравнения проводят в сферической системе координат r, θ, φ , центр которой совпадает с центром ядра атома. В такой системе
Ψ = Ψ(r, θ, φ) , а оператор Лапласа
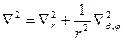 , где
, где 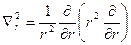 ,
, 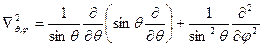
Используя оператор квадрата момента импульса в сферической системе координат
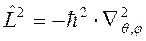
уравнение Шрёдингера преобразуют к виду
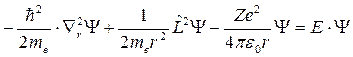
Решение этого уравнения ищут в виде произведения двух функций с разделяющимися переменными
Ψ = X( r ) . Y( θ, φ ).
C учётом естественных требований, налагаемых на Ψ-функцию она должна быть однозначной, конечной, непрерывной и гладкой.
В процессе решения обнаруживается, что этим требованиям можно удовлетворить при любыхположительных значениях энергии Е , но вобласти отрицательных значений Е – только при дискретных значениях, а именно, если
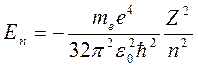 , где п = 1; 2; 3; … ,
, где п = 1; 2; 3; … ,
что соответствует связанным состояниям электрона в атоме.
Таким образом решение уравнения Шрёдингера приводит в случае Е< 0 к тому же результату, что и теория Нильса Бора но без использования каких либо дополнительных постулатов.
Основное различие заключается в интерпретации состояний электрона: в теории Бора – это движение по стационарным круговым орбитам, а в решении уравнения Шрёдингера орбиты теряют физический смысл – их место занимают Ψ-функции.
– Конец работы –
Эта тема принадлежит разделу:
КВАНТОВАЯ 3
Лекция Ядерная модель атома частиц на атомах металлической фольги обосновал... Лекция Волновые функции и квантовые... Энергетический спектр электрона в атоме водорода...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Квантовая теория атома
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов