Гидролиз солей - раздел Химия, Денисова С.А Химический анализ
Растворение Вещества В Воде Часто Сопровождается Химическим В...
Растворение вещества в воде часто сопровождается химическим взаимодействием. Взаимодействие вещества с водой, протекающее с образованием малодиссоциированного соединения, называется гидролизом. Поскольку при этом ионы соли взаимодействуют с ионами Н+ или ОН- воды, гидролиз сопровождается изменением рН раствора. Это происходит, когда равновесие диссоциации воды смещается в результате получения малодиссоциирующих электролитов или ионов. Гидролизу подвержены соединения различных классов, мы будем рассматривать гидролиз солей. Все соли можно разделить на четыре типа:
1) соли, образованные катионом сильного основания и сильной кислоты (NaCl, K2SO4, Ca(NO3)2 и др.);
2) соли, образованные катионом сильного основания и слабой кислоты (Na2CO3, K2S, CH3COONa и др.);
3) соли, образованные катионом слабого основания и сильной кислоты (NH4Cl, CuSO4, ZnCl2 и др.);
4) соли, образованные катионом слабого основания и слабой кислоты ((NH4)2S, Mg(CN)2, CH3COONH4 и др.).
Соли, образованные сильной кислотой и сильным основанием, гидролизу не подвергаются, реакция нейтрализации в этом случае сводится к процессу нейтрализации: Н+ + ОН - = Н2О, а обратная реакция – диссоциация воды на ионы протекает в ничтожно малой степени. В реакции гидролиза вступают соли второго, третьего и четвертого типов.
Рассмотрим гидролиз соли, образованной сильным основанием и слабой кислотой, например, ацетата натрия. Этот процесс можно представить в виде химического уравнения в молекулярной форме:
CH3COONa + H2O D CH3COOH + NaOH
или в ионно-молекулярной форме:
CH3COO - + H2O D CH3COOH + OH-.
Уравнение показывает, что в данном случае гидролизу подвергается анион соли и что реакция сопровождается образованием ионов гидроксила. Так как ионное произведение воды [H+] [OH-] величина постоянная, то при накоплении ионов ОН- концентрация ионов водорода уменьшается. Следовательно, растворы солей, образованных слабой кислотой и сильным основанием, имеют щелочную реакцию.
В случае соли, образованной слабым основанием и сильной кислотой, гидролизу подвергается катион соли и реакция сопровождается образованием ионов Н+, например:
NH4Cl + H2O D NH4OH + HCl
или
NH4+ + H2O D NH4OH + H+.
Накопление ионов Н+ приводит к уменьшению концентрации ионов ОН-, поэтому растворы солей, образованных сильной кислотой и слабым основанием, имеют кислую реакцию среды.
Гидролизу подвергается не все количество находящейся в растворе соли, а только часть его. При этом в растворе устанавливается равновесие между солью и образующими его кислотой и основанием. Доля вещества, подвергающаяся гидролизу, т.е. степень гидролиза, зависит от константы этого равновесия, а также от температуры и от концентрации соли.
Запишем уравнение гидролиза в общем виде, обозначая символом МеА кислоту, а МеОН – основание:
МеА + Н2О D НА + МеОН.
Этому равновесию соответствует константа:
 .
.
Концентрация воды в разбавленных растворах представляет собой постоянную величину. Обозначая К [H2O] = Kг, получим:
 .
.
Величина Кг называется константой гидролиза. Ее значение характеризует способность данной соли подвергаться гидролизу. Чем выше Кг, тем в большей степени (при одинаковых температуре и концентрации соли) протекает гидролиз.
Для солей, образованных сильным основанием и слабой кислотой, Кг связана с константой диссоциации кислоты Ка зависимостью:
 .
.
Это уравнение показывает, что константа гидролиза Кг тем больше, чем меньше Ка. Иными словами, чем слабее кислота, тем в большей степени подвергаются гидролизу ее соли.
Для солей, образованных слабым основанием и сильной кислотой, аналогичное соотношение связывает константу гидролиза с константой диссоциации основания Кв:
 .
.
Поэтому, чем слабее основание, тем в большей степени подвергаются гидролизу образованные им соли.
Для солей, образованных слабой кислотой и слабым основанием, константа гидролиза связана с константами диссоциации кислоты и основания следующим соотношением:
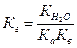 .
.
Степень гидролиза определяется природой соли, ее концентрацией и температурой. Природа соли проявляется в величине константы гидролиза. С разбавлением раствора и с увеличением температуры степень гидролиза увеличивается. Особенно глубоко протекает гидролиз солей, образованных слабой кислотой и слабым основанием. Реакция растворов солей в этом случае зависит от соотношения констант диссоциации кислоты и основания, образующих соль. Если константа диссоциации кислоты больше константы диссоциации основания, то раствор имеет слабокислую реакцию, при обратном соотношении констант диссоциации – слабощелочную.
Гидролиз солей многоосновных кислот или многокислотных оснований происходит по ступеням. Так, первая ступень гидролиза карбоната натрия протекает согласно уравнению:
Na2CO3 + H2O D NaHCO3 + NaOH
Или в ионно-молекулярной форме:
CO32- + H2O D HCO32- + OH-.
Образовавшаяся кислая соль в свою очередь подвергается гидролизу по второй ступени:
NaHCO3 + H2O D H2CO3 + NaOH
или
HCO3- + H2O D H2CO3 + OH-.
Как видно, при гидролизе по первой ступени образуется ион НСО3-, диссоциация которого характеризуется второй константой диссоциации угольной кислоты, а при гидролизе по второй ступени образуется угольная кислота, диссоциацию которой характеризует первая константа ее диссоциации. Поэтому константа гидролиза по первой ступени Кг,1 связана со второй константой диссоциации кислоты, а константа гидролиза по второй ступени Кг,2 – с первой константой диссоциации кислоты:


Так как первая константа диссоциации кислоты всегда больше второй, то константа гидролиза по первой ступени всегда больше, чем по второй.
Аналогично проходит гидролиз солей, образованных слабым основанием многовалентного металла. Например, гидролиз хлорида магния протекает по первой ступени с образованием хлорида гидроксомагния:
MgCl + H2O D MgOHCl + HCl.
Или в ионно-молекулярной форме:
Mg2+ + H2O D MgOH+ +H+.
Гидролиз по второй ступени происходит в ничтожно малой степени:
MgOHCl + H2O D Mg(OH)2 + HCl
MgOH+ + H2O D Mg(OH)2 + H+.
В аналитической практике гидролиз солей во многих случаях мешает выполнению аналитических реакций и его приходится подавлять. Например, при осаждении катионов Са2+, Sr2+ и Ва2+ карбонатом аммония (NH4)2СО3 прибавляют NH4OH для подавления гидролиза этого реагента:
(NH4)2СO3 + H2O D NH4HCO3 + NH4OH.
Соли, образованные некоторыми катионами и слабыми кислотами (например, H2S, H2СO3 и др.) гидролизуются в такой степени, что практически в водных растворах не существуют. Например, хотя большинство катионов осаждается сульфидом аммония (NH4)2S в виде сульфидов, ионы Cr3+ и Al3+ осаждаются в виде гидроксидов Cr(OH)3 и Al(OH)3. Это происходит потому, что концентрация гидроксид-ионов, образующихся при гидролизе (NH4)2S, достаточна, чтобы произведения растворимости Cr(OH)3 и Al(OH)3 были превышены и гидроксиды выпали в осадок. У других катионов этого не наблюдается, так как их гидроксиды более растворимы, чем сульфиды.
Если введение в раствор продуктов, образующихся при гидролизе, подавляет гидролиз, то связывание одного из продуктов в результате какой-нибудь реакции, наоборот, усиливает гидролиз.
Иногда ионы Al3+ и Fe3+ удаляют из раствора действием ацетата натрия CH3COONa. При этом в осадок выпадают не средние, а основные соли, также образующиеся в результате гидролиза:
Fe(CH3COO)3 + H2O D Fe(OH)(CH3COO)2 + CH3COOH
Fe(OH)(CH3COO)2 + H2O D Fe(OH)2(CH3COO) + CH3COOH.
Таким образом, не всегда гидролиз солей препятствует выполнению аналитических операций. Нередко его используют для обнаружения или отделения ионов.
Все темы данного раздела:
Денисова С.А.
Д33 Химия (аналитическая): учеб.-метод. пособие для студентов геолог. ф-та / С.А. Денисова, Л.И. Торопов; Перм. ун-т. – Пермь, 2011. – 122 с.
ISBN 5-7944
Краткий очерк о развитии аналитической химии
Аналитическая химия прошла большой исторический путь. Можно выделить следующие периоды: наука древних; алхимия (IV-XVI вв.), ятрохимия (XVI-XVII вв.), эпоха флогистона (XVII-XVIII в
Химическое равновесие в гомогенной системе. Закон действия масс.
Закон действия масс открыли в 1884 г. норвежские ученые К. Гульдберг и П. Вааге. Этот фундаментальный закон химии является теоретической основой многих методов анализа. Он устанавли
Протолитическая теория кислот и оснований
В 1923 г. Бренстед и Лоури предложили теорию кислот и оснований, получившую название протолитической. Теория основана на особенностях иона водорода. Протон лишен электронной
Степень электролитической диссоциации
Большинство реакций, используемых в аналитической химии, проводится в растворах. Из курса общей химии известно, что многие химические вещества (соли, основания, кислоты) при раствор
Константа диссоциации слабого электролита
Процесс диссоциации молекул электролита является обратимым. В растворе устанавливается равновесие между ионами и недиссоциированными молекулами, поэтому можно использовать закон дей
Коэффициент активности и ионная сила
Для сильных электролитов констант диссоциации не существует, т.к. в растворах они обычно диссоциированы полностью. По этой причине число ионов в них больше, чем в растворах слабых э
Под активностью иона понимают ту эффективную, условную концентрацию его, соответственно которой он действует при химических реакциях.
Между активностью иона a и его действительной концентрацией ссуществует линейная зависимость:
а = f ∙ с,
где f
Диссоциация воды. Водородный и гидроксильный показатели.
Реакции, применяемые в аналитической химии, протекают чаще всего в водных растворах. Вода является слабым электролитом, способным проводить электрический ток. Процесс диссоциации во
Действие одноименных ионов. Буферные растворы.
Степень электролитической диссоциации вещества зависит не только от его концентрации в растворе, но и от присутствия в растворе других электролитов. Степень диссоциации слабого электролита понижает
Произведение растворимости. Произведение активностей ионов
Химические взаимодействия, происходящие в растворах, могут сопровождаться образованием осадков, например:
AgNO3 + HCl D AgCl↓ + HNO3
На
Вопросы для самопроверки
1. В чем заключаются практические задачи аналитической химии? Какова роль аналитической химии в науке и производстве?
2. Назовите наиболее распространенные классификации ме
Особенности аналитических реакций и способы их выполнения
Задача качественного неорганического анализа обычно сводится к обнаружению катионов и анионов, присутствующих в анализируемой пробе. При обнаружении какого-либо компонента обычно фиксируют появлени
Лабораторное оборудование и техника выполнения качественного анализа
При выполнении в практикуме работ по качественному анализу студент использует следующую посуду и оборудование.
1) Пробирки цилиндрические – для выполнения реакций с
Техника выполнения реакций
Реакции, выполняемые в пробирке. Исследуемый раствор (2-3 капли) вносят в пробирку капиллярной пипеткой так, чтобы кончик пипетки не коснулся стенок пробирки. Соблюдая условия пров
Методика выполнения основных операций в полумикроанализе
Нагреваниеи выпаривание.При проведении многих реакций требуется нагревание. Нагревать растворы в пробирках на открытом пламени горелки нельзя. Поэт
Реакции обнаружения катионов
Аналитическая классификация катионов связана с их разделением на аналитические группы при последовательном действии групповыми реагентами. В настоящем пособии рассматривается кислотно-щелочная схем
Первая группа катионов
К I аналитической группе относятся катионы Ag+, Hg22+, Рb2+., соли которых почти все плохо растворимы в воде. Хорошо растворимы лишь нитраты, а также аце
Реакция с хлороводородной кислотой и ее солями.
Хлорид–ионы осаждают из водных растворов солей серебра белый осадок хлорида серебра, нерастворимый в азотной и серной кислотах:
AgNO3 + НCl = AgCl↓ + NaNO3
Реакция с гидроксидами щелочных металлов и аммиаком.
КОН и NaOH выделяют из растворов солей серебра не гидроксид AgOH, который неустойчив, а бурый осадок оксида серебра Ag2O, растворяющийся в NH4OH с образованием аммиачного комп
Реакция с KI.
Иодид калия образует желто-зеленый осадок AgI, нерастворимый в аммиаке, кислотах, но способный растворяться в избытке реагента и тиосульфате натрия Na2S2O3, так как
Вторая группа катионов
Ко II аналитической группе относятся катионы Ca2+, Ba2+, Sr2+. Основные свойства этих металлов выражены сильно, поэтому соли, образованные сильными кислотами, в вод
Реакции ионов кальция
1. Оксалат аммония образует с ионами кальция белый кристаллический осадок СаС2О4∙Н2О:
CaCl2 + (NH4)
Реакции с серной кислотой и ее солями.
При взаимодействии разбавленной серной кислоты или ее растворимых солей с солями бария выпадает белый кристаллический осадок сульфата бария.
BaCl2 + H2SO4
Третья группа катионов
К III аналитической группе относятся катионы Аl3+, Zn2+, Cr3+ , Sn(II), Sn(IV), As(III), As(V). Характерной особенностью катионов III группы является способность их
Реакции ионов хрома (III)
1. Гидроксиды щелочных металлов осаждают Cr(OH)3 серо-зеленого цвета, растворимый в избытке реактива вследствие своих амфотерных свойств.
CrCl3 + 3Na
Окисление хрома(III) в кислой среде.
Окисление Cr3+ перманганатом калия в кислой среде протекает по уравнению:
Cr2(SO4)3 + 2KMnO4 + 5Н2О = К
Четвертая группа катионов
К четвертой аналитической группе относятся катионы Mg2+, Mn2+, Fe2+, Fe3+. Гидроксиды катионов IV группы нерастворимы в избытке щелочей и растворе аммиак
Реакции ионов магния
1. Гидрофосфат натрияобразует с ионами магния в присутствии NH3 при рН 9 белый кристаллический осадок MgNH4PO4∙6Н2
Капельная реакция Тананаева.
Выполнение определения. На полоску фильтровальной бумаги наносят каплю исследуемого раствора, 1 каплю фенолфталеина, 1 каплю раствора аммиака. Бумага окрасится в малиновый цвет. Бумаг
Реакции ионов железа(II)
1. Гексацианоферрат (III) калия (красная кровяная соль) образует с ионами железа (II) синий осадок, называемый "турнбулевой синью":
3FeCl2
Реакции ионов железа(III)
1. Гексацианоферрат (II) калия (желтая кровяная соль) образует с ионами железа (III) темно-синий осадок "берлинской лазури":
4FeCl3 + 3K4[F
Пятая группа катионов
К пятой аналитической группе относятся катионы: Cu2+, Cd2+, Co2+, Ni2+, Hg2+. Их гидроксиды растворимы в избытке раствора аммиака с образовани
Реакции ионов меди
1. Реакция с NH3∙H2O.Раствор аммиака при медленном добавлении к раствору соли меди(II) сначала осаждает основную соль меди зеленовато-голубоватого цвета
Шестая группа катионов
К VI аналитической группе катионов относятся NH4+, Na+ и K+. Соли, образованные катионами натрия и калия и анионами сильных минеральных кислот, хорошо ра
Реакции ионов калия
1. Гексанитрокобальтат (III) натрияв слабокислой среде (pH 4–6) выделяет из растворов солей калия кристаллический желтый осадок:
2КCl + Na3[Co(NO2)
Реакции ионов натрия
1.Реакция с дигидростильбатом калия KH2SbO4:
NaСl + KН2SbО4- = NaH2SbO4↓
Реакции ионов аммония
1. Гидроксид калия (натрия).Реакция со щелочами – одна из немногих специфических реакций в аналитической химии, позволяющая "открыть" катион аммония непосредственно из ан
Особенности анализа катионов VI группы
При проведении анализа необходимо учитывать следующие обстоятельства:
а) присутствие катиона аммония мешает обнаружению калия и натрия при использовании KH2S
Реакции карбонат-ионов
Карбонат-ион является анионом слабой двухосновной угольной кислоты H2CО3 (К1 = 3,5∙10–7, К2 = 5,73∙10–11)
Реакции сульфат-ионов
Большинство сульфатов и гидросульфатов хорошо растворимо в воде, причем гидросульфаты растворимы лучше сульфатов. Малорастворимы сульфаты свинца, бария, стронция, кальция, серебра и ртути (I).
Реакции фосфат-ионов
Фосфат-ион является анионом ортофосфорной кислоты H3РO4, которая относится к кислотам средней силы. Как трехосновная кислота она дает три типа солей: фосфаты –
Реакции хлорид-ионов
Хлорид-ион является анионом сильной хлороводородной кислоты НС1. Большинство хлоридов растворимо в воде. Малорастворимы AgCl, Hg2Cl2, PbCl2, Cu
Реакции нитрат-ионов
Нитрат-ион является анионом сильной азотной кислоты. НNО3 является сильным окислителем. Все соли азотной кислоты растворимы в воде за исключением основных солей висмута, ртути и солей не
Работа 1
Дробное определение катионов:
a) K+, NH4+, Ca2+, Ba2+
b) K+, NH4
Работа 2
Дробное определение катионов Fe2+, Fe3+, Cr3+, Cu2+ и анионов SO42-, CO32-, PO43-
Измерение аналитического сигнала
Первые этапы количественного химического анализа – это отбор и подготовка пробы к анализу. После этих двух стадий наступает стадия, на которой определяют концентраци
Погрешность методов анализа
Содержание той или иной составной части анализируемого вещества не определяют одним измерением, а находят в результате ряда операций и измерений. Между тем выполнение их может быть
Обработка результатов методом математической статистики
Цель всех аналитических исследований – нахождение результата, наиболее близкого к истинному содержанию в пробе.
Общую погрешность метода можно оценить только с привлечением методов математ
Представление экспериментальных данных
xi
n
V (s
или sr
Гравиметрические методы анализа
Гравиметрическим анализом называется метод количественного анализа, основанный на точном измерении массы определяемого компонента пробы, выделенного либо в элементарном виде, либо в виде со
Требования к осаждаемой форме
1. Осаждаемое соединение должно обладать как можно меньшей растворимостью в воде. После осаждения в исследуемом объеме раствора должно оставаться только такое количество данного соединения, которое
Требования к весовой форме
1. Точное соответствие состава определенной химической формуле, иначе невозможно провести вычисление результатов анализа.
2. Достаточная химическая устойчивость. Гравиметрическая форма не
Требования к осадителю
1. Осадитель должен быть летучим соединением. Если примеси не будут полностью удалены при промывании осадка, то они улетучатся при последующем прокаливании. Например, для осаждения Ва2+
Расчет количества осадителя
Согласно правилу произведения растворимости образование осадков происходит лишь при условии, если произведение концентраций соответствующих ионов превысит величину ПР осаждаемого соединения при дан
Образование осадков и их свойства
Осаждение считают важнейшей операцией гравиметрического анализа. При выполнении ее необходимо правильно выбрать осадитель, рассчитать его объем, соблюсти определенные условия осаждения, убедиться в
Условия осаждения кристаллических и аморфных осадков
Условия осаждения
Достигаемый эффект
К р и с т а л л и ч е с к и е о с а д к и
Осаждение ведут из достаточно разбавленног
Фильтрование
Фильтрованием отделяют полученный осадок от раствора, содержащего посторонние примеси. Тщательность выполнения этой операции сказывается на точности определений.
В гравиметрическом анализе
Вычисления в гравиметрическом анализе
Результаты гравиметрических определений чаще всего выражают в абсолютных величинах или в процентах к навеске вещества. Например, если в силикате определяют содержание SiO2, то для вычисл
Вопросы и задачи для самостоятельной подготовки
1. На чем основан гравиметрический метод анализа?
2. Каким требованиям должны удовлетворять осадки в гравиметрическом анализе?
3. Перечислите условия осаждения кристаллических и а
Титриметрический анализ
Этот метод основан на точном измерении объема раствора реактива, затраченного на реакцию с определяемым компонентом. Поэтому ранее этот метод анализа назывался объемным. Измерение проводят с помощь
Способы выражения концентрации растворов
В технологии выполнения химических анализов необходимым этапом является приготовление растворов химических веществ. В химическом анализе используются различные растворенные вещества (реагенты, буфе
Техника работы
Мерные колб
Растворы, применяемые в титриметрии
В титриметрии применяют растворы реагентов с точно известной концентрацией. Эти растворы называются стандартными (или титрованными). Различают первичные и вторичные стандартные растворы. Первичн
Расчеты в титриметрических методах анализа
В основе всех количественных расчетов результатов анализа лежит закон эквивалентов, в соответствии с которым вещества реагируют между собой в строго определенных эквивале
Коэффициент поправки
В некоторых случаях не стремятся получить раствор точно требуемой концентрации (навеску вещества не берут точно теоретически рассчитанной), а вводят понятие поправочный к
Метод кислотно-основного титрования
Метод кислотно-основного титрования основан на протолитической реакции:
Работа 1. Стандартизация раствора хлороводородной кислоты по тетраборату натрия
Бура удовлетворяет всем требованиям, предъявляемым к первичным стандартам - устойчива в широком интервале влажности воздуха, имеет большую массу эквивалента, точно соответствует сво
Работа 2. Определение устранимой жесткости (щелочности) воды
Устранимая или карбонатная жесткость воды обусловлена присутствием в растворе гидрокарбонатов кальция Ca(HCO3)2 и магния Mg(HCO3)2. Нали
Работа 3. Определение содержания гидроксида натрия
Реагенты:
1. Хлороводородная кислота, НСl, 0,1 М раствор.
2. Индикатор метиловый оранжевый, 0,1%-ный водный раствор.
Выполнен
Работа 4. Определение содержания хлороводородной кислоты
Реагенты:
1. Гидроксид натрия, NaOH, 0,1 М раствор.
2. Индикатор метиловый оранжевый, 0,1%-ный водный раствор.
Выполнение раб
Вопросы для самостоятельной подготовки
1. Какие способы выражения концентраций вам известны? Что такое эквивалент, фактор эквивалентности, молярная масса эквивалента?
2. Что такое титрование? Дайте определение п
Комплексонометрическое титрование
Комплексонометрическое титрование основано на реакциях, при которых определяемые ионы металлов образуют комплексы с органическими соединениями – комплексонами (производными аминополикарбоновых кисл
Работа 5. Определение общей жесткости воды
Общая жесткость воды (Жобщ) преимущественно обусловлена наличием в ней суммарных концентраций катионов Са2+ (кальциевая ЖCa) и Mg
Работа 6. Определение кальциевой и магниевой жесткости воды
Раздельное определение Са2+ и Mg2+ в воде основано на хорошей растворимости Ca(OH)2 и малой - Mg(OH)2, а также возможностью комплексономе
Работа 7. Определение содержания меди
Ионы меди образуют с ЭДТА комплексы голубого цвета. Условия прямого титрования определяются выбранным металлоиндикатором. В присутствии мурексида, образующего комплекс с медью зелен
Работа 8. Определение содержания железа (III)
Реагенты:
1. Стандартный раствор ЭДТА, с(ЭДТА) = 0,025 М.
2. Индикатор сульфосалициловая кислота, 25%-ный водный раствор.
Вы
Вопросы для самостоятельной подготовки
1. Изложить сущность метода комплексонометрии.
2. Чему равен фактор эквивалентности ЭДТА?
3. Объяснить особенности прямого, обратного, вытеснительного и косвенного
Окислительно-восстановительное титрование
Титриметрические методы, в которых в качестве титрантов используют растворы окислителей или восстановителей, называют окислительно-восстановительными методами титрования.
В зависимости от
Перманганатометрия
В сильнокислой среде перманганат-ионы обладают высоким окислительно-восстановительным потенциалом, восстанавливаясь до Mn(II). Поэтому КMnO4 применяют для определения многих восстановите
Работа 9. Определение содержания железа (II)
В основе определения лежит реакция:
10FeSO4 + 2KMnO4 + 8H2SO4 = 5Fe2(SO4)3 + 2MnSO4
Вопросы для самостоятельной подготовки
1. Каким требованиям должны удовлетворять реакции окисления-восста-новления, чтобы их можно было использовать для количественного анализа?
2. Назовите особенности окислител
Физико-химические методы анализа
Химические методы анализа не всегда удовлетворяют современным требованиям, особенно при проверке чистоты веществ. Получить абсолютно чистое вещество практически невозможно, так как в нем тотчас про
Спектроскопические методы анализа
Эти методы основаны на способности атомов и молекул вещества испускать, поглощать или рассеивать электромагнитное излучение.
По типу оптических явлений различают спектроскопию испускания,
Электрохимические методы анализа
Эти методы основаны на измерении электрохимических свойств анализируемых образцов (электропроводности, электрического потенциала, величины силы тока). Достоинствами электрохимически
Методы хроматографического анализа
Эти методы основаны на различиях в адсорбируемости веществ, константах ионного обмена, растворимости осадков и т.д. Хроматография – это метод разделения многокомпонентных смесей
Важнейшие физико-химические методы анализа
Метод
Характеристика метода
Аналитический сигнал (измеряемый параметр)
Атомно-эмиссионный спектральный анализ (АЭС)
Мет
Вопросы для самостоятельной подготовки
1. Назовите преимущества физико-химических методов анализа над химическими и их недостатки.
2. Перечислите физические свойства веществ, которые используются в физико-химических методах ана
Титриметрические методы анализа
Пример 1. На титрование 10,00 мл раствора КОН затрачено 15,50 мл 0,1028 М раствора HCl . Вычислить молярную концентрацию раствора КОН.
Решение.
Задачи для самостоятельного решения
1) На титрование навески технической соды массой 0,2005г израсходовано 20,00 мл 0,1010 М раствора HCl. Вычислить массовую долю Na2CO3 в анализируемом образце технической соды.
Геологического факультета
(По рекомендациям Совета по химии УМО университета РФ)
Программа составлена в соответствии с требованиями ГОС ВПО по специальности и направлению «Геология» и «Гидрогеология
Тема 2. Качественный анализ
Основные принципы качественного анализа. Аналитический сигнал. Аналитические химические реакции. Специфические и избирательные (селективные) реакции и реагенты. Аналитические реагенты, их маркировк
Тема 3. Количественный анализ
Методы количественного анализа: химические (гравиметрические и титриметрические) и физико-химические. Выражение результатов анализа. Измерение аналитического сигнала.
Титриметрический анал
Дополнительная.
1. Васильев В.П., Кочергина Л.А., Орлова Т.Д. Аналитическая химия. Сборник вопросов и задач. ДРОФА, 2005. 320 с.
2. Дорохова Е.Н., Прохорова Г.В. Задачи и вопросы по аналитической химии. М
ГЕОЛОГИЧЕСКОГО ФАКУЛЬТЕТА
Редактор Н.И.
Корректор А.В.
Компьютерная верстка С.А. Денисова
Подписано в печать
 .
. .
. .
. .
.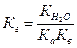 .
.








Новости и инфо для студентов