рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- Электролиз
Реферат Курсовая Конспект
Электролиз
Электролиз - раздел Химия, Основные понятия в химии Электролизом Называется Совокупность Процессов, Протекающих При Прохож...
Электролизом называется совокупность процессов, протекающих при прохождении постоянного электрического тока через систему, состоящую из двух электродов и расплава или раствора электролита.
На электродах происходит разряд ионов и превращение их в нейтральные атомы или молекулы. На отрицательном электроде (катоде) происходит процесс восстановления, а на положительном (аноде) - процесс окисления.
На катоде при электролизе всегда происходит разряд положительных ионов, находящихся в растворе. Если металл находится в ряду напряжений выше алюминия (включая его), то происходит восстановление воды; а если ниже Al, то происходит осаждение металла.
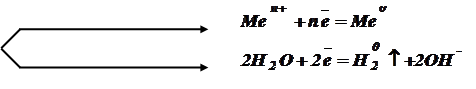 Ме ниже Al
Ме ниже Al
К(-)
Ме выше Al и Al
Процессы, протекающие на аноде, зависят от того, является анод растворимым или нерастворимым. К числу нерастворимых анодов относятся платина, золото, графит, уголь. На них происходит окисление отрицательных ионов, находящихся в растворе. На аноде разряжаются ионы безкислородных кислотных остатков, а разряд анионов кислородсодержащих кислот в обычных условиях электролиза не наблюдается, а вместо этого происходит окисление воды.




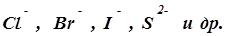
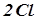
А(+)
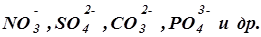
Если анод сделан из металла менее благородного, чем золото и платина, т.е. такого, который может посылать свои ионы в раствор - разряд отрицательных ионов на аноде не происходит. Рассмотрим процесс электролиза CuCl2 с двумя медными электродами. На катоде происходит выделение металлической меди:
Cu+2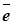 =Cu0
=Cu0
А на аноде происходит растворение металлической меди:
Cu0-2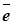 =Cu2+
=Cu2+
Количество CuCl2, находящееся в растворе, остается неизменным, так как процесс электролиза сводится к растворению меди на аноде и выделению ее на катоде. Этот вид электролиза используется для гальванического покрытия металлов и для электролитической очистки металлов (рафинирование).
В 30-х годах XIX века английский физик М. Фарадей установил, что масса вещества, выделившаяся при электролизе, прямо пропорциональна эквивалентной массе выделившегося вещества и количеству прошедшего электричества:
m=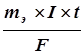 (9.1)
(9.1)
где m - масса выделившегося вещества, г; mэ - эквивалентная масса выделившегося вещества, 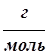 ; I - сила тока, А; t - время электролиза, с; F - постоянная Фарадея, равная 96500 Кл.
; I - сила тока, А; t - время электролиза, с; F - постоянная Фарадея, равная 96500 Кл.
Объем выделившегося газообразного вещества определяется по формуле:
V=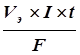 (9.2)
(9.2)
где Vэ - эквивалентный объем выделившегося вещества, 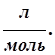
– Конец работы –
Эта тема принадлежит разделу:
Основные понятия в химии
Все вещества состоят из химических элементов Например составными частями серной кислоты Н SO являются элементы водород сера и кислород... Химические элементы составные части простых и сложных веществ каждый... Число нейтронов содержащихся в ядрах данного элемента в отличие от числа протонов может быть различным Атомы...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Электролиз
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов