рефераты конспекты курсовые дипломные лекции шпоры
Реферат Курсовая Конспект
Одноименного иона
Одноименного иона - Лекция, раздел Право, Газовые законы. Основные газовые процессы Одноименными Называют Ионы, Входящие В Состав Рассматриваемого Труднораствори...
Одноименными называют ионы, входящие в состав рассматриваемого труднорастворимого соединения. Если таковые в многокомпонентном растворе отсутствуют, то расчет растворимости ведут также по формуле (5), но с учетом ионной силы раствора. Вкладом труднорастворимого соединения в ионную силу пренебрегают, если его растворимость более, чем в 100 раз ниже концентрации других компонентов раствора. Ионную силу вычисляют как  , а коэффициент активности как
, а коэффициент активности как 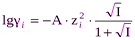 или
или  , подставляя в последние вместо квадрата заряда иона модуль произведения зарядов ионов, образующихся при растворении труднорастворимой соли.
, подставляя в последние вместо квадрата заряда иона модуль произведения зарядов ионов, образующихся при растворении труднорастворимой соли.
Следует подчеркнуть, что с ростом ионной силы g± при не высоких концентрациях электролита понижается, а растворимость увеличивается.
Растворимость в многокомпонентной системе с одноименными ионами
Рассмотрим расчет растворимости соли Мn+Аn- в системе, содержащей хорошо растворимую соль M¢Аn¢с одноименным анионом. Пример такой системы: PbCl2 - NaCl - H2O. В этом случае используют формулу (2). Катионы Mz+переходят в раствор только из осадка, поэтому их концентрация определена растворимостью: [Mz+] = n+S. Однако концентрация анионов в растворе складывается из двух составляющих, обусловленных, во-первых, растворимостью труднорастворимой соли n-S, и, во-вторых, концентрацией соли М¢An¢, которую обозначим n¢С¢. После подстановки в формулу (2) получим:
L = (n+S)n+(n-S + n¢C¢)n-×g±n. (6)
Растворимость находят путем решения степенного уравнения (6). Если растворимость меньше концентрации соли с одноименным ионом в 100 и более раз, то есть n-S < 0,01n¢C¢, то возможны упрощения. Во-первых, пренебрегают в сумме меньшим слагаемым и получают:
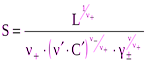 (7)
(7)
Во-вторых, при расчете коэффициента активности пренебрегают вкладом труднорастворимой соли в ионную силу. Аналогично вычисляют растворимость в присутствии одноименного катиона. Следует отметить, что растворимость в присутствии одноименных ионов всегда понижается, так как их концентрация в (7) стоит в знаменателе дроби.
Лекция №12: Гидролиз солей.
Гидролизом солей является процесс химического взаимодействия солей с водой. Таким образом, гидролизом называют взаимодействие вещества с водой, при котором составные части вещества соединятся с составными частями воды. Например, следующие реакции являются реакциями гидролиза:
KCN+H2O=HCN+KOH
AlCl3+H2O=Al(OH)Cl2+HCl
Гидролизу подвергаются следующие соли, образованные:
а) слабой кислотой и слабым основанием;
б) слабой кислотой и сильным основанием;
в) сильной кислотой и слабым основанием.
Соли же, образованные сильной кислотой и сильным основанием, не гидролизуются, а процесс нейтрализации в этом случае сводится к следующему:
Н++ОН- = Н2О. Следует учитывать, что обратная реакция диссоциации воды на ионы протекает в мизерной степени.
Слабыми кислотами являются: HNO2, H2SO3, H2O2, CH3COOH, H2SiO3, HF, H2CO3, HCN, H2S, H3PO4, NH4OH. Сильными кислотами являются: HNO3, H2SO4, HCl, HBr, HJ, НClO4, НMnO4. Cильными основаниями являются все щелочи кроме NH4OH (например КОН, NaOH, Ba(OH)2, Ca(OH)2).
Рассмотрим подробнее основные три случая гидролиза солей:
1. Гидролиз соли, образованной слабой кислотой и сильным основанием (на примере ацетата натрия):
CH3COONa+H2O=CH3COOH+NaOH
CH3COO- +H2O=CH3COOH+OH-
В данном случае гидролизуется анион соли, а реакция сопровождается образованием ионов ОН-. Реакция среды – щелочная.
2. Гидролиз соли, образованной слабым основанием и сильной кислотой:
NH4NO3+H2O=NH4OH+HNO3
NH4++H2O=NH4OH+H+
Здесь гидролизуется катион соли и реакция сопровождается образованием ионов Н+. Реакция среды – кислая.
3. Гидролиз соли, образованной слабой кислотой и слабым основанием:
CH3COONH4+H2O=CH3COOH+NH4OH
CH3COO- + NH4+ +H2O=CH3COOH+NH4OH
Здесь гидролиз идёт и по катиону, и по аниону с образованием сразу двух слабых электролитов. Среда в растворах таких солей зависит от относительной силы образующихся в результате гидролиза кислоты и основания, но в целом близка к нейтральной.
4. Соль, образованная сильной кислотой и сильным основанием, не гидролизуется:
KNO3+H2O¹
KClO4+H2O¹
Гидролизу подвергается не вся соль, а лишь её часть, т.е. в растворе устанавливается равновесие между солью и образующими её кислотой и основанием. Поэтому часть вещества, подвергающаяся гидролизу, характеризуется степенью гидролиза. Степень гидролиза зависит от константы равновесия, температуры и концентрации соли, а также от её природы. Природа соли проявляется в величине константы гидролиза соли.
Константа гидролиза соли Кг характеризует способность данной соли подвергаться гидролизу. Чем больше Кг, тем в большей степени протекает гидролиз (при постоянстве Т и концентрации соли).
Константа гидролиза соли, образованной слабой кислотой и сильным основанием, равна:
Кг=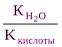 , где Ккислоты – константа диссоциации кислоты. Анализ уравнения показывает, что чем слабее кислота, тем в большей степени подвергаются гидролизу её соли.
, где Ккислоты – константа диссоциации кислоты. Анализ уравнения показывает, что чем слабее кислота, тем в большей степени подвергаются гидролизу её соли.
Константа гидролиза соли, образованной сильной кислотой и слабым основанием, равна:
Кг=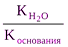 , где Коснования – константа диссоциации основания. Анализ уравнения показывает, что чем слабее основание, тем в большей степени подвергаются гидролизу им образованные соли.
, где Коснования – константа диссоциации основания. Анализ уравнения показывает, что чем слабее основание, тем в большей степени подвергаются гидролизу им образованные соли.
Константа гидролиза соли, образованной слабой кислотой и слабым основанием, равна:
Кг=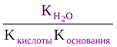 .
.
Зависимость степени гидролиза от концентрации соли проявляется в том, что с разбавлением раствора степень гидролиза растёт. Влияние температуры на степень гидролиза вытекает из рассмотренного ранее принципа Ле Шателье: степень гидролиза растёт с повышением температуры. Поэтому для ослабления гидролиза растворы необходимо хранить концентрированными и при низких температурах. Для солей, образованных сильной кислотой и слабым основанием, фактором подавления гидролиза является подкисление раствора, а в случае соли, образованной слабой кислотой и сильным основанием, таковым фактором является подщелачивание раствора.
Процесс гидролиза может протекать ступенчато, например:
N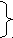
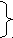 a2CO3+H2O=NaHCO3+NaOH I ступень
a2CO3+H2O=NaHCO3+NaOH I ступень
CO32- +H2O=HCO3- +OH-
NaHCO3- +H2O=H2CO3+OH- II ступень
HCO3- +H2O=H2CO3+OH-
Как видно из уравнения реакции гидролиза, в первой ступени образуется гидрокарбонат ион, диссоциация которого характеризуется второй константой диссоциации угольной кислоты, а во второй ступени происходит гидролиз кислой соли с образованием угольной кислоты, диссоциацию которой характеризует первая константа её диссоциации. Поэтому можно связать константу гидролиза по первой ступени К1 со второй константой диссоциации кислоты К2 кисл, а константу гидролиза по второй ступени К2 с первой константой диссоциации кислоты К1 кисл:
К1= >К2=
>К2= .
.
Гидролиз по первой ступени всегда протекает в большей степени, чем по второй. Аналогично протекает гидролиз соли, образованной слабым основанием многовалентного металла.
Особенно глубоко протекает гидролиз соли, образованной слабой кислотой и слабым основанием, т.к. константа гидролиза для этого случая обратно пропорциональна произведению констант диссоциации кислоты и основания, т.е. её значение крайне велико.
Согласно протонной теории кислот и оснований гидролиз можно представить как частный случай кислотно-основного равновесия: протон переходит от молекулы воды к данному иону или от данного иона к молекуле воды. Примером может служить гидролиз иона аммония:
NH4++H2O= H3О++NH3.
Лекция №13: Окислительно-восстановительные реакции.
Окислительно-восстановительными называются химические реакции, сопровождающиеся изменением степени окисления атомов элементов. Степень окисления – это условный заряд атома в молекуле. Она вычисляется исходя из положения, что все связи между атомами ионные. Окислением называется процесс отдачи электронов, а восстановлением процесс принятия электронов. Окисление и восстановление взаимосвязаны. Окислителем называется вещество, атомы которого принимают электроны, при этом он восстанавливается. Восстановителем называется вещество, атомы которого отдают электроны, при этом он окисляется.
Все окислительно-восстановительные реакции классифицируют следующим образом:
1. Межмолекулярные реакции. Это реакции, в которых окислитель и восстановитель являются различными веществами.
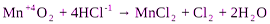 ,
,
где Mn+4 – окислитель, Cl-1 – восстановитель.
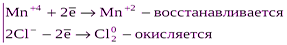
2. Реакции внутримолекулярного окисления. Это реакции, которые протекают с изменением степеней окисления атомов различных элементов одного и того же вещества.
 ,
,
где Mn+7 – окислитель, а O-2 – восстановитель.
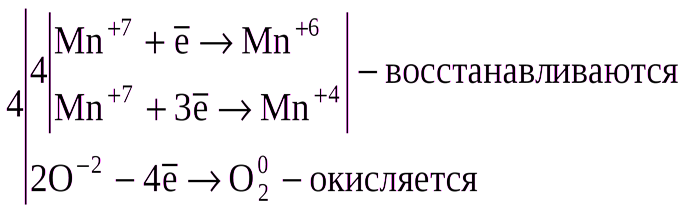
3. Реакции диспропорционирования. В этих реакциях и окислителем и восстановителем является элемент, находящийся в промежуточной степени окисления в составе одного и того же вещества.
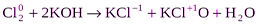 ,
,
где Cl20 – окислитель и восстановитель.

О возможности того или иного вещества проявлять окислительные, восстановительные или двойственные свойства можно судить по степени окисления элементов, выполняющих эти функции.
Элементы в своей высшей степени окисления проявляют только окислительные свойства, а в низшей степени окисления проявляют только восстановительные свойства. Элементы, имеющие промежуточную степень окисления, могут проявлять как окислительные, так и восстановительные свойства. Основные окислители и восстановители приведены ниже.
| Окислители | Схемы реакций | ||
| Простые вещества: Галогены Г2 | 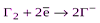 (НГ и их соли) (НГ и их соли)
| ||
| Кислород О2 |  (H2O, оксиды и их производные) (H2O, оксиды и их производные)
| ||
| Неметаллы (S,P,N2) | 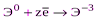 (ЭНn и их соли) (ЭНn и их соли)
| ||
| Сложные вещества: HCl, H2SO4(разбавленные) и т. п. (кроме НNO3). | 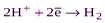
| ||
| H2SO4 конц. | 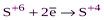 (SO2, H2SO3 и её соли) (SO2, H2SO3 и её соли) 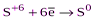 (S¯) (S¯)  (H2S и её соли) (H2S и её соли)
| ||
| HNO3 конц. HNO3 разб. | 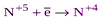 (NO2) (NO2)  (N2O3, HNO2 и её соли) (N2O3, HNO2 и её соли) 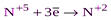 (NO) (NO) 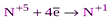 (N2O) (N2O) 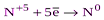 (N2) (N2)  (NH3, NH4+ и соответствующие соли) (NH3, NH4+ и соответствующие соли)
| ||
| Окислители | Схемы реакций | ||
| KMnO4 |   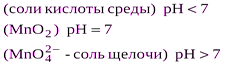
| ||
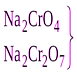
| 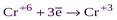 
| ||
| H2O2 | 
| ||
| Катионы металлов высшей степени окисления (Fe+3, Sn+4, и т. п.) | 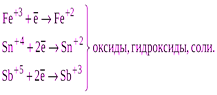
| ||
| Восстановители | Схемы реакций | ||
| Простые вещества: металлы (Ме) | 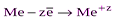
| ||
| Н2 | 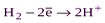 (H2O) (H2O)
| ||
| Неметаллы (S,C,P,N2,…) | 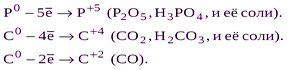
| ||
| H2S и её соли, Na2S2O3 | 
| ||
| НГ и их соли | 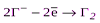
| ||
| Катионы металлов в низших степенях окисления (Fe+2, Sn+2, Sb+3, Cr+3 и т.д.) | 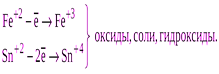 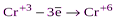 
| ||
| HNO2 и её соли. | 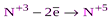 (HNO3 или ее соли). (HNO3 или ее соли).
| ||
| H2SO3 и её соли. | 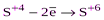 (H2SO4 или ее соли). (H2SO4 или ее соли).
| ||
| H2O2 | 
| ||
– Конец работы –
Эта тема принадлежит разделу:
Газовые законы. Основные газовые процессы
Лекция Основные классы неорганических соединений номенклатура... Основными классами неорганических соединений являются оксиды кислоты соли и... Оксиды представляют собой соединения элементов с кислородом Оксиды подразделяют на солеобразующие и несолеобразующие...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Одноименного иона
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов