рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Образование
- /
- Химическая связь
Реферат Курсовая Конспект
Химическая связь
Химическая связь - раздел Образование, ЗАДАНИЯ И МЕТОДИЧЕСКИЕ УКАЗАНИЯ Выделяют Три Типа Химической Связи: Ковалентную, Ионную И Металлическую. ...
Выделяют три типа химической связи: ковалентную, ионную и металлическую.
Ковалентная связь –химическая связь, осуществляемая общими электронными парами. В соответствии с методом валентных связей (ВС) ковалентная связь между двумя атомами осуществляется общей для этих атомов парой электронов с противоположными спинами. В момент образования связи атомные орбитали перекрываются, что приводит к увеличению электронной плотности между ядрами взаимодействующих атомов и к взаимному притяжению ядер к области повышенной электронной плотности. В результате этого происходит выделение энергии и потенциальная энергия системы уменьшается.
Общая для двух атомов электронная пара может образовываться по двум механизмам: обменному или донорно-акцепторному.
При обменном механизме два связываемых атома (А и В) предоставляют для образования связи по одному неспаренному электрону, как бы обмениваясь ими:
| ↑ |
| ↑↓ |
| ↓ |
А +В→ А В А
Донорно-акцепторный механизмобразования связи заключается в том, что один атом А (донор) на образование связи предоставляет пару электронов, а другой атом В (акцептор) – вакантную атомную орбиталь.
Различают две разновидности ковалентной связи: неполярную и полярную.
Ковалентная неполярная связь – это связь, при которой область повышенной электронной плотности расположена симметрично относительно ядер обоих атомов. Такая связь образуется между атомами с одинаковой электроотрицательностью (ЭО), например, в молекулах Cl2, O2, H2 и др.
Ковалентная полярная связь – это связь, при которой область повышенной электронной плотности смещена к ядру атома с большей ЭО. В результате этот атом приобретает эффективный отрицательный заряд, а на другом менее электроотрицательном атоме возникает равный по величине эффективный положительный заряд. Такая система представляет собой электрический диполь. Полярная связь образуется между атомами с разной ЭО, например, в молекулах HCl, HI, H2O, H2S, CO и др. Чем больше разность электроотрицательностей атомов, образующих связь (∆ЭОА – В), тем выше полярность связи.
Важнейшие свойства ковалентной связи – насыщаемость и направленность. Насыщаемость– это способность атомов образовывать ограниченное число ковалентных связей. В случае обменного механизма число связей равно числу неспаренных валентных электронов атома. Способность атома к образованию химических связей характеризуется валентностью.
Валентность определяется как число химических связей, которыми данный атом соединен с другими атомами. Она зависит от того, в каком состоянии - основном или возбужденном находится атом. Основное состояние – это устойчивое состояние с наименьшей энергией. При возбуждении спаренные валентные электроны разъединяются и переходят с одного подуровня на свободные АО другого, энергетически более высокого подуровня в пределах внешнего энергетического уровня. В результате число неспаренных электронов увеличивается, и атом данного элемента образует максимально возможное для него число химических связей, проявляя при этом высшую валентность и высшую положительную степень окисления, равную номеру группы в Периодической системе (см. примеры решения задач).
Ковалентная связь имеет направленность, которая обусловливает пространственную структуру молекулы, т.е. ее геометрическую форму. В зависимости от способа перекрывания АО различают σ (сигма)- , π (пи)- и
δ (дельта)- связи.
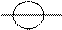
 σ – связь обладает осевой симметрией относительно межъядерной оси, и область перекрывания АО лежит на межъядерной оси. Ее могут образовывать s – АО, p – АО и d – АО. Именно σ – связи определяют пространственную конфигурацию молекул:
σ – связь обладает осевой симметрией относительно межъядерной оси, и область перекрывания АО лежит на межъядерной оси. Ее могут образовывать s – АО, p – АО и d – АО. Именно σ – связи определяют пространственную конфигурацию молекул:
 |
 π – связьобразуется при перекрывании АО, расположенных параллельно друг другу. Область перекрывания лежит по обе стороны от межъядерной оси. В образовании π – связи могут участвовать p – и d – АО:
π – связьобразуется при перекрывании АО, расположенных параллельно друг другу. Область перекрывания лежит по обе стороны от межъядерной оси. В образовании π – связи могут участвовать p – и d – АО:
δ – связиобразуют толькоd – АО.
Сигма – связь является самой прочной связью и всегда образуется в первую очередь. Между двумя атомами в молекуле возможна лишь одна σ – связь.
 Для объяснения геометрической структуры молекул (или направленности ковалентной связи) используют представление о гибридизации атомных орбиталей центрального атома в молекуле АВn.
Для объяснения геометрической структуры молекул (или направленности ковалентной связи) используют представление о гибридизации атомных орбиталей центрального атома в молекуле АВn.
Гибридизация –это выравнивание энергии различных АО у атома А в результате их смешения перед химическим взаимодействием, что приводит к образованию гибридных орбиталей. В гибридизации участвуют только АО одного уровня, например, 2s и 2p. Каждому виду гибридизации АО соответствует определенная геометрическая форма молекулы. Например, sp– гибридизации (две связи) соответствует линейная форма молекулы (BeCl2), sp2– гибридизации (три связи) – плоская треугольная (BCl3), sp3 - гибридизации (четыре связи) – тетраэдрическая (CH4).
Ионная связь – связь между ионами, осуществляемая их электростатическим взаимодействием. Ионная связь возникает между атомами металлов и неметаллов, резко отличающимися по своей электроотрицательности. Механизм образования ионной связи заключается в переходе электронов от одного атома к другому (более электроотрицательному), в результате чего атомы превращаются в противоположно заряженные ионы (катион и анион) и происходит их электростатическое взаимодействие. Свойства ионной связи – ненаправленность и ненасыщаемость.
Металлическая связь – это связь, образованная в результате перекрывания валентных орбиталей атомов металлов, в результате чего электроны свободно перемещаются из одной орбитали в другую, осуществляя связь между всеми атомами кристалла металла.
Примеры решения задач
Пример 1. Объясните механизм образования ковалентной химической связи в молекуле HBr и оцените степень ее полярности.
Р е ш е н и е. 1) Для объяснения механизма образования ковалентной химической связи необходимо определить, какие электроны участвуют в образовании этой связи. Запишем электронные конфигурации атомов и электронные схемы строения их валентных уровней; изобразим форму АО, участвующих в образовании связи.
| ↑ |
 Н 1s1
Н 1s1
Z = +1
Br 1s22s22p63s23p63d104s24p5
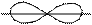 Z = +35 4p
Z = +35 4p
| ↑↓ | ↑↓ | ↓ |
4s
| ↑↓ |
Для образования ковалентной связи атомы водорода и брома предоставляют по одному неспаренному электрону с антипараллельными спинами: атом Н – электрон, находящийся на s – АО (форма АО – сфера), а атом Br – электрон с
p – АО (форма АО – гантель).
2) Покажем механизм образования ковалентной связи в молекуле HBr.
В молекуле HBr связь создается за счет перекрывания двух атомных орбиталей: s – АО и p – АО с образованием между ядрами атомов H и Br зоны повышенной электронной плотности:
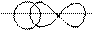 H Br
H Br
– Конец работы –
Эта тема принадлежит разделу:
ЗАДАНИЯ И МЕТОДИЧЕСКИЕ УКАЗАНИЯ
Федеральное государственное автономное образовательное учреждение высшего профессионального образования... Российский государственный профессионально педагогический университет... Машиностроительный институт...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Химическая связь
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов