рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Физика
- /
- Энергия молекулы. Молекулярные спектры.
Реферат Курсовая Конспект
Энергия молекулы. Молекулярные спектры.
Энергия молекулы. Молекулярные спектры. - раздел Физика, Квантовая природа электромагнитного излучения. Формула Эйнштейна Рассмотрим Двухатомные Молекулы. Различают Два Вида Связи В Них: 1) ...
Рассмотрим двухатомные молекулы. Различают два вида связи в них:
1) Если электрон в молекуле можно разделить на две группы, каждая из которых всё время находится около одного из ядер, т. е. ионная связь (гетерополярная).
2) Электроны сосредоточены около обоих ядер (гомеополярная).
Потенциальная энергия:
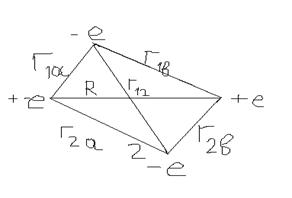
U=K(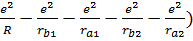
me+>>re-
Тогда уравнение Шредингера, соответствующее данному выражению 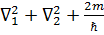 (E-U)=0.
(E-U)=0.
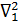 - для координат первого электрона,
- для координат первого электрона, 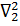 - для координат второго электрона
- для координат второго электрона
Собственные значения энергии получаются зависимыми от расстояния между атомами.
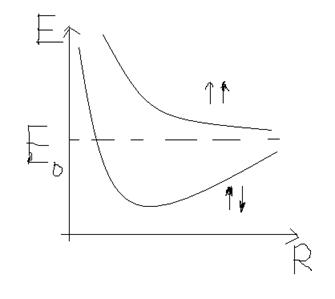
Если меняется электронная энергия или электронная конфигурация молекулы, то меняется кривая E(R).
Ядра могут тоже разным образом колебаться и вращаться относительно общего центра масс. Введём обозначения:
Ee - энергия, обусловленная электронной конфигурацией (электронная энергия)
Ev - энергия, соответствующая колебаниям молекулы (колебательная энергия)
Er – энергия, связанная с вращением молекулы (вращательная энергия).
E= Ee+ Ev+ Er.
En=ћω(n+1/2)
Ev= ћωv(v+1/2), где V – собственные числа (0,1,2,3,…) – колебательные квантовые числа, ωv – классическая частота осциллятора.
Правило отбора ∆V=±1.
Молекулярные спектры состоят из полос, которые составлены из большого числа тесно расположенных линий.
Молекулярные спектры названы полосатыми, и в зависимости от того, каких видов энергии обуславливает испускание молекулой фотона, различают три вида полос: 1) вращательные; 2) колебательно-вращательные; 3) электронно-колебательные.
Для электронно-колебательных характерен резкий край полосы, названный кантом, у остальных полос – размытые края.
Ћω=∆Ee+∆Ev+∆Er=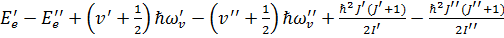
J’ и J’’ – вращательные квантовые числа.
При слабых возбуждениях меняется Er, при сильных Ev, при ещё более сильных Ee.
Er=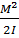 ; где M – момент импульса системы.
; где M – момент импульса системы.
M=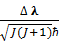
I – момент инерции молекулы относительно оси, проходящей через её центр масс.
Для вращательного квантового числа имеется правило отбора ∆J=±1.
Итак полная энергия молекулы равна E=Ee+(v+1/2)ћωv+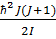 .
.
24. Теплоёмкость твёрдых тел. Теория теплоёмкости Эйнштейна. Теория Дебая.
По классической теории кристалл, состоящий из N атомов, является системой с 3N колебательными степенями свободы, на каждую из которых приходится в среднем энергия kT (kT/2 в виде кинетической энергии и kT/2 в виде потенциальной энергии). Из этих представлений вытекает закон Дюлонга и Пти, который утверждает, что молярная теплоёмкость всех химических простых тел в кристаллическом состоянии одинакова и равна 3R.
Полная энергия ε=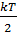 или
или 
U=3N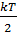 2=3RT
2=3RT
NK=R
Энергия гармонического осциллятора может иметь значения εn=(n+1/2)ћω (n=0,1,2,3,…).
Приняв, что распределение осцилляторов по состояниям с различной энергией подчиняется закону Больцмана, можно найти среднее значение энергии гармонического осциллятора.
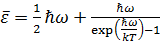 . (*)
. (*)
Теория теплоёмкости кристаллических тел, учитывающая квантование колебательной энергии, была создана Эйнштейном(1907) и впоследствии усовершенствованна Дебаем(1912).
Эйнштейн отождествлял кристаллическую решётку из N атомов с системой 3N независимых гармонических осцилляторов с одинаковой собственной частотой ω. Эйнштейн исходил из планковского значения энергии гармонического осциллятора εn=nћω. Соответственно в использованном Эйнштейном выражении для 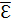 слагаемое ћω/2 отсутствовало.
слагаемое ћω/2 отсутствовало.
Умножив второе слагаемое выражения (*) на 3N, Эйнштейн получил для внутренней энергии кристалла формулу 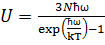 .
.
Продифференцировав это выражение по температуре, Эйнштейн нашёл теплоёмкость кристалла:
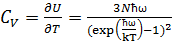 exp(
exp(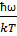 )
)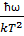 .
.
Рассмотрим два предельных случая.
1. Высокие температуры (kT>> ћω). Тогда exp(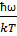 ) ≈1+
) ≈1+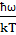 в знаменателе и exp(
в знаменателе и exp(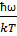 ) ≈1 – в числителе формулы, тогда
) ≈1 – в числителе формулы, тогда 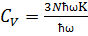 =3NK=3R;
=3NK=3R; 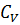 - молярная.
- молярная.
2. Низкие температуры (kT<< ). При этом условии единицей в знаменателе выражения можно пренебречь по сравнению с exp.
). При этом условии единицей в знаменателе выражения можно пренебречь по сравнению с exp. 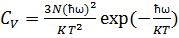 .
.
Экспонента в числителе меняется быстрее, чем T2, поэтому при приближении к абсолютному нулю выражение будет стремиться к нулю по экспоненциальному закону. Опыт показывает, что теплоёмкость кристаллов изменяется вблизи абсолютного нуля не экспоненциально, а по закону T3.
В отличие от Эйнштейна, Дебай предположил, что колебание атомов в кристаллической решётке не являются независимыми, а из-за связи атомов, колебание от одного к другому передаётся как упругая волна.
В твёрдом теле возможно размещение поперечных и продольных звуковых волн, причём Дебай учитывал число нормальных колебаний или нормальных мод системы в интервале частоты от ω до ω+dω и затем суммировал энергию всех мод колебаний с учётом 3-ёх возможных поляризаций, получая при этом внутреннюю энергию системы.
Полученная формула: U=U0+3NAiTD(x)
D(x)=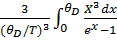
K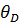 =ωmћ.
=ωmћ.
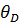 - температура Дебая, которая связанна с max частотой колебаний следующим образом:
- температура Дебая, которая связанна с max частотой колебаний следующим образом:
T<<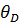
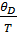 --->∞ =>x--->∞ и интеграл заменяется на
--->∞ =>x--->∞ и интеграл заменяется на 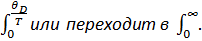
Из ТФКП 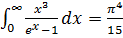 .
.
U=3NAKT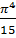 *
*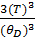 .
.
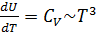 b (b – const в дифференцировании).
b (b – const в дифференцировании).
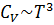 .
.
– Конец работы –
Эта тема принадлежит разделу:
Квантовая природа электромагнитного излучения. Формула Эйнштейна
Принцип неопределенности Гейзенберга произведение неопределенностей значений двух сопряженных переменных не может быть по порядку величины меньше... Энергия и время являются каноническими сопряженными величинами Поэтому для...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Энергия молекулы. Молекулярные спектры.
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов