рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- Щоб виконати роботу, Ви повинні знати!
Реферат Курсовая Конспект
Щоб виконати роботу, Ви повинні знати!
Щоб виконати роботу, Ви повинні знати! - раздел Химия, Техніка безпеки в хімічній лабораторії 1. Корозія Металів- Це Мимовільно Протікаючий Окисно-Відновн...
1. Корозія металів- це мимовільно протікаючий окисно-відновний процес (DG<0) руйнування металу під впливом
навколишнього середовища, що відбувається з виділенням енергії ( DH<0) і розсіюванням речовини (DS >0).
2. Анод- це електрод, на якому відбувається процес окиснення, тобто віддача електронів.
3. Катод- це електрод, на якому відбувається процес відновлення, тобто приєднання електронів.
4. Хімічна корозія- це руйнування металів з окисненням в навколишньому середовищі без виникнення електричного
струму в системі.
5. Електрохімічна корозія -це просторово розділений окисно-відновний процес руйнування металу, який протікає в середовищі
електроліту і супроводжується виникненням усередині системи електричного струму, що зветься
корозійним струмом.
6.Протекторний захистполягає в тому, що до металевого виробу, який піддається електрохімічній корозії, підключають деталь – протектор, виготовлений з більш активного металу, ніж метал виробу. Протектор руйнується, а металевий вироб залишиться незмінним.
Приклад послідовного запису хімізму корозії :
Розглянемо атмосферну корозію сталевого виробу. Сталь - це сплав заліза з вуглецем, в якому вміст вуглецю менше 2%. У сталі присутній цементіт (Fe3C). Під час електрохімічної корозії у вологому повітрі (О2 + 2Н2О) залізо і цементіт утворюють мікрогальванопару, в якій роль анода виконує залізо, а цементіт - роль катода.
Схема процесу: (А-) Fе | О2 + 2Н2О | Fе3С (К+)
Анодний процес: Fе0 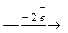 Fе2+ 2 поляризація
Fе2+ 2 поляризація
Катодний процес: О2 + 2Н2О 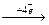 4ОH- 1 деполяризація
4ОH- 1 деполяризація
Сумарне рівняння корозійного процесу руйнування сталевого виробу, що знаходиться у вологому повітрі:
2Fе + 2Н2О + О2 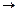 2Fе(ОН)2
2Fе(ОН)2
Для заліза характерніший ступінь окиснення (3+), тому процес окиснення йде далі: 4Fе(ОН)2+ О2 + 2Н2О = 4Fе(ОН)3.
Під час нагрівання Fе(ОН)3 втрачає воду: Fе(ОН)3 →Н2О + FеО(ОН). Продукти корозії Fе(ОН)3 і FеО(ОН).
Література:
[1] с. 76-83; [2] с. 507-529; [3] с. 316-319; [4] с. 195-198;
Завдання для самостійної роботи:
1. Мідь не витісняє водень з розбавлених кислот. Чому? Проте, якщо до мідної пластинки, опущеної в кислоту, доторкнутися цинковою, то на міді починається бурхливе виділення водню. Дайте цьому пояснення, склавши електронні рівняння анодного і катодного процесів. Напишіть рівняння хімічної реакції.
2. Як відбувається атмосферна корозія лудженого заліза і лудженої міді при порушенні покриття? Складіть електронні рівняння анодного і катодного процесів.
3. Якщо пластинку з чистого цинку опустити в розбавлену кислоту, то виділення водню, що починається, незабаром майже припиняється. Проте при дотику до цинку мідною паличкою на останній починається бурхливе виділення водню. Дайте цьому пояснення, склавши електронні рівняння анодного і катодного процесів. Напишіть рівняння хімічної реакції.
4. У чому суть протекторного захисту металів від корозії? Приведіть приклад протекторного захисту заліза в електроліті, що містить розчинений кисень. Складіть електронні рівняння анодного і катодного процесів.
Дайте відповіді на запитання:
| № 1. | Запитання | Ваші відповіді |
| 1. | Дайте визначення поняттю «Корозія». | |
| 2. | Дайте визначення поняттю «Хімічна корозія» | |
| 3. | Дайте визначення поняттю «Електрохімічна корозія» | |
| 4. | Дайте визначення поняттю «Катод» | |
| 5. | Дайте визначення поняттю «Анод» | |
| 6. | Дайте визначення поняттю «Контактна корозія» | |
| 7. | Дайте визначення поняттю «Концентраційна корозія» | |
| 8. | Дайте визначення поняттю «Деполяризація» | |
| 9. | Що означає корозія з водневою деполяризацією? З кисневою? | |
| 10. | Який метал буде руйнуватися або підлягати корозії в зразку, що складається з нікелю Ni та міді Сu? | |
| 11. | Яке покриття краще анодне або катодне і чому? |
Самостійно вирішити задачу № 1125 [5. с. 219]
Виконайте роботу та заповніть лабораторний журнал:
Дотримуйтесь правил техніки безпеки! ! (стор5)
Особливо коли працюєте з розведеною H2SO4 , розчинами K3[Fe(CN)6] і K4[Fe(CN)6]
| № | Зміст роботи | Рівняння реакцій, спостереження, розрахунки | |
| Дослід №1 Типи корозійних руйнувань. Змочіть фільтрувальний папір розчином К3[Fе(СN)6] і покладіть його на зачищену поверхню залізної пластинки. Зверху покладіть 2-3 листи чистого паперу і невеликий вантаж. Через 20 хвилин зніміть фільтрувальний папір і роздивіться форми синіх плям. Зробіть висновок про тип корозійного руйнування: суцільна корозія, плямами або точкова (піттінг)? |
Fe + О2 + 2Н2О 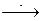 Fе2+ + K3 [Fe(CN)6 ]
Fе2+ + K3 [Fe(CN)6 ] 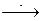
| ||
| 2.1 2.2 2.3 | Дослід №2 Контактна корозія - У пробірку налийте один мл розчину сульфатної кислоти і опустіть одну гранулу цинку. Спостерігайте за швидкістю розчинення цинку. Напишіть рівняння хімічної реакції. - Через одну хвилину до гранули цинку, що знаходиться в розчині Н2SО4 доторкніться мідним дротом. Чому розчинення цинку стало інтенсивнішим? Напишіть схему ГЕ, рівняння реакції,зробіть висновки. - Додайте до гранули цинку, що знаходиться в розчині Н2SО4кілька краплин розчину СuSО4. Чому розчинення цинку стало інтенсивнішим? Напишіть рівняння реакції,зробіть висновки. |
Zn+Н2SО4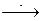 Zn+Н2SО4 + Сu (мідний дріт)
Zn+Н2SО4 + Сu (мідний дріт) 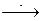 Схема ГЕ:
Процеси:
А:
К:
ЕРСтеор.=
Схема ГЕ:
Процеси:
А:
К:
ЕРСтеор.= 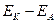 =
Zn+Н2SО4+СuSО4 =
Zn+Н2SО4+СuSО4 Схема:
Процеси:
Схема:
Процеси:
| |
| 3.1 3.2 | Дослід№3 Корозія при порушенні анодного та катодного покриттів. У два стаканчики налийте розчин спецреактиву (Натрій хлориду і червоної кров'яної солі). - У перший стаканчик опустіть пластинку оцинкованого заліза з нанесеними на ній глибокими подряпинами. - У другий стаканчик опустіть пластинку лудженого заліза, теж з подряпинами. У якому стакані іржавіє залізо? Чому? Складіть схеми ГЕ, рівняння анодних і катодних корозійних процесів в кожному випадку. | Оцинковане залізо
Схема:
Процеси:
А:
К:
ЕРСтеор.= 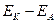 = =
| Луджене залізо
Схема:
Процеси:
А:
K:
ЕРСтеор.= 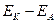 = =
|
| Дослід№4 Атмосферна корозія в результаті різного доступу кисню. Візьміть залізну пластинку і наждачним папером зачистіть на ній невелику ділянку. Обполосніть її водою і обсушіть її фільтрувальним папером. На зачищену ділянку нанесіть краплю спеціального реактиву що складається з 3%NaCl , К3[Fе(СN)6] тафенолфталеїну. Через 3-5 хвилин у центрі краплі з’явиться синій колір, а скраю її - рожеве або малинове забарвлення. Поясніть появу цих забарвлень. Складіть схему утвореної гальванопари. Запишіть рівняння реакції, зробіть висновок. |
Схема ГЕ:
Процеси:
А:
К:
ЕРСтеор.= 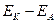 =
Чому в центрі краплі з’явилось синє забарвлення? Напишіть рівняння реакції
Чому з’явилось рожеве забарвлення по краях краплі? =
Чому в центрі краплі з’явилось синє забарвлення? Напишіть рівняння реакції
Чому з’явилось рожеве забарвлення по краях краплі?
|
Висновки і місце для домашніх задач:
Оцінка___________ Дата____________ Підпис викладача____________
Лабораторна робота №
– Конец работы –
Эта тема принадлежит разделу:
Техніка безпеки в хімічній лабораторії
СХІДНОУКРАЇНСЬКИЙ НАЦІОНАЛЬНИЙ УНІВЕРСИТЕТ імені ВОЛОДИМИРА ДАЛЯ... ЛАБОРАТОРНИЙ ЖУРНАЛ...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Щоб виконати роботу, Ви повинні знати!
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов