Строение коферментов - раздел Медицина, БИОХИМИЯ И ЕЁ ЗАДАЧИ Коферменты В Каталитических Реакциях Осуществляют Транспорт Различных Групп А...
Коферменты в каталитических реакциях осуществляют транспорт различных групп атомов, электронов или протонов. Коферменты связываются с ферментами:
- ковалентными связями;
- ионными связями;
- гидрофобными взаимодействиями и т.д.
Один кофермент может быть коферментом для нескольких ферментов. Многие коферменты являются полифункциональными (например, НАД, ПФ). В зависимости от апофермента зависит специфичность холофермента.
Все коферменты делят на две большие группы: витаминные и невитаминные.
Коферменты витаминной природы– производные витаминов или химические модификации витаминов.
1 группа: тиаминовые – производные витамина В1. Сюда относят:
- тиаминмонофосфат (ТМФ);
- тиаминдифосфат (ТДФ) или тиаминпирофосфат (ТПФ) или кокарбоксилаза;
- тиаминтрифосфат (ТТФ).
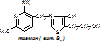
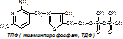
ТПФ имеет наибольшее биологическое значение. Входит в состав декарбоксилазы кетокислот: ПВК, a-кетоглутаровая кислота. Этот фермент катализирует отщепление СО2.
Кокарбоксилаза участвует в транскетолазной реакции из пентозофосфатного цикла.
2 группа: флавиновые коферменты, производные витамина В2. Сюда относят:
- флавинмононуклеотид (ФМН);
- флавинадениндинуклеотид (ФАД).
Ребитол и изоалоксазин образуют витамин В2. Витамин В2 и остаток фосфорной к-ты образуют ФМН. ФМН в соединении с АМФ образуют ФАД.
[рис. изоалоксазиновое кольцо соединено с ребитолом, ребитол с фосфорной к-той, а фосфорная к-та – с АМФ]

ФАД и ФМН являются коферментами дегидрогеназ. Эти ферменты катализируют отщепление от субстрата водорода, т.е. участвуют в реакциях окисления–восстановления. Например СДГ – сукцинатдегидрогеназа – катализирует превращение янтарной к-ты в фумаровую. Это ФАД-зависимый фермент. [рис. COOH-CH2-CH2-COOH® (над стрелкой – СДГ, под – ФАД и ФАДН2) COOH-CH=CH-COOH]. Флавиновые ферменты (флавинзависимые ДГ) содержат ФАД, который в них является первоисточником протонов и электронов. В процессе хим. реакций ФАД превращается в ФАДН2. Рабочей частью ФАД является 2 кольцо изоалоксазина; в процессе хим. реакции идет присоединение двух атомов водорода к азотам и перегруппировка двойных связей в кольцах.
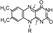
3 группа: пантотеновые коферменты, производные витамина В3 – пантотеновой кислоты. Входят в состав кофермента А, НS-КоА. Этот кофермент А является коферментом ацилтрансфераз, вместе с которой переносит различные группировки с одной молекулы на другую.
4 группа: никотинамидные, производные витамина РР - никотинамида:

Представители:
- никотинамидадениндинуклеотид (НАД);
- никотинамидадениндинуклеотидфосфат (НАДФ).
Коферменты НАД и НАДФ являются коферментами дегидрогеназ (НАДФ-зависимых ферментов), например малатДГ, изоцитратДГ, лактатДГ. Участвуют в процессах дегидрирования и в окислительно-восстановительных реакциях. При этом НАД присоединяет два протона и два электрона, и образуется НАДН2.

Рис. рабочей группы НАД и НАДФ: рисунок витамина РР, к которому присоединяется один атом Н и в результате происходит перегруппировка двойных связей. Рисуется новая конфигурация витамина РР + Н+]

5 группа: пиридоксиновые, производные витамина В6. [рис. пиридоксаля. Пиридоксаль+ фосфорная к-та= пиридоксальфосфат]
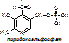
- пиридоксин;
- пиридоксаль;
- пиридоксамин.
Эти формы взаимопревращаются в процессе реакций. При взаимодействии пиридоксаля с фосфорной кислотой получается пиридоксальфосфат (ПФ).
ПФ является коферментом аминотрансфераз, осуществляет перенос аминогруппы от АК на кетокислоту – реакция переаминирования. Также производные витамина В6 входят как коферменты в состав декарбоксилаз АК.
Коферменты невитаминной природы – вещества, которые образуются в процессе метаболизма.
1) Нуклеотиды – УТФ, УДФ, ТТФ и т.д. УДФ-глюкоза вступает в синтез гликогена. УДФ-гиалуроновая к-та используется для обезвреживания различных веществ в трансверных реакциях (глюкоуронил трансфераза).
2) Производные порфирина (гем): каталаза, пероксидаза, цитохромы и т.д.
3) Пептиды. Глутатион – это трипептид (ГЛУ-ЦИС-ГЛИ), он участвует в о-в реакциях, является коферментом оксидоредуктаз (глутатионпероксидаза, глутатионредуктаза). 2GSH«(над стрелкой 2Н) G-S-S-G. GSH является восстановленной формой глутатиона, а G-S-S-G – окисленной.
4) Ионы металлов, например Zn2+ входит в состав фермента АлДГ (алкогольдегидрогеназы), Cu2+ - амилазы, Mg2+ - АТФ-азы (например, миозиновой АТФ-азы).
Могут участвовать в:
-присоединении субстратного комплекса фермента;
-в катализе;
-стабилизация оптимальной конформации активного центра фермента;
-стабилизация четвертичной структуры.
Все темы данного раздела:
Белки и их биологическая роль
Белок (протеины) – protos – предшествующий всему, первичный, наиглавнейший, определяющий всё остальное.
Белки – это высокомолекулярные азотсодержащие органические вещества, состо
Характеристика простых белков
В основе классификации (создана в 1908г.) лежит растворимость белков. По этому признаку выделяют:
I. гистоныипротамины, растворимые в солевых растворах. О
Хромопротеины
Для них простетическая часть окрашена (chromos – краска). К хромопротеинам относятся гемоглобин, миоглобин, каталаза, пероксидаза, ряд флавинсодержащих ферментов (сукцинатдегидрогеназа, альдегидокс
Липид-белковые комплексы
Липид-белковые комплексы – сложные белки, простетическую часть которых составляют различные липидные компоненты. К таким компонентам относятся:
1. предельные и непредельные В
Нуклеопротеины
Нуклеопротеины – это сложные белки, содержащие в качестве небольшой части нуклеиновые кислоты (до 65%).
НП состоят из 2-х частей: белковой (содержит гистоны и протамины, кото
Углевод-белковые комплексы
В качестве простетической группы выступают углеводы. Все углевод-белковые комплексы делятся на гликопротеины и протеогликаны.
Гликопротеины (ГП)– комплекс белков с углеводными ко
Фосфопротеины
Белки, где в качестве простетической группы – фосфорная кислота. Присоединение фосфорной кислоты к полипептидной цепи идет с образованием сложноэфирной связи с АК СЕР или ТРЕ.
Изоферменты
Изоферменты – это изофункциональные белки. Они катализируют одну и ту же реакцию, но отличаются по некоторым функциональным свойствам в силу отличий по:
- аминокислотному составу;
Свойства ферментов
Общие черты ферментов и небиологических катализаторов:
1) и те, и другие катализируют только энергетически возможные реакции;
2) увеличивают скорость реакции;
3) н
Номенклатура ферментов
1) Существует тривиальная номенклатура – названия случайные, без системы и основания, например трипсин, пепсин, химотрипсин.
2) Рабочая номенклатура – название фермента составляется из наз
Современные представления о ферментативном катализе
Первая теория ферментативного катализа была выдвинута в начале 20 века Варбургом и Бейлисом. Эта теория предлагала считать, что фермент адсорбирует на себе субстрат, и называлась адсорбционной, но
Молекулярные эффекты действия ферментов
1) Эффект концентрирования – это адсорбирование на поверхности молекулы фермента молекул реагирующих веществ, т.е. субстрата, что приводит к их лучшему взаимодействию. Пр.: электростатическое притя
Теория кислотно-основного катализа
В составе активного центра фермента имеются как кислые, так и основные функциональные группы. В результате этого фермент проявляет в ходе катализа кислотно-основные свойства, т.е. играет как роль д
Регуляция активности ферментов
Ферменты являются регулируемыми катализаторами. В качестве регуляторов могут выступать метаболиты, яды. Различают:
- активаторы – вещества, увеличивающие скорость реакции;
Переваривание и всасывание белков
Функции белков многообразны, но особенно выделяются структурная, каталитическая и энергетическая функции. Энергетическая ценность белка около 4,1 ккал/г.
Среди всех веществ, поступающих в
Превращение белков в органах пищеварения
Все белки подвергаются действию гидролаз (третий класс ферментов), а именно пептидаз – они, как правило, вырабатываются в неактивной форме, а затем активируются путем частичного протеолиза.
Переваривание сложных белков и их катаболизм
1. Гликопротеины гидролизуются с помощью гликозидаз (амилолитических ферментов).
2. Липопротеины – с помощью липолитических ферментов.
3. Гемсодержащие хромопроте
Гниение белков и обезвреживание его продуктов
Гниение белков – это бактериальный распад белковых веществ и АК под действием микрофлоры кишечника. Идет в толстой кишке, однако может наблюдаться и в желудке – при снижении кислотнос
Метаболизм аминокислот
Фонд АК организма пополняется за счет процессов:
1) гидролиза белков пищи,
2) гидролиза тканевых белков (под действием катепсинов лизосом).
Расходуется АК-фонд на процесс
Общие пути обмена веществ
1. Переаминирование (открыто в 1937 г. Браунштейном и Крицмом).
Временное обезвреживание аммиака
Аммиак токсичен (50 мг аммиака убивает кролика, при этом [NH3]=0,4-0,7 мг/л). Поэтому в тканях аммиак обезвреживается временными путями:
1) в основном – образов
Орнитиновый цикл мочевинообразования
Мочевина содержит 80-90% всего азота мочи. В сутки образуется 25-30 г мочевины NH2-CO-NH2.
1. NH3 + CO
Синтез и распад нуклеотидов
Особенности обмена нуклеотидов:
1. Ни сами нуклеотиды, ни азотистые основания, поступающие с пищей, не включаются в синтез нуклеиновых кислот и нуклеотидов организма. Т.е., нуклеотиды пищи
А. Окисление пуриновых нуклеозидов
Аденозин® (аденозиндезаминаза, +Н2О, –NH4+) инозин® (пуриннуклеозидфосфорилаза, +Фн –рибозил-1-Ф) гипоксантин (6-оксопурин) ® (ксантинокси
Функционирование ДЦ
Субстрат·Н2 → НАД → ФМН → КоQ → 2b → 2c1→ 2c → 2a → 2a3 → O
Репликация (самоудвоение, биосинтез) ДНК
В 1953 г. Уотсон и Крик открыли принцип комплементарности (взаимодополняемости). Так, А=Т, а ГºЦ.
Условия, необходимые для репликации:
1. стр
Транскрипция (передача информации с ДНК на РНК) или биосинтез РНК
При транскрипции, в отличие от репликации, информации передается с небольшого участка ДНК. Элементарной единицей транскрипции является оперон (транскриптон)- участок ДНК, подвергающийся тран
Регуляция биосинтеза белка
Клетки многоклеточного организма содержат одинаковый набор ДНК, но белки синтезируются разные. Например, соединительная ткань активно синтезирует коллаген, а в мышечных клетках такого белка нет. В
Механизмы развития раковой опухоли
Рак – генетическое заболевание, т.е. повреждение генов.
Виды повреждений генов:
1) потеря гена,
2) собственно повреждение гена,
3) активация гена,
Переваривание липидов
Поступая с пищей, липиды в ротовой полости подвергаются только механической обработке. Липолитические ферменты в ротовой полости не образуются. Переваривание липидов будет происходить в тех отделах
Механизм ресинтеза жира
Ресинтез жира в стенке кишечника происходит следующим образом:
1. сначала продукты гидролиза (глицерин, ВЖК) активируются с использованием АТФ. Далее происходит последовательное ацилирован
Транспортные формы липидов в организме
Липиды являются нерастворимыми в воде соединениями, поэтому для их переноса кровью необходимы специальные переносчики, растворимые в воде. Такими транспортными формами являются липопротеины плазмы
Превращение липидов в тканях
В тканях постоянно идут процессы распада и синтеза липидов. Основную массу липидов организма человека составляют ТГ, которые в клетке имеются в виде включений. Период обновления ТГ в разных тканях
Биосинтез глицерина и ВЖК в тканях
Биосинтез глицерина в тканях тесно связан с метаболизмом глюкозы, которая в результате катаболизма проходит стадии образования триоз. Глицеральдегид–3–фосфат в цитоплазме по
Патология липидного обмена
На этапе поступления с пищей. Обильная жирная пища на фоне гиподинамии ведёт к развитию алиментарного ожирения. Нарушение обмена может быть связано с недостаточным поступлением жир
Ионы Са2+.
Образуют соединение с белком - кальмодулин. Комплекс Са2+-кальмодулин активирует ферменты (аденилатциклазу, фосфодиэстеразу, Са2+-зависимую протеинкиназу). Есть группа
Гормоны паращитовидных желез
Парат-гормон, состоит из 84 АК, регулирует уровень Са2+, стимулирует выход кальция (и фосфора) из костей в кровь; Повышают реабсорбцию кальция в почках, но стимулируется выход фосфора; С
Роль витаминов в обмене веществ
1.(!) витамины – предшественники коферментов и простетических групп ферментов.
Напр., В1 – тиамин – входит в состав кофермента декарбоксилаз кетокислот в виде ТПФ (ТДФ), В2 – рибофлавин –
Понятие о гиповитаминозах, авитаминозах и гипервитаминозах
Гиповитаминоз – патологическое состояние, связанное с недостатком витамина в организме.
Авитаминоз – патологическое состояние, вызванное отсутствием витамина в организме.
Причины гиповитаминозов
1. Первичные: недостаток витамина в пище.
2. Вторичные:
а) снижение аппетита;
б) повышенный расход витаминов;
в) нарушения всасывания и утилизации, напр., энтеро
Витамин А
Витамеры: А1 – ретинол и А2 – ретиналь.
Клиническое название: антиксерофтальмический витамин.
По химической природе: циклический непредельный одноатомный спирт на основе кольца b-
Витамин D
Антирахитический витамин. Существуют два витамера:
D2 – эргокальциферол и D3 – холекальциферол.
Витамин D2 содержится в грибах. Витамин D3 синтезируется в орг
Витамин Е
Устар.: антистерильный витамин, антиоксидантный энзим.
В химическом плане это альфа-, бета-, гамма- и дельта-токоферолы, но преобладающим является альфа-токоферол.
Витамин Е устой
Витамин К
Антигеморрагический витамин.
Витамеры: К1 – филлохинон и К2 – менахинон.
Роль витамина К в обмене веществ
Это кофактор карбоксилирования глутамино
Витамин С
Аскорбиновая кислота, антискорбутный витамин (скорбут = цинга).
Является лактоном. Легко окисляется:
О=С─┐ О=С─┐
| │ | │
НО-С
Витамин В1
Тиамин, антиневритный витамин.
Тиамин устойчив в кислой среде (до 140ºС), а в щелочной среде бы
Витамин В2
Рибофлавин
Устойчив в кислой среде, но разрушается в нейтральной и щелочной. Легко окисляется по дво
Витамин РР
Антипеллагрический витамин.
Витамеры: никотиновая к-та, никотинамид, ниацин.
Витамин В6
Антидерматитный витамин.
Пиридоксин → пиридоксаль → пиридоксамин [нарисовать формулы]
Витамин В12
Кобаламин. Антианемический витамин.
Имеет красный цвет. На свету разлагается.
Роль кобаламина в обмене веществ
- транспорт метильных групп;
- участвует в
Витамин В3
Пантотеновая кислота. [рис. формулы НОСН2-С((СН3)2)-СН(ОН)-СО-NH-СН2-СН2-СООН]
Состоит из масляной кислоты с b-аланином.
Гидроксилирование ксенобиотиков с участием микросомальной монооксигеназной системы
1. бензола:
[рис. бензол+ О2 +НАДФН2®(гидроксилаза, цитохром Р450) фенол + НАДФ+ Н2О]
2. индола:
[рис. индол+ О2 +Н
Роль печени в пигментном обмене
Пигментный обмен представляет собой совокупность сложных взаимопревращений окрашенных веществ тканей и жидкостей организма человека.
К пигментам относятся 4 группы веществ:
1. гем
Биосинтез гема
Биосинтез гема идет в большинстве тканей, за исключением эритроцитов, которые не имеют митохондрий. В организме человека гем синтезируется из глицина и сукцинил-КоА, образованного в результате мета
Распад гема
Большая часть гемхромагенных пигментов в организме человека образуется при распаде гема. Главным источником гема является гемоглобин. В эритроцитах содержание гемоглобина составляет 80%, время жизн
Патология пигментного обмена
Как правило, связана с нарушением процессов катаболизма гема и выражается гипербилирубинемией и проявляется в желтушечности кожи и видимых слизистых оболочек. Накапливаясь в ЦНС, билирубин вызывает
Типы изменения биохимического состава крови
I. Абсолютные и относительные.
Абсолютные обусловлены нарушением синтеза, распада, выведения того или иного соединения.
Относительные обусловлены изменением объема ц
Белковый состав крови
Функции белков крови:
1. поддерживают онкотическое давление (в основном за счет альбуминов);
2. определяют вязкость плазмы крови (в основном за счет альбуминов);
Общий белок
В норме общий белок крови 65-85 г/л.
Общий белок – это сумма всех белковых веществ крови.
► Гипопротеинемия – снижение альбуминов. Причины:
Глобулины в норме 20-30 г/л
I. α1 -глобулины
α-антитрипсин – ингибирует трипсин, пепсин, эластазу, некоторые другие протеазы крови. Выполняет антивоспалитель
Остаточный азот
Остаточный азот – это сумма азота всех небелковых азотсодержащих веществ крови. В норме 14-28 ммоль/л.
1. Метаболиты:
1.1. аминокислоты (25%);
1.2. креат
Углеводный обмен
Глюкоза в капиллярной крови натощак 3,3-5,5 ммоль/л.
1. Гипергликемия (повышение глюкозы):
1.1. панкреатическая гипергликемия – при отсутствии инсул
Липидный обмен
Холестерин в норме 3-5,2 ммоль/л. В плазме находится в составе ЛПНП, ЛПОНП (атерогенные фракции) и ЛПВП (антиатерогенная фракция). Вероятность развития атеросклероза
Минеральный обмен
Натрий – это основной внеклеточный ион. На уровень Na+ в крови влияют минералокортикоиды (альдостерон задерживает натрий в почках). Уровень натрия увеличивается за счет гем
Ферменты плазмы крови
Классифицируются:
1. Функционирующие ферменты (собственно плазменные). Напр., ренин (повышает АД через ангиотензин II), холинестераза (расщепляет ацетилхолин). Их активность выше в
Физические свойства мочи здорового человека, их изменения при патологии
I. Количество мочи в норме 1,2-1,5 л.
► Полиурия – увеличение количества мочи из-за:
1) увеличения фильтрации (под действием адреналина увеличивается фи
Показатели химического состава мочи
Общий азот – это совокупность азота всех азотсодержащих веществ в моче. В норме – 10-16 г/сутки. При патологиях общий азот может:
ü увеличиваться – гиперазотурия
Особенности обмена веществ в нервной ткани
Энергетический обмен.
В ткани головного мозга увеличено клеточное дыхание (преобладают аэробные процессы). Мозг потребляет большее количество кислорода, чем постоянно работающее сер
Химическая передача нервного возбуждения
Передача возбуждения с одной клетки на другую происходит с помощью нейромедиаторов:
- нейропептидов;
- АК;
- ацетилхолина;
- биогенных аминов (адреналин,
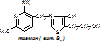
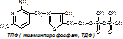





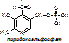







Новости и инфо для студентов