рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Образование
- /
- Концепция теории резонанса (Полинг, 1928 г.).
Реферат Курсовая Конспект
Концепция теории резонанса (Полинг, 1928 г.).
Концепция теории резонанса (Полинг, 1928 г.). - раздел Образование, ОСНОВНЫЕ ПОНЯТИЯ О РЕАКЦИОННОЙ СПОСОБНОСТИ ОРГАНИЧЕСКИХ МОЛЕКУЛ Представление К. Ингольда О Мезомерии Вошли Как Составная Часть В ...
Представление К. Ингольда о мезомерии вошли как составная часть в теорию резонанса, разработанную в 1928–1938 г. Л. Полингом. Согласно Полингу, молекулу можно описать как быстро флуктуирующую структуру между двумя электронными формулами (резонирующими структурами) и приобретающими стабильность большую, чем любая из формул, благодаря резонансной энергии этой флуктуации. Реальная молекула описывается как "резонансный гибрид", в котором распределение электронной плотности является промежуточным между распределением электронной плотности в резонансных гибридных структурах. Сопряженные системы изображают с помощью набора резонансных структур, объединяемых резонансной стрелкой. Реальная структура есть результат суперпозиции нескольких резонансных структур:

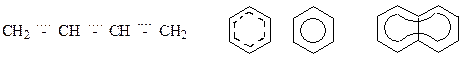
· Бензол может быть изображен пятью резонансными структурами:

· Основные резонансные структуры анилина следующие:

3. Делокализованное π-облако изображается пунктиром (в цикле – сплошной линией).
Концепция мезомерии – резонанса является способом реального электронного строения молекул с помощью граничных структур. Резонансные формулы обладают хорошей наглядностью и позволяют подчеркивать особенности электронной структуры. Дальнейшее развитие представлений о взаимодействии связей и перераспределении электронной плотности в сопряженных молекулах нашло свое воплощение в квантовой органической химии.
Таблица 9 – Соотношение индуктивных и мезомерных эффектов заместителей
| Заместитель | I эффект | М эффект | ЭД- или ЭА- влияние заместителя |
| Алкилы | + I | – | ЭД |
| СН3–, С2Н5– | –I | – | ЭА |
| –ОН | –I | +М | ЭД (+М > –I) |
| –ОСН3 | –I | +М | ЭД (+М > –I) |
| –NH2 | –I | +М | ЭД (+М > –I) |

| –I | –М | ЭА |

| –I | –М | ЭА |

| –I | –М | ЭА |

| –I | –М | ЭА |
| –Cl, –Br, –I | –I | + М | ЭА (+М < –I) |
Электронное строение сопряженных систем. Сопряженная система – система sp2 гибридизованных атомов с общим копланарным σ-скелетом с делокализованным π-облаком и обладающая повышенной термодинами-ческой устойчивостью.

Сопряжение–взаимное перекрывание рz-орбиталей нескольких π- или π, р-систем, приводящее к делокализации π-электронного облака и повышению термодинамической устойчивости.
Энергия сопряжения ER(мера термодинамической устойчивости) – разность энергий образования реально существующей сопряженной молекулы и соответствующей молекулы (реальной или гипотетической) с изолированными двойными связями.
· Пентадиен – 1,3 (I) 

· Пентадиен – 1,4 (II) СН2 = СН – СН2 – СН = СН2

· Бензол

Типы сопряжения. π,π-сопряжение–в сопряжении участвуют π-электроны нескольких π-систем (не менее 4-х центров).

р, π-сопряжение – в сопряжении участвуют π-электроны π-системы и р-электроны на pz-орбитали гетероатома (не менее 3-х центров).

Ароматическая система – замкнутая сопряженная система рz- орбиталей с делокализованными π- или р-электронами, число которых соответствует формуле Хюккеля.
Условия сопряжения. Для ациклических сопряженных систем:
· sp2 гибридизация всех атомов в сопряженном фрагменте;
· копланарность общего σ-скелета, валентный угол 120о.
Для ароматических систем:
· наличие цикла;
· sp2 гибридизация всех атомов в цикле;
· копланарность σ-скелета, отсутствие углового напряжения, валентный угол 120о;
· Число делокализованных электронов должно соответствовать формуле Хюккеля:
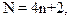
где n – целое число; N – число делокализованных электронов.
– Конец работы –
Эта тема принадлежит разделу:
ОСНОВНЫЕ ПОНЯТИЯ О РЕАКЦИОННОЙ СПОСОБНОСТИ ОРГАНИЧЕСКИХ МОЛЕКУЛ
Концепция теории мезомерии... Делокализацию электронов изображают стрелками...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Концепция теории резонанса (Полинг, 1928 г.).
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов