рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Образование
- /
- Кислотность и основность по Бренстеду-Лоури.
Реферат Курсовая Конспект
Кислотность и основность по Бренстеду-Лоури.
Кислотность и основность по Бренстеду-Лоури. - раздел Образование, ОСНОВНЫЕ ПОНЯТИЯ О РЕАКЦИОННОЙ СПОСОБНОСТИ ОРГАНИЧЕСКИХ МОЛЕКУЛ Кислоты –Вещества, Способные Отдавать Протон (Доноры Про...
Кислоты –вещества, способные отдавать протон (доноры протона).
Основания – вещества, способные присоединять протон (акцепторы протона).
Таблица 13 – Типы органических кислот по Бренстеду.
| Тип кислоты | Нейтральные молекулы | Положительно заряженные ионы | ||
| Класс соединения | Формула | Класс соединения | Формула | |
| CH | Углеводороды | 
| σ-комплекс |

|
| NH | Амины Амиды | 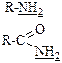
| Алкиламмоний | 
|
| OH | Спирты Фенолы Енолы Карбоновые кислоты Сульфоновые кислоты | 
| Алкилоксоний Арилоксоний |
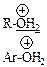
|
| SH | Тиолы | 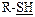
| – | – |
Таблица 14 – Типы органических оснований по Бренстеду.
| Тип основания | Нейтральные молекулы | Отрицательно заряженные ионы | |||
| Класс соединения | Формула | Класс соединения | Формула | ||
| π- | Алкены | 
| карбанион | 
| |
| Продолжение таблицы 14 | |||||
| π- | Алкины Арены |

| карбанион | 
| |
| n- | аммониевые- | амины азометины нитрилы | 
| амид-ион |
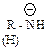
|
| оксониевые- | спирты простые эфиры альдегиды, кетоны карбоновые кислоты | 
| алкоксид-ион карбоксилат-ион | 

| |
| сульфониевые- | тиолы сульфиды | 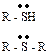
| сульфид-ион | 
| |
| – | – | – | гидрид-ион | 
|
Количественная сравнительная оценка кислотности и основно-сти. Оценивается на основании уравнения кислотно-основного взаимодействия, одним из компонентов которого является растворитель (вода или неводные растворители – ледяная CH3COOH, формамид, диметилформамид, ДМСО и др.).


а – [ от англ. acid – кислота ]; в – [от англ. base – основание]

Качественная сравнительная оценка кислотности и основности органических соединений.Проводится с позиций статического и кинетического факторов.
Статический фактор, обуславливающий собственную кислотность или основность соединения в соответствии с его электронным строением в нереагирующем состоянии. Ка и Кв определяются в газовой фазе.
Кинетический фактор, обуславливающий кислотные и основные свойства в соответствии со стабильностью сопряженных оснований (анион) и кислот (катион), образующихся в результате кислотно-основного взаимодействия.
Таблица 15 – Факторы, определяющие степень кислотности и основности
| Факторы, определяющие степень кислотности и основности | В газовой фазе | В растворах |
| - Электроотрицательность атома кислотного или основного центра. - Поляризуемость атома. - Электронные эффекты заместителей. - Стерические эффекты. - Орто- эффект. - Эффект сольватации. | + + + + + – | + + + + + + |
– Конец работы –
Эта тема принадлежит разделу:
ОСНОВНЫЕ ПОНЯТИЯ О РЕАКЦИОННОЙ СПОСОБНОСТИ ОРГАНИЧЕСКИХ МОЛЕКУЛ
Концепция теории мезомерии... Делокализацию электронов изображают стрелками...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Кислотность и основность по Бренстеду-Лоури.
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов