рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Образование
- /
- Бактериальные эндотоксины.
Реферат Курсовая Конспект
Бактериальные эндотоксины.
Бактериальные эндотоксины. - раздел Образование, МЕТОДИЧЕСКИЕ УКАЗАНИЯ Содержание Бактериальных Эндотоксинов В 1 Г Препарата Не Более 5 Еэ. ...
Содержание бактериальных эндотоксинов в 1 г препарата не более 5 ЕЭ.
Примечание: Тест «Пирогенность» или «Бактериальные эндотоксины» проводят для препарата, используемого для приготовления инъекционных лекарственных форм.
Микробиологическая чистота. Испытания проводят в соответствии с требованиями ГФ XI, вып. 2, с. 193 и Изменения № 3, категория 1.2.Б.
Количественное определение. Не менее 99,5 % и не более 100,5 % в пересчете на сухое вещество.
Около 0,1 г препарата (точная навеска растворяют в 20 мл воды и титруют 0,1 М раствором серебра нитрата до оранжево-желтого окрашивания (индикатор - 0,5 мл 5 % раствора калия хромата). 1 мл 0,1 М раствора серебра нитрата соответствует 0,005844 г NaCl.
Параллельно проводят контрольный опыт.
Упаковка. По 1, 2, 5, 10, 20, 40 кг в пакеты из пленки полиэтиленовой нестабилизированной по ГОСТ 10354-82, снабженные этикетками из бумаги этикеточной по ГОСТ 7625-86 или писчей по ГОСТ 18510-87.
Вторичная и транспортная тара в соответствии с РД 9301-006-05749470-93.
Маркировка. На этикетке указывают предприятие-изготовитель адрес, тел./факс, E-mail, название препарата, субстанция, количество, условия хранения, регистрационный номер, номер серии, срок годности, назначение.
Маркировка транспортной тары в соответствии с ГОСТ 14192-96.
Транспортирование. В соответствии с РД 9301-006-05749470-93.
Хранение. В хорошо укупоренной таре, в сухом месте.
Срок годности. 5 лет.
Для приготовления стерильных и нестерильных лекарственных форм.
Примечание. Реактивы, титрованные растворы и индикаторы, приведенные в настоящей фармакопейной статье предприятия, описаны в соответствующих разделах Государственной фармакопеи XI издания, вып. 2.
Напроксен(ФС 42-0259-07)
(S)-2-(6-Метокси-2-нафтил)пропионовая кислота
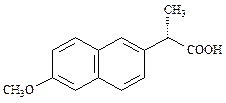
| C14H14O3 | М.м. 230,27 |
Cодержит не менее 98,5 % C14H14O3 в пересчете на сухое вещество.
Описание. Белый или почти белый кристаллический порошок.
Растворимость. Практически нерастворим в воде, растворим в спирте 96 % и метаноле, мало растворим в эфире.
Подлинность. Инфракрасный спектр субстанции, снятый в диске с калия бромидом, в области от 4000 до 400 см-1 по положению полос поглощения должен соответствовать спектру стандартного образца напроксена.
0,01 г субстанции растворяют в метаноле и разбавляют метанолом до 100 мл. 10 мл полученного раствора разбавляют метанолом до 25 мл. Ультрафиолетовый спектр поглощения полученного раствора в области от 220 до 350 нм должен иметь максимумы при 262 нм, 271 нм, 316 нм и 331 нм.
Температура плавления. От 154 до 158 ºС.
Удельное вращение.От + 63 до + 68,5 º в пересчете на сухое вещество (2 % раствор субстанции в хлороформе).
Прозрачность раствора. Раствор 1,25 г субстанции в 25 мл метанола должен быть прозрачным или выдерживать сравнение с эталоном 1.
Цветность раствора. Раствор, полученный в испытании на Прозрачность раствора, должен выдерживать сравнение с эталоном ВY7.
Посторонние примеси. Определение проводят методом ТСХ.
Испытуемый раствор. 0,25 г субстанции растворяют в метаноле и разбавляют метанолом до 5 мл.
Раствор сравнения. 0,5 мл испытуемого раствора разбавляют метанолом до 100 мл.
Раствор для опрыскивания. 0,02 г диметиламинобензальдегида растворяют в 20 мл спирта 96 % и прибавляют 0,5 мл хлористоводородной кислоты концентрированной.
На линию старта пластинки со слоем силикагеля 60 F254 наносят 10 мкл (500 мкг) испытуемого раствора, 10 мкл (2,5 мкг) и 5 мкл (1,25 мкг) раствора сравнения. Пластинку с нанесенными пробами сушат на воздухе, помещают в камеру со смесью уксусная кислота ледяная – тетрагидрофуран – толуол (1:3:30) и хроматографируют восходящим методом. Когда фронт подвижной фазы дойдет до конца пластинки, ее вынимают из камеры, сушат на воздухе и просматривают в УФ свете при 254 нм.
Любое пятно посторонней примеси на хроматограмме испытуемого раствора по совокупности величины и интенсивности поглощения не должно превышать пятно на хроматограмме раствора сравнения (не более 0,5 %). Суммарное содержание примесей должно быть не более 1 %.
Результаты испытания считаются достоверными, если на хроматограмме раствора сравнения (1,25 мкг) четко видно пятно.
Потеря в массе при высушивании. Около 1,0 г (точная навеска) субстанции сушат при температуре от 100 до 105 ºС до постоянной массы. Потеря в массе не должна превышать 0,5 %.
Сульфатная зола и тяжелые металлы. Сульфатная зола из 1,0 г (точная навеска) субстанции не должна превышать 0,1 % и должна выдерживать испытание на тяжелые металлы (не более 0,001 % в субстанции).
Остаточные органические растворители.Всоответствии с требованиями ОФС «Остаточные органические растворители».
Микробиологическая чистота.В соответствии с требованиями ОФС «Микробиологическая чистота».
Количественное определение. Около 0,2 г (точная навеска) субстанции растворяют в смеси 25 мл воды и 75 мл метанола и титруют 0,1 М раствором натрия гидроксида, используя 1 мл 1 % раствора фенолфталеина в качестве индикатора.
1 мл 0,1 М раствора натрия гидроксида соответствует 23,03 мг C14H14O3.
Хранение. Список Б. В сухом, защищенном от света месте.
Новокаина гидрохлорид(ФС 42-0265-07)
[2-(Диэтиламино)этил]-4-аминобензоата гидрохлорид
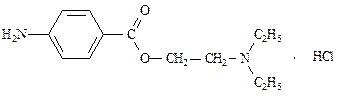
| C13H20N2O2·HCl | М.м. 272,78 |
Cодержит не менее 99,5 % и не более 101,0 % C13H20N2O2·HCl в пересчете на сухое вещество.
Описание.Белый кристаллический порошок или бесцветные кристаллы.
Растворимость. Очень легко растворим в воде, растворим в спирте
96 %, мало растворим в хлороформе.
Подлинность. Инфракрасный спектр субстанции, снятый в диске с калия бромидом, в области от 4000 до 400 см-1 по положению полос поглощения должен соответствовать рисунку спектра новокаина гидрохлорида.
0,05 г субстанции растворяют в 2 мл воды. Раствор дает характерную реакцию на первичные ароматические амины с образованием оранжево-красного окрашивания, переходящего в вишнево-красное.
0,05 г субстанции растворяют в 2 мл воды, прибавляют 0,15 мл серной кислоты разведенной 16 % и 1 мл 0,1 М раствора калия перманганата; фиолетовое окрашивание сразу исчезает.
Субстанция дает характерную реакцию на хлориды.
Температура плавления. От 154 до 158 ºС.
Прозрачность раствора. Раствор 1 г субстанции в 10 мл воды должен быть прозрачным или выдерживать сравнение с эталоном I.
Цветность раствора. Раствор, полученный в испытании на Прозрачность раствора, должен быть бесцветным или выдерживать сравнение с эталоном В9.
рН. От 6,0 до 7,5 (1 % раствор).
Посторонние примеси. Определение проводят методом ТСХ.
Испытуемый раствор. 0,2 г субстанции растворяют в 0,6 мл воды и разбавляют спиртом 96 % до 10 мл.
Раствор сравнения. 0,01 г 4-аминобензойной кислоты и 0,01 г анестезина растворяют в 100 мл спирта 96 %. 1 мл полученного раствора разбавляют спиртом 96 % до 10 мл.
На линию старта пластинки со слоем силикагеля 60 F254 наносят 20 мкл (400 мкг) испытуемого раствора и 20 мкл (0,2 мкг 4-аминобензойзойной кислоты и 0,2 мкг анестезина) раствора сравнения. Пластинку с нанесенными пробами сушат на воздухе, помещают в камеру со смесью бензол - ацетон (4:1) и хроматографируют восходящим методом. Когда фронт подвижной фазы дойдет до конца пластинки, ее вынимают из камеры, сушат на воздухе и просматривают в УФ свете при 254 нм.
Пятна посторонних примесей на хроматограмме испытуемого раствора, находящиеся на уровне пятен 4-аминобензойной кислоты и анестезина, по совокупности величины и интенсивности поглощения не должны превышать соответствующие пятна на хроматограмме раствора сравнения (не более
0,05 % каждой примеси).
Потеря в массе при высушивании. Около 1,0 г (точная навеска) субстанции сушат при температуре от 100 до 105 ºС до постоянной массы. Потеря в массе не должна превышать 0,5 %.
Сульфатная зола и тяжелые металлы. Сульфатная зола из 1,0 г (точная навеска) субстанции не должна превышать 0,1 % и должна выдерживать испытание на тяжелые металлы (не более 0,001 % в субстанции).
Остаточные органические растворители.Всоответствии с требованиями ОФС «Остаточные органические растворители».
Бактериальные эндотоксины. Не более 0,14 ЕЭ на 1 мг субстанции.
Для проведения испытания готовят исходный раствор субстанции (концентрация 100 мг/мл), а затем разводят его не менее чем в 400 раз.
Испытание проводят для субстанции, предназначенной для приготовления стерильных лекарственных форм.
Микробиологическая чистота.В соответствии с требованиями ОФС «Микробиологическая чистота».
Количественное определение. Около 0,3 г (точная навеска) субстанции растворяют в смеси 10 мл воды и 10 мл хлористоводородной кислоты разведенной 8,3 %. Полученный раствор титруют нитритометрически. Параллельно проводят контрольный опыт.
1 мл 0,1 М раствора натрия нитрита соответствует 27,28 мг C13H20N2O2·HCl.
Хранение. Список Б. В сухом, защищенном от света месте.
Пропранолола гидрохлорид(ФС 42-0273-07)
(RS)-1-(Изопропиламино)-3-(1-нафтилокси)пропан-2-ола гидрохлорид
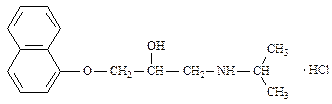
| C16H21NO2 . HCl | М.м. 295,81 |
Cодержит не менее 99,0 % и не более 101,0 % C16H21NO2 . HCl в пересчете на сухое вещество.
Описание. Белый или почти белый порошок.
Растворимость. Растворим в воде и спирте 96 %.
Подлинность. Инфракрасный спектр субстанции, снятый в диске с калия бромидом, в области от 4000 до 400 см-1 по положению полос поглощения должен соответствовать спектру стандартного образца пропранолола гидрохлорида.
Субстанция дает характерную реакцию на хлориды.
Температура плавления. От 163 до 166 ºС (метод 1а).
Прозрачность раствора. Раствор 1 г субстанции в 10 мл метанола должен быть прозрачным или выдерживать сравнение с эталоном I.
Цветность раствора. Раствор, полученный в испытании на Прозрачность раствора, должен выдерживать сравнение с эталоном Y6.
Кислотность или щелочность.0,2 г субстанции растворяют в 20 мл свежепрокипяченной и охлажденной воды, прибавляют 0,2 мл раствора метилового красного и 0,2 мл 0,01 М раствора хлористоводородной кислоты; раствор становится красным. Прибавляют 0,4 мл 0,01 М раствора натрия гидроксида; раствор становится желтым.
Посторонние примеси. Определение проводят методом ВЭЖХ.
Подвижная фаза (ПФ). 1,6 г натрия лаурилсульфата и 0,31 г тетрабутиламмония дигидрофосфата растворяют в смеси 450 мл воды, 550 мл ацетонитрила и 1 мл серной кислоты концентрированной и доводят рН раствора раствором натра едкого до 3,3.
Испытуемый раствор. 0,02 г субстанции растворяют в 10 мл ПФ.
Раствор сравнения. 1 мл испытуемого раствора помещают в мерную колбу вместимостью 50 мл, доводят объем раствора ПФ до метки и перемешивают. 1 мл полученного раствора переносят в мерную колбу вместимостью 10 мл, доводят объем раствора ПФ до метки и перемешивают.
Раствор для проверки пригодности системы. 0,01 г стандартной смеси пропранолола гидрохлорида и примесей (Propranolol hydrochloride for performance test CRS, стандарт ВР) растворяют в 10 мл ПФ.
Хроматографические условия
| Колонка | - | 25 × 0,46 см с октадецилсилил силикагелем (С18), 5 мкм; |
| Скорость потока | - | 1,8 мл/мин; |
| Детектор | - | спектрофотометрический, 292 нм; |
| Объем пробы | - | 20 мкл. |
Хроматографируют раствор для проверки пригодности системы. Полученная хроматограмма по виду и параметрам разделения должна соответствовать хроматограмме, прилагаемой к образцу стандартной смеси.
Хроматографируют раствор сравнения и испытуемый раствор. Время регистрации хроматограммы испытуемого раствора должно не менее чем в 5 раз превышать время удерживания основного пика.
На хроматограмме испытуемого раствора площадь пика любой посторонней примеси должна быть не более половины площади пика пропранолола на хроматограмме раствора сравнения (не более 0,1 %); суммарная площадь пиков посторонних примесей не должна более чем в 2 раза превышать площадь пика пропранолола на хроматограмме раствора сравнения (не более 0,4 %).
Потеря в массе при высушивании. Около 1 г (точная навеска) субстанции сушат при температуре от 100 до 105 ºС до постоянной массы. Потеря в массе не должна превышать 0,5 %.
Сульфатная зола.Не более 0,1 %. Определение проводят из точной навески субстанции около 1 г.
Тяжелые металлы. Сульфатная зола из 0,5 г субстанции должна выдерживать испытание на тяжелые металлы (не более 0,002 % в субстанции).
Остаточные органические растворители.Всоответствии с требованиями ОФС «Остаточные органические растворители»
Микробиологическая чистота.В соответствии с требованиями ОФС «Микробиологическая чистота».
Количественное определение. Около 0,25 г (точная навеска) субстанции растворяют в 25 мл спирта 96 % и титруют 0,1 М раствором натрия гидроксида. Конечную точку титрования определяют потенциометри-чески.
1 мл 0,1 М раствора натрия гидроксида соответствует 29,58 мг
C16H21NO2 . HCl.
Хранение. Список Б. В плотно закрытой упаковке в защищенном от света месте.
Рибоксин(ФС 42-0275-07)
9-(b-D-Рибофуранозил)-1H-пурин-6(9H)-он
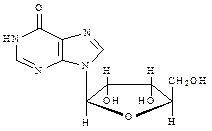
| C10H12N4O5 | М.м. 268,22 |
Cодержит не менее 96,0% и не более 102,0 % C10H12N4O5 в пересчете на сухое вещество.
Описание. Белый или почти белый кристаллический порошок.
Растворимость. Умеренно (медленно) растворим в воде, очень мало растворим в спирте 96 %, практически нерастворим в хлороформе.
Подлинность. Инфракрасный спектр субстанции, снятый в диске с калия бромидом, в области от 4000 до 400 см-1 по положению полос поглощения должен соответствовать спектру ГСО рибоксина.
Время удерживания основного пика на хроматограмме испытуемого раствора (раздел «Количественное определение») должно соответствовать времени удерживания основного пика на хроматограмме стандартного раствора.
0,1 г субстанции растворяют в 20 мл воды. К 2 мл полученного раствора прибавляют 5 мл 0,1 % раствора железа(III) хлорида в хлористоводородной кислоте концентрированной и 5 мл 10 % раствора орцина в спирте 96 %. Смесь выдерживают в течение 20 мин в кипящей водяной бане; появляется зеленое окрашивание.
Прозрачность раствора. Раствор 0,1 г субстанции в 10 мл воды должен быть прозрачным или выдерживать сравнение с эталоном I.
Цветность раствора. Раствор, полученный в испытании на Прозрачность раствора, должен быть бесцветным или выдерживать сравнение с эталоном B9.
Удельное вращение. От –47 до –54 º в пересчете на сухое вещество
(1 % раствор субстанции).
рН.От 4,8до 5,8 (1 % раствор).
Посторонние примеси. Определение проводят методом ВЭЖХ в условиях, описанных в разделе «Количественное определение».
Испытуемый раствор. 0,05 г субстанции растворяют в 50 мл ПФ.
Раствор сравнения. 1 мл испытуемого раствора помещают в мерную колбу вместимостью 100 мл, доводят объем раствора ПФ до метки и перемешивают.
Хроматографируют раствор сравнения и испытуемый раствор. Время регистрации хроматограммы испытуемого раствора должно не менее чем в 2 раза превышать время удерживания основного пика. Примеси гуанозина и гипоксантина на хроматограмме испытуемого раствора идентифицируют по хроматограмме раствора для проверки пригодности системы.
Сумма площадей пиков гуанозина и гипоксантина на хроматограмме испытуемого раствора не должна более чем в 2,5 раза превышать площадь пика на хроматограмме раствора сравнения (не более 2,5 %), сумма площадей пиков неидентифицированных примесей должна быть не более половины площади пика на хроматограмме раствора сравнения (не более 0,5 %).
Потеря в массе при высушивании. Около 1 г (точная навеска) субстанции сушат при температуре от 100 до 105 ºС до постоянной массы. Потеря в массе не должна превышать 1,0 %.
Сульфатная зола и тяжелые металлы. Сульфатная зола из 1 г (точная навеска) субстанции не должна превышать 0,1 % и должна выдерживать испытание на тяжелые металлы (не более 0,001 % в субстанции).
Железо.Сульфатная зола из 2 г субстанции должна выдерживать испытание на железо (не более 0,0015 % в субстанции).
Медь.1,5 г субстанции прокаливают в фарфоровом тигле, остаток растворяют в 5 мл азотной кислоты, разбавляют водой до 15 мл и фильтруют. К 5 мл фильтрата прибавляют 5 мл 10 % раствора аммиака и фильтруют; фильтрат не должен окрашиваться в голубой цвет.
Остаточные органические растворители.Всоответствии с требованиями ОФС «Остаточные органические растворители».
Бактериальные эндотоксины.Не более 0,29 ЕЭ на 1 мг субстанции.
Для проведения испытания готовят исходный раствор субстанции (концентрация 20 мг/мл), а затем разводят его не менее чем в 60 раз.
Испытание проводят для субстанции, предназначенной для приготовления инъекционных лекарственных форм.
Микробиологическая чистота.В соответствии с требованиями ОФС «Микробиологическая чистота».
Количественное определение. Определение проводят методом ВЭЖХ.
Фосфатный буферный раствор с рН 5,5-5,6. 2,72 г калия фосфата однозамещенного растворяют в 700 мл воды, доводят рН раствора раствором калия гидроксида до 5,5-5,6, доводят объем раствора водой до 1000 мл, перемешивают, фильтруют и дегазируют.
Испытуемый раствор. Около 0,05 г (точная навеска) субстанции помещают в мерную колбу вместимостью 50 мл, растворяют в подвижной фазе (ПФ), доводят объем раствора ПФ до метки и перемешивают.
Стандартный раствор. Около 0,05 г (точная навеска) ГСО рибоксина помещают в мерную колбу вместимостью 50 мл, растворяют в ПФ, доводят объем раствора ПФ до метки и перемешивают.
Раствор для проверки пригодности системы. 0,002 г гипоксантина и 0,002 г гуанозина растворяют в 10 мл стандартного раствора.
Хроматографические условия
| Колонка | - | 15 × 0,39 см с октадецилсилил силикагелем (С18), 5 мкм; |
| ПФ | - | фосфатный буферный раствор с рН 5,5-5,6; |
| Температура колонки | - | 50 ºС; |
| Скорость потока | - | 0,6 мл/мин; |
| Детектор | - | спектрофотометрический, 254 нм; |
| Объем пробы | - | 10 мкл. |
Хроматографируют раствор для проверки пригодности системы. Порядок элюирования компонентов: гипоксантин, рибоксин, гуанозин. Разрешение (R) между соседними пиками должно быть не менее 1,25; эффективность колонки (N), рассчитанная для пика рибоксина, должна быть не менее 3400 теоретических тарелок; хвостовой фактор (Т) пика рибоксина должен быть не более 1,1.
Шесть раз хроматографируют стандартный раствор. Относительное стандартное отклонение для площади пика рибоксина должно быть не более 2 %.
Хроматографируют испытуемый и стандартный растворы.
Содержание C10H12N4O5 в субстанции в пересчете на сухое вещество в процентах (Х) рассчитывают по формуле:
S1 × а0 × Р × 100
X = ————––––––––
S0 × a1 × (100-W)
| где | S1 | - | площадь пика рибоксина на хроматограмме испытуемого раствора; |
| S0 | - | площадь пика рибоксина на хроматограмме стандартного раствора; | |
| a1 | - | навеска субстанции в граммах; | |
| а0 | - | навеска ГСО рибоксина в граммах; | |
| Р | - | содержание C10H12N4O5 в ГСО рибоксина в процентах; | |
| W | - | потеря в массе при высушивании субстанции в процентах. |
Хранение. В сухом, защищенном от света месте.
Сульфадиметоксин(ФС 42-0278-07)
4-Амино-N-(2,6-диметоксипиримидин-4-ил)бензолсульфонамид
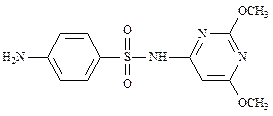
| C12H14N4O4S | М.м. 310,33 |
Cодержит не менее 99,0 % C12H14N4O4S в пересчете на сухое вещество.
Описание. Белый или почти белый кристаллический порошок.
Растворимость. Практически нерастворим в воде, очень мало растворим в хлороформе, мало растворим в спирте 95 %, растворим в хлористоводородной кислоте разведенной 8,3 %, легко растворим в растворах едких щелочей.
Подлинность. Инфракрасный спектр субстанции, снятый в диске с калия бромидом, в области от 4000 до 400 см-1 по положению полос поглощения должен соответствовать спектру стандартного образца сульфадиметоксина.
0,075 г субстанции помещают в мерную колбу вместимостью 100 мл, растворяют в 5 мл 0,1 М раствора натрия гидроксида и доводят объем раствора водой до метки. 5 мл полученного раствора разбавляют водой до 250 мл. По 20 мл полученного раствора помещают в две конические колбы, в первую прибавляют 0,4 мл 0,5 М раствора натрия гидроксида, а во вторую 0,4 мл хлористоводородной кислоты концентрированной.
Ультрафиолетовый спектр поглощения щелочного раствора, снятый относительно кислого раствора, в области от 240 до 280 нм должен иметь максимумы при 253 нм и 268 нм и минимум при 260 нм.
Ультрафиолетовый спектр поглощения кислого раствора, снятый относительно щелочного раствора, в области от 285 до 300 нм должен иметь максимум при 288 нм.
Раствор 0,05 г субстанции в 2 мл хлористоводородной кислоты концентрированной дает характерную реакцию на первичные ароматические амины.
Температура плавления. От 198 до 204 ºС.
Прозрачность раствора. Раствор 0,4 г субстанции в 10 мл 1 М раствора натрия гидроксида должен быть прозрачным или выдерживать сравнение с эталоном I.
Цветность раствора. Раствор, полученный в испытании на Прозрачность раствора, должен быть бесцветным или выдерживать сравнение с эталоном В9.
Кислотность. 1 г субстанции нагревают при температуре 70 ºС с 50 мл воды, свободной от углекислого газа, в течение 5 мин, быстро охлаждают и фильтруют. На титрование 25 мл фильтрата должно пойти не более 0,1 мл 0,1 М раствора натрия гидроксида (индикатор 0,1 мл 0,04 % раствора бромтимолового синего).
Посторонние примеси. Испытание проводят методом ТСХ.
Испытуемый раствор. 0,1 г субстанции растворяют в смеси спирт 96 % - раствор аммиака концентрированный 25 % (9:1) и разбавляют той же смесью до 10 мл.
Раствор сравнения. 0,005 г сульфаниламида растворяют в смеси спирт 96 % - раствор аммиака концентрированный 25 % (9:1) и разбавляют той же смесью до 100 мл.
Раствор для опрыскивания. 0,02 г диметиламинобензальдегида растворяют в 20 мл спирта 96 % и прибавляют 0,5 мл хлористоводородной кислоты концентрированной.
На линию старта пластинки со слоем силикагеля 60 F наносят 10 мкл (100 мкг) испытуемого раствора и 10 мкл (0,5 мкг) раствора сравнения. Пластинку с нанесенными пробами сушат на воздухе, помещают в камеру со смесью хлороформ – метанол – диметилформамид (20:2:1) и хроматографируют восходящим методом. Когда фронт подвижной фазы дойдет до конца пластинки, ее вынимают из камеры, сушат при температуре
100 – 105 ºС в течение 10 мин и опрыскивают раствором диметиламинобензальдегида.
На хроматограмме испытуемого раствора пятно, находящееся на уровне пятна сульфаниламида, по совокупности величины и интенсивности окраски не должно превышать пятно на хроматограмме раствора сравнения (не более 0,5 %).
Потеря в массе при высушивании. Около 1,0 г (точная навеска) субстанции сушат при температуре от 100 до 105 ºС до постоянной массы. Потеря в массе не должна превышать 0,5 %.
Хлориды. 0,5 г субстанции встряхивают в течение 3 мин со смесью
0,5 мл азотной кислоты разведенной 16 % и 9,5 мл воды и фильтруют. 4 мл фильтрата, разведенные водой до 10 мл, должны выдерживать испытание на хлориды (не более 0,01 % в субстанции).
Сульфаты. 1 г субстанции встряхивают в течение 3 мин со смесью
0,5 мл хлористоводородной кислоты разведенной 8,3 % и 19,5 мл воды и фильтруют. 10 мл фильтрата должны выдерживать испытание на сульфаты (не более 0,02 % в субстанции).
Сульфатная зола и тяжелые металлы. Сульфатная зола из 1,0 г (точная навеска) субстанции не должна превышать 0,1 % и должна выдерживать испытание на тяжелые металлы (не более 0,001 % в субстанции).
Остаточные органические растворители.Всоответствии с требованиями ОФС «Остаточные органические растворители».
Микробиологическая чистота.В соответствии с требованиями ОФС «Микробиологическая чистота».
Количественное определение. Около 0,5 г (точная навеска) субстанции растворяют в смеси 75 мл воды и 10 мл хлористоводородной кислоты концентрированной и титруют нитритометрически. Конец титрования устанавливают по йодкрахмальной бумаге.
1 мл 0,1 М раствора натрия нитрита соответствует 31,03 мг C12H14N4О4S.
Хранение. Список Б. В сухом, защищенном от света месте.
– Конец работы –
Эта тема принадлежит разделу:
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
профессионального образования Сибирский государственный медицинский университет Федерального агентства по здравоохранению... и социальному развитию ГБОУ ВПО СибГМУ Росздрава... Кафедра фармацевтической химии...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Бактериальные эндотоксины.
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов