рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- Експериментальна частина
Реферат Курсовая Конспект
Експериментальна частина
Експериментальна частина - раздел Химия, ЗАГАЛЬНА ХІМІЧНА ТЕХНОЛОГІЯ 2.2.1 Опис Лабораторної Установки І Порядок Виконання Роботи...
2.2.1 Опис лабораторної установки і порядок виконання роботи
Лабораторна флотаційна машина (рисунок 2.2) за принципом роботи відноситься до механічних флотаційних машин із можливістю примусового барботажу повітря.
Перемішування пульпи здійснюється мішалкою (поз.3); флотаційний концентрат, що міститься у пінному шарі флотаційної камери (поз. 2), вивантажується механічною лопаткою (поз.4) у порцеляновий стакан (поз. 1).
Операції по збагаченню виконуються в наступному порядку:
1. На технічних терезах зважують наважку руди (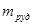 ) в кількості приблизно 25 г.
) в кількості приблизно 25 г.
2. Наважку завантажують до камери (поз. 2) флотаційної машини (рисунок 2.2).
3. Камеру флотаційної машини заповнюють водопровідною водою до позначки та додають флотаційні реагенти в кількості 4 ÷ 5 крапель кожного (соснове або ялицеве масо, гас, розчин поверхнево-активних речовин, крохмаль) та 2 ÷ 3 краплі силікатного клею.

1 – порцеляновий стакан; 2 – флотаційна камера; 3 – мішалка; 4 – механічна лопатка для зняття піни та концентрату; 5 – двигун; 6 - станина.
Рисунок 2.2 - Схема лабораторної флотаційної машини з механічним перемішуванням.
4. Вмикають перемішування у флотаційній машині і ведуть флотацію на протязі 10 хвилин. При необхідності через відповідний штуцер у камеру машини нагнітають повітря.
5. Отриманий і зібраний у порцеляновому стакані пінний флотоконцентрат фільтрують під вакуумом на воронці Бюхнера. Вологий флотоконцентрат розміщують у сушильній шафі і висушують за температури 333 ÷ 343 К, зважують на технічних терезах (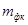 , г).
, г).
6. Флотаційні хвости, що залишилися на дні камери, через отвір в нижній частині виводять у приймальну ємність, фільтрують під вакуумом на воронці Бюхнера. Вологі флотаційні хвости розміщують у сушильній шафі і висушують за температури 333 ÷ 343 К, зважують на технічних терезах ( , г). Результати за операціями 1, 5, 6 заносять до таблиці.
, г). Результати за операціями 1, 5, 6 заносять до таблиці.
7. Після розвантаження флотаційної машини її треба промити водою від залишків сировини та флотореагентів.
Таблиця 2.1- Експериментальні дані
| Величина, що вимірюється | Позна-чення | Значення |
| Маса вихідної руди, яку піддають флотації, г | 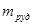
| |
| Маса отриманого сухого флотоконцентрату, г | 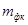
| |
| Маса отриманих сухих флотаційних хвостів, г | 
| |
| Наважка вихідної руди (аналіз на вміст сульфуру), г | 
| |
| Наважка флотоконцентрату для аналізу на вміст сульфуру, г | 
| |
| Наважка флотаційних хвостів для аналізу на вміст сульфуру, г | 
| |
| Об’єм розчину йоду, витраченого на титрування зразка вихідної сульфурної руди, см3 | 
| |
| Об’єм розчину йоду, витраченого на титрування зразка флотаційного концентрату, см3 | 
| |
| Об’єм розчину йоду, витраченого на титрування зразка флотаційних хвостів, см3 | 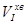
|
2.2.2 Методика хімічного аналізу
Для знаходження кількісних характеристик процесу флотації необхідно визначити вміст сульфуру (масову частку, %) у вихідній руді, в отриманому флотаційному концентраті та у флотаційних хвостах. Ці аналізи є типовими і виконуються за однаковою методикою, що базується на хімічній реакції взаємодії елементарного сульфуру з сульфітом натрію Na2SO3 з утворенням тіосульфату натрію.
S + Na2SO3 ® Na2S2O3 . (2.1)
Порядок виконання аналізу:
1. Наважку вихідної руди ( , бажана кількість 0,0900 ÷ 0,1200 г), або флотаційного концентрату (
, бажана кількість 0,0900 ÷ 0,1200 г), або флотаційного концентрату ( , бажана кількість 0,0900 ÷ 0,1200 г), або флотаційних хвостів (
, бажана кількість 0,0900 ÷ 0,1200 г), або флотаційних хвостів ( , бажана кількість 0,3000 ÷ 0,5000 г), зважену на аналітичних терезах з точністю до 0,0001 г, переносять до термостійкої конічної колби ємністю 250 см3, додають ~8 ÷ 10 см3 розчину сульфіту натрію з масовою часткою 20 % (відмірюють мірним циліндром) та ~100 см3 дистильованої води (відмірюють циліндром).
, бажана кількість 0,3000 ÷ 0,5000 г), зважену на аналітичних терезах з точністю до 0,0001 г, переносять до термостійкої конічної колби ємністю 250 см3, додають ~8 ÷ 10 см3 розчину сульфіту натрію з масовою часткою 20 % (відмірюють мірним циліндром) та ~100 см3 дистильованої води (відмірюють циліндром).
2. Колбу накривають скляним холодильником, заповненим водою (для запобігання сильному випаровуванню), нагрівають до кипіння і кип’ятять на протязі 45 ÷ 60 хвилин.
3. Після закінчення кип’ятіння колбу обов’язково охолоджують до кімнатної температури (можна обережно омивати колбу ззовні струменем холодної водопровідної води під краном).
4. Після охолодження до колби додають 8 ÷ 10 см3 розчину формаліну з масовою часткою 40 % (об’єм відміряють циліндром) для зв’язування надлишку сульфіту натрію в наступну формальдегідну сполуку за реакцією:
Na2SO3 + CH2O + H2O = H2C(OH)O-SO2-Na + NaOH. (2.2)
5. До розчину, який знаходиться в колбі, додають 1 ÷ 2 краплі індикатору фенолфталеїну. Поява малинового забарвлення свідчить про присутність лугу у розчині згідно реакції (2.2), тобто про повний перебіг даної реакції. Луг нейтралізують розчином оцтової кислоти з масовою часткою 10 % (додають краплями) до зміни забарвлення розчину з малинового на безбарвне. Додають додатково ще невеликий надлишок оцтової кислоти (~3 ÷ 5 см3).
6. Далі до колби додають 4 ÷ 5 крапель розчину крохмалю (індикатор) і титрують розчином йоду з молярною концентрацією еквіваленту  = 0,1 моль/дм3. Йод із бюретки по краплях дозують до колби при постійному перемішуванні до появи стійкого (незникаючого на протязі 30 секунд) синьо-чорного забарвлення. При титруванні розчину йодом перебігає хімічна реакція з утворенням йодиду натрію і тетратіонату натрію:
= 0,1 моль/дм3. Йод із бюретки по краплях дозують до колби при постійному перемішуванні до появи стійкого (незникаючого на протязі 30 секунд) синьо-чорного забарвлення. При титруванні розчину йодом перебігає хімічна реакція з утворенням йодиду натрію і тетратіонату натрію:
2Na2S2O3 + I2 ® 2NaI + Na2S4O6 . (2.3)
За результатами титрування визначають:
- об’єм розчину йоду, витраченого на титрування зразка вихідної сульфурної руди ( , см3);
, см3);
- об’єм розчину йоду, витраченого на титрування зразка флотаційного концентрату (
 , см3);
, см3);
- об’єм розчину йоду, витраченого на титрування зразка флотаційних хвостів (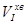 , см3);
, см3);
- масову частку (%) сульфуру у руді ( ) обчислюють за формулою:
) обчислюють за формулою:
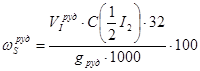 , (2.4)
, (2.4)
де - молярна концентрація еквівалента розчину йоду, 0,1 моль/дм3; 32 – молярна маса сульфуру, г/моль.
- молярна концентрація еквівалента розчину йоду, 0,1 моль/дм3; 32 – молярна маса сульфуру, г/моль.
Масову частку (%) сульфуру у флотаційному концентраті ( ) обчислюють за формулою:
) обчислюють за формулою:
 . (2.5)
. (2.5)
Масову частку (%) сульфуру у флотаційних хвостах (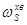 ) обчислюють за формулою:
) обчислюють за формулою:
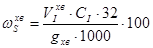 . (2.6)
. (2.6)
2.3 Обробка і представлення результатів
Виходом ( ) у хімічній технології зветься відношення кількості практично отриманого продукту до його максимальної (теоретично можливої) кількості. Вихід за флотоконцентратом - відношення маси отриманого концентрату (
) у хімічній технології зветься відношення кількості практично отриманого продукту до його максимальної (теоретично можливої) кількості. Вихід за флотоконцентратом - відношення маси отриманого концентрату (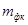 ) до маси вихідної руди (
) до маси вихідної руди (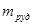 , 25 г):
, 25 г):
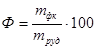 . (2.7)
. (2.7)
Ступінь вилучення сульфуру (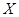 , %) – це відношення абсолютної кількості сульфуру у флотаційному концентраті (г) до її кількості у вихідній руді (г):
, %) – це відношення абсолютної кількості сульфуру у флотаційному концентраті (г) до її кількості у вихідній руді (г):
 (2.8)
(2.8)
де А - абсолютна кількість сульфуру в концентраті, г;  - абсолютна кількість сульфуру у вихідній руді, г.
- абсолютна кількість сульфуру у вихідній руді, г.
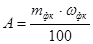 , (2.9)
, (2.9)
 . (2.10)
. (2.10)
Коефіцієнт концентрування 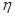 – це відношення масової частки сірки в отриманому збагаченому концентраті до масової частки сульфуру у вихідній руді:
– це відношення масової частки сірки в отриманому збагаченому концентраті до масової частки сульфуру у вихідній руді:
 =
= /
/ . (2.11)
. (2.11)
Матеріальний баланс збагачення за сульфуром:
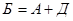 , (2.12)
, (2.12)
де 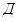 - абсолютна кількість сульфуру у флотаційних хвостах, г,
- абсолютна кількість сульфуру у флотаційних хвостах, г,
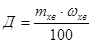 . (2.13)
. (2.13)
Нев’язка (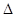 ) матеріального балансу, %:
) матеріального балансу, %:
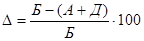 . (2.14)
. (2.14)
2.4 Техніка безпеки
1. Не торкатися до рухомих частин флотаційної машини.
2. Дотримуватися правил роботи з хімічними речовинами, електричними приладами.
2.5 Контрольні запитання
- Допуск до роботи.
1. Мета роботи. Техніка безпеки. Фізико-хімічні основи процесу флотації.
2. Принцип аналізу на вміст сульфуру у сировині і продуктах збагачення.
- Захист роботи:
1. Методи збагачення твердої сировини, порівняйте їх із точки зору простоти, екологічності, апаратурного оформлення.
2. Яку роль виконують флотореагенти у процесі флотаційного збагачення?
3. Методи збагачення (концентрування) рідкої та газоподібної сировини.
3 Пом’якшення води
Мета роботи: провести пом’якшення води методом іонного обміну та реагентним методом, виконати аналізи на твердість вихідної і пом’якшеної води, визначити ступінь пом’якшення вихідної води, порівняти отриману ступінь пом’якшення води за обома методами.
3.1 Стислі теоретичні відомості
У різних виробництвах хімічної промисловості воду застосовують дуже широко. Її використовують як універсальний розчинник для великої кількості твердих, рідких та газоподібних речовин. Дуже поширеним є застосування її як хімічної сировини у виробництві водню, сульфатної (сірчаної) та нітратної (азотної) кислот, гідроксиду натрію, вапна, в реакціях гідратації та гідролізу. Крім технологічних цілей, у ще більшій кількості воду використовують як теплоносій та холодоагент (відведення тепла в екзотермічних реакціях, охолодження атомних реакторів тощо). На підприємствах витрати води різного призначення вимірюють мільйонами кубічних метрів за добу. З метою економії витрат води використовують так звану оборотну воду, тобто використану та повернуту у виробничий цикл. До води, яку використовують для технологічних та теплотехнічних цілей, висувають дуже жорсткі вимоги щодо вмісту в ній розчинних речовин, механічних домішок, мікроорганізмів та ін. Якість води визначають за такими фізичними та хімічними характеристиками як прозорість, колір, запах, температура, загальний солевміст, твердість, окиснюваність та реакція води. Ці характеристики показують наявність чи відсутність тих або інших домішок.
Загальний солевміст характеризує наявність у воді мінеральних та органічних домішок. Для більшості виробництв основним якісним показником є твердість води, яка зумовлена наявністю у воді солей кальцію та магнію. Твердість виражається в мілімоль на 1 дм3 іонів Са2+ та Mg2+ (ммоль/дм3).
У лабораторіях і в енергетиці як і раніше використовують розмірність (формально застарілу) мг-екв/л (мг-екв/дм3).
Розрізняють три види твердості води: тимчасову, сталу та загальну.
Тимчасова (карбонатна або усувна) твердість обумовлена наявністю у воді гідрокарбонатів кальцію та магнію, які при кип’ятінні води утворюють нерозчинні сполуки у вигляді щільного осаду (накипу):
 ; (3.1)
; (3.1)
 . (3.2)
. (3.2)
Стала (не карбонатна) твердість обумовлена наявністю у воді усіх інших солей кальцію та магнію, які залишилися після кип’ятіння в розчинному вигляді. Сума тимчасової та сталої твердості утворює загальну твердість, тобто загальна твердість - сумарна концентрація катіонів кальцію і магнію.
Вода, яка потрапляє у виробництво, піддається очищенню різними методами залежно від характеру домішок та вимог, які висуваються до води даним виробництвом.
Промислова водопідготовка являє собою комплекс операцій, які забезпечують очищення води - видалення з неї шкідливих домішок, що перебувають у молекулярно розчинному, колоїдному та завислому стані. Основні операції водопідготовки: відстоювання, фільтрування, пом’якшення, демінералізація, нейтралізація, дегазація та знезараження.
Для пом’якшення води, тобто для її очищення від кальцію та магнію, використовують термічні, реагентні, іонообмінні та комбіновані методи. За реагентами, які використовуються для пом’якшення розрізняють наступні способи: вапняний (гашене вапно), содовий (кальцинована сода), натронний (гідроксид натрію) та фосфатний (тринатрійфосфат).
Суть іонообмінного методу полягає у видаленні із води іонів кальцію та магнію за допомогою іонітів - речовин, здатних обмінювати іони, що входять до їх складу, на іони солей, які є у воді. До іонітів належать штучні речовини (пермутити), природні мінерали (цеоліти, глауконіт тощо), а також синтетичні смоли, сульфоване вугілля та ін. Розрізняють процеси катіонного та аніонного обміну, відповідно іоніти називають катіонітами та аніонітами.
В основі катіонного процесу пом’якшення води лежить реакція обміну іонів натрію або водню катіонітів на іони Са2+, Мg2+. Обмін іонів натрію називають Nа-катіонування, а іонів водню - Н-катіонування:
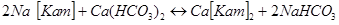 ; (3.3)
; (3.3)
 ; (3.4)
; (3.4)
 . (3.5)
. (3.5)
Прикладом аніонного обміну може бути реакція обміну аніонів за рівнянням:
 . (3.6)
. (3.6)
Реакції іонного обміну зворотні, і для відновлення обмінної властивості проводять процес регенерації. Розчином хлориду натрію здійснюють регенерацію Na-катіонітів, за допомогою мінеральних кислот (HCI, H2SO4, HNO3 ) - Н-катіонітів:
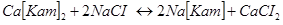 ; (3.7)
; (3.7)
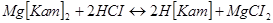 . (3.8)
. (3.8)
Регенерацію аніонітів проводять розчином лугу:
 . (3.9)
. (3.9)
Очищення промислових стічних вод методом іонного обміну дозволяє добувати й утилізувати важливі, а також шкідливі й токсичні домішки (сполуки арсену, фосфору, а також хром, цинк, свинець, ртуть, інші метали), поверхнево-активні, радіоактивні речовини. Застосовуючи іоніти можна очистити стічні води до гранично допустимих концентрацій з подальшим використанням води у технологічних процесах або у системах оборотного водопостачання.
Реагентні методи дозволяють перевести розчинні у воді сполуки кальцію та магнію у майже нерозчинні. Як реагенти для пом’якшення води використовують вапно, кальциновану соду, гідроксиди натрію або барію, щавлеву кислоту, фосфати натрію тощо. Серед реагентних методів найбільше розповсюджений вапняно-содовий метод. Сутність його полягає в процесах, що описують такими рівняннями:
 ; (3.10)
; (3.10)
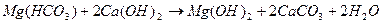 ; (3.11)
; (3.11)
 (3.12)
(3.12)
Сода усуває некарбонатну кальцієву твердість води:
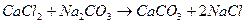 ; (3.13)
; (3.13)
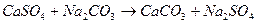 . (3.14)
. (3.14)
Повністю усунути твердість води реагентними методами неможливо через те, що такі сполуки, як СаСO3 та Мg(ОН)2, все ж розчиняються у воді. Тому вапняно-содовий метод застосовують, якщо природну воду треба пом’якшити до відносно неглибокої залишкової твердості (приблизно 1 ммоль/дм3). Більш глибокого пом’якшення води можливо досягти використовуючи фосфатний (реагентний) або іонообмінний метод.
– Конец работы –
Эта тема принадлежит разделу:
ЗАГАЛЬНА ХІМІЧНА ТЕХНОЛОГІЯ
Національний технічний університет України... Київський політехнічний інститут... ЕЛЕКТРОННЕ НАВЧАЛЬНЕ ВИДАННЯ...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Експериментальна частина
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов