Общие условия равновесия - раздел Химия, ФИЗИЧЕСКАЯ ХИМИЯ Любая Закрытая Система, Находящаяся В Равновесии При Постоянных Давлении И Те...
Любая закрытая система, находящаяся в равновесии при постоянных давлении и температуре, характеризуется соотношением: 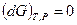
Для системы переменного состава (смотри (III, 58)):
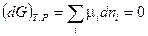 (IV, 11)
(IV, 11)
Если при постоянных Р и Т из фазы 1 в фазу 2 переходит 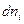 молей i-ого компонента, то
молей i-ого компонента, то
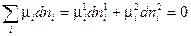 (IV, 12),
(IV, 12),
где верхний индекс относится к фазе, а нижний индекс — к компоненту.
При переходе dni молей i-ого компонента из фазы 1 в фазу 2 его количество в одной из фаз убывает, а в другой фазе увеличивается на ту же самую величину, следовательно, 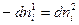 . Тогда уравнение (IV, 12) можно записать в следующем виде:
. Тогда уравнение (IV, 12) можно записать в следующем виде:
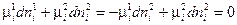
или 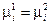 (IV, 13)
(IV, 13)
Таким образом, химический потенциал i-ого компонента в фазе 1 равен химическому потенциалу в фазе 2.
Обобщая этот результат на все фазы и все компоненты гетерогенной системы, получим условие равновесия:
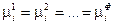 (IV, 14),
(IV, 14),
где Ф — число фаз.
Таким образом, гетерогенная система будет находиться в состоянии равновесия при выполнении равенств (IV, 14) и ряда тождеств:
T1 = T2 = ... = TФ = T
P1 = P2 = ... = PФ = P
Покажем, что равенство интенсивных переменных — температур, давлений и химических потенциалов компонентов есть также условие равновесия в изолированных системах, что непосредственно вытекает из второго закона термодинамики.
Воспользуемся обобщенной формой записи первого и второго законов термодинамики (смотри (III, 63)):
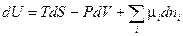
Перепишем это уравнение относительно dS :
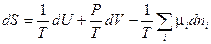 (IV, 15)
(IV, 15)
Из этого уравнения следует, что частные производные энтропии по экстенсивным переменным U,V и ni выражаются через интенсивные свойства системы Т, Р и mi:
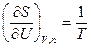 (IV, 16)
(IV, 16)
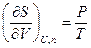
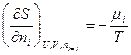
Рассмотрим изолированную систему, состоящую из двух подсистем «А» и «В», открытых по отношению друг к другу (смотри рис.14).
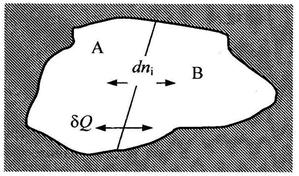
Рис. 14. Изолированная система, состоящая из двух подсистем, открытых по отношению друг к другу.
Эти подсистемы способны обмениваться энергией и веществом, но оболочка, ограничивающая систему в целом, остается несжимаемой и исключает теплообмен. Внутренняя энергия, энтропия, объем и количества компонентов — функции экстенсивные. Поэтому для изолированной системы, состоящей из «А» и «В», справедливы следующие соотношения:
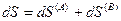 (IV, 17)
(IV, 17)
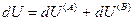
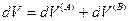
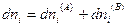
и поскольку U,V и n всей системы имеют постоянные значения (изолированная система), то
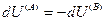 (IV, 18)
(IV, 18)
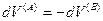
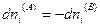
Энтропия — внутреннее свойство термодинамической системы; согласно постулатам термодинамики, при равновесии она является функцией внутренней энергии и внешних переменных.
Если в качестве внешних переменных для каждой из подсистем «А» и «В» выбрать их объем и количества веществ, то полный дифференциал функции S = S(U,V,n) для каждой из подсистем запишется в виде (IV, 15), а частные производные будут выражены формулами (IV, 16).
С учетом этого и соотношений (IV, 18) общее изменение энтропии изолированной системы запишется следующим образом:
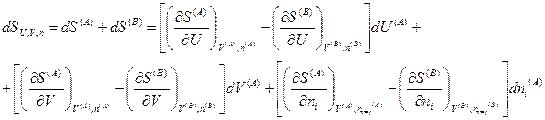
Согласно второму закону термодинамики, при равновесии энтропия изолированной системы достигает максимума, т. е. dSU,V,n = 0. Изменения dUA, dVA и 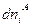 являются независимыми, поэтому равенство нулю dSU,V,n возможно только в том случае, если равен нулю каждый из коэффициентов, стоящих в квадратных скобках, т. е.
являются независимыми, поэтому равенство нулю dSU,V,n возможно только в том случае, если равен нулю каждый из коэффициентов, стоящих в квадратных скобках, т. е.
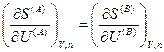
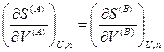
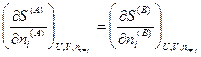
Если теперь принять во внимание выражения для частных производных энтропии (смотри (IV, 16)), то получим следующие соотношения:
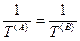
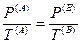
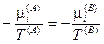
Из последних трех уравнений очевидным образом следуют общие условия равновесия изолированной термодинамической системы:
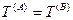 — термическое равновесие,
— термическое равновесие,
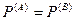 — механическое равновесие,
— механическое равновесие,
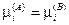 — химическое равновесие.
— химическое равновесие.
Если хотя бы некоторые из этих условий не выполняются, то система является неравновесной и в ней могут происходить процессы, сопровождающиеся выравниванием соответствующих интенсивных параметров.
Все темы данного раздела:
Предмет физической химии и её значение
Взаимосвязь химических и физических явлений изучает физическая химия. Этот раздел химии является пограничным между химией и физикой. Пользуясь теоретическими и экспериментальными методами об
Краткий очерк истории развития физической химии
Термин «физическая химия» и определение этой науки впервые были даны М.В.Ломоносовым, который в 1752-1754 гг. читал студентам Академии наук курс физической химии и оставил рукопись этого курса «Вве
Энергия. Закон сохранения и превращения энергии
Неотъемлемым свойством (атрибутом) материи является движение; оно неуничтожимо, как и сама материя. Движение материи проявляется в разных формах, которые могут переходить одна в другую. Мерой движе
Предмет, метод и границы термодинамики
Сосредотачивая своё внимание на теплоте и работе, как формах перехода энергии при самых различных процессах, термодинамика вовлекает в круг своего рассмотрения многочисленные энергетические зависим
Теплота и работа
Изменения форм движения при его переходе от одного тела к другому и соответствующие превращения энергии весьма разнообразны. Формы же самого перехода движения и связанных с ним превращений энергии
Эквивалентность теплоты и работы
Постоянное эквивалентное отношение между теплотой и работой при их взаимных переходах установлено в классических опытах Д.П.Джоуля (1842-1867). Типичный эксперимент Джоуля заключается в следующем (
Внутренняя энергия
Для некругового процесса равенство (I, 1) не соблюдается, так как система не возвращается в исходное состояние. Вместо этого равенства для некругового процесса можно записать (опуская коэффициент
Первый закон термодинамики
Первый закон (первое начало) термодинамики непосредственно связан с законом сохранения энергии. Он позволяет рассчитывать баланс энергии при протекании различных процессов, в том числе и химических
Уравнения состояния
Многие свойства системы, находящейся в равновесии, и составляющих её фаз являются взаимозависимыми. Изменение одного из них вызывает изменение других. Количественные функциональные зависимости межд
Работа различных процессов
Под названием работы объединяются многие энергетические процессы; общим свойством этих процессов является затрата энергии системы на преодоление силы, действующей извне. К таким процессам относится
Теплоёмкость. Вычисление теплоты различных процессов
Опытное определение удельной (с) или мольной (С) теплоёмкости тела заключается в измерении теплоты Q, поглощаемой при нагревании одного грамма или одного моля вещества н
Калорические коэффициенты
Внутренняя энергия системы U, будучи функцией состояния, является функцией независимых переменных (параметров состояния) системы.
В простейших системах будем рассматривать внутренню
Применение первого закона термодинамики к идеальному газу.
Рассмотрим идеальный газ, т. е. газ, состояние одного моля которого описывается уравнением Менделеева‑Клапейрона:
Адиабатические процессы в газах
Говорят, что термодинамическая система совершает адиабатический процесс, если он обратим и если система термически изолирована, так что во время процесса не происходит теплообмена между системой и
Энтальпия
Уравнение первого закона термодинамики для процессов, где совершается только работа расширения, приобретает вид:
δQ = dU + PdV (I, 51)
Если процесс идет при постоянном
Химическая переменная. Формулировка первого закона термодинамики для процессов, сопровождающихся химическими и фазовыми превращениями
Уравнения (I, 27), (I, 28) и ранее приведённые формулировки первого закона термодинамики справедливы для любой равновесной закрытой системы вне зависимости от того, происходят в ней химические или
Термохимия. Закон Гесса
При химических превращениях происходит изменение внутренней энергии системы, обусловленное тем, что внутренняя энергия продуктов реакции отличается от внутренней энергии исходных веществ.
Зависимость теплового эффекта от температуры. Уравнение Кирхгофа.
По закону Гесса можно вычислить тепловой эффект реакции при той температуре, при которой известны теплоты образования или теплоты сгорания всех реагентов (обычно это 298К). Однако, часто воз
Самопроизвольные и несамопроизвольные процессы
Из первого закона термодинамики и вытекающих из него закономерностей обмена энергией между телами при различных процессах нельзя сделать вывода о том, возможен ли, вообще говоря, данный процесс и в
Второй закон термодинамики
Наиболее часто встречающимися и безусловно самопроизвольными являются процессы передачи теплоты от горячего тела к холодному (теплопроводность) и перехода работы в теплоту (трение). Многовековая жи
Методы расчета изменения энтропии
Уравнения (II, 12) и (II, 13), определяющие энтропию, являются единственными исходными уравнениями для термодинамического расчета изменения энтропии системы. Заменяя элементарную теплоту в уравнени
Постулат Планка
По уравнению (II, 3) невозможно вычислить абсолютное значение энтропии системы. Такую возможность дает новое, недоказуемое положение, не вытекающее из двух законов термодинамики, которое было сформ
Абсолютные значения энтропии
Постулат Планка используется при термодинамическом исследовании химических процессов для вычисления абсолютных значений энтропии химических соединений — величин, которые имеют большое значение при
Стандартная энтропия. Изменение энтропии при протекании химической реакции
Энтропию, как и другие термодинамические функции, принято относить к стандартному состоянию вещества.
Напомним, что стандартное состояние характеризуется стандартными усло
Статистическая интерпретация энтропии
В основу понятия энтропии как функции состояния положена макроскопическая концепция. Справедливость второго закона термодинамики связана с реальностью необратимых процессов. В отличие от необратимы
Энергия Гельмгольца
Напомним, что второй закон термодинамики определяет критерии самопроизвольного протекания процессов в изолированных системах. Однако, подобные условия (отсутствие обмена энергией и веществом с окр
Энергия Гиббса
Желая учесть в общей форме другие виды работы, кроме работы расширения, представим элементарную работу как сумму работы расширения и других видов работы:
dW = PdV + dW' (III, 15)
Характеристические функции. Фундаментальные (канонические) уравнения состояния
Ранее мы определили следующие термодинамические функции — свойства системы: внутреннюю энергию U, энтальпию H, энтропию S, энергию Гельмгольца F, энергию Гиббса G
Соотношения Максвелла.
Рассмотрим теперь вторые смешанные производные характеристических функций. Принимая во внимание уравнения (III, 26), можем записать:
Уравнение Гиббса‑Гельмгольца
Уравнение Гиббса-Гельмгольца позволяет определять изменение энергии Гиббса, сопровождающее химические реакции при любой заданной температуре, если известна зависимость теплоты химических реакций от
Энергия Гиббса смеси идеальных газов. Определение химического потенциала.
Энергия Гиббса является экстенсивной функцией, что позволяет рассчитать ее значение для смеси идеальных газов.
Представим себе резервуар, разделенный перегородками на секции, как показано
Химический потенциал
Чтобы прояснить смысл понятия «химический потенциал», продифференцируем выражение (III,51) как произведение при постоянных Р и Т:
Фазовые переходы. Уравнение Клапейрона-Клаузиуса.
В системе, состоящей из нескольких фаз чистого вещества, находящихся в равновесии, возможны переходы вещества из одной фазы в другую. Такие переходы называются фазовыми переходами.
Фазовые переходы первого рода. Плавление. Испарение
Фазовые переходы, характеризующиеся равенством изобарных потенциалов двух сосуществующих в равновесии фаз и скачкообразным изменением первых производных по энергии Гиббса (энтропии и объема) при пе
Фазовые переходы второго рода
Фазовый переход второго рода — это равновесный переход вещества из одной фазы в другую, при котором скачкообразно изменяются только вторые производные от энергии Гиббса по температуре и давлению.
Зависимость давления насыщенного пара от температуры
Давление насыщенного пара жидкости резко увеличивается с повышением температуры. Это видно из рисунка 12, на котором изображены кривые давления пара некоторых жидкостей, начинающиеся в точках плавл
Правило фаз Гиббса
В 1876 г. Гиббс вывел простую формулу, связывающую число фаз (Ф), находящихся в равновесии, число компонентов (К) и число степеней свободы (С) системы. При равновесии должны бы
Применение правила фаз Гиббса к однокомпонентным системам. Диаграммы состояния воды и серы
Для однокомпонентной системы К =1 и правило фаз записывается в виде:
С = 3 – Ф
Если Ф = 1, то С =2 , говорят, что система бивариантна;
Фазовая диаграмма воды.
Состояние воды изучено в широком диапазоне температур и давлений. При высоких давлениях установлено существование не менее десяти кристаллических модификаций льда. Наиболее изученным является лед I
Фазовая диаграмма серы.
Кристаллическая сера существует в виде двух модификаций — ромбической (Sр) и моноклинной (Sм). Поэтому возможно существование четырех фаз: ромбической, мо
Закон действующих масс. Константа равновесия для газофазных реакций
Допустим, что между газообразными веществами А1, А2 … Аi, А’1, А’2 … А’i протекает химически обратимая реакция по уравнению:
Уравнение изотермы химической реакции
Предположим, в смеси идеальных газов протекает химическая реакция по уравнению
Допустим, что в момент приг
Представление о химическом сродстве
Из того факта, что одни вещества реагируют друг с другом легко и быстро, другие с трудом, третьи — совсем не реагируют, возникает предположение о наличии или отсутствии особого химического сродства
Использование закона действующих масс для расчета состава равновесных смесей
Для определения состава системы при установившемся равновесии, а следовательно, и выхода продукта (продуктов) реакции необходимо знать константу равновесия и состав исходной смеси.
Состав
Гетерогенные химические равновесия
Закон действующих масс был выведен с использованием закона состояния идеальных газов и применим в первую очередь к газовым смесям. Однако его без существенных изменений можно применить и к значител
Влияние температуры на химическое равновесие. Уравнение изобары химической реакции
Для определения зависимости K0от температуры в дифференциальной форме воспользуемся уравнением Гиббса‑Гельмгольца (III, 41)
Принцип Ле Шателье‑Брауна
Выведенная из состояния равновесия система вновь возвращается к состоянию равновесия. Ле Шателье и Браун высказали простой принцип, которым можно воспользоваться для предсказания того, в каком напр
Тепловая теорема Нернста
Прямой и простой расчет изменения энергии Гиббса, а, следовательно, и констант равновесия химических реакций не вызывает затруднений, если известны теплота химической реакции и абсолютные значения
Химическое равновесие в неидеальных системах
Закон действующих масс (V, 5) применим, как уже говорилось, лишь к идеальным газам (или идеальным растворам). Для таких систем произведение равновесных относительных парциальных давлений реагирующи
Зависимость энтальпии веществ и тепловых эффектов химических реакций от давления
При рассмотрении зависимости энтальпии от давления воспользуемся хорошо нам известным выражением ее полного дифференциала (III, 27):
dH = VdP + TdS
Разделим е
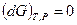
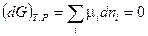 (IV, 11)
(IV, 11)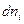 молей i-ого компонента, то
молей i-ого компонента, то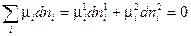 (IV, 12),
(IV, 12),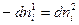 . Тогда уравнение (IV, 12) можно записать в следующем виде:
. Тогда уравнение (IV, 12) можно записать в следующем виде: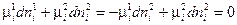
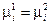 (IV, 13)
(IV, 13)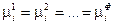 (IV, 14),
(IV, 14),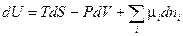
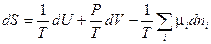 (IV, 15)
(IV, 15)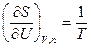 (IV, 16)
(IV, 16)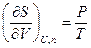
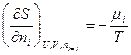

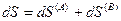 (IV, 17)
(IV, 17)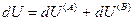
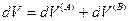
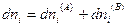
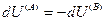 (IV, 18)
(IV, 18)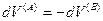
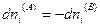
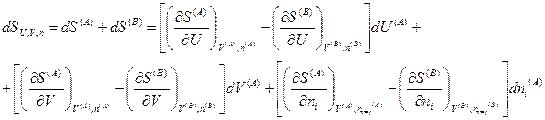
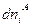 являются независимыми, поэтому равенство нулю dSU,V,n возможно только в том случае, если равен нулю каждый из коэффициентов, стоящих в квадратных скобках, т. е.
являются независимыми, поэтому равенство нулю dSU,V,n возможно только в том случае, если равен нулю каждый из коэффициентов, стоящих в квадратных скобках, т. е.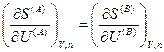
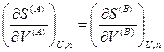
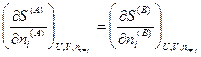
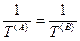
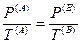
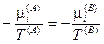
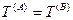 — термическое равновесие,
— термическое равновесие,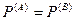 — механическое равновесие,
— механическое равновесие,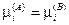 — химическое равновесие.
— химическое равновесие.






Новости и инфо для студентов