рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Образование
- /
- Способы получения
Реферат Курсовая Конспект
Способы получения
Способы получения - раздел Образование, СОЕДИНЕНИЯ АРОМАТИЧЕСКОГО РЯДА 1. Из Природных Источников. Главными Источниками Получен...
1. Из природных источников. Главными источниками получения нафталина являются каменноугольная смола (содержит около 10 % нафталина) и нефть (6–7 %). Из нефти нафталин получают при переработке масла,содержащее нафталин и алкилнафталины, полученного при каталитическом риформинге бензина:
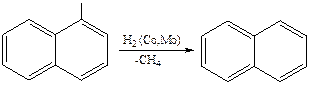
2. Циклизация ацетилена и бензола:
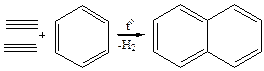
3. Дегидроциклизация алканов:

Химические свойства.По химическим свойствам нафталин является ароматическим соединением и напоминает бензол. Однако он проявляет более ненасыщенный характер и легче чем бензол вступает в реакции присоединения.
1. Реакции замещения. Реакции протекают по механизму SE2. π-Электронное облако является источником электронов, доступных для электрофильного реагента, который атакует кольцо и с очень большой скоростью образует π-комплекс. Следующей (лимитирующей) стадией является формирование σ-комплекса, в котором происходит нарушение ароматичности одного из колец. После отщепления протона от σ-комплекса происходит восстановление ароматичности нафталина. Электрофильный реагент атакует преимущественно α-положение, так как при этом образуется более устойчивый σ-комплекс с эффективной делокализацией положительного заряда (две предельные структуры). Второе кольцо в делокализации заряда не принимает участия, так как это связано с нарушением его ароматичности, что является энергетически невыгодным.
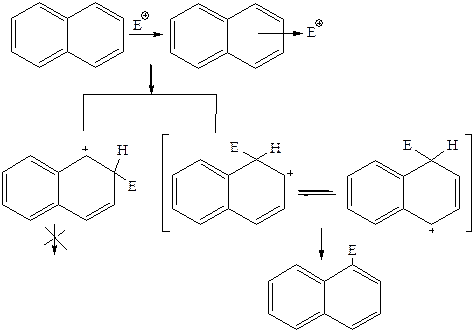
1.1 Нитрование. Реакцию проводят нитрующей смесью при температуре 60°С. Эта реакция протекает легко с образованием α-нитронафталина с небольшой примесью (3-нитронафталина (1,7–5 %):
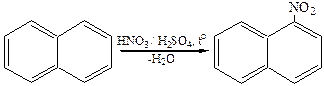
1.2 Галогенирование.При хлорировании хлор пропускают через расплавленный нафталин при 110–120 °С в присутствии кислот Льюиса:

1.3 Реакции Фриделя–Крафтса:
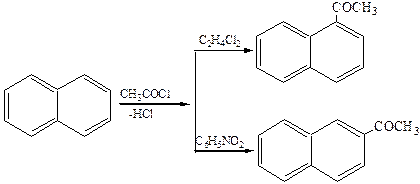
1.4 Сульфирование. В зависимости от температуры образуется α- или β-изомер:
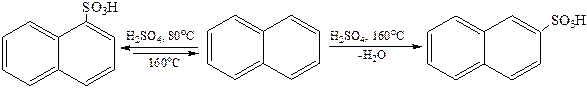
1.4 Окисление:
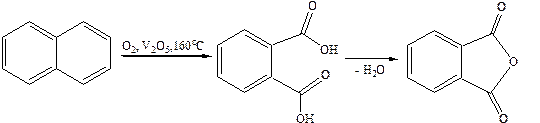
1.5 Гидрирование:
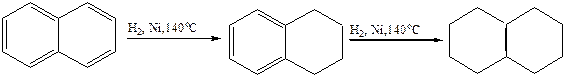
тетралин декалин
Экологические аспекты. Бифенил (дифенил). В окружающую среду он может поступать с промышленных предприятий по производству красителей, синтетических смол, фунгицидов и предприятий по термической обработке полимеров. Бифенил вызывает лейкоцитоз и анемию. Отмечены случаи поражения печени и ЦНС. Воздействуя на мембраны митохондрий, бифенил нарушает энергетический обмен в клетках. В организм он поступает через легкие и с пищей, подвергается метаболизму до гидроксибифенилов, которые образуют конъюгаты с глюкуроновой кислотой и выделяются с желчью.
Нафталин поступает в окружающую среду с коксохимического производства, а также с производств по очистке бензола, синтезу красителей, синтетических смол, изоляционных материалов и пестицидов. Из окружающей среды он удаляется в результате окисления под действием УФ и путем биодеградации под влиянием бактерий. Продуктами окисления являются нафтохинон, бензофуранон, этоксибензофуранон и некоторые другие вещества. Отравление нафталином возможно при вдыхании паров, пыли и при проникновении через кожу, при этом происходит поражение нервной системы, желудочно-кишечного тракта, почек, поверхностное помутнение роговицы. При хронических отравлениях наблюдаются изменения в крови: разрушение эритроцитов и лейкоцитов, снижение содержания гемоглобина. Хронические отравления нафталином приводят к нарушению секреторной деятельности желудочно-кишечного тракта, белковообразо-вательной и антитоксической функции печени.
Нафтолы применяются в производстве инсектицидов, в медицине, в парфюмерной промышленности. В окружающую среду они поступают с выхлопными газами автотранспорта, с предприятий по производству синтетического каучука, красителей, пестицидов и резинотехнических изделий. Есть данные, свидетельствующие о канцерогенных и мутагенных свойствах и эмбриотоксическом действии этих веществ. При отравлении 1-нафтолом возможен летальный исход. При хроническом воздействии наблюдается желтушность кожи, увеличение печени и селезенки.
Антрацен поступает в окружающую среду главным образом при перегонке каменноугольной смолы и окисляется под действием УФ и бактериальной флоры с образованием продуктов окисления, главным из которых является антрахинон. При продолжительном контакте происходит пигментация участков кожи и ее ороговение. Токсическое действие антрацена заметно усиливается на солнечном свету.
Фенантрен попадает в окружающую среду с выбросами коксохимических, алюминиевых, металлургических, нефте- и сланце-перерабатывающих предприятий, а также при работе двигателей внутреннего сгорания, отопительных и энергетических систем.
Бензо[а]пирен кристаллическое вещество бледно-желтого цвета, плохо растворимое в воде. Антропогенными источниками загрязнения окружающей среды могут являться различные промышленные предприятия, теплоэлектростанции, мелкие отопительные системы и автотранспорт. Полициклические ароматические углеводороды и бензопирен образуются при лесных пожарах и в результате вулканической деятельности. В окружающей среде бензопирен подвергается различным воздействиям, которые приводят к потере его канцерогенных свойств.
При попадании в организм полициклические углеводороды под действием ферментов образуют эпоксисоединения, которые реагируют с гуанином, препятствуя синтезу ДНК и вызывая различные нарушения, в том числе и мутации, способствуют развитию раковых заболеваний.
– Конец работы –
Эта тема принадлежит разделу:
СОЕДИНЕНИЯ АРОМАТИЧЕСКОГО РЯДА
На сайте allrefs.net читайте: СОЕДИНЕНИЯ АРОМАТИЧЕСКОГО РЯДА.
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Способы получения
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов