рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Образование
- /
- Цитогенетический метод
Реферат Курсовая Конспект
Цитогенетический метод
Цитогенетический метод - раздел Образование, Тема ХРОМОСОМНАЯ ТЕОРИЯ Основа Метода — Микроскопическое Изучение Хромосом Человека. Цитогенетические...
Основа метода — микроскопическое изучение хромосом человека. Цитогенетические исследования стали широко использоваться с начала 20-х гг. XX в. для изучения морфологии хромосом человека, подсчета хромосом, культивирования лейкоцитов для получения метафазных пластинок.
Развитие современной цитогенетики человека связано с именами цитологов Д.Тио и А.Левана. В 1956 г. они первыми установили, что у человека 46 (а не 48, как думали раньше) хромосом, что положило начало широкому изучению митотических и мейотических хромосом человека.
В 1959 г. французские ученые Д. Лежен, Р.Тюрпен и М. Готье установили хромосомную природу болезни Дауна. В последующие годы были описаны многие другие хромосомные синдромы, часто встречающиеся у человека. Цитогенетика стала важнейшим разделом практической медицины. В настоящее время цитогенетический метод применяется для диагностики хромосомных болезней, составления генетических карт хромосом, изучения мутационного процесса и других проблем генетики человека.
В 1960 г. в г. Денвере (США) была разработана первая Международная классификация хромосом человека. В ее основу легли размеры хромосом и положение первичной перетяжки — центромеры
Все хромосомы по форме разделены на метацентрические, субметацентрические и акроцентрические и подразделены на 7 групп, обозначенных латинскими буквами А, В, С, D, Е, F и G. Каждая пара хромосом была наделена порядковым номером от 1 до 22, выделены отдельно и поименованы латинскими буквами — X и Y половые хромосомы (Табл. 2.4).

В 1971 г. на IV Пражской конференции генетиков в дополнении к Денверской классификации были представлены методы дифференциальной окраски хромосом, благодаря которым каждая хромосома приобретает свой неповторимый рисунок, что помогает точной идентификации.
Основные сведения о морфологии хромосом человека получены при изучении их в метафазах митоза и профазе-метафазе мейоза. При этом важно, чтобы количество делящихся клеток, было достаточно высоко. Важнейшие цитогенетические работы выполнены на лимфоцитах периферической крови, поскольку культивирование лимфоцитов в течение 2-3 суток в присутствии фитогемагглютинина позволяет получить множество метафазных пластинок для хромосомного анализа.
Цитогенетическому анализу подвергают однослойные метафазные пластинки с раздельно лежащими хромосомами Для этого делящиеся клетки обрабатывают колхицином и некоторыми другими химическими веществами (гипотоническим раствором солей, метанол-уксусным фиксатором и др.).
Важным этапом цитогенетического анализа является окраска полученных препаратов. Ее проводят простыми, дифференциальными и флюоресцентными методами.
Простая окраска обеспечивает групповую идентификацию хромосом. Используется она для количественного учета хромосомных аномалий при определении мутагенности среды (действия радиации, химических мутагенов и др.). С помощью этого типа окраски были открыты многие хромосомные болезни, а также хромосомные аберрации), вызывающие самопроизвольные аборты, врожденные пороки развития, канцерогенез и т.п.
В 70-е гг. XX в. в медицинской практике начали применяться методы дифференциального окрашивания, выявляющие структурную разнородность хромосом по длине, что выражается в виде чередования светлых и темных полос (эу- и гетерохроматических районов). Отмечается, что протяженность и рисунок полос специфичны для каждой хромосомы.
Дифференциальное окрашивание хромосом можно проводить рядом способов. Первоначально использовали акрихин- иприт — флюоресцентное алкилирующее вещество (Q-метод). Действие его основано на способности метафазиых хромосом дифференциально связывать флюорохромы. После окрашивания акрихинипритом сегменты приобретают яркое флюоресцирующее свечение. Для просмотра таких препаратов используют люминесцентный микроскоп.
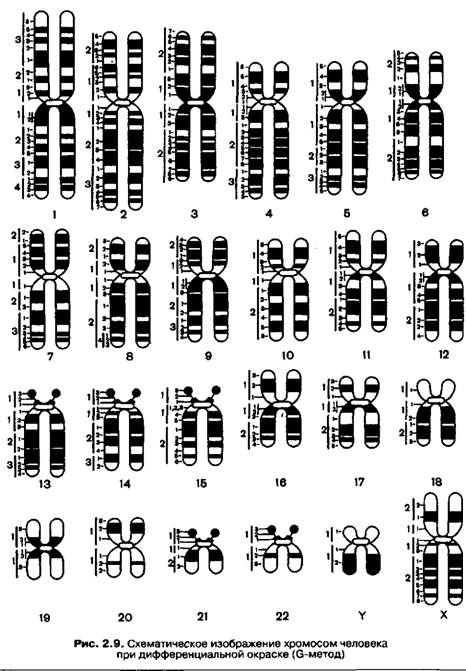
В дальнейшем был разработан способ окраски хромосом без флюоресцентных красителей. Это — G-окраска (краситель Гимза). После предварительной инкубации в солевом растворе хромосомы обрабатываются протеазой. В результате они приобретают сегментированный вид благодаря чередованию темно и светлоокрашенных участков. Механизм образования сегментов пока недостаточно ясен. Предполагается, что окрашенные сегменты — это гетерохроматиновые участки с повторяющимися последовательностями ДНК, а неокрашенные — эухроматиновые районы с кодирующими последовательностями ДНК (рис. 2.9).
К разновидностям дифференциального окрашивания по методу Гимзы относятся R-окрашиваемость и С-окрашиваемость. Эти разновидности дифференциального окрашивания получают при определенном изменении времени инкубации препаратов, окрашенных по методу Гимзы. В нервом случае распределение окрашенных и неокрашенных сегментов будет обратным тому, что наблюдается при G и Q-окрашивании. На R-окрашенных хромосомах гетерохроматиновые и околоцентромерные районы остаются светлыми. В случае же С-окраски выявляются районы структурного гетерохроматина, наиболее устойчивого к химическим и физическим повреждениям. В аутосомах и Х-хромосомах человека эти районы локализованы в околоцентромерных участках, а в Y-хромосоме — в дистальной половине длинного плеча. Наиболее крупные блоки С-хроматина имеются в аутосомах 1, 9 и 16 в области их вторичных перетяжек, а также в Y-хромосоме. Самыми мелкими центромерными блоками обладают Y-хромосома и аутосома 2 (рис. 2.10).
Одной из особенностей хромосом человека является асинхронность (неодновременность) репликации по длине. В каждой хромосоме есть рано и поздно реплицирующиеся участки. Для выявления последовательности репликации применяется 5-бромдезоксиури-дин — аналог тимина. Включившие его участки окрашиваются слабо.
Применяется 5-бром-дезоксиури-дин и для дифференциальной окраски сестринских хроматид, если он вводится на полный клеточный цикл. В этом случае вновь образуемая хроматида, включит этот аналог тимина и будет окрашена слабо, а другая (старая) окрасится интенсивно (рис. 2.11). Этот метод позволяет выявлять участки обмена между сестринскими хроматидами (СХО).
При воздействии различными мутагенными факторами число СХО увеличивается, следовательно, этот метод пригоден для изучения мутационного процесса у человека.
Успехи молекулярной цитогенетики человека позволяют разрабатывать новые методы изучения хромосом. Так, следует отметить метод флюоресцентной гибридизации in situ (FISH), который дает возможность исследовать широкий круг вопросов : от локализации гена до расшифровки сложных перестроек между несколькими хромосомами. Метод FISH может применяться и для диагностики анеуплоидий в интерфазных ядрах (см. главу 6).
Таким образом, соединение цитогенетических и молекулярно-генетических методов в генетике человека делает почти неограниченными возможности диагностики хромосомных аномалий.

– Конец работы –
Эта тема принадлежит разделу:
Тема ХРОМОСОМНАЯ ТЕОРИЯ
Хххххххх хххххххх хххххх Тема ХРОМОСОМНАЯ ТЕОРИЯ... Занятие Генные мутации... Занятие Хромосомные и геномные мутации...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Цитогенетический метод
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов