рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- МНОГОАТОМНЫЕ СПИРТЫ
Реферат Курсовая Конспект
МНОГОАТОМНЫЕ СПИРТЫ
МНОГОАТОМНЫЕ СПИРТЫ - раздел Химия, ОКСИПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ В Многоатомных Спиртах Атомность Исчисляют По Количеству Гидроксильных Групп ...
В многоатомных спиртах атомность исчисляют по количеству гидроксильных групп в молекуле. В ряду многоатомных спиртов большое значение имеют двухатомные спирты, или гликоли (названы так за сладкий вкус), трехатомные спирты (глицерин), а также многоатомные спирты с большим числом углеродных атомов в цепи: эритриты – четырехатомные, пентиты – пятиатомные и т. д. Многоатомные спирты называют также глицитами. Систематическое название многоатомного спирта строится по известным правилам с добавлением соответствующего окончания (-диол, -триол и т. д.) и указанием положения заместителей.
Таблица 11 – Номенклатура и физические свойства многоатомных спиртов
| Формула | Номенклатура | Тпл., оС | Ткип., оС | Растворимость, г/100 г Н2О | |
| тривиальная | систематческая | ||||
| HOCH2–CH2OH | Этилен- гликоль | Этандиол-1,2 | –18 | Неограниченно | |
| HOCH2CH(OH)CH3 | Пропилен- гликоль | Пропандиол-1,2 | – | » | |
| HOCH2CH2CH2OH | Триметилен-гликоль | Пропандиол-1,3 | –30 | » | |
| HOCH2CH(OH)CH2OH | Глицерин | Пропантриол-1,2,3 | » |
Устойчивыми являются производные, в которых гидроксильные группы находятся при разных атомах углерода. Вещества с двумя гидроксилами при одном атоме углерода (гемдиолы) неустойчивы при обычных условиях и превращаются в карбонильные соединения, отщепляя воду (правило Эльтекова-Эрленмейера):
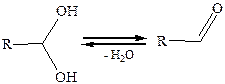
Увеличение числа гидроксильных групп в молекуле спирта приводит к усилению ассоциации молекул вследствие образования межмолекулярных водородных связей как между молекулами спирта, так и между спиртом и молекулами воды в водных растворах. Поэтому температуры кипения и вязкость многоатомных спиртов еще выше, чем одноатомных, и они значительно лучше растворимы в воде (табл. 11).
Способы получения
1. Гидролиз природных жиров:
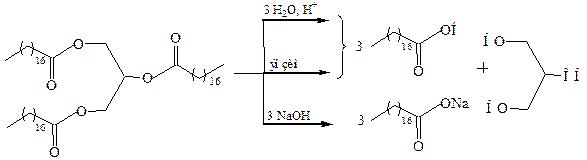
2. Из пропиленовой фракции газов крекинга нефти. В синтезе используется реакция алильного замещения:
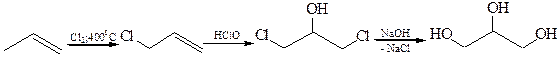
3. Из газов крекинга нефти получают этиленгликоль:
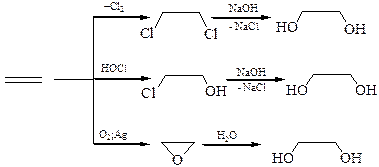
4. Восстановление углеводов:
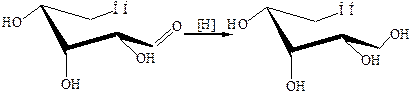
Химические свойства. У многоатомных спиртов сохраняются все свойства спиртового гидроксила. Отличия состоят в том, что в реакции участвует одна или более ОН-групп, в результате могут получаться полные или неполные производные. Ряд реакций обусловлен взаимным влиянием гидроксильных групп (например, кислотные свойства).
Кислотные свойства.У многоатомных спиртов кислотные свойства выражены сильнее по сравнению с одноатомными. Отрицательный индукционный эффект вновь появившихся гидроксильных групп вызывает увеличение полярности связи О–Н, что и приводит к увеличению кислотных свойств аналогично влиянию хлора у 2-хлорэтанола:
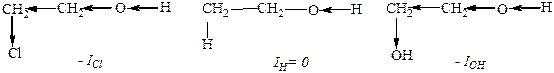
– Конец работы –
Эта тема принадлежит разделу:
ОКСИПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
На сайте allrefs.net читайте: ОКСИПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ.
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: МНОГОАТОМНЫЕ СПИРТЫ
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов