рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- Геохронология. Ядерные реакции. Нуклеосинтез в природе
Реферат Курсовая Конспект
Геохронология. Ядерные реакции. Нуклеосинтез в природе
Геохронология. Ядерные реакции. Нуклеосинтез в природе - раздел Химия, Химическая связь и строение вещества Скорость Радиоактивного Распада Различных Изотопов (И Соответственно Среднее ...
Скорость радиоактивного распада различных изотопов (и соответственно среднее время их жизни) отличается на много порядков.
В качестве меры скорости распада принято использовать период полураспада, t0,5, – время, за которое распадается 50 % исходных ядер. Например, период b+-распада изотопа 14С составляет 5760 лет. Следовательно, независимо от начального количества изотопа, n0, (1 г, 4 моль или 1020 атомов), через 5760 лет останется не распавшимися n0/2 (0,5 г, 2 моль, 0,5·1020 атомов соответственно), через 2t0,5 = 11520 лет n0/4 (0,25 г, 0,25·105 атомов) и т. д.; за время mt0,5 – n0(1/2)m, или n = n0(1/2)(t/t0,5).
Такие зависимости часто встречаются в природе. Их принято записывать в виде показательной функции по основанию натуральных логарифмов е (экспоненциальная зависимость), а не по 1/2:
n = n0e–kt (3)
График уравнения (3) приведен на рис. 2. Здесь t – время; k – константа скорости распада, имеющая смысл доли ядер, распавшихся за время единицу времени; скорость распада dn/dt = –nt; k и период полураспада связаны соотношением k = (ln2)/t0,5; 1/k – среднее время жизни радиоактивного ядра. Уравнение (3), называемое кинетическим уравнением 1-го порядка, описывает очень простую ситуацию: каждое ядро распадается независимо от остальных, с собственной вероятностью распада, равной 1/2 за время полураспада t0,5. Такому же уравнению подчиняется скорость многих (но не всех!) химических реакций.
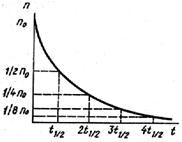 Рис. 2. Количество распавшихся ядер от времени при радиоактивном распаде
Рис. 2. Количество распавшихся ядер от времени при радиоактивном распаде
|
Примеры периодов полураспада для некоторых изотопов, варьирующиеся от долей секунды у 212Po и многих изотопов трансурановых элементов до 1021 лет у 130Te, представлены в табл. 3.
С точки зрения радиационной безопасности короткоживущие изотопы более опасны, так как количество высвечиваемой ими радиации (a-, b-, g-частиц) от одного и того же исходного количества радиоактивных атомов в единицу времени больше, чем для долгоживущих. Но снижение излучения до допустимого, считающегося безопасным, уровня, для них произойдет за меньшее время, чем для долгоживущих.
Таблица 3
– Конец работы –
Эта тема принадлежит разделу:
Химическая связь и строение вещества
На сайте allrefs.net читайте: "Химическая связь и строение вещества"
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Геохронология. Ядерные реакции. Нуклеосинтез в природе
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов