рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Образование
- /
- Статистична обробка результатів аналізу
Реферат Курсовая Конспект
Статистична обробка результатів аналізу
Статистична обробка результатів аналізу - раздел Образование, Титриметричний аналіз Якiсть Вимiрювань У Кількісному Аналізі Характеризується Правильністю, Відтво...
Якiсть вимiрювань у кількісному аналізі характеризується правильністю, відтворюваністю та точністю [1, с. 38].
Правильність відображає близькiсть систематичної похибки до нуля .
Відтворюваність показує близькiсть один до одного результатiв вимiрювань, якi виконуються у рiзних умовах (неоднаковий час чи методи).
Точність характеризує наближеність результатiв вимірювань до iстинного значення вимiрюваної величини.
Висока точнiсть вимiрювань вiдповiдає малим значенням похибок всiх видiв, як систематичних, так i випадкових. Результат аналiзу, який наближається до iстинного вмiсту настiльки, що може використовуватися замiсть нього, називають дійсним вмiстом. Вважають, що результати визначень за ймовірністю їх появи відповідають закону розподілу Гауса.
В аналiтичнiй хімiї кількість паралельних визначень (n) переважно є невеликою (n = 3 - 5). Для характеристики точності визначення розраховують наведені нижче статистичні параметри [5].
Вибіркова сукупність (випадкова вибірка) – це сукупнiсть отриманих результатiв паралельних визначень (x1, x2, x3, ..., xn).
Вибіркове середнє ( ) - це середнє арифметичне значення результатiв випадкової вибірки, яке розраховується за формулою:
) - це середнє арифметичне значення результатiв випадкової вибірки, яке розраховується за формулою:
 .
.
Випадкове вiдхилення (di) – це рiзниця мiж результатом окремого визначення та вибірковим середнiм  , що розраховується за формулою:
, що розраховується за формулою:
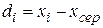 .
.
Вибіркове стандартне відхилення (s) – це величина, яка характеризує розсіювання результатів вимірювань відносно середнього значення:
 .
.
Cтандартне відхилення середнього значення вибiрки ( ) – це величина, яка використовується для оцiнки відтворюваності отриманих результатів і обчислюється за формулою:
) – це величина, яка використовується для оцiнки відтворюваності отриманих результатів і обчислюється за формулою:
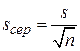 .
.
Абсолютна похибка ( ) або довірчий інтервал середнього арифметичного – це інтервал значень вимірюваної величини, в який з певною довірчою ймовірністю р потрапляє істинне значення випадкової вибірки результатів вимірювання і який розраховують за формулою:
) або довірчий інтервал середнього арифметичного – це інтервал значень вимірюваної величини, в який з певною довірчою ймовірністю р потрапляє істинне значення випадкової вибірки результатів вимірювання і який розраховують за формулою:

де 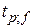 – критерiй Стьюдента (знаходять за таблицею) для числа ступенів свободи f = n - 1 та довірчої ймовірності р.
– критерiй Стьюдента (знаходять за таблицею) для числа ступенів свободи f = n - 1 та довірчої ймовірності р.
– Конец работы –
Эта тема принадлежит разделу:
Титриметричний аналіз
національний університет Львівська політехніка... Титриметричний аналіз Методичні вказівки для студентів хімічних...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Статистична обробка результатів аналізу
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов