Кислотно-основные свойства аминокислот - раздел Химия, ПРОГРАММА БЛОКА ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ Аминокислоты – Амфотерные Вещества, Которые Могут Существовать В Виде Катионо...
Аминокислоты – амфотерные вещества, которые могут существовать в виде катионов или анионов. Это свойство объясняется наличием как кислотной (–СО2Н), так и основной (–NH2) группы в одной и той же молекуле.
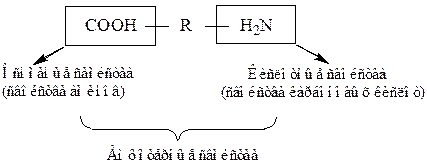
В очень кислых растворах NH2-гpyппa аминокислоты протонируется, и эта кислота становится катионом. В сильнощелочных растворах карбоксильная группа аминокислоты депротонируется и кислота превращается в анион.
В твердом состоянии аминокислоты существуют в виде цвиттер-ионов (известных также под названием диполярных ионов или внутренних солей). В подобных цвиттер-ионах протон переносится от карбоксильной группы к аминогруппе.
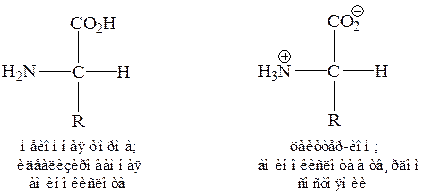
Если поместить аминокислоту в среду, обладающую проводимостью, и опустить туда пару электродов, то в кислых растворах аминокислота будет мигрировать к катоду, а в щелочных растворах – к аноду. При некотором значении рН, характерном для данной аминокислоты, она не будет передвигаться ни к катоду, пи к аноду, так как каждая молекула находится в виде цвиттер-иона (иными словами, она несет как положительный, так и отрицательный заряды). Это значение рН называется изоэлектрической точкой (pI) данной аминокислоты (таблица 2). Изоэлектрическая точка аминокислот редко равна 7, так как зависит от кислотности иона алкиламмония, оснoвности карбоксилат-аниона, влияния на них радикала и присутствия любой дополнительной основной или кислотной группы.
При пропускании постоянного тока через раствор, содержащий смесь нескольких аминокислот, каждая из них будет двигаться к катоду или аноду со скоростью, зависящей от природы этой аминокислоты и от рН среды. Разделение и анализ смесей аминокислот, oснованные на этом явлении, называются электрофорезом.
2. Аминокислоты как биполярные ионы. Хотя аминокислоты обычно изображают как соединения, содержащие амино- и карбоксильную группу H2NCHRCOOH, некоторые их свойства, как физические, так и химические, не согласуются с этой структурой:
· в противоположность аминам и карбоновым кислотам аминокислоты представляют собой нелетучие кристаллические вещества, плавящиеся с разложением при довольно высокой температуре;
· они не растворимы в неполярных растворителях типа петролейного эфира, бензола или эфира и заметно растворимы в воде;
· их водные растворы ведут себя подобно растворам веществ с высоким дипольным моментом;
· константы кислотности и основности для групп СООН и NH2 необычайно малы.
Все эти свойства вполне соответствуют структуре диполярного иона для аминокислот H3N+–CHR–COO–. Физические свойства – температура плавления, растворимость, высокие дипольные моменты – отвечают ожидаемым для подобных солей. Кислотно-основные свойства также становятся понятными, если учесть, что измеряемая Ка в действительности относится к кислотности иона аммония RNH3+
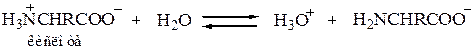
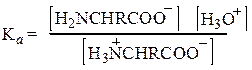
а Кb в действительности относится к основности карбоксилат-иона
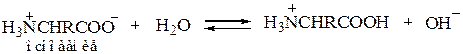
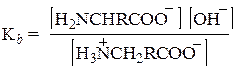
В водном растворе кислотность и основность кислоты и ее сопряженного основания (например, СН3СООН и СН3СОО– или СH3NH3+ и CH3NH2) связаны уравнением Ка·Кb = 10-14. На этом основании можно рассчитать, что Ка = 1,6×10–10 для NH3+-группы глицина означает Кb = 6,3×·10-5для NН2-группы, что кажется вполне приемлемой величиной для алифатического амина. Аналогично Кb = 2,5×10–12 для группы СОО– глицина означает, что Ка = 4×10–3 для СООН-группы, что кажется вполне приемлемой величиной для карбоновой кислоты, содержащей сильную электроноакцепторную (увеличивающую кислотность) NH3+-гpyппy.
При подщелачивании раствора аминокислоты диполярный ион I превращается в анион II; более сильное основание, гидроксил-ион, отрывает протон от иона аммония и вытесняет более слабое основание — амин
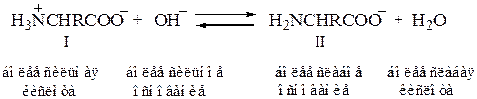
Если подкислить раствор аминокислоты, то диполярный ион I превращается в катион III; более сильная кислота Н3О+ отдает протон карбоксилат-иону и вытесняет более слабую карбоновую кислоту
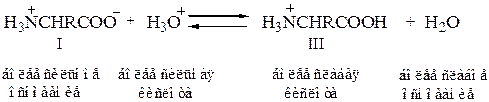
Итак, кислой группой в простых аминокислотах типа глицина является не СООН–, a NH3-гpyппa, а основной — не NH2-гpyппa, а группа COО–.
Необходимо иметь в виду, что ионы II и III, содержащие свободную NH2- или СООН-группу, находятся в равновесии с диполярным ионом I; поэтому аминокислоты вступают в реакции, характерные для аминов и карбоновых кислот. По мере удаления иона II, например при реакции с бензоилхлоридом, равновесие сдвигается в сторону образования иона II, так что постепенно аминокислота полностью бензоилируется.
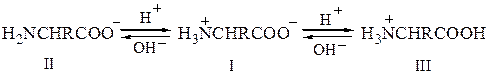
В тех случаях, когда это возможно, желаемую реакцию можно ускорить, создавая нужную концентрацию кислоты или основания в растворе так, чтобы увеличить концентрацию реакционноспособной частицы.
Все темы данного раздела:
ПРОГРАММА БЛОКА ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ.
Углеводы. Моносахариды.Определение, общая формула. Классификация. Номенклатура, изомерия. Структурные и проекционные формулы, антиподы, диастереомеры. D- и L-ряды. Фо
УГЛЕВОДЫ
Углеводы являются важным классом природных органических соединений. Значение углеводов определяется той доминирующей ролью, которая отводится им в живых организмах, и сложностью выполняемых ими фун
МОНОУГЛЕВОДЫ
Классификация. Моносахариды (монозы) классифицируют по количеству атомов углерода и по характеру карбонильной группы.
По количеству атомов углерода:
Химическое строение моносахаридов
Карбонильные формы моносахаридов.Для выяснения строения и стереохимии моносахаридов химикам потребовалось более ста лет. В результате многолетних исследований было установлено,
Способы получения моносахаридов
1. Гидролиз ди- и полисахаридов, который происходит под действием кислот или ферментов, водные растворы щелочей не способствуют гидролизу:
Реакции карбонильных форм моносахаридов
1.1 Окисление. Реакции окисления используют в структурных исследованиях и биохимических анализах для обнаружения моносахаридов. Монозы легко окисляются, причем в зависимости от
Реакции с участием всех гидроксильных групп
2.2.1 Алкилирование. При действии на моносахариды более сильных алкилирующих агентов, например алкилгалогенидов, наряду с гликозидным гидроксилом в реакцию вступают все спиртов
ОЛИГОСАХАРИДЫ
Олигосахариды – сахароподобные сложные углеводы, характеризую-щиеся сравнительно невысокой (несколько сотен) молекулярной массой, хорошей растворимостью в воде, легкой кристаллизацией и, как правил
ДИСАХАРИДЫ
Строение дисахаридов.В зависимости от моносахаридных компонентов олигосахариды (подобно полисахаридам) делятся на:
· гомоолигосахариды, построенные из молекул одного монос
Получение дисахаридов
Практически дисахариды извлекают из природных источников в виде гликозидов. Некоторые из них могут быть получены путем неполного гидролиза полисахаридов. Природные источники являются в настоящее вр
Номенклатура олигосахаридов
Большинство встречающих в природе олигосахаридов имеют тривиальные, общеупотребимые названия (целлобиоза, лактоза, мальтоза, трегалоза, стахиоза, сахароза, рафиноза и целлотриоза), которые им были
Свойства дисахаридов
Дисахариды представляют собой твердые вещества или некристаллизующиеся сиропы, которые растворимы в воде. Как аморфные, так и кристаллические дисахариды плавятся в некотором интервале температур и,
Отдельные представители дисахаридов
Мальтоза, солодовый сахар.Дисахарид получается из крахмала при действии солода, содержащего фермент b-амилазу. Солод (от лат. maltum) – это проросшие, а затем высушенные
Отдельные представители трисахаридов
Принципы построения трисахаридов такие же, как и дисахаридов, т. е. трисахариды могут быть как восстанавливающие, так и невосстанавливающие. Многие из трисахаридов содержатся в растениях. Из трисах
Природные гликозиды
Гликозиды – это простые или сложные эфиры моносахаридов и олигосахаридов, образованные с участием полуацетального гидроксила. Гликозиды чрезвычайно распространены в животном и особенно в растительн
Строение высших полиоз
Несахароподобные полиозы – высокомолекулярные соединения, содержащие сотни и тысячи остатков моносахаридов. Остатки моноз связаны между собой кислородными мостиками, образованными за счет полуацета
ГОМОПОЛИСАХАРИДЫ
Крахмал представляет собой не однородное вещество, а смесь полисахаридов, отличающихся не только степенью полимеризации, но и строением. Изучение химических превращений крахмала бы
ГЕТЕРОПОЛИСАХАРИДЫ
Пектиновые вещества – широко распространенные в природе соединения. Различают растворимые пектиновые вещества и нерастворимые (протопектин). Растворимые пектиновые вещества содержа
Изомерия.
Структурная:
· скелетная;
· взаимного положения;
· метамерия.
Пространственная:
· оптическая
Все природные ам
Получение α-аминокислот
1.1 Из природных веществ. Белки при гидролизе в водных растворах в присутствии кислоты дают смесь α-аминокислот, которые можно выделить и разделить. Все они оптичес
Изоэлектрическая точка аминокислот
Если раствор аминокислоты поместить в электрическое поле, то в зависимости от кислотности или основности раствора будет наблюдаться различная картина. В сильнощелочном растворе концентрация анионов
Комплексные соли с ионами меди
Аминокислоты с ионами переходных металлов (Сu, Zn, Co, Pb, Ag, Hg) образуют прочные хелатные комплексы (от греч. сhele – клешня). Малорастворимые хелаты меди (II) имеют глубокую синюю
Образование сложных эфиров (этерификация).
Карбоксильная группа аминокислоты легко этерифицируется обычными методами. Например, метиловые эфиры получают, пропуская сухой газообразный хлористый водород через раствор аминокислоты в метаноле.
Качественные реакции аминокислот
Особенностью химии аминокислот является многочисленность качественных (цветных) реакций, которые необходимы при исследовании их физико-химическими методами (хроматография, электрофорез).
Практическое применение аминокислот
Аминокислоты широко используются в современной медицине в качестве лекарственных средств. К таким аминокислотам относится глутаминовая кислота, метионин, гистидин, глицин, цистеин.
Глут
ОКСИКИСЛОТЫ
Оксикислотами называются карбоновые кислоты, в которых на ряду с карбонильной группой содержится гидроксильная группа.
Классификация оксикислот, как и других бифункциональ
Способы получения оксикарбоновых кислот.
1. Гидролиз α-галогенкарбоновых кислот
Cинтез из ненасыщенных кислот.
9. Дегидратация (образование лактона).Д
Химические свойства оксикарбоновых кислот.
Оксикислоты, благодаря наличию спиртовой группы, реагируют не только, как кислоты, но и как спирты; гидроксильная группа в этих соединениях может быть замещена галогеном или ацилирована. Некоторые
Оксикислоты
Характерным отличием β-оксикислот от -оксикислот является легкость, с кото
Реакции нуклеофильного замещения α-галогенкарбоновых кислот.
Галоген в α-галогенкарбоновых кислотах легко замещается под действием различных нуклеофильных агентов. В результате этих реакций из α-галогенокарбоновых кислот получают &
Реакции со щелочами
.
2. Взаимодействие со спиртами.
Б) Реакции гидроксильной группы
1. Реакция ацилирования.При ацилировании гидроксикарбоновых кислот галогенангидридами получаются сложные эфиры. Для ацилирования можно использовать и ангидриды кислот:
ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
Гетероциклическими соединениями называют соединения, содержащие циклы, в которых имеется один или несколько гетероатомов – N, О, S или другие атомы, способные образовывать не м
ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ
Общая характеристика пятичленных гетероциклов с одним гетероатомом.К простейшим ароматическим пятичленным гетеро-циклическим соединениям с одним гетероатомом относятся фуран, пирро
Представители пятичленных гетероциклических соединений с одним гетероатомом
Фуран представляет собой пятичленный ароматический гетероцикл с атомом кислорода в кольце:
Производные фурана
Тетрагидрофуран.Тетрагидрофуран получается гидрированием фурана в присутствии никелевого катализатора.
Химические свойства
1. Реакция галогенирования. Для галогенирования тиофена можно использовать бром или хлор при низкой температуре, при этом могут образовываться как моно-, так и полигалогентиофе
Практическое применение тиофена и его производных
Циклическая система тиофена встречается в природе в некоторых продуктах растительного происхождения, но гораздо большее значение имеет это соединение в составе синтетических лекарственных препарато
Основные способы получения
1. Сухой перегонкой аммонийной соли слизевой кислоты или действием аммиака на фуран в присутствии оксида алюминия:
Химические свойства
1.Галогенирование. Осуществляется с помощью хлористого сульфурила, брома в спиртовом растворе и триодид-иона (йод в растворе иодида калия), причем в результате иодирования обра
Применение пиррола и его производных
Пиррол содержится в каменноугольной смоле. Цикл пиррола – структурный фрагмент природных пигментов (например, гема, хлорофиллов, желчи, витамина В12, некоторых антибиотиков), а та
Гемоглобин
Строение и функции гемоглобина.Гемоглобин вляется переносчиком кислорода от легких к тканям тела, представляет собою белок глобин, координационно связанный с гемом (гем – по
Химические свойства
Реакции индола и его простых производных сходны с реакциями пиррола.
1. Индол обладает слабоосновными свойствами и в то же время слабокислыми, образует металлические производные –
Триптофан.
Триптофан [2-амино-3-(3'-индолил)-пропионовая кислота] — бесцветное кристаллическое вещество, Тш = 283–285 °С, растворим в воде, плохо растворим в этаноле и не растворим в
ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
Среди гетероциклических соединений наиболее многочисленна и разнообразна группа пятичленных гетероциклов, содержащих более одного гетероатома. Большинство этих циклических систем можно формально по
Оксазол
Электронное строение.Ароматические свойства оксазола связаны с наличием циклической сопряженной π-электронной системы, построенной из двух π-электронов связ
Пиридин
Способы получения пиридина и пиридиновых оснований. В небольших количествах пиридини его метил- и этилпроизводные получают из каменноугольной смолы, которая содержит около 0,2 % см
Химические свойства
1. Восстановление водородом. При восстановлении водородом в момент выделения (действуя натрием на спиртовой раствор пиридина А.Н. Вешнеградский) или над катализатором пиридин п
ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
Пиримидин. Является важнейшим из шестичленных гетероциклов с двумя атомами азота. Пиримидиновый цикл входит в многочисленные природные соединения: нуклеиновые кислоты, витамины, коферменты, являетс
Химические свойства
1. Основные свойства:
Образование солей:
ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ДВУМЯ РАЗНЫМИ ГЕТЕРОАТОМАМИ
Оксазины. Оксазиновое кольцо входит в состав многих органических веществ, имеющих большое практическое значение. Среди последних – широко распространенные красители, лекарст
Нобелевские премии по органической химии
Герман Эмиль Фишер
"За эксперименты по синтезу веществ с сахаридными и пуриновыми группами".
Адольф фон Бай
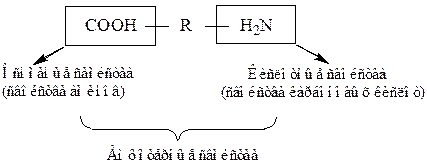
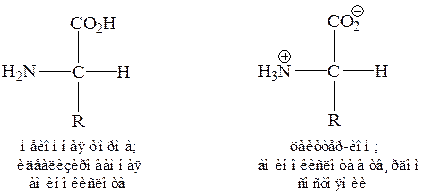
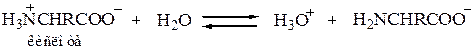
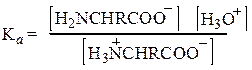
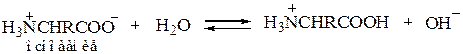
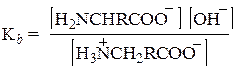
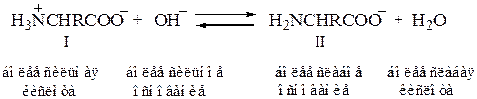
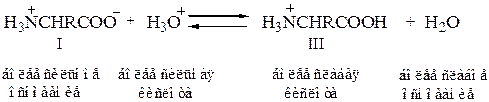
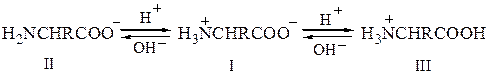







Новости и инфо для студентов