рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
Реферат Курсовая Конспект
ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ - раздел Химия, ПРОГРАММА БЛОКА ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ Пиримидин. Является Важнейшим Из Шестичленных Гетероциклов С Двумя Атомами Аз...
Пиримидин. Является важнейшим из шестичленных гетероциклов с двумя атомами азота. Пиримидиновый цикл входит в многочисленные природные соединения: нуклеиновые кислоты, витамины, коферменты, является составной частью кольца пуринов, например мочевой кислоты:
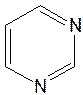
Сопряженная кольцевая система молекулы пиримидина состоит из шести p-электронов (4 электрона от атомов углерода и 2 электрона от двух атомов азота) и обеспечивает его высокую ароматичность, энергия сопряжения 109,2 кДж/моль (для бензола 150,7 кДж/моль). Наличие двух электроотрицательных атомов азота в цикле приводит к еще более неравномерному распределению электронной плотности, чем в пиридине. Здесь наблюдается сильное наложение мезомерного и индуктивного эффектов.
В положениях 2,4 и 6, где влияние–I эффекта атомов азота проявляется особенно сильно, будет наибольший положительный электронный заряд, т. е. наименьшая электронная плотность, в то же время положение 5 испытывает наименьшую потерю электронов, где и будет наибольшая электронная плотность. Нуклеофильные реагенты атакуют положения 2, 4, 6, а электрофильные – положение 5 в соответствии с поляризацией этих положений.
Взаимодействие НЭП атомов азота с p-электронами в ароматической системе приводит к уменьшению основности атомов азота пиримидина и поэтому она значительно ниже, чем у пиридина. Вследствие этого протонирование по атомам азота пиримидина протекает лишь в очень сильных кислотах и приводит к образованию соли только по одному атому азота. Сам пиримидин инертен к электрофильной атаке. И только введение электронодонорных заместителей (–NH2, –OH, –SH) в положения 2, 4, 6 делает возможным электрофильную атаку положения 5 кольца пиримидина. Пиримидин с двумя электронодонорными заместителями вступает в электрофильное замещение как бензол, а с тремя электронодонорными заместителями в кольце реагирует легко, подобно фенолу. Например, нитрование требует двух электронодонорных групп (при взаимодействии 2 амино-4-гидроксипиримидина с азотной кислотой получается 2-амино-4-гидрокси-5-нитропиримидин):
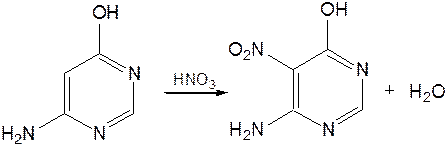
Для галогенирования достаточно одной электронно-донорной группы. Так, 2-аминопиримидин хлорируется и бромируется в положение 5:
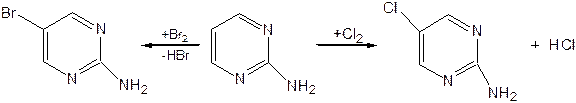
Значительно больше распространены в ряду пиримидина реакции нуклеофильного замещения. При этом речь идет о нуклеофильном замещении различных групп, находящихся в положениях 2, 4, 6. Так, при действии амида натрия на 6-метилпиридин образуются 2-амино- и 2,4-диамино-6-метилпиримидин:
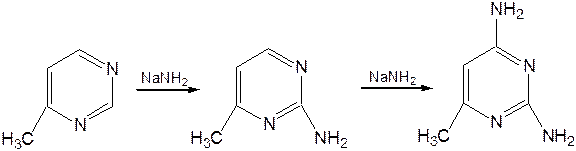
Следует отметить, что алкильные группы в положениях 2, 4 и 6 пиримидина обладают повышенной активностью: легко вступают в конденсацию с альдегидами и в реакцию азосочетания.
Тимин, цитозин, урацил.При гидролизе нуклеиновых кислот получаются три важных производных пиримидина: цитозин (4-амино-2-гидроксипиримидин), тимин (2,4-дигидрокси-5-метилпиримидин) и урацил (2,4-дигидроксипиримидин), которые относятся к группе пиримидиновых оснований. Одним из важных свойств пиримидиновых азотистых оснований является возможность их существования в двух таутомерных формах – лактим-лактамной формах, в зависимости от значения рН среды, при рН 7,0 они находятся в лактамной форме, которая и является главной таутомерной формой. Лактимные и лактомные формы цитозина, тимина и урацила:
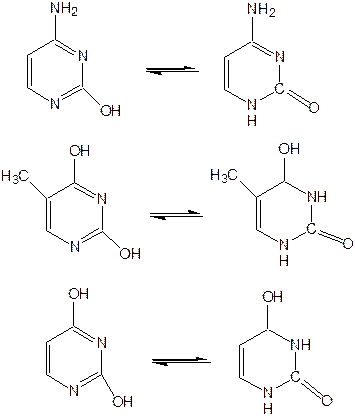
Лактимная форма присутствует только в растворах в кислой среде в весьма незначительном количестве. Помимо главных пиримидиновых оснований в составе нуклеиновых кислот открыты минорные пиримидиновые основания: 5-метил и 5-оксиметилцитозин, дигидроурацил, псевдоурацил, 1-метилурацил, 4-тиоурацил и др. На долю минорных оснований приходится до 10 % всех нуклеотидов транспортных рибонуклеиновых кислот (т-РНК), что имеет важный физиологический смысл – защита молекулы РНК от действия гидролитических ферментов.
Витамин В1(тиамин) тоже содержит пиримидиновый цикл, соединенный метиленовой связью с кольцом тиазола:
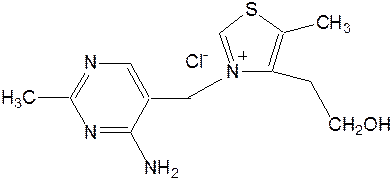
Отсутствие витамина В1 в пище, например, при питании ободранным рисом (он содержится в рисовых отрубях), вызывает известное на востоке нервное заболевание бери-бери. Суточная потребность в витамине В1 для человека – 4 мг. Необходимость в нем связана с тем, что витамин В1 в виде дифосфата ТДФ (тиаминдифосфат) входит в структуру двух сложных ферментных систем: пируват- и a-кетоглутаратдегидрогеназных комплексов, катализирующих окислительное декарбоксилирование пировиноградной и a-кетоглутаровой кислот и других оксокислот, образующихся при распаде аминокислот с разветвленной боковой цепью. Основное количество витамина В1 человек получает с растительной пищей, а также им богаты печень, почки, мозг.
Диазины.Нуклеофильное замещение галогена в диазинах идет по механизму присоединения – элиминирования (А-Е). Однако существуют примеры нуклеофильного замещения с принципиально другим механизмом. Один из этих процессов – взаимодействие 2-хлоро-4-фенилпиримидина с амидом калия в жидком аммиаке, приводящее к 2-амино-4-фенилпиримидину. Очевидно, что нуклеофильное замещение в данном случае протекает через промежуточное раскрытие цикла. Нуклеофильная атака амид-ионом по положению 6 пиримидин ового кольца объясняет распределение меченых атомов азота в аминопроизводном.
Все хлородиазины более активны, чем хлоропиридины, что обусловлено присутствием второго атома азота, причем факторы скоростей замещения лежат довольно в узком интервале. Наиболее быстро замещение хлора протекает в 2- и 4-хлоропиримидинах, тогда как атом хлора в положении 5 пиримидина наименее активен. Это согласуется с селективной активацией положений 2, 4 и 6 пиримидина, обсужденной выше. Нуклеофильное замещение при С4 в 4-хлоропиримидине протекает через интермедиат, в резонансной стабилизации которого принимают участие два гетероатома.
Пурин. Бициклическая система пурина состоит из двух гетероциклов – пиримидина и имидазола, сконденсированных между собой. Открыл пурин немецкий химик Э. Фишер:
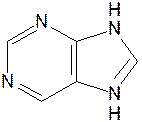
Производные пурина имеют исключительное биологическое значение прежде всего потому, что входят вместе с пиримидиновыми основаниями в структуру нуклеиновых кислот и имеют, таким образом, отношение к программированию синтеза белков и к явлениям наследственности.
Пурин является ароматической системой с энергией делокализации, равной 243,6 кДж/моль (для бензола – 150,7 кДж/моль). Пиримидиновое кольцо в пурине в целом имеет дефицит электронов, а имидазольное кольцо – избыток электронов. Поскольку в пурине имеет место перекрывание p-электронных облаков двух моноциклических систем, то электронная плотность в каждом цикле в определенной степени может изменяться в результате перехода электронов из имидазольного цикла в пиримидиновый.
Таким образом, пурин – это ароматическая система сильно делокализованных p-электронов, обладающая лабильной «переливающейся» электронной плотностью, в результате чего возможны таутомерные превращения. Кроме этого, эта система является прекрасным донором электронов вследствие низкой энергии высшей заполненной молекулярной орбитали.
Электронно-донорные заместители в кольце пиримидина способствуют восстановлению электронной плотности в имидазольном цикле. Реакции нуклеофильного замещения в пурине идут в основном в положение 8 имидазольного кольца, но возможна атака нуклеофильными реагентами атомов углерода в положениях 2 и 6 пиримидинового цикла. Реакции электрофильного замещения возможны лишь при наличии электронодонорных заместителей в кольце пиримидина, и замещение происходит по углероду С8 имидазольного цикла.
Все реакции пуриновых соединений можно разделить на две группы: реакции по атомам азота и реакции по атомам углерода кольца. Пуриновые основания – сравнительно слабые основания, но электрофильная атака по атому азота весьма распространена, причем выбор атома азота при электрофильной атаке определяется степенью основности того или иного атома азота. В незамещенном пурине таким является N1, в мочевой кислоте алкилированию сначала подвергается N9, а затем N3 и N1; в кислой среде алкилирование замещенных пуринов происходит в основном в положение 9. Аденин, единственный их всех пуринов, показывает небольшую реакционную способность в положении 3.
Аденин(6-аминопурин) является одним из наиболее распространенных пуриновых оснований (амино- и имино-форма):

Аденин существует практически в амино-форме, т. к. энергия делокализации для амино-формы наибольшая. В связанном виде аденин содержится в нуклеиновых кислотах и легко получается при их гидролизе. В свободном состоянии встречается в некоторых растениях (чай, сахарная свекла, хмель), в грибах, дрожжах, бактериях и т. д. Аденин является наиболее устойчивым в термодинамическом отношении соединением среди природных пуриновых и пиримидиновых оснований.
Гуанин(2-амино-6-гидроксипурин) вместе с аденином и пиримидиновыми основаниями входит в состав нуклеиновых кислот (лактимная и лактамная формы):
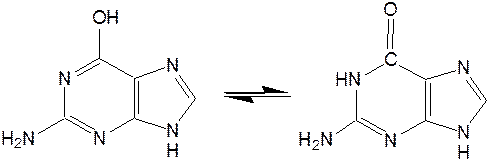
Наиболее устойчивой является лактамная форма, в которой гуанин и находится в природных нуклеиновых кислотах. Значительные количества гуанина содержатся в чешуе и коже рыб, пресмыкающихся и амфибий, от чего зависит их блеск. К таким соединениям относится аденозинтрифосфат (АТФ) – переносчик энергии в биохимических реакциях и фосфорилирующий агент.
Мочевая кислота.Мочевая кислота является первым соединением пуринового ряда, открытым Шееле еще в 1776 г. Однако прошло более ста лет, пока строение ее было точно установлено. В настоящее время принято считать, что мочевая кислота существует в оксоформе.
Она является одним из ключевых соединений в синтезе пуриновых оснований служит мочевая кислота (2, 6, 8-тригидроксипурин), играющая у птиц и рептилий роль вещества, выводящего из организма избыток азота (как мочевина у млекопитающих). Соли мочевой кислоты (ураты) откладывается при неправильной работе организма в суставах и в виде почечных камней. Мочевая кислота (окси- и оксо-форма):
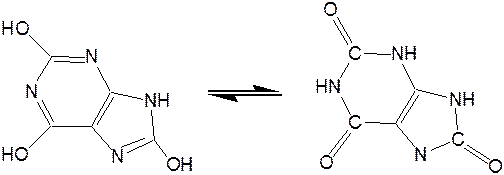
Алкалоиды.Представляют собой азотистые основания природного происхождения с сильным биологическим действием.
Физические свойства.Алкалоиды – основания нерастворимы в воде (кроме кофеина, никотина), но растворимы в органических растворителях. Соли алкалоидов растворимы в воде, но нерастворимы органических растворителях (исключение – хинин HBr растворим в CHCl3).
– Конец работы –
Эта тема принадлежит разделу:
ПРОГРАММА БЛОКА ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ
ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ УГЛЕВОДЫ Углеводы служат основным... НЕСАХАРОПОДОБНЫЕ ПОЛИСАХАРИДЫ Строение высших... АМИНОКИСЛОТЫ...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов