рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- ПРОГРАММА БЛОКА ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ
Реферат Курсовая Конспект
ПРОГРАММА БЛОКА ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ
ПРОГРАММА БЛОКА ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ - раздел Химия, Программа Блока Гетерофункциональ...
ПРОГРАММА БЛОКА ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ.
Дисахариды.Общие формулы. Типы дисахаридов. Проекционные и перспективные формулы. Отличие химических свойств восстанавли-вающих и… Полисахариды.Природные полимеры. Крахмал, образование в растениях, строение.… Аминокислоты.Изомерия, номенклатура. Синтез аминокислот. Получение аминокислот из природных веществ. Аминирование.…КОНСПЕКТ ЛЕКЦИЙ
ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ
УГЛЕВОДЫ
Углеводы служат основным компонентом пищи млекопитающих, а человека обеспечивают пищей, одеждой и жилищем. Только растения способны осуществлять… солнечнаяМОНОУГЛЕВОДЫ
По количеству атомов углерода: · триозы – сахара с тремя атомами углерода; · тетрозы – с четырьмя;Химическое строение моносахаридов
Это доказано восстановлением её в 2-иодгексан при действии йодистого…Способы получения моносахаридов
2. Альдольная конденсация формальдегида – первый синтез сахаров был произведен еще А.М. Бутлеровым, в качестве…Реакции карбонильных форм моносахаридов
1.1.1 При использовании мягких окислителей типа бромной воды, гипохлоритов, разбавленной азотной кислоты окисляется только альдегидная группа и…Реакции с участием всех гидроксильных групп
Большое практическое значение имеют триметилсилиловые эфиры моносахаридов (ТМС-эфиры). Моносахариды – нелетучие…ОЛИГОСАХАРИДЫ
В зависимости от количества остатков моносахаридов, входящих в молекулы олигосахаридов, различают: · дисахариды (биозы), гидролизующиеся на две молекулы моносахаридов; · трисахариды (триозы), гидролизующиеся на три молекулы моносахаридов и т.д.ДИСАХАРИДЫ
· гомоолигосахариды, построенные из молекул одного моносахарида; · гетероолигосахариды, в состав которых входят остатки различных… По химическому строению дисахариды являются гликозидами моносахаридов (полные ацетали), агликонами которых служат…Получение дисахаридов
Номенклатура олигосахаридов
Дисахариды.Невосстанавливающий дисахарид может быть назван как гликозил-гликозид, а восстанавливающий как гликозил-гликоза, по образующим его… Трисахариды. Невосстановливающий трисахарид рафиноза имеет название:…Свойства дисахаридов
В соответствии со своим химическим строением все дисахариды являются гликозидами и поэтому легко гидролизуются минеральными кислотами и сравнительно… Мальтоза + Н2O ¾® a-D-глюкоза + a-D-глюкозаОтдельные представители дисахаридов
Мальтоза кристаллизуется из водных растворов в виде моногидрата, не имеющего резко выраженной точки плавления. Водные растворы мальтозы… Под действием фермента a-глюкозидазы (мальтазы) солодовый сахар гидролизуется… Схемы мутаротации мальтозы:Отдельные представители трисахаридов
Рафиноза(мелитриоза) С18Н32О16. Встречается во многих растениях, в частности в семенах хлопчатника и в сахарной свекле; не имеет сладкого вкуса.…Природные гликозиды
Гликозид амигдалин содержится в семенах горького миндаля, в косточках персика, абрикосов и слив, вишен, яблок, груш, в листьях лавровишни и т. д.…НЕСАХАРОПОДОБНЫЕ ПОЛИСАХАРИДЫ
Строение высших полиоз
Таким образом, полимерные цепи полиоз по своему строению представляют собой полигликозиды (полиацетали). В полисахаридах растительного происхождения… Классификация высокомолекулярных полисахаридов.По строению высшие полиозы… · гомополисахариды, состоящие из остатков одного какого-либо моносахарида.ГОМОПОЛИСАХАРИДЫ
Крахмал представляет собой белый аморфный порошок («картофельная мука»). Высушенный при 100–110 °С крахмал очень гигроскопичен. В холодной воде он… Крахмал практически не обладает восстанавливающей способностью: он не…ГЕТЕРОПОЛИСАХАРИДЫ
Основу всех пектиновых веществ составляет полигалактуроновая (пектовая) кислота, построенная из остатков D-галактуроновой кислоты, соединенных…АМИНОКИСЛОТЫ
Аминокислоты – органические гетерофункциональные соединения, молекулы которых содержат одновременно амино- (–NH2) и карбоксильную (–COOH) группы. Общая формула:
(NH2)m R(COOH)n,
где m – число аминогрупп, а n – число карбоксильных групп. В более широком смысле к аминокислотам могут быть отнесены и соединения с иной кислотной функцией, например, аминосульфоновые кислоты.
Классификация аминокислот
По числу функциональных (амино и карбоксильных) групп:
· моноаминомонокарбоновые;
· диаминомонокарбоновые;
· аминодикарбоновые и т. д.
От природы углеводородного радикала аминокислоты:
· ароматические
· гетероциклические
От взаимного расположения амино- и карбоксильной групп:
· α-аминокислоты;
· β-аминокислоты;
· γ-аминокислоты и т. д.
По отношению к биологическим организмам:
· Заменимые. Синтезируются в организме человека. К ним относятся глицин, аланин, глутаминовая кислота, серин, аспарагиновая кислота, тирозин, цистеин.
· Незаменимые. Не синтезируются в организме человека в количествах, достаточных для того, чтобы удовлетворить физиологические потребности организма, поступают с пищей.
Номенклатура аминокислот. Простейшим соединением ряда аминокислот является глицин NH2–CH2–COOH.
Для названия аминокислот используют следующие номенклатуры:
· тривиальная;
· рациональная;
· систематическая.
Тривиальная. Родоначальники гомологических рядов алифатических и ароматических аминокислот – глицин и аминобензойная кислота соответственно. Происхождение этих исторических названий связано со свойствами и названиями продуктов, из которых они впервые были выделены. Глицин имеет сладкий вкус, впервые был выделен из «животного клея» (от греч. glycos – сладкий и kolla – клей и произошло название гликокол). Цистин выделен из камней желчного пузыря (от греч. «цистис» – пузырь). Лейцин получен из молочного белка – казеина (от греч. «леукос» – белый). Аспарагиновая кислота изолирована от ростков спаржи (от греч. «аспарагус» – спаржа). Орнитин выделен из помёта птиц (от греч. «орнитус» – птица).
Рациональная. Производится путём прибавления к названию соответствующей карбоновой кислоты (название кислоты используется тривиальное), приставки амино-. Буквой греческого алфавита указывается положение аминогруппы по отношению к карбоксильной группе.
Систематическая номенклатура. Название производится от названия соответствующей карбоновой кислоты с указанием местоположения аминогруппы и заместителей при помощи локантов. В названиях алифатических аминокислот по заместительной номенклатуре аминогруппа обозначается префиксом амино-, а карбоксильная группа как старшая – суффиксом -овая кислота. В названиях ароматических аминокислот в качестве родоначальной структуры используется бензойная кислота. Для аминокислот, участвующих в построении белков, применяются в основном тривиальные названия. В природе встречается свыше 70 аминокислот, но только 20 из них играют важную роль в живых системах (таблица 1).
Все аминокислоты, за исключением пролина и оксипролина, имеют структуру R–CH(NΗ2)CO2H; различия между аминокислотами определяются природой радикала.
Таблица 1 – Названия аминокислот по различным номенклатурам
| № | Формула | Название соединения | ||
| Тривиальное | Рациональное | Систематическое | ||
| NH2–CH2–COOH | Глицин (гликокол) (Gly) | аминоуксусная | аминоэтановая | |
| CH3––CHNH2–COOH | Аланин (Ala) | α-амино-ропионовая | 2-аминопропановая кислота | |
| NH2–(CH2)2–COOH | β-Аланин (Ala) | β-амино- пропионовая | 3-аминопропановая кислота | |
| (CH3)2–(CH)2NH2–COOH | Валин (Val) | α-амино- изовалериановая | 2-амино-3-метил-бутановая | |
| CH3–CH2–CHNH2–COOH | – | α-амино- масляная | 2-аминобутановая | |
| CH3–CHNH2–CH2–COOH | – | β-амино- масляная | 3-аминобутановая | |
| NH2–(CH2)3–COOH | – | y-амино- масляная | 4-аминобутановая | |
| NH2C–(CH3)2–COOH | – | α-амино- изомасляная | 2-амино-2-метил-пропановая | |
| (CH3)2–CH–CH2–CH(NH2)–COOH | Лейцин (Leu) | α-амино- изокапроновая | 2-амино-4-метилпентановая | |
| CH3–CH2–CH(CH3)–CH(NH2)–COOH | Изолейцин (Ile, ileu) | α-амино- β-метил-β-этил- пропионовая | 2-амино-3-метилгексановая | |
| C6H5–CH2–CH(NH2)–COOH | Фенилаланин (Phe) | α-амино-β-фенил- пропионовая | 2-амино-3-фенилпропановая | |
| HO–CH2–CH(NH2)–COOH | Серин (Ser) | α-амино-β-окси-пропионовая | 2-амино-3-оксипропановая | |

| Пролин (Pro) | пирролидин-α-карбоновая | пирролидин-2-карбоновая | |
| NH–OH–(CH2)2–(CH)2–COOH | Оксипролин (Hydro) | y-оксипирролидин-α-карбоновая | 3-оксипирролидин-2-карбоновая | |
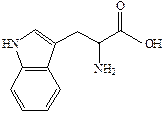
| Триптофан (Try) | α-амино-β-индолил-пропионовая | 2-амино-3-индолил-пропановая | |
| CH3–S–(CH2)2–CH(NH2)–COOH | Метионин (Met) | α-амино-y-метил-тиомасляная | 2-амино-4-метилтио-бутановая | |
| COOH–CH2–CH(NH2)–COOH | Аспарагиновая кислота (Asp) | аминоянтарная | аминобутан-диовая | |
| NH2–CO–CH2–CH(NH2)–COOH | Аспарагин [Asp(NH2) или asn] | |||
| COOH–(CH2)2–CH(NH2)–(COOH)2 | Глутаминовая кислота (Glu) | α-аминоглутаровая | 2-аминопентан-диовая | |
| NH2–CO–(CH2)2–CH(NH2)–COOH | Глутамин [Glu(NH2)] | |||
| NH2–(CH2)4–CH(NH2)–COOH | Лизин (Lys) | α,ε-диамино-капроновая | 2,6-диамино-гексановая | |
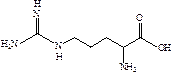
| Аргинин (Arg) | α-амино- δ-гуанидино-валериановая | 2-амино-5-гуанидино-пентановая | |

| Гистидин (His) | α-амино- β-имидазолил-пропионовая | 2-амино-3-имидазолил-пропановая | |
| CH3–CH(OH)–CH(NH2)–COOH | Треонин (Thr) | α-амино-β-окси-масляная | 2-амино-3-оксибутановая | |
| HO–(C6H4)–CH2–CH(NH2)–COOH | Тирозин (Tyr) | α-амино-β-(n-гидроксифенил)-пропионовая | 2-амино-3-(n-гидроксифенил)-пропановая | |
| HS–CH2–CH(NH2)–COOH | Цистеин (Cys) | α-амино-β-тио-пропионовая; α-амино- β-меркапто-пропионовая | 2-амино- 3-меркапто- пропановая | |
| COOH–CH(NH2)–CH2–S2–CH2–CH(NH2)–COOH | Цистин (Cys-scy) | β,β'-дитиоди- α-амино- пропионовая | 3,3'-дитио- 2-амино-пропановая |
Изомерия.
· скелетная; · взаимного положения; · метамерия.Получение аминокислот
Получение α-аминокислот
1.2 Получение из α-галогенкарбоновых кислот in vitro (аминирование или аммонолиз, реакция Геля–Фольгарда–Зелинского). Реакция протекает по…Кислотно-основные свойства аминокислот
Изоэлектрическая точка аминокислот
Комплексные соли с ионами меди
4. Образование медной соли аминоуксусной кислоты. В комплексной медной соли аминоуксусной кислоты двувалентная медь связана ковалентными связями с…5.1.1

5.1.2
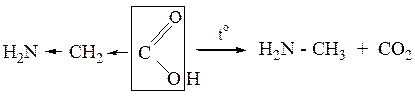
5.1.3
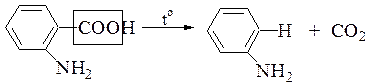
5.1.4 Реакция декарбоксилирования используется для идентификации соответствующих кислот по образованию СО2.
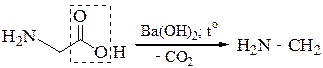
В живых организмах эта реакция протекает под воздействием ферментов-декарбоксилаз. При этом образуются биогенные амины, обладающие высокой физиологической активностью. При карбоксилировании аминокислоты гистидина образуется гистамин, который снижает кровяное давление и усиливает действие желез внутренней секреции:

Декарбоксилирование глутаминовой кислоты приводит к образованию γ-масляной кислоты – главного тормозного медиатора системы.
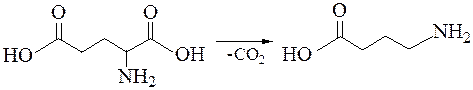
Некоторые амины обладают ярко выраженной биологической активностью, и декарбоксилирование аминокислот служит важным источником их возникновения. Особенно существенным является образование дофамина при декарбоксилировании диоксифенилаланина, поскольку дофамин — это биологический предшественник адреналина.
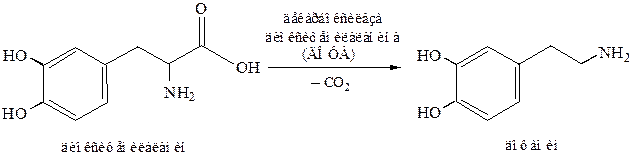
Декарбоксилирование глутаминовой кислоты играет важную роль, так как возникающую в результате реакции y-аминомасляную кислоту можно рассматривать как природный «транквилизатор».
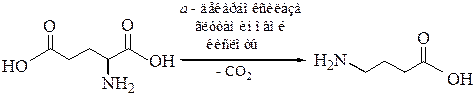
Декарбоксилаза глутаминовой кислоты нуждается в присутствии пиридоксальфосфата для того, чтобы катализировать превращение глутаминовой кислоты в у-аминомасляную. Животные, пища которых не содержит пиридоксина (предшественника пиридоксальфосфата), страдают судорогами, напоминающими эпилепсию. Потребность живых организмов в «витамине В6» — группе соединений, включающей пиридоксаль, пиридоксин и пиридоксамин, связана с тем, что около двадцати биологических реакций аминокислот нуждаются в пиридоксальфосфате в качестве «кофермента».
1. Взаимодействие с основаниями. Существование бетаинов даёт возможность образованию обычных солей. В результате взаимодействия глицина с гидроксидом натрия получается соль глицинат натрия и вода.

2. Превращение карбоксильной группы в галогенангидридную. При действии на аминокилоту хлорида фосфора (V) образуются соли её хлорангидрида:
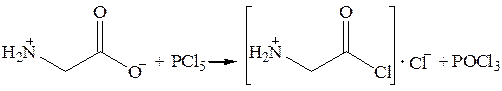
Нейтрализация кислоты (HCl) приводит к образованию очень неустойчивых свободных хлорангидридов.
3. Образование комплексонов. С ионами тяжёлых металлов образуются соли, в которых возможна внутрикомплексная связь.
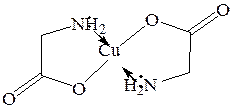
Наиболее известным комплексоном является этилендиаминтетрауксусная кислота.
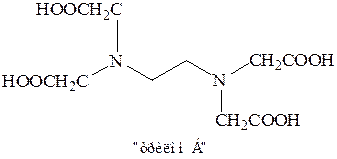
Образование сложных эфиров (этерификация).
Качественные реакции аминокислот
1. Нингидриновая реакцияприменяется для качественного и количественного анализа (обнаружения) в аминокислотных анализаторах для…Практическое применение аминокислот
Глутаминовая кислота участвует в обмене белков и углеводов, способствует синтезу нейромедиатора ацетилхолина, АТФ, переносу ионов К+, стимулирует… Метионин относится к числу незаменимых аминокислот, необходимых для… Метионин применяют для лечения и предупреждения заболеваний и токсических поражений печени (цирроз, отравление…ОКСИКИСЛОТЫ
Классификация оксикислот, как и других бифункциональных соединений, основана: · на взаимном расположении функциональных групп; · природе углеводородного радикала;Изомерия оксикислот
Структурная:
· скелетная;
· изомерия взаимного положения;
· метамерия.
Пространственная:
· оптическая.
Способы получения оксикарбоновых кислот.
Окисление непредельных кислот по Вагнеру
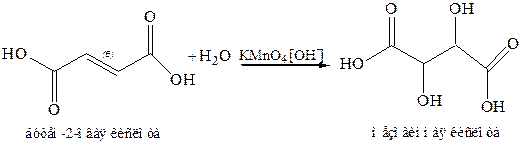
Брожение сахаров
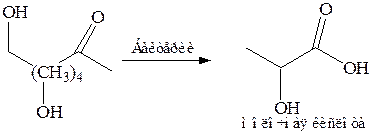
Синтез из альдегидов
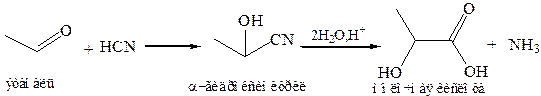
Cинтез из ненасыщенных кислот.
9. Дегидратация (образование лактона).Для оксикислот разных типов дегидратация… Выше уже говорилось о том, что β-оксикислоты ( подобно β-оксиальдегидам или β-оксикетонам) легко…Физические свойства оксикислот
Таблица – 1. Основные свойства оксикислот
| Название кислоты | Ткип, ⁰С | Кдис в воде при 25 ⁰С |
| Гликолевая | 1,48×10-4 | |
| D, L-молочная | 1,39×10-4 | |
| D-молочная | 8,4×10-4 | |
| L-молочная | – | – |
| Оксипропионовая | – | – |
| Тартронная | 5×10-3 | |
| D, L-яблочная | 130–131 | 3,9×10-4 |
| D-яблочная | 98–99 | – |
| L-яблочная | – | – |
| виноградная | 204–206 | 1,04×10-3 |
| D-винная | 1,1×10-3 | |
| L-винная | – | – |
| мезовинная | 6,0×10-4 | |
| лимонная | 8,3×10-4 | |
| D-глюконовая | 125–126 | – |
Химические свойства оксикарбоновых кислот.
Оксикислоты
1. 1. Нагревание α-оксикислот c разбавленными растворами серной или соляной кислот.α-Оксикислоты расщепляются с образованием кислоты и соответствующего альдегида
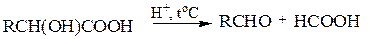
Оксикислоты
1. Нагревание β-оксикислотc разбавленными растворами серной или соляной кислот:Оксикислоты
3.1 Образование лактонов. При выделении свободных γ-оксикислот из их солей, они более или менее легко превращаются в соответственные лактоны:

Реакции нуклеофильного замещения α-галогенкарбоновых кислот.
α-Галогензамещенные кислоты реагируют и со слабыми нуклеофильными реагентами, причем особый интерес представляет нуклеофильное замещение,…А) Реакции карбоксильной группы
Реакции со щелочами
. 2. Взаимодействие со спиртами.В кислой среде гидроксикислоты со спиртами образуют сложные эфиры (реакция…Б) Реакции гидроксильной группы
2. Реакция с галогеноводородами.Происходит нуклеофильное замещение спиртовой гидроксильной группировки на галоген и…ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
2Н, 3Н-оксол 1,3-диазин 4H,1,4-тиазин Номенклатура гетероциклических соединений.ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ
фуран тиофен пиррол Способы получения.Для построения пятичленного гетеро-циклического кольца чаще всего применяют разнообразные реакции…Представители пятичленных гетероциклических соединений с одним гетероатомом
Реакция диенового синтеза с малеиновым ангидридом

Производные фурана
Тиофен
История открытия.В. Мейер утверждал, что открытие им тиофена в 1883 г. было делом случая. В ходе лекции ему понадобилось показать образование индофенина – вещества темно-голубого цвета, которое образуется при смешивании бензола, выделенного из каменноугольной смолы, с изатином и концентрированной серной кислотой. До этого времени образование голубого вещества считалось характерной пробой на бензол. Мейер, который был осторожным и искусным экспериментатором, получил индофенин из каменноугольного бензола как раз перед началом лекции. Естественно, что он был весьма удивлен, когда оказался не в состоянии получить голубое вещество при демонстрации во время лекции. После того как его ассистент Зандмейер сообщил ему, что для лекционной демонстрации был взят другой образец бензола, а именно полученный декарбоксилированием бензойной кислоты. Мейер сразу же принялся за исследование обычного бензола, получаемого из каменноугольной смолы, и обнаружил, что он содержит небольшое количество органического сернистого соединения; оказалось, что индофенин образуется не из бензола, а из этого вещества. Было установлено, что оно является новым родоначальным соединением, которое хотя и весьма отличается от бензола по своему строению, однако поразительно сходно с ним по некоторым физическим и химическим свойствам, включая значительное число типичных реакций бензола, и во многих случаях дает производные, подобные производным бензола. Желая подчеркнуть это сходство, а также отразить наличие серы, Мейер назвал новое соединение тиофеном и немедленно начал изучение его свойств. В 1888 г. Мейер опубликовал монографию по тиофену и его производным, которая содержала огромное число сведений относительно химии этого уникального гетероциклического соединения.
Электронное строение.Электронная структура тиофена, как пиррола и фурана, основана на ароматическом секстете электронов, состоящем из 4 π-электронов, двух двойных углерод-углеродных связей и двух p-электронов атома серы. Однако в отличие от атомов азота и кислорода атом серы обладает еще и свободными d-орбиталями, которые, как показали исследования, также могут участвовать в образовании тиофенового кольца.
Современные электронные модели тиофена и строятся либо с учетом s-орбиталей, либо без учета их. В последнем случае тиофеновый цикл отличается по электронной структуре от фуранового или пиррольного цикла лишь меньшей электроотрицательностью атома серы по сравнению с атомами кислорода или азота.
Уменьшение электроотрицательности атома серы связано с увеличением электронной оболочки атома серы и появлением экранирующего электронного «пояса» между ядром атома и внешними электронами. Поэтому неподеленная электронная пара атома серы, входящая в кольцевую сопряженную систему тиофена, более делокализована, чем соответствующие неподеленные пары электронов у атомов кислорода или азота в фуране и пирроле. Этим обстоятельством объясняется большая ароматичность молекулы тиофена по сравнению с фураном и пирролом. По значению энергии делокализации 130,2 кДж/моль тиофен заметно приближается к бензолу.
Химические свойства
Получение тиофена
1. В промышленности тиофен получают из бутана и паров серы или диоксида серы (SO2) при высокой температуре:
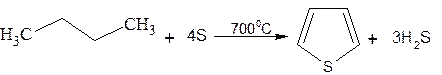
2. Пиролизом:
2.1

2.2
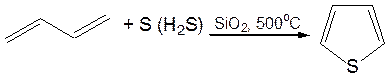
2.3

Практическое применение тиофена и его производных
Производные тиофена находят практическое применение в производстве различных красителей, пластификаторов, пластмасс, аналитических реагентов,… Тиоиндиго – кубовый краситель красного цвета. Синтез тиоиндиго проводится по… Используют тиофен в органическом синтезе.Основные способы получения
Химические свойства
2. Сульфирование. Пиррол осмоляются при действии минеральных кислот (проявляют…Применение пиррола и его производных
Пиррол умеренно токсичен; его пары вызывают стойкое и упорное повышение температуры тела, ЛД50 74 мг/кг (кролики, перорально). Пиррол используют для синтеза пирролидина и некоторых лекарственных средств.… Кольцо пиррольно структурного фрагмента содержит биологически активных соединения, например никотин, алкалоиды группы…Гемоглобин
Способы получения индола
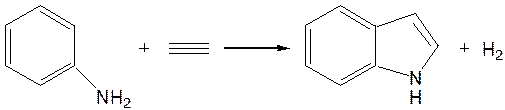
1. Реакция А.Е.Чичибабина пропускание смеси анилина и ацетилена через нагретые трубы при 700 °С:
2.Реакция Э.Фишера нагревание фенилгидразонов с хлоридом цинка, серной или фосфорной кислотами:

Химические свойства
1. Индол обладает слабоосновными свойствами и в то же время слабокислыми, образует металлические производные – индол-калий, индол-натрий:Производные индола
Гетероауксинили 3-индолилуксусная кислота получают используя N-магнийиндол. Он стимулирует рост корней растений и является гормоном роста:
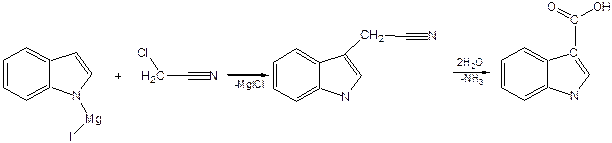
Триптофан.
ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
Имидазол – более сильное основание, чем пиразол, что проявляется в образовании межмолекулярных водородных связей, а, следовательно, и в более…Оксазол
Избыток положительного заряда на атоме кислорода объясняется тем, что кислород отдает НЭП в кольцевую систему электронов оксазола; положительный… Химические свойства.Оксазолы являются очень слабыми основаниями. По-видимому,… Один из механизмов кислотного гидролиза оксазолов предполагает присоединение протона по атому азота с последующей…ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ
Пиридин
Пиридиновые основания извлекают также из каменноугольной смолы путем обработки разбавленной серной кислотой легкого (Ткип. до 160 °С) и среднего… Кроме того, смесь пиридина и его метилпроизводных может быть получена в… Синтез пиридинового цикла. Рамзай (1877 г.) получил пиридин измененным синтезом Бертло, пропуская смесь ацетилена с…Химические свойства
ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
Химические свойства
Образование солей: · растворимых в воде хлоридов, бромидов, сульфатов, нитратов, фосфатов (используются как лекарственные формы…ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ДВУМЯ РАЗНЫМИ ГЕТЕРОАТОМАМИ
Тетрагидро-1,4-оксазины (морфолины). Изучены значительно лучше, чем остальные соединения оксазинового ряда, и за последние годы нашли практическое… Бензоксазины изучены примерно в такой же степени, как и моноциклические азины.…Нобелевские премии по органической химии
· Органическая химия – 28; · Физическая химия (включая кинетику химических реакций, строение вещества,… · Биологическая химия – 23;– Конец работы –
Используемые теги: программа, Блока, гетерофункциональные, углеводороды0.069
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: ПРОГРАММА БЛОКА ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов