Представители пятичленных гетероциклических соединений с одним гетероатомом - раздел Химия, ПРОГРАММА БЛОКА ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ Фуран Представляет Собой Пятичленный Ароматический Гетероцик...
Фуран представляет собой пятичленный ароматический гетероцикл с атомом кислорода в кольце:
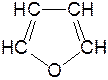
Важное место в ряду фурана занимают бензофуран и дибензофуран – соединения, в которых фурановое кольцо сконденсировано с одним или двумя бензольными кольцами:
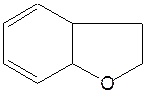
| 
|
| бензофуран
| дибензофуран
|
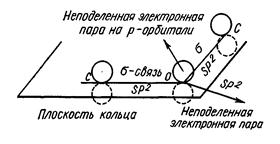
Электронная структура фурана. Фуран является ароматическим соединением с энергией делокализации, равной 92,4 кДж/моль. Ароматические свойства фурана определяются наличием кольцевого секстета π-электронов. Секстет электронов образуется за счет 4 π-электронов двух двойных углерод-углеродных связей и неподеленной пары электронов, поставляемой атомом кислорода. Другая неподеленная пара электронов кислорода остается свободной и в определенных условиях может участвовать в образовании оксониевых соединений. Состояние электронов в атоме кислорода при вхождении его в фурановый цикл соответствует состоянию sp2-гибридизации. Две тригональные гибридные орбитали образуют две δ-связи с соседними атомами углерода. На третьей тригональной орбитали располагается первая неподеленная пара электронов. Все три тригональные орбитали согласно представлениям о sр2-гибридизации лежат в одной плоскости, совпадающей с плоскостью фуранового цикла. Вторая неподеленная пара электронов кислорода находится на чистой р-орбитали, перпендикулярной к плоскости фуранового кольца. Эта неподеленная пара электронов и участвует в сопряжении с π-электронами двойных связей фурана, образуя ароматический секстет электронов. Таким образом, атом кислорода предоставляет для образования фуранового кольца два электрона и одну атомную орбиталь:
Физические свойства.Фуран представляет собой дважды ненасыщенное гетероциклическое соединение, содержащее 4 атома углерода и 1 атом кислорода, значение которых все более возрастает. Это соединение упоминалось ранее под названием фурфуран, но впоследствии за ним твердо укоренилось наименование фуран.
Таблица 6 – Основные физические характеристики
| Свойства С4Н4О
| Показатели
|
| агрегатное состояние
| жидкость
|
| молярная масса
| 68,03
|
| температура кипения
| 31-32оС (760٠мм.рт.ст)
|
| растворимость в воде
| нерастворим
|
| растворимость в спирте и эфире
| легко растворим
|
| запах
| хлороформа
|
| цвет
| бесцветный
|
Основные методы получения фурана.В настоящее время известно большое число методов получения фурана и его производных.
1.Замыкание в цикл диенольной формы 1,4-дикарбонильных соединений с выделением молекулы воды:
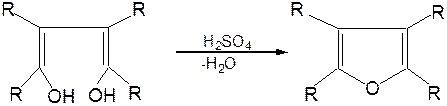
Значение этого метода ограничивается доступностью исходных дикарбонильных соединений.
2. Получение фурана из углеводов. Промышленным сырьем для получения фурана и его производных являются природные углеводы – пентозы, которые могут быть выделены при переработке растительного сырья в различных сельскохозяйственных и текстильных производствах.
Первым продуктом фуранового ряда, получаемым из пентоз, является фурфурол – простейший фурановый альдегид. Фурфурол с хорошим выходом получается при действии разбавленной минеральной кислоты (H2SО4 или Н3РО4) на пентозы: при действии разбавленной минеральной кислоты (H2SО4 или Н3РО4) на пентозы:
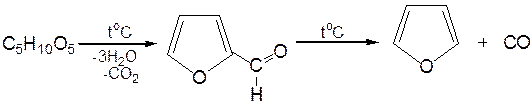
Следующая стадия заключается в декарбонилировании фурфурола. Эта реакция протекает также с хорошим выходом в условиях гетерогенного катализа при температуре 440–460 °С. В качестве катализаторов обычно используются хромит цинка и железа, окись марганца, окись кальция:
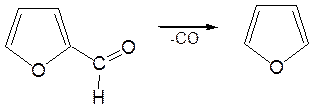
3. Сухая перегонка пирослизевой кислоты. При сухой перегонке слизевой кислоты (2,3,4,5-тетрагидроксигександиовой) образуется пирослизевая кислота, при декарбоксилировании которой (при нагревании в запаянной трубке) получается фуран:
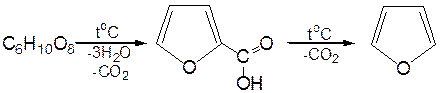
Химические свойства фурана.Наиболее характерными реакциями фурана являются реакции электрофильного замещения. Для фурана характерны реакции галогенирования, сульфирования, нитрования, ацилирования и т.д. Во всех этих реакциях фуран ведёт себя активнее бензола, аналогично ароматическим аминам и фенолам. Электрофильное замещение происходит в положения 2, 5 (a-положения), т. е. по месту наибольшей электронной плотности.
1. Реакция галогенирования. Взаимодействие фурана с галогенами при низкой температуре происходит через промежуточную стадию присоединения молекулы галогена в положения 2, 5 фуранового кольца. Образующиеся продукты присоединения отщепляют галогеноводород и дают a-галогенфураны. При повышенных температурах для галогенирования используют комплексы галогенов с пиридином или диоксаном.
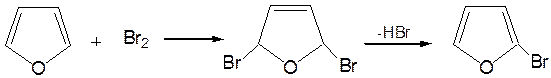
2. Реакция нитрования. Для нитрования используют «мягкий» нитрующий агент – ацетилнитрит (смесь уксусного ангидрида с азотной кислотой) в пиридине, при этом образуются a-нитропроизводные:
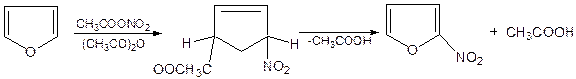
3.Реакция ацилирования. Реакцию ацилирования по Фриделю-Крафтсу проводят используя более «мягкие» катализаторы (SnCl2, SnCl4, ZnCl2, BF3) и с помощью ангидридов кислот:
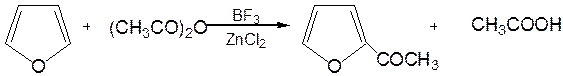
4. Реакция сульфирования.В качестве «мягкого» сульфирующего агента в ряду фурана применяется пиридинсульфотриоксид. Методика применения этого реагента была тщательно разработана А.П. Терентьевым с сотрудниками. При наличии в фурановом кольце электроноакцепторного заместителя можно осуществить сульфирование, применяя непосредственно концентрированную серную кислоту. Фуран-2-карбоновая кислота сульфируется таким образом до фуран-2-карбоновой-5-сульфокислоты с хорошим выходом.
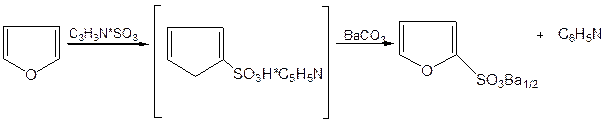
4. Реакция гидрирования.Гидрирование фурана приводит к насыщенным гетероциклическим системам, лишенным ароматических свойств. Фуран гидрируется над никелевым или платиновым катализатором до тетрагидрофурана (ТГФ):
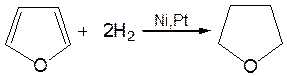
5. Реакция окисления. Фурановое кольцо чувствительно к действию окислителей. Уже на воздухефурансамоокисляется, одновременно полимеризуясь. В условиях каталитического окисления он с хорошим выходом превращается в малеиновый ангидрид:
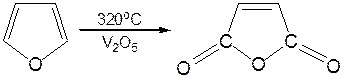
Все темы данного раздела:
ПРОГРАММА БЛОКА ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ.
Углеводы. Моносахариды.Определение, общая формула. Классификация. Номенклатура, изомерия. Структурные и проекционные формулы, антиподы, диастереомеры. D- и L-ряды. Фо
УГЛЕВОДЫ
Углеводы являются важным классом природных органических соединений. Значение углеводов определяется той доминирующей ролью, которая отводится им в живых организмах, и сложностью выполняемых ими фун
МОНОУГЛЕВОДЫ
Классификация. Моносахариды (монозы) классифицируют по количеству атомов углерода и по характеру карбонильной группы.
По количеству атомов углерода:
Химическое строение моносахаридов
Карбонильные формы моносахаридов.Для выяснения строения и стереохимии моносахаридов химикам потребовалось более ста лет. В результате многолетних исследований было установлено,
Способы получения моносахаридов
1. Гидролиз ди- и полисахаридов, который происходит под действием кислот или ферментов, водные растворы щелочей не способствуют гидролизу:
Реакции карбонильных форм моносахаридов
1.1 Окисление. Реакции окисления используют в структурных исследованиях и биохимических анализах для обнаружения моносахаридов. Монозы легко окисляются, причем в зависимости от
Реакции с участием всех гидроксильных групп
2.2.1 Алкилирование. При действии на моносахариды более сильных алкилирующих агентов, например алкилгалогенидов, наряду с гликозидным гидроксилом в реакцию вступают все спиртов
ОЛИГОСАХАРИДЫ
Олигосахариды – сахароподобные сложные углеводы, характеризую-щиеся сравнительно невысокой (несколько сотен) молекулярной массой, хорошей растворимостью в воде, легкой кристаллизацией и, как правил
ДИСАХАРИДЫ
Строение дисахаридов.В зависимости от моносахаридных компонентов олигосахариды (подобно полисахаридам) делятся на:
· гомоолигосахариды, построенные из молекул одного монос
Получение дисахаридов
Практически дисахариды извлекают из природных источников в виде гликозидов. Некоторые из них могут быть получены путем неполного гидролиза полисахаридов. Природные источники являются в настоящее вр
Номенклатура олигосахаридов
Большинство встречающих в природе олигосахаридов имеют тривиальные, общеупотребимые названия (целлобиоза, лактоза, мальтоза, трегалоза, стахиоза, сахароза, рафиноза и целлотриоза), которые им были
Свойства дисахаридов
Дисахариды представляют собой твердые вещества или некристаллизующиеся сиропы, которые растворимы в воде. Как аморфные, так и кристаллические дисахариды плавятся в некотором интервале температур и,
Отдельные представители дисахаридов
Мальтоза, солодовый сахар.Дисахарид получается из крахмала при действии солода, содержащего фермент b-амилазу. Солод (от лат. maltum) – это проросшие, а затем высушенные
Отдельные представители трисахаридов
Принципы построения трисахаридов такие же, как и дисахаридов, т. е. трисахариды могут быть как восстанавливающие, так и невосстанавливающие. Многие из трисахаридов содержатся в растениях. Из трисах
Природные гликозиды
Гликозиды – это простые или сложные эфиры моносахаридов и олигосахаридов, образованные с участием полуацетального гидроксила. Гликозиды чрезвычайно распространены в животном и особенно в растительн
Строение высших полиоз
Несахароподобные полиозы – высокомолекулярные соединения, содержащие сотни и тысячи остатков моносахаридов. Остатки моноз связаны между собой кислородными мостиками, образованными за счет полуацета
ГОМОПОЛИСАХАРИДЫ
Крахмал представляет собой не однородное вещество, а смесь полисахаридов, отличающихся не только степенью полимеризации, но и строением. Изучение химических превращений крахмала бы
ГЕТЕРОПОЛИСАХАРИДЫ
Пектиновые вещества – широко распространенные в природе соединения. Различают растворимые пектиновые вещества и нерастворимые (протопектин). Растворимые пектиновые вещества содержа
Изомерия.
Структурная:
· скелетная;
· взаимного положения;
· метамерия.
Пространственная:
· оптическая
Все природные ам
Получение α-аминокислот
1.1 Из природных веществ. Белки при гидролизе в водных растворах в присутствии кислоты дают смесь α-аминокислот, которые можно выделить и разделить. Все они оптичес
Кислотно-основные свойства аминокислот
Аминокислоты – амфотерные вещества, которые могут существовать в виде катионов или анионов. Это свойство объясняется наличием как кислотной (–СО2Н), так и основной (–NH2
Изоэлектрическая точка аминокислот
Если раствор аминокислоты поместить в электрическое поле, то в зависимости от кислотности или основности раствора будет наблюдаться различная картина. В сильнощелочном растворе концентрация анионов
Комплексные соли с ионами меди
Аминокислоты с ионами переходных металлов (Сu, Zn, Co, Pb, Ag, Hg) образуют прочные хелатные комплексы (от греч. сhele – клешня). Малорастворимые хелаты меди (II) имеют глубокую синюю
Образование сложных эфиров (этерификация).
Карбоксильная группа аминокислоты легко этерифицируется обычными методами. Например, метиловые эфиры получают, пропуская сухой газообразный хлористый водород через раствор аминокислоты в метаноле.
Качественные реакции аминокислот
Особенностью химии аминокислот является многочисленность качественных (цветных) реакций, которые необходимы при исследовании их физико-химическими методами (хроматография, электрофорез).
Практическое применение аминокислот
Аминокислоты широко используются в современной медицине в качестве лекарственных средств. К таким аминокислотам относится глутаминовая кислота, метионин, гистидин, глицин, цистеин.
Глут
ОКСИКИСЛОТЫ
Оксикислотами называются карбоновые кислоты, в которых на ряду с карбонильной группой содержится гидроксильная группа.
Классификация оксикислот, как и других бифункциональ
Способы получения оксикарбоновых кислот.
1. Гидролиз α-галогенкарбоновых кислот
Cинтез из ненасыщенных кислот.
9. Дегидратация (образование лактона).Д
Химические свойства оксикарбоновых кислот.
Оксикислоты, благодаря наличию спиртовой группы, реагируют не только, как кислоты, но и как спирты; гидроксильная группа в этих соединениях может быть замещена галогеном или ацилирована. Некоторые
Оксикислоты
Характерным отличием β-оксикислот от -оксикислот является легкость, с кото
Реакции нуклеофильного замещения α-галогенкарбоновых кислот.
Галоген в α-галогенкарбоновых кислотах легко замещается под действием различных нуклеофильных агентов. В результате этих реакций из α-галогенокарбоновых кислот получают &
Реакции со щелочами
.
2. Взаимодействие со спиртами.
Б) Реакции гидроксильной группы
1. Реакция ацилирования.При ацилировании гидроксикарбоновых кислот галогенангидридами получаются сложные эфиры. Для ацилирования можно использовать и ангидриды кислот:
ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
Гетероциклическими соединениями называют соединения, содержащие циклы, в которых имеется один или несколько гетероатомов – N, О, S или другие атомы, способные образовывать не м
ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ
Общая характеристика пятичленных гетероциклов с одним гетероатомом.К простейшим ароматическим пятичленным гетеро-циклическим соединениям с одним гетероатомом относятся фуран, пирро
Производные фурана
Тетрагидрофуран.Тетрагидрофуран получается гидрированием фурана в присутствии никелевого катализатора.
Химические свойства
1. Реакция галогенирования. Для галогенирования тиофена можно использовать бром или хлор при низкой температуре, при этом могут образовываться как моно-, так и полигалогентиофе
Практическое применение тиофена и его производных
Циклическая система тиофена встречается в природе в некоторых продуктах растительного происхождения, но гораздо большее значение имеет это соединение в составе синтетических лекарственных препарато
Основные способы получения
1. Сухой перегонкой аммонийной соли слизевой кислоты или действием аммиака на фуран в присутствии оксида алюминия:
Химические свойства
1.Галогенирование. Осуществляется с помощью хлористого сульфурила, брома в спиртовом растворе и триодид-иона (йод в растворе иодида калия), причем в результате иодирования обра
Применение пиррола и его производных
Пиррол содержится в каменноугольной смоле. Цикл пиррола – структурный фрагмент природных пигментов (например, гема, хлорофиллов, желчи, витамина В12, некоторых антибиотиков), а та
Гемоглобин
Строение и функции гемоглобина.Гемоглобин вляется переносчиком кислорода от легких к тканям тела, представляет собою белок глобин, координационно связанный с гемом (гем – по
Химические свойства
Реакции индола и его простых производных сходны с реакциями пиррола.
1. Индол обладает слабоосновными свойствами и в то же время слабокислыми, образует металлические производные –
Триптофан.
Триптофан [2-амино-3-(3'-индолил)-пропионовая кислота] — бесцветное кристаллическое вещество, Тш = 283–285 °С, растворим в воде, плохо растворим в этаноле и не растворим в
ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
Среди гетероциклических соединений наиболее многочисленна и разнообразна группа пятичленных гетероциклов, содержащих более одного гетероатома. Большинство этих циклических систем можно формально по
Оксазол
Электронное строение.Ароматические свойства оксазола связаны с наличием циклической сопряженной π-электронной системы, построенной из двух π-электронов связ
Пиридин
Способы получения пиридина и пиридиновых оснований. В небольших количествах пиридини его метил- и этилпроизводные получают из каменноугольной смолы, которая содержит около 0,2 % см
Химические свойства
1. Восстановление водородом. При восстановлении водородом в момент выделения (действуя натрием на спиртовой раствор пиридина А.Н. Вешнеградский) или над катализатором пиридин п
ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С НЕСКОЛЬКИМИ ГЕТЕРОАТОМАМИ
Пиримидин. Является важнейшим из шестичленных гетероциклов с двумя атомами азота. Пиримидиновый цикл входит в многочисленные природные соединения: нуклеиновые кислоты, витамины, коферменты, являетс
Химические свойства
1. Основные свойства:
Образование солей:
ШЕСТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ДВУМЯ РАЗНЫМИ ГЕТЕРОАТОМАМИ
Оксазины. Оксазиновое кольцо входит в состав многих органических веществ, имеющих большое практическое значение. Среди последних – широко распространенные красители, лекарст
Нобелевские премии по органической химии
Герман Эмиль Фишер
"За эксперименты по синтезу веществ с сахаридными и пуриновыми группами".
Адольф фон Бай
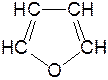
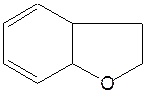


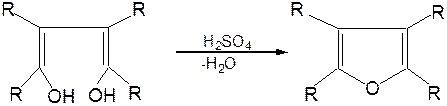
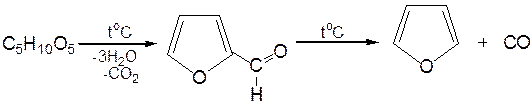
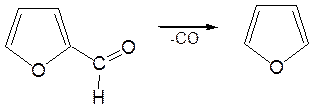
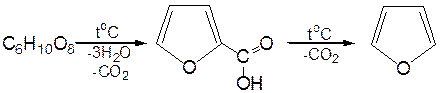
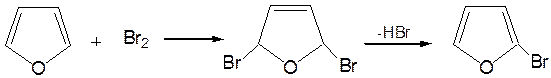
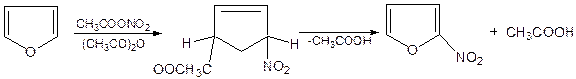
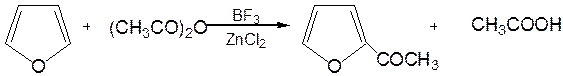
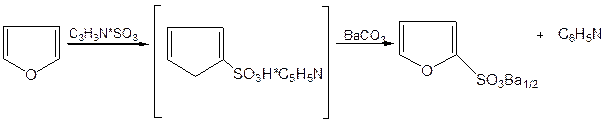
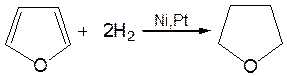
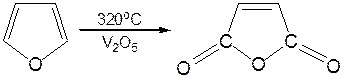







Новости и инфо для студентов