рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- Реакции карбонильных форм моносахаридов
Реферат Курсовая Конспект
Реакции карбонильных форм моносахаридов
Реакции карбонильных форм моносахаридов - раздел Химия, ПРОГРАММА БЛОКА ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ 1.1 Окисление. Реакции Окисления Используют В Структурны...
1.1 Окисление. Реакции окисления используют в структурных исследованиях и биохимических анализах для обнаружения моносахаридов. Монозы легко окисляются, причем в зависимости от условий окисления образуются различные продукты. Окисление альдоз без деструкции (разрушения) углеродного скелета проводят в нейтральной или кислой среде и получают различные кислоты.
1.1.1 При использовании мягких окислителей типа бромной воды, гипохлоритов, разбавленной азотной кислоты окисляется только альдегидная группа и образуются гликоновые (альдоновые) кислоты:
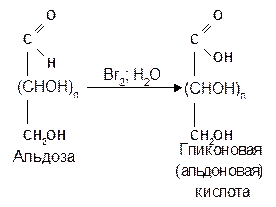
1.1.2 С помощью сильного окислителя – концентрированной азотной кислоты – концевые группы альдоз (альдегидная и первичноспиртовая) одновременно окисляются в карбоксильные группы, образуя гликаровые кислоты (называемые также сахарными):
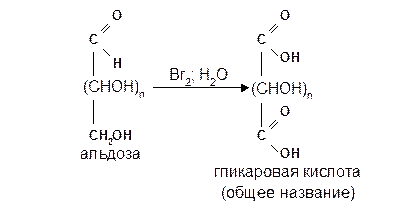
Получающаяся из D-галактозы галактаровая (слизевая) кислота трудно растворима в воде, что используется для обнаружения галактозы методом окисления ее азотной кислотой.
1.1.3 Избирательное окисление первичной спиртовой группы, если предварительно защитить склонную к окислению альдегидную группу (например, превращением альдозы в гликозид), то становится возможным избирательное окисление первичной спиртовой группы и образуются гликуроновые (уроновые) кислоты:
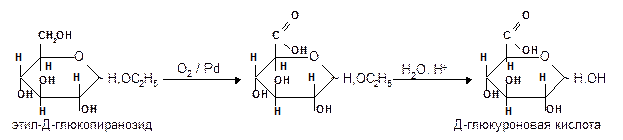
Уроновые кислоты при нагревании их солей с металлами (никель, магний) подвергаются декарбоксилированию. При этом из гексуроновых кислот образуются пентозы. В организме за счет ферментативной реакции декарбоксилирования D-глюкуроновой кислоты получается D-ксилоза:
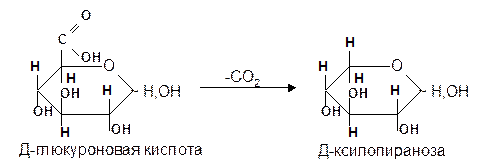
Приведенная реакция показывает генетическую связь пентоз с гексозами, являющимися продуктами фотосинтеза. Пектиновые вещества плодов и ягод представляют собой продукты поликонденсации D-галактуроновой кислоты. Уроновые кислоты выполняют в организме важную функцию – они образуют с лекарственными веществами, их метаболитами, токсичными веществами водорастворимые гликозиды и выводят их из организма.
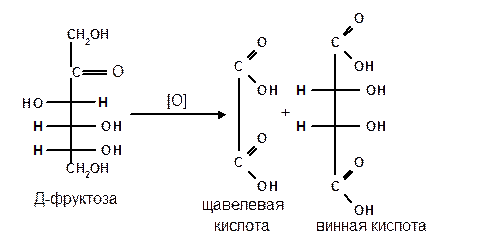
1.1.4 Окисление кетоз. Кетозы не окисляются слабыми окислителями. При действии сильных окислителей происходит расщепление молекул. Так, например, при окислении фруктозы получаются винная и щавелевая кислоты:
1.1.5 Реакция Толленса. Слабые окислители в щелочной среде (аммиачный раствор оксида серебра, соединения Сu2+) превращают монозы в сложную смесь продуктов окисления и служат для качественного и количественного определения альдоз и кетоз. Подобно обычным альдегидам, альдозы легко дают реакцию “серебряного зеркала” с аммиачным раствором оксида серебра (реактив Толленса):
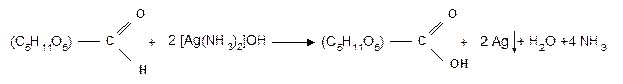
1.1.6 Окисление реактивом Фелинга. При нагревании реактива Фелинга (смесь равных обьемов водного раствора сульфата меди и щелочного раствора натрий-калиевой соли винной кислоты) в присутствии альдозы выпадает красный осадок Сu2О. Реакцию используют для количественного определения сахаров:
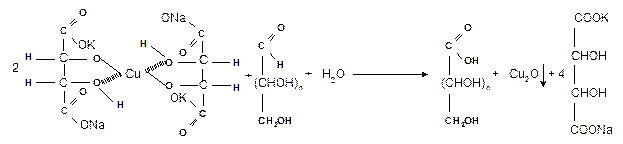
Кетозы тоже способны восстанавливать катионы металлов, так как они в щелочной среде изомеризуются в альдозы.
1.2 Восстановление. При восстановлении моноз образуются многоатомные спирты, называемые альдитами (глицитами). Эти кристаллические, легко растворимые в воде вещества обладают сладким вкусом и часто используются как заменители сахара (ксилит, сорбит):
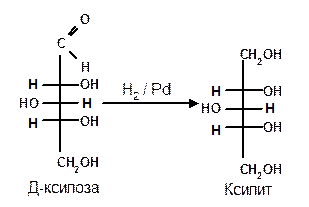
Восстановление моносахаридов проводят водородом в присутствии металлических катализаторов (Pd, Ni). Шестиатомные спирты – глюцит (сорбит), дульцит и маннит – получаются при восстановлении соответственно глюкозы, галактозы и маннозы. Восстановление глюкозы в сорбит является одной из стадий промышленного синтеза аскорбиновой кислоты. При восстановлении альдоз получается лишь один полиол, кетоз – смесь двух полиолов. Например, при восстановлении D-фруктозы борогидридом натрия NaBН4 образуются D-глюцит (сорбит) и D-маннит:

| D-фруктоза | D-глюцит | D-маннит |
1.3 Присоединение синильной кислоты. Монозы присоединяют синильную кислоту, образуя нитрилы высших глюконовых кислот (Килиани, 1887):
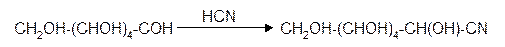
Этим методом можно удлинять углеродную цепь и переходить от низших моносахаридов к высшим (см. способы получения моноз).
1.4 Действие гидроксиламина. Реакция с гидроксиламином используется для установления строения сахаров и для перехода от высших моносахаридов к низшим:
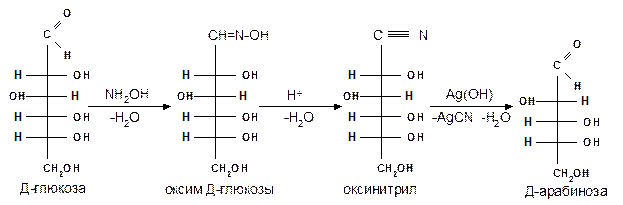
1.5 Действие фенилгидразина. Одной из наиболее важных реакций, которая позволяет выделять в чистом виде отдельные монозы, а также устанавливать тождество моноз различного происхождения, является взаимодействие моноз с фенилгидразином. Сначала фенилгидразин действует на монозы так же, как на простейшие альдегиды и кетоны, т. е. с выделением воды и образованием фенилгидразона:
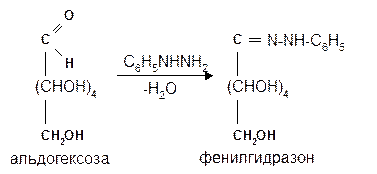
Затем при нагревании полученного гидразона с фенилгидразином соседняя с карбонильной группой первичная или вторичная спиртовая группа окисляется в карбонильную, причем фенилгидразин восстанав-ливается до анилина и аммиака. Вновь образовавшаяся карбонильная группа (для кетоз – альдегидная, а для альдоз – кетонная) вступает в реакцию с третьей молекулой фенилгидразина и получается озазон монозы:
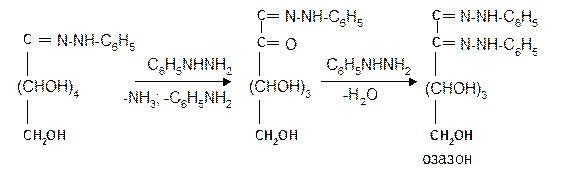
Из альдоз и кетоз могут получиться озазоны одинакового строения. Поскольку реакция образования озазона затрагивает только углероды С1 и С2 моносахаридов, то, следовательно, эпимерные альдозы и изомерные им кетозы дают один и тот же озазон. Озазоны представляют собой кристаллические вещества, трудно растворимые в воде, благодаря чему их легко выделить в кристаллическом виде из водных растворов моноз:
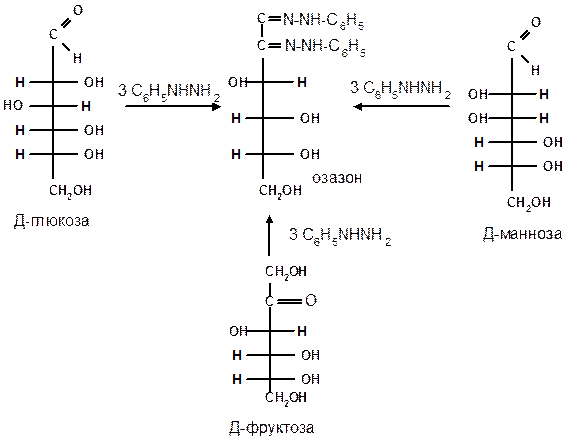
Озазоны при действии кислот гидролизуются в озоны:
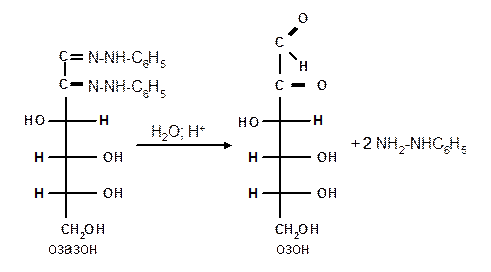
При восстановлении озонов амальгамой натрия в слабокислой среде происходит избирательное восстановление альдегидной группы до первичной спиртовой группы. Этим методом можно осуществлять переход от альдоз к кетозам через озазоны и озоны:
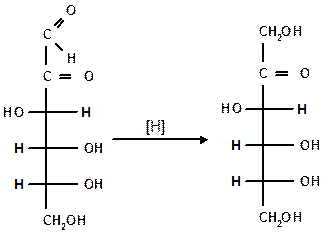
| озон | кетогексоза |
1.6 Действие щелочей. В разбавленных растворах щелочей при комнатной температуре происходит изомеризация моносахаридов, т. е. получение из одного моносахарида равновесной смеси моноз, отличающихся конфигурацией первого и второго атомов углерода. Процесс изомеризации проходит через стадию образования промежуточного продукта – ендиола, который для глюкозы, маннозы и фруктозы является общим:
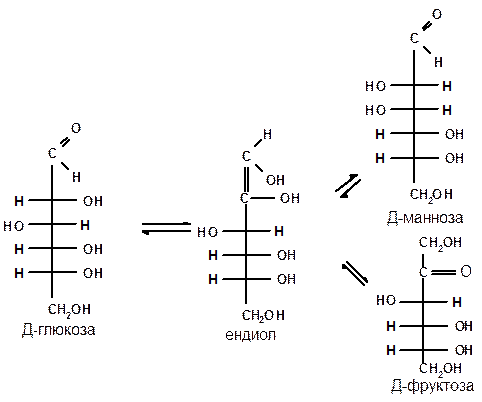
Происходящие при этих превращениях изменения конфигурации у второго углеродного атома альдоз носит название эпимеризации, а альдозы, отличающиеся лишь конфигурацией второго углеродного атома, называются эпимерами.
Способностью альдоз и кетоз к взаимному переходу друг в друга в слабощелочной среде обьясняются некоторые необычные свойства фруктозы, в частности – способность к положительным реакциям с реактивом Толленса и фелинговой жидкостью.
Превращение 6-фосфата-D-глюкопиранозы в 6-фосфат-D-фруктозы протекает в организме под действием фермента фосфоглюкоизомеразы и является одной из стадий катаболизма глюкозы.
2. Реакции с участием гидроксильных групп. Гидроксильные группы имеются в открытых и циклических формах моноз, но содержание циклических форм значительно выше, поэтому реакции идут в циклических ( полуацетальных ) формах:
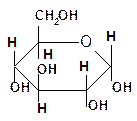
Гидроксилы отличаются по реакционной способности: при С1 –гликозидный (наиболее реакционноспособный); при С6 – первичный; при С2-С4 – вторичные.
2.1 Реакции с участием гликозидного гидроксила. При взаимодействии моносахаридов с гидроксилсодержащими соединениями (спиртами, фенолами и др.) в условиях кислотного катализа образуются производные только по гликозидной ОН-группе – циклические ацетали, называемые гликозидами. Cпиртовые гидроксилы моноз в этих условиях не реагируют.
В зависимости от размера оксидного цикла гликозиды делятся на пиранозиды и фуранозиды. Ацетали глюкозы называют глюкозидами, рибозы – рибозидами, фруктозы – фруктозидами и т.п. (окончание «оза» монозы заменяется на «озид»). Растворы гликозидов не мутаротируют.
Удобным способом получения гликозидов является пропускание газообразного хлороводорода ( катализатор ) через раствор моносахарида в спиртах, например, этаноле, метаноле и т. д. При этом соответственно получаются этил- или метилгликозиды. В названии гликозидов указываются сначала наименования введенного радикала, затем конфигурация аномерного центра и название углеводного остатка с суффиксом «озид».
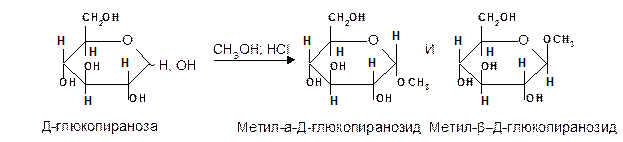
Вследствие таутомерии и обратимости реакции образования гликозида в растворе в равновесии в общем случае могут находиться таутомерные формы исходного моносахарида и соответственно 4 диастереомерных гликозида (a- и b-аномеры фуранозидов и пиранозидов).
Гликозиды легко гидрализуются разбавленными кислотами, но проявляют устойчивость к гидролизу в слабощелочной среде. Более напряженные пятичленные циклы фуранозидов расщепляются гидролитическим путем быстрее пиранозидов. Гидролиз гликозидов в кислой среде приводит к соответствующим спиртам и моносахаридам и представляет собой реакцию, обратную их образованию.
Для гидролитического расщепления гликозидов широко применяется ферментативный гидролиз, преимущество которого заключается в его специфичности. Например, фермент a-глюкозидаза из дрожжей расщепляет только a-глюкозидную связь. На этом основании ферментативный гидролиз часто применяется в целях установления конфигурации аномерного атома углерода. Гидролиз гликозидов лежит в основе гидролитического расщепления полисахаридов, осуществляемого в организме, а также используется во многих промышленных процессах.
Молекулу гликозида формально можно представить состоящей из двух частей – углеводной и агликоновой. В роли гидроксилсодержащих агликонов могут выступать и сами моносахариды. Гликозиды, образованные с ОН- содержащими агликонами, называют О-гликозидами. В свою очередь гликозиды, образованные с NH-содержащими соединениями (например, аминами), называют N-гликозидами. К ним принадлежат нуклеозиды, имеющие важное значение в химии нуклеиновых кислот.
– Конец работы –
Эта тема принадлежит разделу:
ПРОГРАММА БЛОКА ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ
ГЕТЕРОФУНКЦИОНАЛЬНЫЕ УГЛЕВОДОРОДЫ УГЛЕВОДЫ Углеводы служат основным... НЕСАХАРОПОДОБНЫЕ ПОЛИСАХАРИДЫ Строение высших... АМИНОКИСЛОТЫ...
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Реакции карбонильных форм моносахаридов
Что будем делать с полученным материалом:
Если этот материал оказался полезным ля Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов