рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Философия
- /
- ЛЕКЦИЯ № 24 Тема: Водно-солевой и минеральный обмен
Реферат Курсовая Конспект
ЛЕКЦИЯ № 24 Тема: Водно-солевой и минеральный обмен
ЛЕКЦИЯ № 24 Тема: Водно-солевой и минеральный обмен - раздел Философия, Лекция № 24 ...
ЛЕКЦИЯ № 24
Тема: Водно-солевой и минеральный обмен
Водно-солевой обмен – обмен воды и основных электролитов организма (Na+, K+, Ca2+, Mg2+, Cl-, HCO3-, H3PO4).
Электролиты – вещества, диссоциирующие в растворе на анионы и катионы. Их измеряют в моль/л.
Неэлектролиты – вещества, недиссоциирующие в растворе (глюкоза, креатинин, мочевина). Их измеряют в г/л.
Минеральный обмен – обмен любых минеральных компонентов, в том числе и тех, которые не влияют на основные параметры жидкой среды в организме.
Вода – основной компонент всех жидкостей организма.
Биологическая роль воды
1. Вода является универсальным растворителем для большинства органических (кроме липидов) и неорганических соединений.
2. Вода и растворенные в ней вещества создают внутреннюю среду организма.
3. Вода обеспечивает транспорт веществ и тепловой энергии по организму.
4. Значительная часть химических реакций организма протекает в водной фазе.
5. Вода участвует в реакциях гидролиза, гидратации, дегидратации.
6. Определяет пространственное строение и свойства гидрофобных и гидрофильных молекул.
7. В комплексе с ГАГ вода выполняет структурную функцию.
ОБЩИЕ СВОЙСТВА ЖИДКОСТЕЙ ОРГАНИЗМА
Объем. У всех наземных животных жидкости составляет около 70% от массы тела. Распределение воды в организме зависит от возраста, пола, мышечной массы,… При полном лишении воды смерть наступает через 6-8 дней, когда количество воды в организме снижается на 12%.РЕГУЛЯЦИЯ ВОДНО-СОЛЕВОГО БАЛАНСА ОРГАНИЗМА
В организме водно-солевой баланс внутриклеточной среды поддерживается постоянством внеклеточной жидкости. В свою очередь, водно-солевой баланс внеклеточной жидкости поддерживается через плазму крови с помощью органов и регулируется гормонами.
Органы, регулирующие водно-солевой обмен
Поступление воды и солей в организм происходит через ЖКТ, этот процесс контролируется чувством жажды и солевым аппетитом. Выведение излишков воды и солей из организма осуществляют почки. Кроме того, воду из организма выводят кожа, легкие и ЖКТ.
Баланс воды в организме
Изменения в работе почек, кожи, легких и ЖКТ может привести к нарушению водно-солевого гомеостаза. Например, в жарком климате, для поддержания…Гормоны, регулирующие водно-солевой обмен
Антидиуретический гормон (АДГ), или вазопрессин — пептид с молекулярной массой около 1100 Д, содержащий 9 АК, соединённых одним дисульфидным… АДГ синтезируется в нейронах гипоталамуса, переносится в нервные окончания… Высокое осмотическое давление внеклеточной жидкости активирует осморецепторы гипоталамуса, в результате возникают…Ренин-ангиотензин-альдостероновая система
Ренин
Ренин — протеолитический фермент, продуцируемый юкстагломерулярными клетками, расположенными вдоль афферентных (приносящих) артериол почечного тельца. Секрецию ренина стимулирует падение давления в приносящих артериолах клубочка, вызванное уменьшением АД и снижением концентрации Na+. Секрецию ренина также способствует снижение импульсации от барорецепторов предсердий и артерий в результате уменьшения АД. Секрецию ренина ингибирует Ангиотензин II, высокое АД.
В крови ренин действует на ангиотензиноген.
Ангиотензиноген — α2-глобулин, из 400 АК. Образование ангиотензиногена происходит в печени и стимулируется глюкокортикоидами и эстрогенами. Ренин гидролизует пептидную связь в молекуле ангиотензиногена, отщепляя от него N-концевой декапептид - ангиотензин I, не имеющий биологической активности.
Под действием антиотензин-превращающего фермента (АПФ) (карбоксидипептидилпептидазы) эдотелиальных клеток, лёгких и плазмы крови, с С-конца ангиотензина I удаляются 2 АК и образуется ангиотензин II (октапептид).
Ангиотензин II
Ангиотензин II функционирует через инозитолтрифосфатную систему клеток клубочковой зоны коры надпочечников и ГМК. Ангиотензин II стимулирует синтез и секрецию альдостерона клетками клубочковой зоны коры надпочечников. Высокие концентрации ангиотензина II вызывают сильное сужение сосудов периферических артерий и повышают АД. Кроме этого, ангиотензин II стимулирует центр жажды в гипоталамусе и ингибирует секрецию ренина в почках.
Ангиотензин II под действием аминопептидаз гидролизуется в ангиотензин III (гептапептид, с активностью ангиотензина II, но имеющий в 4 раза более низкую концентрацию), который затем гидролизуется ангиотензиназами (протеазы) до АК.
Альдостерон
Синтез и секрецию альдостерона стимулируют ангиотензин II, низкая концентрация Na+ и высокая концентрацией К+ в плазме крови, АКТГ, простагландины.… Рецепторы альдостерона локализованы как в ядре, так и в цитозоле клетки.… В результате альдостерон стимулирует реабсорбцию Na+ в почках, что вызывает задержку NaCl в организме и повышает…Схема регуляции водно-солевого обмена
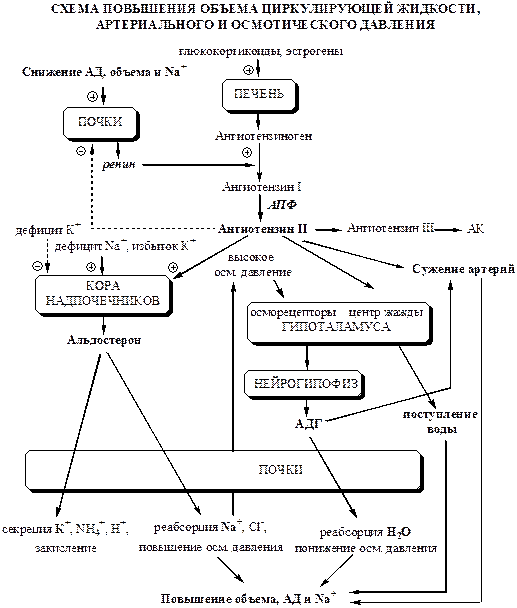
Роль системы РААС в развитии гипертонической болезни
Повышение ренина возникает, например, при атеросклерозе почечных артерий, который возникает у пожилых. Гиперсекреция альдостерона – гиперальдостеронизм, возникает в результате… Причиной первичного гиперальдостеронизма (синдром Конна) примерно у 80% больных является аденома надпочечников, в…Распределение кальция, магния и фосфатов в организме
1. Кости и зубы содержат 99% кальция. В костях 99% кальция находится в виде малорастворимого гидроксиапатита [Са10(РО4)6(ОН)2Н2О], а 1% - в виде… 2. Внеклеточная жидкость 1%. Кальций плазмы крови представлен в виде: а).… 3. Внутриклеточная жидкость содержит кальция в 10000-100000 раз меньше чем внеклеточной жидкости.Обмен кальция, магния и фосфатов в организме
С пищей в сутки должно поступать кальция - 0,7-0,8г, магния - 0,22-0,26г, фосфора – 0,7-0,8г. Кальций всасывается плохо на 30-50%, фосфор хорошо – на 90%.
Помимо ЖКТ, кальций, магний и фосфор поступают в плазму крови из костной ткани, в процессе ее резорбции. Обмен между плазмой крови и костной тканью по кальцию составляет 0,25-0,5г/сут, по фосфору – 0,15-0,3г/сут.
Выводится кальций, магний и фосфор из организма через почки с мочой, через ЖКТ с калом и через кожу с потом.
Регуляция обмена
Основными регуляторами обмена кальция, магния и фосфора являются паратгормон, кальцитриол и кальцитонин.
Паратгормон
Секрецию паратгормона стимулирует низкая концентрация Са2+, Mg2+ и высокая концентрация фосфатов, ингибирует витамин Д3. Скорость распада гормона уменьшается при низкой концентрации Са2+ и… Паратгормон действует на кости и почки. Он стимулирует секрецию остеобластами инсулиноподобного фактора роста 1 и…Гиперпаратиреоз
Гиперпаратиреоз вызывает: 1. разрушение костей, при мобилизации из них кальция и фосфатов.… 2. гиперкальциемию, при усилении реабсорбции кальция в почках. Гиперкальциемия приводить к снижению нервно-мышечной…Гипопаратиреоз
Гипопаратиреоз обусловлен недостаточностью паращитовидных желёз и сопровождается гипокальциемией. Гипокальциемия вызывает повышение нервно-мышечной проводимости, приступы тонических судорог, судороги дыхательных мышц и диафрагмы, ларингоспазм.
Кальцитриол
1. В коже под влиянием УФ-излучения из 7-дегидрохолестерола образуется… 2. В печени 25-гидроксилаза гидроксилирует холекальциферол в кальцидиол (25-гидроксихолекальциферол, 25(OH)Д3).…Кальцитонин
Кальцитонин — полипептид, состоит из 32 АК с одной дисульфидной связью, секретируется парафолликулярными К-клетками щитовидной железы или С-клетками паращитовидных желёз.
Секрецию кальцитонина стимулирует высокая концентрация Са2+ и глюкагона, подавляет низкая концентрация Са2+.
Кальцитонин:
1. подавляет остеолиз (снижая активность остеокластов) и ингибирует высвобождение Са2+ из кости;
2. в канальцах почек тормозит реабсорбцию Са2+, Mg2+ и фосфатов;
3. тормозит пищеварение в ЖКТ,
Изменения уровня кальция, магния и фосфатов при различных патологиях
1. гипофункции паращитовидных желез; 2. беременности; 3. алиментарной дистрофии;Роль микроэлементов: Mg2+, Mn2+, Co, Cu, Fe2+, Fe3+, Ni, Mo, Se, J. Значение церулоплазмина, болезнь Коновалова-Вильсона.
Марганец –кофактор аминоацил-тРНК синтетаз.
Биологическая роль Na+, Cl-, K+, HCO3- - основных электролитов, значение в регуляции КОС. Обмен и биологическая роль. Анионная разность и ее коррекция.
Тяжелые металлы (свинец, ртуть, медь, хром и др.), их токсическое действие.
Снижение содержания хлоридов в сыворотке крови: алкалоз гипохлоремический (после рвоты), ацидоз респираторный, избыточное потоотделение, нефрит с… Повышенное выделение хлоридов с мочой: гипоальдостеронизм (болезнь Аддисона),… Снижение выведения хлоридов с мочой: Потеря хлоридов при рвоте, диареи, болезнь Кушинга, терминальная фаза почечной…ЛЕКЦИЯ № 25
Тема: КОС
2 курс. Кислотно-основное состояние (КОС) - относительное постоянство реакции…Биологическое значение регуляции рН, последствия нарушений
Отклонение рН от нормы на 0,1 вызывает заметные нарушения со стороны дыхательной, сердечно-сосудистой, нервной и других систем организма. При ацидемии возникает: 1. усиление дыхания до резкой отдышки, нарушение дыхания в результате бронхоспазма;Основные принципы регуляции КОС
В основе регуляции КОС лежат 3 основных принципа:
1. постоянство рН. Механизмы регуляции КОС поддерживают постоянство рН.
2. изоосмолярность. При регуляции КОС, концентрация частиц в межклеточной и внеклеточной жидкости не изменяется.
3. электронейтральность. При регуляции КОС, количество положительных и отрицательных частиц в межклеточной и внеклеточной жидкости не изменяется.
МЕХАНИЗМЫ РЕГУЛЯЦИИ КОС
Принципиально существуют 3 основных механизма регуляции КОС:
1. Физико-химический механизм, это буферные системы крови и тканей;
2. Физиологический механизм, это органы: легкие, почки, костная ткань, печень, кожа, ЖКТ.
3. Метаболический (на клеточном уровне).
В работе этих механизмов есть принципиальные различия:
| № | Показатели | Буферные системы | Органы |
| Скорость регуляции КОС | быстро: секунды | медленно: минуты - часы | |
| Степень регуляции КОС | частично | полностью | |
| Расходование при регуляции КОС | расходуются | не расходуются |
Физико-химические механизмы регуляции КОС
Буфер – это система, состоящая из слабой кислоты и ее соли с сильным основанием (сопряженная кислотно-основная пара).
Принцип работы буферной системы состоит в том, что она связывает Н+ при их избытке и выделяет Н+ при их недостатке: Н+ + А- ↔ АН. Таким образом, буферная система стремиться противостоять любым изменениям рН, при этом один из компонентов буферной системы расходуется и требует восстановления.
Буферные системы характеризуются соотношением компонентов кислотно-основной пары, емкостью, чувствительностью, локализацией и величиной рН, которую они поддерживают.
Существует множество буферов как внутри, так и вне клеток организма. К основным буферным системам организма относят бикарбонатный, фосфатный белковый и его разновидность гемоглобиновый буфер. Около 60% кислых эквивалентов связывают внутриклеточные буферные системы и около 40% -внеклеточные.
Бикарбонатный (гидрокарбонатный) буфер
Состоит из Н2СО3 и NaНСО3 в соотношении 1/20, локализуется в основном в межклеточной жидкости. В сыворотке крови при рСО2 = 40 мм.рт.ст., концентрации Na+ 150 ммоль/л он поддерживает рН=7,4. Работа бикарбонатного буфера обеспечивается ферментом карбоангидразой и белком полосы 3 эритроцитов и почек.
Бикарбонатный буфер является одним из самых важных буферов организма, что связано с его особенностями:
1. Несмотря на низкую емкость – 10%, бикарбонатный буфер очень чувствителен, он связывает до 40% всех «лишних» Н+;
2. Бикарбонатный буфер интегрирует работу основных буферных систем и физиологических механизмов регуляции КОС.
В связи с этим, бикарбонатный буфер является индикатором КОС, определение его компонентов – основа для диагностики нарушения КОС.
Фосфатный буфер
Состоит из кислого NaН2РО4 и основного Na2НРО4 фосфатов, локализуется в основном в клеточной жидкости (фосфатов в клетке 14%, в межклеточной жидкости 1%). Соотношение кислого и основного фосфатов в плазме крови составляет ¼, в моче - 25/1.
Фосфатный буфер обеспечивает регуляцию КОС внутри клетки, регенерацию бикарбонатного буфера в межклеточной жидкости и выведение Н+ с мочой.
Белковый буфер
Наличие у белков амино и карбоксильных групп придает им амфотерные свойства – они проявляют свойства кислот и оснований, образуя буферную систему.
Белковый буфер состоит из протеин-Н и протеин-Na, локализуется он преимущественно в клетках. Наиболее важный белковый буфер крови – гемоглобиновый.
Гемоглобиновый буфер
Гемоглобиновый буфер находиться в эритроцитах и имеет ряд особенностей:
1. у него самая высокая емкость (до 75%);
2. его работа напрямую связана с газообменом;
3. он состоит не из одной, а из 2 пар: HHb↔H+ + Hb- и HHbО2↔H+ + HbО2-;
HbО2 является относительно сильной кислотой, он даже сильнее угольной кислоты. Кислотность HbО2 по сравнению с Hb в 70 раз выше, поэтому, оксигемоглобин присутствует в основном в виде калийной соли (КHbО2), а дезоксигемоглобин в виде недиссоциированной кислоты (HHb).
Работа гемоглобинового и бикарбонатного буфера
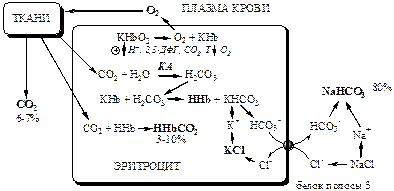
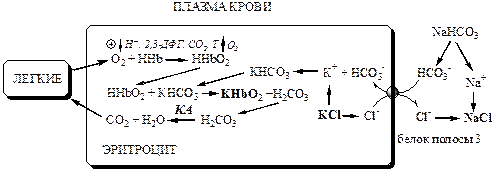
Физиологические механизмы регуляции КОС
1. выведением из организма кислот и оснований; 2. превращением кислот и оснований в нейтральные вещества. Образующиеся в организме кислоты и основания могут быть летучими и нелетучими. Летучая Н2СО3, образуется из СО2,…Роль легких в регуляции КОС
Регуляция газообмена в легких и соответственно выделение Н2СО3 из организма осуществляется через поток импульсов от хеморецепторов и… В норме за сутки легкие выделяют 480л СО2, что эквивалентно 20 молям Н2СО3.… Легочные механизмы поддержания КОС являются высокоэффективными, они способны нивелировать нарушение КОС на 50-70%.…Роль почек в регуляции КОС
Почки регулируют КОС: 1. выведением из организма H+ в реакциях ацидогенеза, аммониогенеза и с… 2. задержкой в организме Na+. Na+,К+-АТФаза реабсорбирует Na+ из мочи, что вместе с карбоангидразой и ацидогенезом…Роль костей в регуляции КОС
1. Са3(РО4)2 + 2Н2СО3 → 3 Са2+ + 2НРО42- + 2НСО3- 2. 2НРО42- + 2НСО3- + 4НА → 2Н2РО4- (в мочу) + 2Н2О + 2СО2 + 4А- 3. А- + Са2+ → СаА (в мочу)Роль печени в регуляции КОС
Печень регулирует КОС:
1. превращением аминокислот, кетокислот и лактата в нейтральную глюкозу;
2. превращением сильного основания аммиака в слабо основную мочевину;
3. синтезируя белки крови, которые образуют белковый буфер;
4. синтезирует глутамин, который используется почками для аммониогенеза.
Печеночная недостаточность приводит к развитию метаболического ацидоза.
В тоже время печень синтезирует кетоновые тела, которые в условиях гипоксии, голодания или сахарного диабета способствуют ацидозу.
Влияние ЖКТ на КОС
ЖКТ влияет на состояние КОС, так как использует HCl и НСО3- в процессе пищеварения. Сначала в просвет желудка секретируется HCl, при этом в крови накапливаются НСО3- и развивается алкалоз. Затем НСО3- из крови с панкреатическим соком поступают в просвет кишечника и равновесие КОС в крови восстанавливается. Так как пища, которая поступает в организм, и кал, который выделяется из организма в основном нейтральны суммарный эффект на КОС оказывается нулевым.
При наличии ацидоза в просвет выделяется больше HCl, что способствует развитию язвы. Рвота способна компенсировать ацидоз, а диарея – усугубить. Длительная рвота вызывает развитие алкалоза, у детей она может иметь тяжелые последствия, вплоть до летально исхода.
Клеточный механизм регуляции КОС
Кроме рассмотренных физико-химический и физиологических механизмов регуляции КОС существует еще клеточный механизм регуляции КОС. Принцип его работы заключается в том, что избыточные количества H+ могут размещаться в клетках в обмен на К+.
ПОКАЗАТЕЛИ КОС
1. рН - (power hydrogene - сила водорода) – отрицательный десятичный логарифм (-lg) концентрации Н+. Норма в капиллярной крови 7,37 - 7,45,… 2. рСО2 – парциальное давление углекислого газа, находящегося в равновесии с… 3. рО2 – парциальное давление кислорода в цельной крови. Норма в капиллярной крови 83 - 108 мм.рт.cт., в венозной –…НАРУШЕНИЯ КОС
Коррекция КОС – приспособительная реакция со стороны органа, вызвавшего нарушение КОС. Выделяют два основных вида нарушений КОС – ацидоз и алкалоз.Ацидоз
I. Газовый (дыхательный). Характеризуется накоплением в крови СО2 (рСО2=↑, AB, SB, BB=N,↑).
1). затруднение выделения СО2, при нарушениях внешнего дыхания (гиповентиляция легких при бронхиальной астме, пневмонии, нарушениях кровообращения с застоем в малом круге, отёке лёгких, эмфиземе, ателектазе легких, угнетении дыхательного центра под влиянием ряда токсинов и препаратов типа морфина и т.п.) (рСО2=↑, рО2=↓, AB, SB, BB=N,↑).
2). высокая концентрация СО2 в окружающей среде (замкнутые помещения) (рСО2=↑, рО2, AB, SB, BB=N,↑).
3). неисправности наркозно-дыхательной аппаратуры.
При газовом ацидозе происходит накопление в крови СО2, Н2СО3 и снижение рН. Ацидоз стимулирует реабсорбцию в почках Na+ и через некоторое время в крови происходит повышение AB, SB, BB и как компенсация, развивается выделительный алкалоз.
При ацидозе в плазме крови накапливается H2PO4-, который не способен реабсорбироваться в почках. В результате он усиленно выделяется, вызывая фосфатурию.
Для компенсации ацидоза почки с мочой усиленно выделяются хлориды, что приводит к гипохроремии.
Избыток H+ поступает в клетки, взамен из клеток выходит К+ вызывая геперкалиемию.
Избыток К+ усиленно выводится с мочой, что в течение 5-6 дней приводит к гипокалиемии.
II. Негазовый. Характеризуется накоплением нелетучих кислот (рСО2=↓,N, AB, SB, BB=↓).
1). Метаболический. Развивается при нарушениях тканевого метаболизма, которые сопровождаются избыточным образованием и накоплением нелетучих кислот или потерей оснований (рСО2=↓,N, АР = ↑, AB, SB, BB=↓).
а). Кетоацидоз. При сахарном диабете, голодании, гипоксии, лихорадке и т.д.
б). Лактоацидоз. При гипоксии, нарушении функции печени, инфекциях и т.д.
в). Ацидоз. Возникает в результате накопления органических и неорганических кислот при обширных воспалительных процессах, ожогах, травмах и т.д.
При метаболическом ацидозе происходит накопление нелетучих кислот и снижение рН. Буферные системы, нейтрализуя кислоты, расходуются, в результате в крови снижается концентрация AB, SB, BBи повышается АР.
Н+ нелетучих кислот при взаимодействии с НСО3- дают Н2СО3, которая распадается на Н2О и СО2, сами же нелетучие кислоты образуют с Na+ бикарбонатов соли. Низкая рН и высокое рСО2 стимулирует дыхание, в результате рСО2 в крови нормализуется или снижается с развитием газового алкалоза.
Избыток Н+ плазме крови перемещает внутрь клетки, а взамен из клетки выходит К+, в плазме крови возникает транзиторная гиперкалиемия, а клетках - гипокалигистия. К+ интенсивно выводится с мочой. В течение 5-6 дней содержание К+ в плазме нормализуется и затем становится ниже нормы (гипокалиемия).
В почках усиливаются процессы ацидо-, аммониогенеза и восполнения дефицита бикарбоната плазмы. В обмен на НСО3- в мочу активно экскретируется Сl-, развивается гипохлоремия.
Клинические проявления метаболического ацидоза:
- расстройства микроциркуляции. Происходит уменьшение притока крови и развитие стаза под действием катехоламинов, изменяются реологические свойства крови, что способствует углублению ацидоза.
- повреждение и повышение проницаемости сосудистой стенки под влиянием гипоксии и ацидоза. При ацидозе повышается уровень кининов в плазме и внеклеточной жидкости. Кинины вызывают вазодилатацию и резко повышают проницаемость. Развивается гипотония. Описанные изменения в сосудах микроциркуляторного русла способствуют процессу тромбообразования и кровоточивости.
- при рН крови менее 7,2 возникает снижение сердечного выброса.
- дыхание Куссмауля (компенсаторная реакция направленная на выделение избытка СО2).
2. Выделительный. Развивается при нарушении процессов ацидо- и аммониогенеза в почках или при избыточной потере основных валентностей с каловыми массами.
а). Задержка кислот при почечной недостаточности (хронический диффузный гломерулонефрит, нефросклероз, диффузный нефрит, уремия). Моча нейтральная или щелочная.
б). Потеря щелочей: почечная (почечный канальцевый ацидоз, гипоксия, интоксикация сульфаниламидами), гастроэнтеральная (диарея, гиперсаливация).
3. Экзогенный.
Прием кислой пищи, лекарств (хлористого аммония; переливание больших количеств кровозамещающих растворов и жидкостей для парентерального питания, рН которых обычно <7,0) и при отравлениях (салицилаты, этанол, метанол, этиленгликоль, толуол и др.).
4. Комбинированный.
Например, кетоацидоз + лактоацидоз, метаболический + выделительный и т.д.
III. Смешанный (газовый + негазовый).
Возникает при асфиксии, сердечно-сосудистой недостаточности и т.д.
Алкалоз
1). усиленное выведение СО2, при активации внешнего дыхания (гипервентеляция легких при компенсаторной одышке, сопровождающей ряд заболеваний, в том… 2). Дефицит О2 во вдыхаемом воздухе вызывает гипервентеляцию легких и… Гипервентиляция приводит к снижению в крови рСО2 и повышению рН. Алкалоз ингибирует реабсорбцию в почках Na+,…Негазовый алкалоз
– Конец работы –
Используемые теги: Лекция, Тема, Водно-солевой, Минеральный, Обмен0.088
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: ЛЕКЦИЯ № 24 Тема: Водно-солевой и минеральный обмен
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов