рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Образование
- /
- Лекция №1 Основные классы неорганических соединений, номенклатура
Реферат Курсовая Конспект
Лекция №1 Основные классы неорганических соединений, номенклатура
Лекция №1 Основные классы неорганических соединений, номенклатура - раздел Образование, Лекция №1 Основные Классы Неорганических Соединений, Номенклатура....
Лекция №1
Основные классы неорганических соединений, номенклатура.
Основными классами неорганических соединений являются оксиды, кислоты, соли и основания.
Оксиды представляют собой соединения элементов с кислородом. Оксиды подразделяют на солеобразующие и несолеобразующие. Солеобразующие оксиды делят на основные (образуют соли с кислотами), кислотные (образуют соли с основаниями) и амфотерные (образуют соли как с кислотами, так и с основаниями). Основным оксидам отвечают основания, кислотным – кислоты, а амфотерным – гидраты, которые проявляют как кислотные, так и амфотерные свойства. Кислотные оксиды представляют собой ангидриды кислот (SO2 – серный ангидрид, N2O5 – азотный ангидрид).
Примеры: N2O, NO - несолеобразующие оксиды; SO3, SiO2 - кислотные оксиды; СаО, МgО – основные оксиды и т.д.
В настоящее время общепринятой является международная номенклатура оксидов. Согласно международной номенклатуре в названии оксида указывается валентность элемента: СuO и Cu2O – оксиды меди [II] и [III] соответственно. Существует также русская номенклатура, согласно которой окисью называется единственно возможный оксид элемента, в остальных случаях название дается в соответствии с числом атомов кислорода. Оксиды, в которых элемент проявляет низшую валентность, называются закисями.
Примеры: MgO – окись магния; NiO – одноокись никеля; Ni2O3 – полутораокись никеля; Сu2О – полуокись меди.
Пероксиды (перекиси) металлов являются солями перекиси водорода Н2О2 и лишь формально относятся к оксидам. Приставка пер в названии соединений обычно указывает на принадлежность соединения к перекисным, но существуют исключения: соли кислот НMnO4 (перманганаты) и НСlO4 (перхлораты) перекисными не являются, а приставка пер в названии этих соединений указывает на максимальную насыщенность соединений кислородом.
Гидроксиды (основания) классифицируют по их силе (сильные – все щелочи кроме NH4OH и слабые), а также по растворимости в воде (растворимые – щелочи и нерастворимые). Важнейшими щелочами являются КОН (едкое кали) и NaOH (едкий натр).
В состав кислот входит водород, способный замещаться металлом, а также кислотный остаток. Коэффициент х, отвечающий количеству атомов водорода, а, следовательно, равный валентности кислотного остатка, называют основностью кислоты. Кислоты классифицируют по их силе (H2SO4, HNO3 – сильные кислоты; HCN – слабая кислота), на кислородсодержащие (H2SO4, HNO3) и бескислородные (HCN, HI); а также по основности (х) -
HCN – одноосновная кислота, H2SO3 – двухосновная кислота, H3РO4 – трехосновная кислота. Важнейшим свойством кислот является их способность образовывать соли с основаниями. Названия кислот образуют от того элемента, которым образована кислота, при этом названия бескислородных кислот оканчивается словом водород (HCN –циановодород или синильная кислота). Названия кислородсодержащих кислот образуют от того элемента, которым образована кислота, с добавлением слова кислота (H3AsO4 – мышьяковая кислота, H2CrO4 – хромовая кислота). В случаях, когда один элемент образует несколько кислот различие между кислотами проявляют в окончаниях названий (на ная или овая оканчиваются названия тех кислот, в которых элемент проявляет наивысшую валентность; на истая или овистая оканчиваются названия тех кислот, в которых элемент проявляет валентность ниже максимальной).
Примеры:HNO3 – азотная кислота, а HNO2 - азотистая кислота; H3AsO4 – мышьяковая кислота, а H3AsO3 – мышьяковистая кислота.
Одному и тому же оксиду могут соответствовать несколько кислот, при этом наиболее богатая водой форма имеет в названии приставку орто, а наименее богатая – мета (ортофосфорная кислота H3РO4 – на одну молекулу ангидрида Р2О5 приходится три молекулы воды; метафосфорная кислота HРO3 – на одну молекулу ангидрида Р2О5 приходится одна молекула воды). Следует также учитывать и то, что ряд кислот имеют исторически сложившиеся названия.
Соли являются продуктом замещения водорода в кислоте на металл или гидроксогрупп в основании на кислотный остаток. Нормальные (средние) соли получаются при полном замещении; кислые – при неполном замещении водорода кислоты на металл; основные – при неполном замещении гидроксогрупп основания на кислотный остаток. Кислая соль может быть образована только кислотой, основность которой 2 и более, а основная – металлом, заряд которого 2 и более.
Примеры:NaHS, KHCO3 – кислые соли (гидросульфид натрия и гидрокарбонат натрия); MgOHCl, CaOHCl – основные соли (хлориды гидроксо магния и кальция); NaCl, CuS – нормальные соли (хлорид натрия и сульфид меди).
| Название кислоты | Формула | Пример соли | Название соли |
| Серная | H2SO4 | K2SO4 | сульфат К |
| сернистая | H2SO3 | Na2SO3 | сульфит Na |
| соляная | HCl | Ca(Cl)2 | хлорид Са |
| иодоводородная | HI | KI | иодид К |
| сероводородная | H2S | Na2S | cульфид Na |
| азотная | HNO3 | KNO3 | нитрат К |
| азотистая | HNO2 | NaNO2 | нитрит Na |
| ортофосфорная | H3РO4 | K3РO4 | ортофосфат К |
| хлорная | НСlO4 | NaСlO4 | перхлорат Na |
| хлорноватая | НClO3 | NaСlO3 | хлорат Na |
| хлористая | НClO2 | NaСlO2 | хлорит Na |
| хлорноватистая | НСlO | NaСlO | гипохлорит Na |
| кремниевая | H2SiO3 | CaSiO3 | силикат Сa |
Продолжение табл.
| Название кислоты | Формула | Пример соли | Название соли |
| алюминиевая | H3AlO3 | K3AlO3 | алюминат К |
| ортоборная | H3BO3 | K3BO3 | ортоборат К |
| мышьяковая | H3AsO4 | K3AsO4 | арсенат К |
| мышьяковистая | H3AsO3 | K3AsO3 | арсенит К |
| двуфосфорная | H4P2O7 | K4P2O7 | дифосфат К |
| угольная | H2CO3 | K2CO3 | карбонат К |
| фосфористая | H3PO3 | K3PO3 | фосфит К |
| фтороводород | HF | KF | фторид К |
| хромовая | Н2СrO4 | K2СrO4 | хромат К |
| синильная | НCN | KCN | цианид К |
Лекция№ 2
Основные законы общей химии. Стехиометрия.
Химический эквивалент.
2. Закон кратных отношений. Установлен Дальтоном в 1803г. В случае, когда два элемента образуют между собой несколько химических соединений, тогда… Законы постоянства состава и кратных отношений не носят всеобщего характера, в… 3. Закон объёмных отношений. Этот закон в качестве обобщения вывел французский ученый Гей-Люссак (второе название…Газовые законы. Основные газовые процессы. Газовые законы
Для описания состояния идеального газа пользуются уравнением Менделеева-Клапейрона: РV=, где: P – давление газа, Па; V – объём газа, м3; T – температура газа, К;… Уравнением, объединяющим газовые законы Бойля-Мариотта и Гей-Люссака, является:Основные газовые процессы
1. Изохорный процесс. Объём системы остаётся постоянным (dV=0). Поэтому элементарная работа расширения системы dАр=PdV=0, а вся теплота, сообщенная… 2. Изобарный процесс. Давление Р=соnst. Таким образом dQp=d(U+PV), а работа… Ар=Р(V2-V1).Лекция №3
Строение атома.
Введение
Большую роль в установлении сложной природы атома и расшифровке его структуры сыграло открытие и изучение радиоактивности (явление испускания некоторыми элементами излучения, способного проникать через вещества, ионизировать воздух, вызывать засвечивание фотографических пластинок). Впервые в 1896г. радиоактивность обнаружена А. Беккерелем у соединений урана. Мария и Пьер Склодовские-Кюри обнаружили радиоактивность и у соединений тория, а в 1898 г. они открыли в составе урановых руд присутствие двух новых радиоактивных элементов – полония и радия. Опыты супругов Кюри показали, что атомы радия в процессе радиоактивного излучения распадаются, превращаясь в атомы других элементов, в частности, в атомы гелия. Впоследствии было установлено, что другим продуктом распада радия является инертный газ радон.
В 1903 г. Дж. Томсон предложил модель строения атома, согласно которой атом состоит из положительного ядра и электронов. Развивая эти представления, Э. Резерфорд в 1911г. предложил ядерную модель строения атома. Существенным шагом в развитии представлений о строении атома стала предложенная в 1913г. Н. Бором теория, объединившая, по сути, ядерную модель атома с квантовой теорией света. Основные положения своей теории Бор сформулировал в виде следующих постулатов: 1) электрон может вращаться вокруг ядра только по некоторым определенным круговым орбитам (стационарным орбитам); 2) Двигаясь по стационарной орбите, электрон не излучает электромагнитной энергии; 3) Излучение происходит при скачкообразном переходе электрона с одной стационарной орбиты на другую.
В 1900г. М. Планк предположил, что лучистая энергия испускается и поглощается телами не непрерывно, а дискретно. При этом, он определил энергию каждой такой порции как Е=h*n (уравнение Планка), где n – частота излучения; h=6,626*10-34 Дж*с – постоянная Планка. Т.о. согласно определению Планка квант – это минимальная порция электромагнитного излучения с определенной частотой. В 1905г. А. Эйнштейн при изучении явления фотоэлектрического эффекта пришел к выводу, что электромагнитная энергия существует только в форме квантов, а излучение представляет собой поток неделимых материальных «частиц» - фотонов, энергия которых определяется уравнением Планка. Фотон не является ни частицей, ни волной – ему свойственна корпускулярно-волновая двойственность.
Атом и его строение
Согласно современным представлениям, электрон обладает одновременно свойствами волны и частицы, поэтому для описания его поведения нельзя… Состояние электрона в атоме характеризуется волновой функцией, являющейся… Каждой АО соответствует область пространства определённого размера, формы и ориентации, равноценная понятию…Лекция №4
Химическая связь. Основные типы химической связи.
Методы ВС и МО.
Химическая связь – это вид межатомных взаимодействий в молекулах, ионах, кристаллах, характеризуемый определенной энергией. При всем многообразии… Механизм образования химической связи может быть смоделирован различными… Метод валентных связей рассматривает химическую связь как результат притяжения ядер двух атомов к одной или нескольким…Лекция №5
Периодический закон и периодическая система элементов
Д.И. Менделеева.
Периодичность в изменении свойств химических элементов, расположенных в порядке возрастания заряда ядра их атомов, является результатом… Химический элемент – это вид атомов, характеризующихся определённым зарядом… Химические соединения состоят из атомов или ионов, находящихся в связанном состоянии, и характеризуются определённым…Лекция №6.
Основы термодинамики. I,II и III начало термодинамики. Основы термодинамических расчетов
I закон термодинамики
Q=DU+W dQ=dU+dW Теплота, полученная системой (dQ; Q), расходуется на работу (dW; W), совершаемую системой и увеличение ее внутренней…Q=ådQ=ònC(T)dT
с(T)=a+bT+cT2+ c/T-2 Где: а, в, с, с/ - коэффициенты, зависящие от природы и агрегатного состояния… В случае приближенных расчетов обычно достаточно использование выражения:Закон Гесса. Тепловые эффекты химических реакций
Для расчета тепловых эффектов различных процессов, (в том числе и состоящих из нескольких этапов) в термодинамике применяют закона Гесса (установлен… DrH0298=ånкон(DfH0298)кон-ånнач(DfH0298 )нач Для различных веществ при нормальных условиях (Р0=101,3 кПа; Т0=298К) энтальпии образования обозначаются как DfН0298,…Закон Кирхгофа. Зависимость теплового эффекта химической реакции от температуры
dQp/dT=d(DrH)/dT=å(nCp)кон-å(nCp)исх=DrCp Закон Кирхгофа справедлив для любых процессов при условии, что W/=0, т.е.…II закон термодинамики. Теорема Карно-Клаузиуса
Коэффициент полезного действия (кпд) тепловой машины, работающей по квазистатическому циклу Карно, не зависит от природы рабочего тела, а… , где: Q1 – теплота, сообщенная рабочему телу при температуре Т1 от источника… Основной формулировкой второго закона является формулировка Больцмана: «Все процессы в природе переводят систему из…III закон термодинамики. Теорема Нернста. Постулат Планка
при Т®0 S=0 и dS=0. Важнейшим следствием этой гипотезы является то, что энтропия правильно сформированного (бездефектного) идеального кристалла при… На основе этого закона разработаны современные методы вычислений изменения…Определение термодинамической вероятности осуществления процесса
-D(TS), DHх.р.=ånкон(DfH0298)кон-ånнач(DfH0298 )нач; DSх.р=å(nS0298)кон-å(nS0298)нач. Если значение DG>0, то процесс термодинамически мало вероятен, причем, чем… Если значение DG=0, то система находится в равновесии.Энергия Гельмгольца
Величина F=U-TS является функцией состояния системы и носит название изохорно-изотермического потенциала или энергии Гельмгольца (размерность энергии (Дж)). При Т,Р=const энергия Гельмгольца может служить признаком наличия равновесия или самопроизвольности процессов. При равновесии она постоянна и минимальна по величине. Самопроизвольно могут протекать только процессы, которые приводят к ее убыли.
Расчет энергетических величин и выражения первого закона термодинамики для предельных процессов идеального газа
Лекция №7
Химическая кинетика и химическое равновесие.
Химическая кинетика – это раздел химии, изучающий скорости химических реакций. Химические реакции могут протекать с различными скоростями (от малых… Скорость гомогенной реакции – это количество вещества, вступающего в реакцию… vгомог=; vгетерог=. Т.е. скорость гомогенной реакции можно определить как изменение концентрации какого-либо из…Химическое равновесие. Принцип Ле Шателье
Влияние концентрации. Если увеличить концентрацию исходных веществ, то система будет стремиться быстрее их израсходовать, то есть сместится в… Влияние давления. Изменение давления наиболее существенно в случае реакций,… При увеличении общего давления равновесие смещается таким образом, что общее давление снижается, то есть, смещается в…Лекция №8
Теория электролитической диссоциации. Электролиты.
Предположение Сванте Аррениуса о том, что причиной крайне высокого осмотического давления растворов электролитов является диссоциация этих… Однако теория Аррениуса не учитывала всей сложности явлений в растворах. Ей… Пусть концентрация электролита, распадающегося на 2 иона, равна С, а степень его диссоциации в данном растворе…Лекция №9
Водородный показатель кислотности и щелочности водных растворов. Ионное произведение воды. Растворимость.
рН=-lg[H+], где [H+]=[моль/л]. Таким образом, по характеру среду растворы можно подразделить на кислые… Характер среды (раствора) Величина рН Концентрация [Н+], моль/л кислая …Таблица 2. Важнейшие индикаторы
| Название индикатора | Цвет индикатора в различных средах | ||
| в кислой | в нейтральной | в щелочной | |
| Метиловый оранжевый | красный (рН<3,1) | оранжевый (3,1<рН<4,4) | желтый (рН>4,4) |
| Метиловый красный | красный (рН<4,2) | оранжевый (4,2<рН<6,3) | желтый (рН>6,3) |
| Фенолфталеин | бесцветный (рН<8,0) | бледно-малиновый (8,0<рН<9,8) | малиновый (рН>9,8) |
| Лакмус | красный (рН<5,0) | оранжевый (5,0<рН<8,0) | желтый (рН>8,0) |
Для воды и разбавленных водных растворов при Т=const:
Н+]·[ОН-]=const=KH2O, где KH2O – ионное произведение воды.
При Т=298К (25°С) для чистой воды [Н+]=[ОН-]=10-7 моль/л, поэтому:
KH2O=10-7·10-7=10-14 или р[Н+]+р[ОН-]=14, т.е. р[Н+]=14-р[ОН-].
Т.о. сумма водородного и гидроксильного показателей в водных растворах при 25°С равна 14.
При увеличении температуры значение ионного произведения воды возрастает (например, при 100°С оно достигает величины 5,5·10-13).
Однако следует учитывать, что каковой бы ни была величина реакции раствора (рН), произведение концентраций [Н+]·[ОН-] остаётся неизменным. Величина ионного произведения воды может измениться только при изменении температуры, но не при увеличении [Н+] или [ОН-].
Расчет растворимости солей и минералов
Мn+Аn-(т)=n+Мz+(р-р)+n-Аz-(р-р). (1) Константу данного равновесия называют произведением растворимости соли и… L = a+n+×a-n- = [Mz+]n+×[Az-]n-×g±n, (2)Растворимость в бинарной системе соль - вода
Подставим эти соотношения в (2). L=(n+S)n+(n-S)n-×g±n. После преобразования получим: L=(n±g±S)n, где среднеионный стехиометрический… Отсюда получаем формулу для расчета растворимости соли в воде: (5)Растворимость в многокомпонентной системе в отсутствие
Одноименного иона
Следует подчеркнуть, что с ростом ионной силы g± при не высоких концентрациях электролита понижается, а растворимость увеличивается.Растворимость в многокомпонентной системе с одноименными ионами
L = (n+S)n+(n-S + n¢C¢)n-×g±n. (6) Растворимость находят путем решения степенного уравнения (6). Если… (7)Лекция №10. Гидролиз солей.
KCN+H2O=HCN+KOH AlCl3+H2O=Al(OH)Cl2+HCl Гидролизу подвергаются следующие соли, образованные:Лекция №10
Окислительно-восстановительные реакции.
Все окислительно-восстановительные реакции классифицируют следующим образом: 1. Межмолекулярные реакции. Это реакции, в которых окислитель и восстановитель… ,Лекция №11
Растворы. Способы выражения их концентрации.
Систематическое изучение свойств растворов в зависимости от их составов началось лишь во второй половине XIX-го века. Так своё исследование,… Полярно противоположная точка зрения на растворы, получившая название… Якоб Вант-Гофф пришел к выводу о полной аналогии свойств разбавленных растворов свойствам газов, о применимости к ним…Лекция №12
Классификация растворов. Коллигативные свойства растворов.
1. Идеальные растворы. Физической моделью идеального раствора является совокупность невзаимодействующих частиц, имеющая объем, аддитивно складывающийся из объемов отдельных компонентов. Наиболее важными свойствами идеальных растворов являются: а) Идеальные растворы образуются из чистых компонентов, находящихся в том же агрегатном состоянии, что и раствор, атермально, т.е. без теплового эффекта. б) Объем идеального раствора, образованного из чистых компонентов, находящихся в том же агрегатном состоянии, что и раствор, аддитивно складывается из объемов отдельных компонентов. Основное назначение концепции идеальных растворов – служить эталоном, с которым сравниваются реальные растворы. Все свойства идеальных растворов, в отличие от реальных, легко рассчитываются исходя только из их концентрации и свойств отдельных компонентов.
2. Предельно разбавленные растворы. Предельно разбавленным (п.р.) раствором называют раствор, в котором свойства растворителя практически остались неизменными по сравнению с чистым растворителем ввиду низкой концентрации раствора, в то время как свойства растворенного вещества могут очень сильно отличаться от его свойств в чистом виде ввиду попадания в среду растворителя. Свойствами п.р. растворов обладают обычно все разбавленные растворы вплоть до определенной концентрации, характерной для каждой системы. Чем ближе свойства компонентов, тем до более высокой концентрации сохраняют их растворы свойства п.р. растворов. Для растворов электролитов этот предел очень низок, так как ионы заметно изменяют свойства растворителя уже при миллимолярных концентрациях.
3. Реальные растворы. Различные свойства реальных растворов в той или иной степени отклоняются от идеальных (например, термодинамические). Для адекватного описания этих отклонений обычно требуются различные физические модели, учитывающие межчастичные парные и коллективные взаимодействия, размеры частиц, расстояния между ними и т.д. В некоторых простейших случаях такие модели приводят к результатам, хорошо совпадающим с экспериментом. Однако наиболее универсальный и полностью формальный способ учета неидеальности компонентов раствора был предложен Г. Льюисом в 1907 г., который сохранил ту же форму выражения химического потенциала компонента в реальном растворе, что и в идеальном, но вместо концентрации компонента использовал в нем активности.
По концентрации растворенного вещества растворы можно подразделить на концентрированные (с большой концентрацией растворенного вещества) и разбавленные (с малой концентрацией растворенного вещества).
Важное значение при описании свойств растворов имеет закон Генри: «Масса газа, растворяющегося при постоянной температуре в данном объёме жидкости, прямо пропорциональна парциальному давлению газа». Математически это можно записать так: С=k·р, где k – константа Генри, С – массовая концентрация газа в насыщенном растворе. Важнейшим следствием этого закона является то, что объём газа, растворяющегося при постоянной температуре в данном объёме жидкости, не зависит от его парциального давления.
Коллигативными свойствами раствора называются свойства, зависящие от концентрации частиц растворенного вещества и мало или совсем не зависящие от природы растворителя. К таким свойствам относят:
- давление насыщенного пара растворителя;
- понижение температуры замерзания раствора;
- повышение температуры кипения раствора;
- осмотическое давление.
1. Давление насыщенного пара растворителя. Под давлением насыщенного пара вещества понимают давление его паров в отсутствие других газов, в частности воздуха. Относительное понижение давления пара над раствором равно:
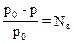 , где р0 – давление насыщенного пара растворителя над чистым растворителем; р - давление насыщенного пара растворителя над раствором; Nв – мольная доля растворенного вещества. Это уравнение является математической формулировкой закона Рауля: «относительное понижение давления насыщенного пара над раствором равно мольной доле растворенного вещества». Явление понижения давления насыщенного пара над раствором вытекает из принципа Ле Шателье.
, где р0 – давление насыщенного пара растворителя над чистым растворителем; р - давление насыщенного пара растворителя над раствором; Nв – мольная доля растворенного вещества. Это уравнение является математической формулировкой закона Рауля: «относительное понижение давления насыщенного пара над раствором равно мольной доле растворенного вещества». Явление понижения давления насыщенного пара над раствором вытекает из принципа Ле Шателье.
2. Осмотическое давление. Осмотическое давление - это такое давление, которое нужно приложить к раствору, отделенному от растворителя полупроницаемой перегородкой, чтобы наступило состояние равновесия. Процесс осмоса, в свою очередь, характеризуется самопроизвольным проникновением молекул растворителя через полупроницаемые перегородки.
В 1886 г. Вант-Гофф cформулировал закон (закон Вант-Гоффа), согласно которому «в разбавленном растворе растворенное вещество ведет себя подобно идеальному газу» и показал, что для растворов неэлектролитов невысоких концентраций осмотическое давление Рос равно:
Рос=С·R·Т=103·(m/M)·RT, где С=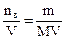 – молярность, моль/м3; R=8,31 Дж/(моль·К) – универсальная газовая постоянная; Т – абсолютная температура раствора, К.
– молярность, моль/м3; R=8,31 Дж/(моль·К) – универсальная газовая постоянная; Т – абсолютная температура раствора, К.
Для растворов электролитов величина Рос составляет:
Рос=i·С·R·Т,
где i – изотонический коэффициент, показывающий, во сколько раз осмотическое давление данного раствора выше нормального. Для каждого раствора этот коэффициент определяется экспериментально.
3. Понижение температуры замерзания раствора (криоскопия). Из всех коллигативных свойств чаще других используются криоскопические измерения ввиду простоты и высокой точности измерения температуры замерзания. Последняя обычно измеряется с помощью специальных метастатических ртутных термометров (термометров Бекмана) с ценой деления 0.01 К. Такие термометры имеют шкалу только на 5 К, но снабжены дополнительным резервуаром для ртути, позволяющим настроить его на любые абсолютные температуры от 260 до 380 К.
Понижение температуры замерзания можно найти как:
Dtзам=i·К·m, где m – моляльность; К - криоскопическая константа, зависящая только от природы растворителя и не зависящая от природы растворенного вещества. Для воды К=1.86, для бензола К=5,07.
4. Повышение температуры кипения раствора (эбуллиоскопия). Помимо криоскопического метода в химии применяется эбуллиоскопический метод, основанный на измерении температуры кипения растворов.
Повышение температуры кипения можно найти как:
Dtкип=i·Е·m, где m – моляльность; Е - эбуллиоскопическая константа, зависящая только от природы растворителя и не зависящая от природы растворенного вещества. Для воды Е=0.52, для бензола Е=2,6.
Оба рассмотренные методы позволяют определять молекулярные массы веществ.
– Конец работы –
Используемые теги: Лекция, основные, Классы, неорганических, соединений, Номенклатура0.091
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Лекция №1 Основные классы неорганических соединений, номенклатура
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов