рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- Химия №96 от 13.04.2009
Реферат Курсовая Конспект
Химия №96 от 13.04.2009
Химия №96 от 13.04.2009 - раздел Химия, ###title### Химия №96 От 13.04.2009 ...
###TITLE###
Химия №96 от 13.04.2009
###THEMES###
Химия
Theme 1
Score 1
Type 1
Time 0:00:00
Наименьшая частица вещества, химически неделимая называется
-{00}Протон
-{00}Химический элемент
+{00}Атом
-{00}Изотоп
Theme 1
Score 1
Type 1
Time 0:00:00
Порядковый номер элемента в ПСХЭ соответствует
-{00}Количеству нейтронов
+{00}Количеству протонов в ядре и электронов в атоме
-{00}Количеству электронов в ядре
-{00}Массовому числу атома
Theme 1
Score 1
Type 1
Time 0:00:00
Способность атомов притягивать недостающие электроны называется
-{00}Электропритяжением
+{00}Электроотрицательностью
-{00}Магнетизмом
-{00}Изотопом
Theme 1
Score 1
Type 1
Time 0:00:00
Металличность это:
+{00}Способность отдавать электроны
-{00}Способность притягивать электроны
-{00}Способность отдавать и принимать электроны
-{00}Способность образовывать новые соединения
Theme 1
Score 1
Type 1
Time 0:00:00
У какого элемента сильнее выражена неметалличность
+{00}O
-{00}C
-{00}N
-{00}B
Theme 1
Score 1
Type 1
Time 0:00:00
Верны ли суждения о том, что изотопы – химические элементы, имеющие: I. одинаковый заряд ядра, но различную атомную массу;II. одинаковые заряд ядра и атомную массу.
+{00}Верно суждение I
-{00}Верно суждение II
-{00}Оба суждения не верны
-{00}Оба суждения верны
Theme 1
Score 1
Type 1
Time 0:00:00
Номер периода в Периодической системе определяется
-{00}Зарядом ядра атома
-{00}Числом электронов в наружном слое атома
+{00}Числом электронных слоев в атоме
-{00}Числом электронов в атоме
Theme 1
Score 1
Type 1
Time 0:00:00
Атомные ядра были открыты
-{00}Д. Менделеевым
+{00}Э. Резерфордом
-{00}Дж. Томсоном
-{00}Д. Чедвигом
Theme 1
Score 1
Type 1
Time 0:00:00
Форму электронных орбиталей характеризует
-{00}Главное квантовое число
-{00}Магнитное квантовое число
+{00}Орбитальное квантовое число
-{00}Спиновое квантовое число
Theme 1
Score 1
Type 1
Time 0:00:00
р-элементом является
-{00}Скандий
-{00}Барий
+{00}Мышьяк
-{00}Гелий
Theme 1
Score 1
Type 1
Time 0:00:00
Амфотерным гидроксидом является вещество, формула которого
+{00}Zn(OH)2
-{00}Mg(OH)2
-{00}Ca(OH)2
-{00}Cr(OH)2
Theme 1
Score 1
Type 1
Time 0:00:00
Элемент Э с электронной формулой 1s22s22p63s23p63d104s24p1образует высший оксид, соответствующий формуле
-{00}Э2О
+{00}Э2О3
-{00}ЭО2
-{00}ЭО3
Theme 1
Score 1
Type 1
Time 0:00:00
Изотоп кальция, в ядре которого содержится 22 нейрона, обозначают:
-{00}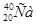
-{00}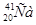
-{00}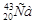
+{00}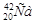
Theme 1
Score 1
Type 4
Time 0:00:00
Установите соответствие. Элемент:
-{00}[05]Al
-{00}[08]Cu
-{00}[07]Se
-{00}[06]Mg
-{00}[00]1s22s22p63s23p1
-{00}[00]1s22s22p63s2
-{00}[00]1s22s22p63s23p63d104s24p4
-{00}[00]1s22s22p63s23p63d104s1
Theme 1
Score 1
Type 5
Time 0:00:00
На основании положения в Периодической системе расположите элементы в порядке убывания окислительных свойств:
-{00}[04]Германий
-{00}[03]Мышьяк
-{00}[01]Сера
-{00}[02]Фосфор
Theme 1
Score 1
Type 1
Time 0:00:00
Верны ли суждения о том, что электролиты – вещества, расплавы и растворы которых: I. проводят электрический ток;II. не проводят электрический ток.
+{00}Верно суждение I
-{00}Верно суждение II
-{00}Оба суждения не верны
-{00}Оба суждения верны
Theme 1
Score 1
Type 1
Time 0:00:00
Верны ли суждения о том, что в растворах слабых электролитов: I. равновесие смещается в сторону образования молекул; II. в сторону обратной реакции.
-{00}Верно суждение I
-{00}Верно суждение II
-{00}Оба суждения не верны
+{00}Оба суждения верны
Theme 1
Score 1
Type 1
Time 0:00:00
Масса 5 моль углекислого газа СО2равна
-{00}22 г
+{00}220 г
-{00}44 г
-{00}88 г
Theme 1
Score 1
Type 1
Time 0:00:00
Укажите ряд элементов, расположенных в порядке усиления металлических свойств:
-{00}Mg – Ca – Zn
+{00}Al – Mg – Ca
-{00}Sr – Rb – K
-{00}Ge – Si – Sb
Theme 1
Score 1
Type 2
Time 0:00:00
Укажите пары элементов, между которыми образуется ковалентная полярная связь:
+{00}N и H
-{00}O и O
+{00}H и O
-{00}Na и F
Theme 1
Score 1
Type 1
Time 0:00:00
Укажите формулу соединения с ковалентной связью
-{00}NaCl
+{00}HCl
-{00}BaO
-{00}MgO
Theme 1
Score 1
Type 1
Time 0:00:00
Верны ли суждения: I. σ- связь возникакет в результате бокового перекрывания орбиталей.II. π- связь возникает в результате бокового перекрывания орбиталей.
-{00}верно суждение I
+{00}верно суждение II
-{00}оба суждения не верны
-{00}оба суждения верны
Theme 1
Score 1
Type 2
Time 0:00:00
Атомную кристаллическую решетку имеют
+{00}Графит
-{00}Хлорид натрия
-{00}Йод
+{00}Оксид кремния
Theme 1
Score 1
Type 1
Time 0:00:00
Укажите элемент, у которого возможна аллотропия
-{00}Хлор
+{00}Углерод
-{00}Алюминий
-{00}Бром
Theme 1
Score 1
Type 1
Time 0:00:00
Из приведенных элементов укажите металлический
-{00}S
-{00}Li
+{00}Ba
-{00}Al
Theme 1
Score 1
Type 1
Time 0:00:00
Укажите металл, способный вытеснять водород из воды
-{00}Cu
+{00}Li
-{00}Pb
-{00}Sn
Theme 1
Score 1
Type 2
Time 0:00:00
Из раствора соли сульфата меди (II) медь не вытесняют
-{00}Zn
+{00}Ca
-{00}Fe
+{00}Na
Theme 1
Score 1
Type 2
Time 0:00:00
Верны ли суждения о том, что амфотерные соединения – оксиды и гидроксиды, как правило: I. образованы переходными элементами;II. образованы неметаллами.
+{00}Верно суждение I
-{00}Верно суждение II
-{00}Оба суждения не верны
-{00}Оба суждения верны
Theme 1
Score 1
Type 4
Time 0:00:00
Установите соответствие между формулой и названием у следующих соединений:
-{00}[06]MgO
-{00}[07]NaCl
-{00}[08]Cu(OH)2
-{00}[00]H2SO4
-{00}[00]Серная кислота
-{00}[00]Оксид магния
-{00}[00]Хлорид натрия
-{00}[00]Гидроксид меди
Theme 1
Score 1
Type 1
Time 0:00:00
Укажите, вещество, у которого наиболее ярко выражены кислотные свойства:
-{00}HNO2
-{00}HPO3
-{00}H2SO3
+{00}HNO3
Theme 1
Score 1
Type 1
Time 0:00:00
Ионное уравнение реакции H++ OH-= H2O соответствует взаимодействию:
+{00}Гидроксида калия и азотной кислоты
-{00}Гидроксида бария и серной кислоты
-{00}Гидроксида лития и хлорида бария
-{00}Аммиака и бромоводородной кислоты
Theme 1
Score 1
Type 1
Time 0:00:00
Укажите формулы продуктов взаимодействия концентрированной серной кислоты с серебром
-{00}H2и AgSO4
+{00}SO2, H2O и AgSO4
-{00}H2S, H2O4и AgSO4
-{00}Реакция не идёт
Theme 1
Score 1
Type 4
Time 0:00:00
Установите соответствие между левой частью молекулярного уравнения и правой частью ионного уравнения
-{00}[08]Ca + 2HCl =
-{00}[05]Ca(OH)2+ Na2CO3=
-{00}[06]CaO + 2HCl =
-{00}[00]CaCO3 + 2HCl =
-{00}[00]CaCO3↓+H2O
-{00}[00]Ca+2+ H2O
-{00}[00]Ca+2+ CO2↑+ H2O
-{00}[00]Ca+2+ H20
Theme 1
Score 1
Type 2
Time 0:00:00
Из приведенных формул укажите кислоты:
-{00}СО2
-{00}H2O
+{00}Cr2O3
+{00}ZnO
-{00}N2O5
-{00}CO
-{00}CuO
-{00}MgO
Theme 1
Score 1
Type 1
Time 0:00:00
Верны ли суждения о том, что оксиды получают: I. при взаимодействии неметалла или металла с кислородом;II. при разложении кислородсодержащих кислот или нерастворимых оснований, или некоторых солей.
-{00}Верно суждение I
-{00}Верно суждение II
-{00}Все суждения не верны
+{00}Все суждения верны
Theme 1
Score 1
Type 1
Time 0:00:00
Для приготовления 10% раствора соли массой 60г надо взять:
+{00}6 г соли и 54 г воды
-{00}3 г соли и 57 г воды
-{00}10 г соли и 50 г воды
-{00}50 г соли и 10 г воды
Theme 1
Score 1
Type 1
Time 0:00:00
Элементы группы IIIА имеют формулу высшего оксида
-{00}RO
+{00}R2O3
-{00}RO3
-{00}R2O
Theme 1
Score 1
Type 1
Time 0:00:00
Для осуществления цепочки превращений: карбонат кальция→1гидрокарбонат кальция→2хлорид кальция необходимы вещества:
+{00}1 – углекислый газ и вода; 2 – соляная кислота
-{00}1 – углекислый газ и вода; 2 – хлорид натрия
-{00}1 – соляная кислота; 2 – хлорид натрия
-{00}1 – гидрокарбонат натрия; 2 – соляная кислота
Theme 1
Score 1
Type 4
Time 0:00:00
Установите соответствие:
-{00}[07]Fe + CuSO4= FeSO4+ Cu
-{00}[08]HCl + KOH = KCl + H2O
-{00}[05]Ca + S = CaS
-{00}[06]2KClO3= 2KCl + 3O2
-{00}[00]Реакция разложения
-{00}[00]Реакция соединения
-{00}[00]Реакция замещения
-{00}[00]Реакция обмена
Theme 1
Score 0
Type 2
Time 0:00:00
Из приведенных формул укажите несолеобразующие оксиды
-{00}Mn2О7
-{00}Cl2O5
-{00}Cr2O3
-{00}Fe2O3
+{00}N2O
+{00}CO
-{00}CuO
-{00}MgO
Theme 1
Score 1
Type 2
Time 0:00:00
Из приведенных формул укажите амфотерные оксиды:
-{00}Na2О
-{00}H2O
+{00}Cr2O3
+{00}ZnO
-{00}N2O5
-{00}CO
-{00}CuO
-{00}MgO
Theme 1
Score 1
Type 1
Time 0:00:00
Укажите общую формулу алкенов
-{00}СnH2n+1OH
-{00}CnH2n+2
-{00}CnH2n-2
+{00}CnH2n
Theme 1
Score 1
Type 2
Time 0:00:00
Укажите формулу этилового спирта
-{00}С2H5OСОСH3
-{00}CH3СООН
+{00}C2H5ОН
-{00}C3H7ОН
Theme 1
Score 1
Type 2
Time 0:00:00
Укажите функциональную группу карбоновых кислот
+{00}– СООН
-{00} – ОН
-{00}– О –
-{00} – NH2
Theme 1
Score 1
Type 2
Time 0:00:00
Верны ли суждения о том, что радикал - это: I. частица с неспаренным электроном;II. частица с одной свободной химической связью.
-{00}Верно суждение I
-{00}Верно суждение II
-{00}Все суждения не верны
+{00}Все суждения верны
Theme 1
Score 1
Type 1
Time 0:00:00
Верны ли суждения о том, что изомеры - это: I. вещества, имеющие одинаковый количественный и качественный состав, но отличающиеся по своему строению и свойствам;II. вещества, имеющие одинаковый состав, строение и свойства.
+{00}Верно суждение I
-{00}Верно суждение II
-{00}Все суждения не верны
-{00}Все суждения верны
Theme 1
Score 1
Type 1
Time 0:00:00
Этилен реагирует с
+{00}Бромом
-{00}Водой
-{00}Уксусной кислотой
-{00}Ацетиленом
Theme 1
Score 1
Type 1
Time 0:00:00
Алканы реагируют с
-{00}Водородом
-{00}Спиртами
+{00}Галогенами
-{00}Бензолом
Theme 1
Score 1
Type 1
Time 0:00:00
Этиловый спирт реагирует со всеми веществами группы
-{00}Серная кислота, оксид меди (II), пропиловый спирт
+{00}Уксусная кислота, метиловый спирт, муравьиная кислота
-{00}Глицерин, диэтиловый эфир, этан
-{00}Этиловый спирт, глицерин, эфир
Theme 1
Score 1
Type 1
Time 0:00:00
Уксусная кислота реагирует с
-{00}Алюминием
-{00}Метиловым спиртом
-{00}Глицерином
+{00}Гидроксидом натрия
Theme 1
Score 1
Type 1
Time 0:00:00
Метан не реагирует с
-{00}Бромом
+{00}Этиленом
-{00}Водой
-{00}Водородом
Theme 1
Score 1
Type 1
Time 0:00:00
Гидролизу не подвергается
-{00}Крахмал
-{00}Целлюлоза
+{00}Глюкоза
-{00}Сахароза
Theme 1
Score 1
Type 1
Time 0:00:00
Химическая реакция, уравнение которой 2С3Н7СООН + Mg→(С3Н7СОО)2Mg + Н2↑, относится к реакциям
-{00}Ионного обмена
-{00}Этерификации
+{00}Замещения
-{00}Окисления
Theme 1
Score 1
Type 1
Time 0:00:00
При нагревании крахмала с разбавленной серной кислотой образуется
+{00}Глюкоза
-{00}Сахароза
-{00}Фруктоза
-{00}Этанол
Theme 1
Score 1
Type 1
Time 0:00:00
Укажите уравнение соответствующее процессу этерификации
-{00}СН3СНОС3Н7+ Н2O→ СН3СOOН + С3Н7ОН
-{00}СН3ОН + СН3ОН → СН3 – O – СН3+ H2O
+{00}С3Н7ОН + СН3СООН→ СН3СOО С3Н7+ H2O
-{00}С2Н5СООН + NaOH→ С2Н5СООNa + H2O
Theme 1
Score 1
Type 1
Time 0:00:00
Осадок красного цвета образуется при нагревании аммиачного раствора оксида серебра с раствором:
-{00}Этилового спирта
+{00}Глюкозы
-{00}Этиленгликоля
-{00}Фенола
Theme 1
Score 1
Type 4
Time 0:00:00
Установите соответствие
-{00}[06]НСООН
-{00}[07]С12Н22О11
-{00}[05]С2Н4
-{00}[08]С6Н14
-{00}[00]Этилен
-{00}[00]Муравьиная кислота
-{00}[00]Сахароза
-{00}[00]Гексан
Theme 1
Score 0
Type 1
Time 0:00:00
Укажите в схеме превращений: С4Н9ОН + HBr→X1+ NaOH(р-р)→ X2веществами X1и X2являются соответственно:
-{00}2- бромбутанол и бутилат натрия
-{00}Бромбутан и бутилат натрия
+{00}Бромбутан и бутанол
-{00}Бромбутен и бутанол
Theme 1
Score 0
Type 1
Time 0:00:00
Укажите в схеме превращений: С2Н4+ H2О→X1+ Na→ X2веществами X1и X2являются соответственно:
-{00}Уксусная кислота и ацетат натрия
-{00}Этаналь и уксусная кислота
-{00}Этанол и ацетат натрия
+{00}Этанол и этилат натрия
Theme 1
Score 0
Type 1
Time 0:00:00
Укажите, что произойдет при пропускании через бромную воду смеси газов пропана, этана и этена
-{00}Раствор не изменит свою окраску
-{00}Масса смеси газов увеличится
+{00}Раствор обесцветится
-{00}Смесь газов полностью растворится
– Конец работы –
Используемые теги: Химия, 04, 20090.063
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Химия №96 от 13.04.2009
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов