рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Производство
- /
- Состояние системы, при котором энтальпийный и энтропийный факторы уравновешиваются, т.е. ∆r GТ = 0
Реферат Курсовая Конспект
Состояние системы, при котором энтальпийный и энтропийный факторы уравновешиваются, т.е. ∆r GТ = 0
Состояние системы, при котором энтальпийный и энтропийный факторы уравновешиваются, т.е. ∆r GТ = 0 - раздел Производство, ...
| |||
 |
THORN; Возможности самопроизвольного протекания прямой и обратной реакции равновероятны.
THORN; Парциальные давления и концентрации всех компонентов реакции постоянны во времени и во всех точках системы - равновесные давления и концентрации.
: : При равновесии химической реакции:
aA(г)+bB(г)+ dD(к) Û eE(г)+ fF(г)
Û eE(г)+ fF(г)
изотерма Вант-Гоффа:
. Δr GТ = ∆r G 0Т + RT ln 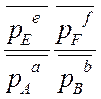 = 0Þ
= 0Þ
………………… ……… …… ……………………………………….
. ∆r G 0Т = - RT ln 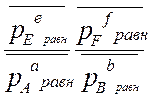 : :
: :
Pравн. !
Если реакция
aA(р-р)+bB(р-р)+dD(к) Û eE(р-р)+fF(р-р) протекает в идеальном растворе:Равновесные равновесные .
Относительные молярные .
Парциальные концентрации
Давления расворенных
Газов веществ
Р РАВН [атм ] С РАВН [моль/л]
R G 0Т = - RT lnКр - для реакций в газовых
Системах
..
R G 0Т = - RT lnКс - для реакций в
Конденсированных системах
R=8,31 Дж /моль.К.
Связь между Кр и Кс через основной закон
Газового состояния:
для каждого газа Þ p = cRT Þ
 |
E + f) – (a + b) – изменение числа молей газов в результате реакции, ! ! R = 0,082 атм .л/моль.К ю.. !
Выражение Кр - через равновесные количества молей газообразных компонентов ni(равн)
и общее давление P0:
Парциальное давление конкретного газа - pi = 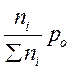
Кр= =..
Σni = nE равн + nF равн + nA равн + nB равн (для газов !)
……..……………
Кр и Кс - характеризуют
выход продуктов реакции:
Чем > К тем > больше продуктов в равновесной смеси
Кр и Кс не зависят от: !
● парциальных давлений
● концентраций компонентов
●общего давления в системе
Кр и Кс зависят от: !
● температурыС учетом ≈ ∆r H0 ¹ f (T) и ∆r S0 ¹ f (T) имеем
▓ уравнение изобары Вант-Гоффа:
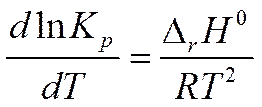
Вывод:
· если ∆r H0 < 0 Þ dlnKp/dT < 0
Т Þ ¯Кр т.е. с повышением температуры Þ
Кр уменьшается Þ равновесие смещается влево
· если ∆rH0 > 0 Þ dlnKp/dT > 0
Т Þ Кр т.е. с повышением температуры Þ Кр увеличивается Þ равновесие смещается вправо
Изменение концентраций реагентов
aA(г) +bB(г)+ dD(к) Û eE( г) +fF(г) Þ таблица материального баланса: [моль/л] A (г) B (г) D(к) E (г) F (г)Г г ж
юКС = 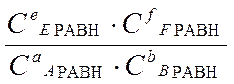 ю Þ
ю Þ
THORN; юKC = ю
THORN; решаем уравнение относительно Х Þ С равн.
Для всех реагентов химической реакции.
Равновесие смещается: · при увеличении Т - в сторону.. эндотермической реакции;Задача Для реакции
С(к) + СО2(г) Û 2СО(г)
Рассчитать Кр и Кс при 298 К и 1000 К. Сделайте вывод о выходе продукта реакции и определите знак энтальпии реакции.
Решение
: Кр = ; : Кс = : ∆r G0Т = - RTlnКр Þ : Kp = exp(-∆G0Т /RT) для данной реакции было рассчитано ранее - см. Пример расчета выше:R G0298 = 120,15 кДж; ∆r G01000 = - 3,16 кДж
Кр 298= exp(-120.103/8,31.298) = ехр(-48,5) = 8×10-22
Kp 1000 =exp(+3160/8,31.1000) = ехр(0,38) = 1, 46
(обратите внимание на размерность!)
Кс = = = 0,018
∆ν = 2-1= 1 (изменение числа молей газообр. веществ ! )
· При 298К - Кр ® 0 Þ в равновесной смеси практически отсутствуют продукты и смещение равновесия относительно стандартного состояния Þ в сторону исходных веществ, влево.
· При 1000 К - Кр > 1 Þ в равновесной смеси начинают преобладать продукты, их выход растет с увеличением Т, равновесие смещается вправо.
Т.к. при Т Þ Кр Þ ∆rH0 > 0 (с учетом изобары Вант-Гоффа), процесс эндотермический.
▼ Задача Для реакции:
А(г) Û 2В(г) (Р,Т – const)
Кр1 = 0,02 при 400 К и Кр2 = 4,00 при 600 К.
Определить ∆rH0298 , ∆rS0298 и Кр3 при 800 К.
Решение
∆rG0Т1 = ∆rH0298 –T1∆rS0298 = -RT1lnКр1 ∆rG0Т2 = ∆rH0298 –T2∆rS0298 = -RT2lnКр2 ∆rH0298 – 400∆rS0298 = - 8,31.400 ln2.10-2RH0298 – 600∆rS0298 = - 8,31.600 ln4
THORN; ∆rH0298 = 52833(Дж) = 52,833 кДж
THORN; ∆rS0298 = 99,575 Дж/К
Используем изобару Вант-Гоффа:
ln 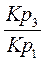 = ln
= ln 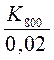 =
= 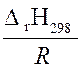 (
(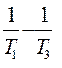 )
)
Ln = ln=()= 7,95 Þ К800 = 56,55
При Т Þ Кр Þ ∆rH0 > 0, процесс эндотермический.
Задача. Определить равновесный состав системы
С(к) + СО2(г) Û 2СО(г)
Т= 1000 К, Робщ = 2атм, n исх CO2 = 5 моль
Решение.Реакция идет при постоянном давлении Робщ !
Kp =exp(-∆G0Т /RT) , ∆r G01000 = - 3,16 кДж
Kp1000 = exp(+3160/8,31.1000)= ехр(0,38) = 1, 46
Материальный баланс:
| Компонент | С | СО2 | 2СО |
| Нач. состав, моль | - | ||
| Изменение, моль | - | х | 2 x |
| Равновесный, моль | - | 5 – x | 2 x |
Кр = 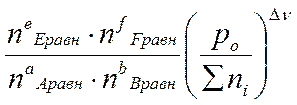 =
= 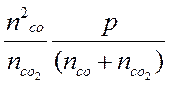 =
=
= = 1,46
Решаем уравнение относительно х Þ х = 1,7 моль
Равновесный состав: n(СО2) = 5 - 1,7=3,3 молей
N(СО) = 2×1,7 = 3,4 молей
Задача. Определить равновесные концентрации С равн СО2 и СО для реакции
С(к) + СО2(г) Û 2СО(г)
Т= 1000 К , Vсосудa = 2л, mисх (СО2) = 44г,
Обратите внимание: реакция идет при V=const !
Определить, на сколько изменится давление в системе при равновесии по сравнению с исходным.
Решение
ССО2 = = =0,5моль/л; Кс1000 = 0,018
(см.выше)
Таблица материального баланса:
| Компонент | С | СО2 | 2СО |
| Нач.концентрации, Сисх, моль/л | - | 0,5 | |
| Изменение конц.,ΔС, моль/л | - | х | 2 x |
| Равновесные конц., Сравн., моль/л | - | 0,5 – x | 2 x |
Кс = = 0,018 Þ х = 0,0387моль/л
ССО равн = 2. 0,0387 = 0,0774моль/л
ССО2равн = 0,5 - 0,0387 = 0,4613 моль/л
Начальное состояние
Р0 = сRT = 0,5.0,082•1000 = 41атм только СО2
Равновесное состояние
Рравн = [( 0,5-х) + 2х) ]RT = 44,17 атм СО2 и СО
Изменение давление в системе Þ DР = 3,17 атм
В равновесной системе 3 моля газов:
N = 3, nСО2= 1, nСО = 2.
Равновесное парциальное давление газов:
РСО2= 1/3(Рравн) = 14,72 атм, РСО= 2/3(Рравн) = 29,45 атм.
Задача. Предложите способы увеличения выхода продуктов реакции
С(к) + СО2(г) Û 2СО(г)
Решение. Для повышения выхода продукта СО нужно Þ равновесие сместить вправо.
Для смещения равновесия вправо нужно:
* Тсистемы, т.к. ∆r H0298 > 0;
* ¯ Рсистемы , т.к. прямая реакция идет с увеличением числа молей газообразных веществ;
* РСО2 ;
Macr; РСО (выводить из сферы реакции).
ОПЫТЫ
СМЕЩЕНИЕ РАВНОВЕСИЯ. «ГЛИКОЛЬ»
CuSO4 + 2NH2CH2COOH Û Cu(NH2CH2COOH )2+ H2SO4
голубой гликоль синий
цвет цвет
3 цилиндра:
1 – для сравнения
2 – добавляем CuSO4 → синий цв.
3 – добавляем гликоль → синий цв.
4 – добавляем H2SO4 ← голубой цв.
5 – добавляем NаОH → синий цв.
– Конец работы –
Используемые теги: состояние, системы, котором, энтальпийный, энтропийный, факторы, уравновешиваются, GТ0.112
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: Состояние системы, при котором энтальпийный и энтропийный факторы уравновешиваются, т.е. ∆r GТ = 0
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов