рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Химия
- /
- А. А. Шидловский: Развитие химии и физики горения
Реферат Курсовая Конспект
А. А. Шидловский: Развитие химии и физики горения
А. А. Шидловский: Развитие химии и физики горения - раздел Химия, А. А. Шидловский Основы Пир...
А. А. Шидловский
ОСНОВЫ ПИРОТЕХНИКИ
Допущено Министерством высшего и среднего специального образования СССР в качестве учебного пособияПРЕДИСЛОВИЕ
Многочисленные и весьма разнообразные пиротехнические средства находят широкое применение в военном деле и в различных отраслях народного хозяйства.
Развитие химии и физики горения обеспечивает возможность создания новых видов пиротехнических составов.
В настоящее время в этой области накоплен значительный опыт. В предлагаемом учебном пособии (4-е издание) авторы стремились по возможности обобщить этот опыт. При написании книги были использованы опубликованные за последние годы работы как советских, так и иностранных специалистов.
Излагаемый в книге материал курса «Основы пиротехники» состоит из двух частей.
В первой части дана классификация составов, рассматриваются методы испытания, общие для всех видов пиротехнических составов.
Особое внимание при этом уделено рассмотрению процессов горения. Авторы стремились обобщить накопленный к настоящему времени материал о факторах, определяющих скорость горения составов, показать на некоторых примерах возможный механизм их горения.
Вторая часть книги посвящена описанию отдельных видов пиротехнических составов и их специфических свойств. Здесь же дается краткое описание устройств и действия некоторых пиротехнических средств. Эта часть книги написана заново (гл. XI— XXII), обновлены главы II, VII, VIII, дано много новых рисунков. Параграфы 1—2 и 6—8 гл. XI, гл. XII, XIII и § 1—6 гл. XV написаны канд. техн. наук И. И. Вернидубом, гл. XVIII—канд. техн. наук Е. С. Шахиджановым и гл. XXII—канд. техн. наук В. И. Коноваловым. Параграф 9 гл. XI и частично § 6 гл. VI написаны инж. А. В. Сметана.
Автор весьма признателен кандидатам техн. наук Н. Н. Ивановой и Н. А. Бильдюкевич за многие ценные замечания и указания, сделанные ими при рецензировании рукописи.
Все замечания и пожелания по книге автор просит направлять по адресу: Москва, Б-78, 1-й Басманный пер., 3, издательство «Машиностроение».
Часть первая
ОБЩИЕ СВОЙСТВА ПИРОТЕХНИЧЕСКИХ СОСТАВОВ И ИХ КОМПОНЕНТОВ
ГЛАВА I
ОБЩЕЕ ПОНЯТИЕ О ПИРОТЕХНИЧЕСКИХ СРЕДСТВАХ И СОСТАВАХ
Пиротехника - это наука о свойствах пиротехнических (огневых) составов и изделий из них и способах их изготовления. Пиротехнические составы при сжигании (или взрыве) дают световой, тепловой,… Применению пиротехнических составов в народном хозяйстве (в промышленности, на транспорте, при научных исследованиях и…КЛАССИФИКАЦИЯ
Пиротехническими составами снаряжают следующие виды средств военного назначения:
1) осветительные средства (авиабомбы, артиллерийские снаряды, авиационные факелы и др.), используемые для освещения местности в ночных условиях;
2) фотоосветительные средства (фотобомбы, фотопатроны), используемые при ночной аэрофотосъемке: и для других целей;
3) трассирующие средства, делающие видимой траекторию полета пуль и снарядов (и других подвижных объектов) и тем самым облегчающие пристрелку по быстро движущимся целям;
4) средства инфракрасного излучения, используемые для слежения за полетом ракет и в качестве ложных целей;
5) ночные сигнальные средства (патроны и др.), применяемые для подачи сигналов;
6) дневные сигнальные средства (патроны и др.), используемые для той же цели, но в дневных условиях;
7) зажигательные средства (бомбы, снаряды, пули и многие Др.), служащие для уничтожения военных объектов противника;
8) маскирующие средства (дымовые шашки, снаряды и др.), употребляемые для получения дымовых завес;
9) ракеты различного назначения и дальности полета, использующие твердое пиротехническое топливо;
10) учебно-имитационные средства, употребляемые как на маневрах и ученьях, так и в боевой обстановке. Они имитируют действие атомных бомб, фугасных снарядов и бомб, а также различные явления на поле боя: орудийные выстрелы, пожары и др., и могут этим дезориентировать службу наблюдения противника;
11) целеуказательные средства (снаряды, бомбы и др.), указывающие местонахождение объектов противника;
12) пиротехнические газогенераторы, используемые для различных целей.
Пиротехнические составы используются также и в различных областях народного хозяйства.
К пиротехническим составам военного назначения можно отнести следующие:
1) осветительные;
2) фотоосветительные (фотосмеси);
3) трассирующие;
4) инфракрасного излучения;
5) зажигательные;
6) ночных сигнальных огней;
7) цветных сигнальных дымов;
8) маскирующих дымов;
9) твердое пиротехническое топливо;
10) безпазовые (для замедлителей);
11) газогенерирующие;
12) воспламенительные, содержащиеся в небольшом количестве во всех пиротехнических средствах;
13) прочие: имитационные, свистящие и др.
Многие составы применяются в самых различных видах средств; так, например, осветительные составы часто используют в трассирующих средствах; составы маскирующих дымов могут быть использованы и в учебно-имитационных средствах и т. д.
Пиротехнические составы можно также классифицировать по характеру процессов, протекающих три их горении.
Пламенные составы
1. Белопламенные.
2. Цветнолламенные.
3. Составы инфракрасного излучения.
Тепловые составы
1. Термитно-зажигательные.
2. Безгазовые (малогазовые).
Дымовые составы
1. Белого и черного дыма.
2. Цветного дыма.
Вещества и смеси, сгорающие за счет кислорода воздуха
1. Металлы и сплавы металлов.
2. Фосфор, его растворы и сплавы. 3. Смеси нефтепродуктов.
4. Различные вещества и смеси, загорающиеся при соприкосновении с водой или воздухом.
ГОРЕНИЕ СОСТАВОВ
Процесс горения характеризуется: 1) наличием подвижной зоны реакции, имеющей высокую температуру (сотни и… 2) отсутствием скачка давления в зоне реакции (в пламени); этим процессы горения существенно отличаются от процессов…ТРЕБОВАНИЯ, ПРЕДЪЯВЛЯЕМЫЕ К ПИРОТЕХНИЧЕСКИМ СРЕДСТВАМ И СОСТАВАМ
Для трассирующих средств, специальный эффект определяется хорошей видимостью полета пули или снаряда. Видимость, в свою очередь, определяется силой… Для зажигательных средств хороший специальный эффект обуславливается (при… Для маскирующих дымовых средств, специальный эффект определяется созданием возможно большей, густой и устойчивой…НАЗНАЧЕНИЕ КОМПОНЕНТОВ
а) горючие; б) окислители; в) связующие (цементаторы) - органические полимеры, обеспечивающие механическую прочность уплотненных (спрессованных)…ВОЗМОЖНЫЕ ВЫСОКОЭКЗОТЕРМИЧЕСКИЕ РЕАКЦИИ
Очевидно, тепло будет выделяться в том случае, когда разрываемые связи будут слабыми, а вновь образуемые - более прочными. Наиболее прочные связи образуются при соединении атомов элементов,… Фтор и кислород являются при обычных условиях газами, что исключает возможность их применения в пиротехнических…СПОСОБНОСТЬ К ГОРЕНИЮ РАЗЛИЧНЫХ ВЕЩЕСТВ И СМЕСЕЙ
Для подтверждения этого положения автор книги провел ряд термохимических расчетов, а затем доказал экспериментально способность к горению некоторых… К числу таких веществ относятся аммонийные соли многих кислот, многие соли… Также способными к горению оказались двойные смеси высококалорийных металлов (Mg, A1) с водой, карбонатами металлов,…ГЛАВА II
ОКИСЛИТЕЛИ
Сгорание горючих веществ на воздухе протекает обычно медленнее, чем сгорание их за счет кислорода окислителя, и поэтому смеси, не содержащие в себе… Кроме кислородных соединений, в качестве окислителей используются иногда и… Окислителями могут быть и простые вещества — неметаллы, находящиеся при обычных условиях в твердом состоянии.ВЫБОР ОКИСЛИТЕЛЕЙ
1) содержать максимальное количество кислорода; 2) легко отдавать кислород при горении состава; 3) быть устойчивым в интервале от -60 до +60 C и не разлагаться от действия воды;СВОЙСТВА ОКИСЛИТЕЛЕЙ
1) плотность; 2) температура плавления; 3) температура интенсивного разложения;ГИГРОСКОПИЧНОСТЬ
Количество воды, поглощаемой солями из воздуха, зависит от влажности и температуры воздуха, от индивидуальных свойств соли и от величины поверхности… Если относительная влажность воздуха в помещении больше указанной в… и «выветривание» из кристаллогидратов кристаллизационной воды.ТЕХНИЧЕСКИЕ ТРЕБОВАНИЯ
1. Максимальное содержание основного вещества (обычно не менее 98—99%). 2. Минимальное содержание влаги (не более 0,1—0,2%). 3. Минимальное содержание примесей гигроскопичных солей и солей тяжелых металлов.ГЛАВА III
ГОРЮЧИЕ
ВЫБОР И КЛАССИФИКАЦИЯ
При выборе горючего необходимо учитывать все требования, предъявляемые к составу.
Наилучший специальный эффект в зажигательных, осветительных и трассирующих составах достигается при высокой температуре их горения; в этом случае необходимо применять высококалорийные горючие. В твердом пиротехническом топливе также должны использоваться высококалорийные горючие.
Для дымовых составов высокая температуру горения в большинстве случаев нежелательна; часто для их изготовления или выбирают горючее со средней калорийностью или осуществляют неполное сгорание горючего (например, сгорание углерода в СО).
Большое значение при выборе горючего имеют также физико-химические свойства продуктов его окисления, в первую очередь их агрегатное состояние при комнатной температуре и при температуре горения состава. Для осветительных составов важно соблюдать некоторое оптимальное соотношение между количеством газообразных продуктов, которые сильно влияют на размеры пламени (следовательно, и на силу света), и концентрацией в пламени твердых и жидких частиц излучателей. Как избыток, так и недостаток газообразных продуктов вызывают снижение силы света.
В продуктах горения твердого пиротехнического топлива и газогенераторных составов должно содержаться максимальное количество газов и по возможности меньшее количество твердых веществ.
В дымовых составах количество газов, образующихся при горении, должно быть весьма значительным, потому что они выталкивают в атмосферу лары дымообразующих веществ.
* В данной главе рассматриваются свойства горючих веществ, не выполняющих в составах функции связующих.
Количество газов, образующихся при горении безгазовых составов, как следует из самого их названия, должно быть минимальным.
При выборе горючего для пламенных составов необходимо учитывать интенсивность светового излучения продуктов его окисления, а также и распределение энергии излучения по спектру.
Большую роль при выборе горючего играет легкость его окисления. Например, кремний или графит с большим трудом окисляются даже при применении самых энергичных окислителей (горение в чистом кислороде или в смеси с КСlO3 вследствие чего применение их в качестве горючих крайне ограничено.
Алюминий, взятый в виде мелкодисперсного порошка или пудры, горит достаточно энергично как за счет кислорода окислителя, так при некоторых условиях и за счет кислорода воздуха (здесь имеется в виду горение взвеси алюминиевой пудры в воздухе).
Магний, являясь одним из легкоокисляемых горючих, даже не будучи тонко измельчен может полностью сгорать за счет кислорода воздуха.
Некоторые горючие окисляются чересчур легко, вследствие чего смеси их с окислителями чрезмерно чувствительны к удару и трению или же обладают слишком низкой температурой воспламенения. Так, например, белый фосфор не только нельзя смешивать ни с каким окислителем, но и нельзя хранить на воздухе во избежание самовоспламенения. Применение смесей красного фосфора с окислителями также весьма ограничено: красный фосфор при смешении с хлоратами самовоспламеняется, а смесь его с другими окислителями (например, с нитратами) обладает большой чувствительностью к удару и трению.
Желательно, чтобы для сгорания весовой единицы горючего требовалось как можно меньше кислорода, так как большое содержание в составе окислителя невыгодно: оно ведет к уменьшению количества горючего, а следовательно, и к уменьшению количества выделяемого составом тепла.
Кроме того, при выборе горючего должна быть обеспечена достаточная химическая стойкость состава при хранении. Следует учесть, что некоторые комбинации горючих с окислителями являются недостаточно химически стойкими (подробнее см. гл.Х).
Таким образом, применяемые в составах горючие должны удовлетворять следующим требованиям:
1) иметь теплоту горения, обеспечивающую наилучший специальный эффект состава;
2) достаточно легко окисляться за счет кислорода окислителя или за счет кислорода воздуха;
3) давать при сгорании продукты, обеспечивающие получение наилучшего специального эффекта;
4) требовать для своего сгорания минимальное количество
кислорода;
5) быть химически и физически стойкими при температуре от —60 до +60° С, быть по возможности устойчивыми к действию слабых растворов кислот и щелочей;
6) быть негигроскопичными (мало гигроскопичными);
7) легко измельчаться;
8) не оказывать токсического действия на человеческий организм.
Применяемые горючие можно разделить на следующие категории.
Неорганические горючие
1. Высококалорийные металлы: магний, алюминий, их сплавы; значительно реже используются цирконий, его сплавы и титан.
2. Металлы средней калорийности: цинк, железо, марганец, вольфрам, сурьма.
3. Неметаллы: фосфор, углерод (в виде сажи или древесного угля), сера, реже бор.
4. Неорганические соединения:
а) гидриды — бороводороды B10H14и их производные;
б) сульфиды—фосфора (Р4Sз), сурьмы (Sb2Sз) и др.;
в) прочие неорганические соединения — карбиды, силициды, фосфиды металлов.
Органические горючие
1. Индивидуальные углеводороды: бензол, толуол, нафталин и др.
2. Смеси углеводородов алифатического и карбоциклического
ряда - бензин, керосин, нефть, мазут, парафин и др.
3. Углеводы: крахмал, сахара (молочный, свекловичный),
древесные опилки.
4. Органические вещества других классов: стеарин, уротропин, дициандиам, тиомочевина и др.
ВЫСОКОКАЛОРИЙНЫЕ ГОРЮЧИЕ
металлы — литий, бериллий, магний, кальций, алюминии, титан и цирконий; неметаллы — водород, бор, углерод, кремнии и фосфор. К высококалорийным металлам следует отнести еще Nb, V, а также Sc и Y Эллерн приводит рецепты составов с ниобием и…ТЕХНИЧЕСКИЕ ТРЕБОВАНИЯ К ПОРОШКАМ МЕТАЛЛОВ
2. Содержание примесей железа и кремния не более десятых долей процента. 3. Содержание примесей тяжелых металлов (меди, свинца) только следы. 4. Содержание жиров не более десятых долей процента; иногда совершенно не допускается.ПРОИЗВОДСТВО ПОРОШКОВ МЕТАЛЛОВ
1) механическим измельчением; 2) распылением жидких металлов; 3) восстановлением оксидов;НЕОРГАНИЧЕСКИЕ ГОРЮЧИЕ СРЕДНЕЙ КАЛОРИЙНОСТИ
Теплота образования оксидов сравнительно малокалорийных элементов (считая по характеристикам Q1 и Q2) приведена в табл. 3.5. В качестве горючих в пиротехнике могут использоваться не только простые… Очевидно, теплота горения соединения будет тем больше, чем меньше теплота его образования из элементов. Таким образом,…ОРГАНИЧЕСКИЕ ГОРЮЧИЕ
Таблица 3.6 Свойства нефтепродуктов Температура, в С Нефтепродукт Плотность, г/см3 … Количество тепла при сгорании 1 г составляет для бензина 11,2 ккал (46,8 кДж),… Скипидар получается из смолы хвойных деревьев; главной составной частью его является пинен (С10H16). Скипидар…ГЛАВА IV
СВЯЗУЮЩИЕ - ОРГАНИЧЕСКИЕ ПОЛИМЕРЫ
РОЛЬ СВЯЗУЮЩИХ. ИСПЫТАНИЕ ПРОЧНОСТИ ЗВЕЗДОК
В некоторых случаях введение связующих имеет целью придать неооходимую прочность зерненым составам; при этом должна быть обеспечена необходимая… Одним из методов испытания прочности изделий является определение усилия,… Машина ИМ-4Р имеет механический привод и рычажно-ма-ятниковыи силоизмерительный механизм; она имеет .самопишущие…ФАКТОРЫ, ВЛИЯЮЩИЕ НА ПРОЧНОСТЬ
1) от .свойств основной смеси окислитель — горючее; 2) от свойств связующего и количества его в составе; 3) от степени измельчения компонентов;КЛАССИФИКАЦИЯ СВЯЗУЮЩИХ ИХ СВОЙСТВА
Чаще других используют связующие:
1) искусственные смолы — идитол, бакелит, эпоксидные смолы и др.;
2) смолы естественного происхождения и продукты их переработки: канифоль, резинаты;
3) высыхающие масла — олифу;
4) клей — декстрин.
Кроме того, возможно применение различных асфальтов и битумов. В некоторых случаях применяют растворы нитроклетчатки и каучука в соответствующих растворителях. Для нитроклетчатки растворителем может служить спирто-эфирная смесь, ацетон, для каучука бензол, бензин и др.
В твердом пиротехническом топливе в качестве связующих используются лолиуретаны, тиоколы, каучуки.
Характерными .свойствами смол являются:
1) нерастворимость в воде;
2) растворимость в органических растворителях;
3) способность к образованию пленки при высыхании раствора смолы;
4) полная сопротивляемость гниению (отличие от клеящих веществ животного происхождения).
Идитол — это «новолачная» смола, получаемая конденсацией избытка фенола с формальдегидом в присутствии кислого катализатора (например, НС1).
Реакция в начальной стадии протекает следующим образом:
СН20+2СбН50Н=СН2(С6Н40Н)2+Н20.
Продукт первичной конденсации, полимеризуясь, переходит при нагревании в смолу.
При расчетах для идитола употребляют условную формулу C13H12O2.
Теплота образования идитола (вычисленная на основании -теплоты горения технического образца) составляет 0,74 ккал/г (3,10 кДж/г), плотность — 1,25—1,30. Идитол хорошо растворяется в этиловом спирте.
Новолачные смолы хорошо растворимы в алкоголях, не растворимы в углеводородах и минеральных маслах. Они стойки по отношению к воде, кислотам, аммиаку и слабым растворам щелочей. Крепкий раствор щелочи разлагает их.
Технические образцы идитола всегда содержат свободный фенол, чем объясняется их красноватая окраска.
Для идитола нормируется температура его размягчения (для разных сортов не ниже 90—97° С), содержание в нем фенола (от 0,1 до 3,0%) и проводится испытание на отсутствие в нем канифоли.
Бакелит — смола, получаемая конденсацией фенола с избытком формальдегида в присутствии щелочного катализатора аммиака).
Реакция вначале протекает так:
CH2O + C6H5OH = С6Н4(ОН) CH2OH.
Далее, при нагревании образуется бакелит А:
2С6Н4(ОН)СН20Н = (С6Н4СН20Н)2O+Н20.
Его температура размягчения 75—100° С; он хорошо растворим в этиловом спирте. Нагревание бакелита А до более высокой температуры приводит к образованию бакелита В. При дальнейшем нагревании бакелита В при его полимеризации образуется бакелит С.
Последний — это неллавкое (но размягчающееся пр'и нагревании) вещество, не растворимое в большинстве органических растворителей.Он очень устойчив к химическим воздействиям ,и обладает большой механической прочностью.
Бакелит А образуется при температуре около 100° С. Переход его через форму В в форму С осуществляется уже при 120— 150° С или даже выше (до 180° С). В составы бакелит А вводится в виде порошка или в виде спиртового лака; переход его в форму С (бакелизация) осуществляется нагреванием спрессованного состава1 до 150° С; плотность бакелитов 1,20—1,29.
При расчетах для бакелита пользуются условной сформулой C12H11O2.
Применяется бакелит в качестве связующего в тех составах и изделиях, где требуется особая механическая прочность.
Канифоль получают из смол хвойных деревьев. Главной ее составной частью являются ненасыщенные циклические кислоты — абиетиновая (С20Н30O2) и пимаровая. Плотность канифоли 1,0—1,1; температура размягчения не ниже 65°С. Канифоль
* Имеются в виду термитно-зажигательные составы.
растворима в этиловом спирте, эфире, бензоле, частично в бензине; при нагревании растворяется в олифе.
Резинатами называют продукты взаимодействия канифоли с гидроксидами или солями соответствующих металлов. Резинат кальция получается сплавленном канифоли с гашеной известью при температуре 230—240° С. Однако эта реакция не протекает до конца; резинат кальция характеризуется определенным кислотным числом (не более 80), правда, значительно. меньшим, чем для канифоли (160—180). Температура пазмягче-ния резината кальция 120—150° С. Состав его приближенно может быть выражен формулой (C19H29COO)2Ca.
В качестве растворителей для резината кальция применяют бензин или спирто-бензиновую смесь (1 : 1).
Возможно также применение резината стронция, когда требуется красная окраска пламени.
Иногда в пиротехнических составах используют мономеры, которые после полимеризации становятся связующими: метилметакрилат, винилиденхлорид, стирол, акрилонитрил, ви-нилацетат. Значения теплоты полимеризации указанных выше веществ при расчете на .моль мономера лежат в пределах от 13 Д'о 21 ккал (от 54 до 88 кДж), что отвечает 130—325 малым ка-лория1М (540—1360 Дж) на грамм вещества.
Из органических связующих, не относящихся к классу смол, следует отметить еще олифу и декстрин.
Олифа натуральная (ГОСТ 7931-56) получается при полимеризации и частичной оксидации льняного или конопляного масла. Это - вязкая жидкость светло-желтого или светло-копичневого цвета, имеющая плотность 0,93—0,94. Получают олифу продуванием воздуха через нагретое до 1,60° С льняное (конопляное) масло. Для ускорения высыхания олифы в нее добавляют сиккативы или «сушители»: резинаты или линолеаты марганца, свинца или кобальта. В пиротехнике используют лучшие сорта олифы без сиккативов: иногда в качестве связующего применяют раствор канифоли в олифе.
Декстрин - растительный клей, получается при нагревании крахмала с разбавленными кислотами. Формула его (C6H10O5)n . Плотность 1,04. Декстрин легко растворяется в холодной и горячей воде.
В табл. 4.2 приведены некоторые свойства органических горючих (как связующих, так и веществ, не обладающих цементирующими свойствами).
Для упрощения расчетов в табл. 4.2 условные эмпирические формулы даны и для высокомолекулярных соединений; формулы эти имеют только рабочее значение.
Таблица 4.2
Некоторые свойства органических горючих веществ
Из неорганических связующих веществ в пиротехнике иногда применяют серу. При холодном прессовании введение ее в составы мало отражается на их… В составы целесообразно вводить не более 10—12% связующего (это не относится к… Следует помнить, что все органические связующие выполняют в составе одновременно и роль горючего, а следовательно,…ПРИНЦИПЫ РАСЧЕТА ПИРОТЕХНИЧЕСКИХ СОСТАВОВ
Тройные и многокомпонентные смеси рассматривались им как состоящие из двух или большего числа двойных смесей. Соотношение между двойными смесями,…ДВОЙНЫЕ СМЕСИ
KC104+4Mg=KCl+4MgO. (5.1) На 139 г перхлората калия приходится 24,3 Х 4=97,2 г (округленно 97 г) магния.… ......................139*100ТРОЙНЫЕ И МНОГОКОМПОНЕНТНЫЕ СМЕСИ
В числе продуктов горения такого состава могут быть ВаО, А120з, Ва(A102)2, BaS, Al2S3, SO2, N2 и др. Состав продуктов горения зависит не только от соотношения компонентов в… При ориентировочных расчетах для тройных составов, содержащих в себе окислитель, порошок металла и органическое…СОСТАВЫ С ОТРИЦАТЕЛЬНЫМ КИСЛОРОДНЫМ БАЛАНСОМ
Это происходит потому, что для многих видов составов (осветительных, зажигательных и др.) специальный эффект повышается с увеличением теплоты… Хороший специальный эффект от составов, содержащих в себе избыток горючего,… Типичным примером такого горючего является магний. Во многих случаях рационально построение на основе магния таких…МЕТАЛЛОХЛОРИДНЫЕ СОСТАВЫ
Окислителя в этом случае должно быть взято столько, чтобы содержащегося в нем хлора хватило бы на полное окисление металла. Исходя из этого уравнение реакции между гексахлорэтаном и цинком напишется… C2Cl6+3Zn=2C+3ZnCl2. (5. 10)СОСТАВЫ С ФТОРНЫМ БАЛАНСОМ
Роль окислителей выполняют соединения фтора (фториды малоактивных металлов или фторорганические соединения), роль горючих — порошки активных… Для упрощения расчетов может быть использована табл.5.2; в ней указывается, какое количество окислителя отдает при распаде 1 г фтора (L1) и количество металла, соединяющегося…ТЕПЛОТА ГОРЕНИЯ, ГАЗООБРАЗНЫЕ ПРОДУКТЫ И ТЕМПЕРАТУРА ГОРЕНИЯ СОСТАВОВ
Теплота горения пиросоставов может быть определена двумя путями:
1) вычислением;
2) экспериментально — сжиганием составов в калориметрической бомбе.
ВЫЧИСЛЕНИЕ ТЕПЛОТЫ ГОРЕНИЯ
Следовательно, если система один раз переходит из состояния 1 в состояние 3 непосредственно, а в другом случае — через ряд промежуточных состояний,… Иначе говоря: Ql,3=Ql,2+Q2,3,Q2,3 = Ql,3 + Ql,2
Q2,3 - теплота горения пиротехнического состава
Ql,3 -теплота образования продуктов горения
Ql,2 -теплота образования компонентов состава
Горение пиросоставов протекает обычно с небольшой скоростью и большей частью в открытом пространстве, т. е. при постоянном давлении. Так как в термохимических таблицах [l42] приводится теплота образования соединений при постоянном давлении, то и по приведенной выше формуле вычисляется Q2, 3 при постоянном давлении, т. е. Qp.
Этим расчет теплоты горения пиросоставов отличается от расчета теплоты взрыва ВВ, при котором вычисляют теплоту реакции при постоянном объеме Qv- Переход от Qp к Qv осуществляется по формуле
Qv=Qp + 0,57n ,
где п — число молей газов, образующихся при реакции.
Стандартные теплоты образования веществ из элементов (—H298).
Стандартная теплота образования окислителей, продуктов их разложения и продуктов окисления горючих приведена в гл. II и III.
В табл. 6.1 приведена стандартная теплота образования некоторых солей и органических веществ.
Таблица 6.1
Стандартная теплота образования (—H298) некоторых компонентов составов и продуктов их горения.
| Соединение | Теплота образования, ккал/моль | Соединение | Теплота образования. ккал/моль | Соединение | Теплота образования. ккал/моль |
| NaF | SrO3 | Крахмал | |||
| Na3AIF6 | Sr3N2 | 1/n (СбН10O5)n | |||
| Na2SiF6 | SrS04 | Молочный сахар | |||
| NaHCO3 | SrCl2 | Cl2H24Ol3 | |||
| Na2CO3 | ВаСОз | Этиловый спирт | |||
| Na2C2C4 | Ва2К2 | С2Н6О ж | |||
| NaNO3 | A1N | Идитол C13H12O2 | |||
| Na2S04 | Рb(NОз)2 | Тротил С7Н5N2О6 | |||
| КгСОз | FeCI3 | Гексоген | -21 | ||
| K2S04 | NH3 гaз | СзН6N6О6 | |||
| Cu(OH)2 | NH4C1 | Уротропин | -30 | ||
| СuСОз | HCl гaз | C6H12N4 | |||
| CuCNS | (-10) | CCl4 | Сероуглерод | —21 | |
| CuCl | C2Cl6 | Жидкий CS2 | |||
| CuCI2 | Метан CH4 | Пироксилин | +656 | ||
| MgCO3 | Бензол С6Н6 ж | —13 | (13% N) | ||
| Mg3N2 | Нафталин C10H8 | —16 | С24Н29(ОNO2)11O9в | ||
| SrCO3 | Антрацен C14H10 | -32 | Коллоидный хло | +639 | |
| SrC2O4 | (288) | пок | |||
| C24H3l(ON02)9O11 | |||||
| 1 Цифровой материал дан с точностью, необходимой для технических расчетов; | |||||
Пример 1. Вычислить теплоту горения смеси:
ЗВа(NОз)2+10А1=ЗВаО+ЗN2+5А1203. Теплота образования продуктов горения (в ккал):
5А12Оз ....... 400-5=2000
ЗВаО .......... 133.3=399
------------------------------
.....................2399
Теплота образования компонентов состава
ЗВа(NОз)2 ...... 237.3=711
Теплота реакции горения
(3=2399—711=1688. Сумма по весу Ва(�з)з и алюминия
ЛГ=261,4-3+27,0.10=1054. Теплота горения состава
q = 1688/1054 = 1,60 ккал/г (6,67 кДж/г).
Такой метод расчета достаточно точен, но не дает наглядного представления об энергетическом вкладе горючего и окислителя, взятых в отдельности, в общий тепловой баланс состава. Анализ этот можно провести, воспользовавшись несколько другими приемами расчета. Покажем это на примере смеси
Ba(NO3)2 68%,
Mg 32%.
Находим, что 0,32 г магния при горении выделяют 0,32-5,9=1,87 ккал. На разложение 261 г Ва(NОз)2 требуется 104 ккал, а на разложение 0,68 г Ва(NОз)2—0,27 ккал. В результате получаем теплоту горения смеси
q=1,87—0,27 =l,60 ккал/г (6,67 кДж/г).
В данном случае на разложение окислителя затрачивается 14% от того количества тепла, которое выделяется при горении магния. Используя тот же прием для вычисления теплоты горения термита (РезС>4 75%, А1 25%), находим <7= 1,82—0,86= =0,96 ккал/г (4,02 кДж/г). На разложение окислителя расходуется в данном случае 47% от теплоты, выделяющейся при горении алюминия.
В табл. 6.2 приведены расчетные данные теплоты горения некоторых составов.
Если не считать веществ, сгорание которых происходит за счет кислорода воздуха, то наибольшую теплоту горения имеют составы фотосмесей, затем следуют осветительные и трассирующие составы; меньшее количество тепла выделяют при горении безгазовые составы, составы сигнальных огней и, наконец, наименьшее количество тепла выделяется при горении дымовых составов. Рецепты зажигательных составов настолько многочисленны и разнообразны, что теплота, получаемая при их горении, изменяется в весьма широких пределах.
Таблица 6.2
Теплота горения пиротехнических составов (без учета догорания за счет кислорода воздуха)
| Рецепт состава. % | Теплота горения, к к ал/г | Назначение состава (тип состава) |
| КС104—83, Be—17 КС104—60, Mg—40 | 3,19 2,24 | На практике не применяется Фотосмесь |
| Ba(NOs)2-68, Mg—32 | 1,61 | |
| КС104—66, А1—34 NaNO3-60, Al—40 | 2,45 2,00 | Зажигательный Осветительный (без связующего) |
| Fe2O3—75, А1—25 Ba(N03)2—76, Mg—21, идитол-4 | 0,96 1,23 | Термит Осветительный |
| Ва(NОз)2—63 Al—27, сера—10 | 1,40 | » |
| Ba(N03)2—69, Mg—25, резинат кальция—6 | 1,48 | Трассирующий |
| NH4C104—90, смола—10 NH4C104—80, смола—20 | 1,26 1,01 | Ссмесевое ракетное топливо То же |
| Ва(С10з)2-Н20—88, идитол— 12 | 0,99 | Сигнальный, зеленого огня |
| КСlOз—57, CгСОз—25, шеллак—18 | 0,61 | Сигнальный, красного огня |
| C2C6-81, А1—119 С2С1б—17, КС104—22, Zn—61 | 0,96 0,52 | Дымовой маскирующий То же |
| КСlOз—35, молочный сахар— 25, краситель родамин—40 | 0,38 | Дымовой, красного дыма |
| КNОз—75, уголь—15, сера—10 Mg—90, Al—10 | 0,66 6,10 | Порох дымный Сплав «электрон» (горение засчет кислорода воздуха) |
| Примечание. 1 ккал-4,186 кДж. |
Составы с отрицательным кислородным балансом, если в процессе их горения участвует кислород воздуха, дают большее количество тепла, чем стехиометрические составы из тех же компонентов. Для составов с отрицательным кислородным балансом иногда используют термин — теплотворная способность. Под этим термином (в отличие от термина «калорийность состава») понимают то максимальное количество тепла, которое может быть получено лри сгорании состава с участием кислорода воздуха.
ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ
Объем калориметрической бомбы составляет обычно 300— 400 см3, вес воды в калориметре — около 3 кг (вода взвешивается с точностью до 1 г). Калориметрическая бомба в большинстве случаев заполняется воздухом, реже —… Для составов с отрицательным кислородным балансом при сжигании их с участием воздуха стремятся обеспечить максимальное…СВЯЗЬ МЕЖДУ НАЗНАЧЕНИЕМ СОСТАВОВ И ТЕПЛОТОЙ ИХ ГОРЕНИЯ
Фотосмеси . ........................................................... 1,7—3,0 Осветительные и трассирующие составы . .......... 1,5—2,0 Смесевые пороха (ориентировочные данные) ..... 1,0—1,5ГАЗООБРАЗНЫЕ ПРОДУКТЫ ГОРЕНИЯ
В составах осветительных, трассирующих и сигнальных огней и в фотосмесях образование газов при горении необходимо для того, чтобы при горении… В дымовых составах наличие газов необходимо для выталкивания из сферы реакции… При горении зажигательных составов образование газов также желательно, так как это значительно расширяет создаваемый…ОПРЕДЕЛЕНИЕ ТЕМПЕРАТУРЫ ГОРЕНИЯ
Температуру горения можно определить: 1) вычислением по формуле (6.6) (см. ниже). При этом используется… 2) .непосредственным намерением пр,и помощи оптических пирометров ил'и термопар (см. § 6 этой главы).Tк
Очевидно, теплота испарения (кипения) соединений значительно больше теплоты их плавления.
Максимальную температуру горения вычисляют по формуле
t = Q - E (Qs + Qk) / E Cp
где Q—теплота горения;
E Ср — сумма теплоемкостей продуктов горения;
E(Qs+Qk.)—сумма скрытых теплот плавления и кипения
продуктов горения.
Пример 3. Вычислить максимальную температуру пламени состава красного огня, содержащего 65% КСlOз, 20% SrСОз и 15 % C13H12O2 (идитола).
Реакция горения приближенно может быть выражена уравнением
7,1 КС10з+ l,8SrC03+C13H1202=7,l KC1 +1,85гСОз+ +6Н20 пар+4,ЗС02+8,7СО.
Расчет теплоты горения ведется в ккал (1 ккал =4,11186 кДж) с использованием закона Гесса
Ниже приводится теплота образования начальных и конечных продуктов реакции; теплота образования идитола принята равной 0,74 ккал/г.
Для Н20 пар. .... 6.57,4=344
Для СО2 ...... 4,3.94=404
ДляСО2 ...... 8,7-26=22б
Для КСl . . . . 7,1.106=752
--------------------------------------
.................................1726 ккал
Для C13H1202 . . . 0,74.200=148
Для КСlOз ..... 7,1.96=682
-----------------------------
.................................803 ккал
Количество тепла, выделяющееся при горении, равно 1726—830=896 ккал.
Теплоемкость Ср газов и водяного пара в интервале О—1500° С (см. табл. 6.7) равна:
для Н2О. ....... 6.9,5=57,0
для С02. . . . . . . . 4,3.11,9=51,2
для СО . . . . . . . . 8,7.7,5=65,2
-------------------------------------------
173,4
Теплоемкость KC1 и SrСОз принимаем равной соответственно 12,8 и 32,0 кал/град моль и суммируем Отсюда
12,8*7,1=90,9
32,0 1,8=57,6
------------------------
148,5
и окончательно
E Ср= 173,44-148,5=321,9 кал/град,
откуда
t=567*1000 / 321,9 = 1760 C
Если бы мы приняли во внимание частично протекающую в пламени термическую диссоциацию: SrCO3=SrO+CO2, то при расчете получили бы значение температуры порядка 1600° С.
Аналогичным методом был проведен расчет [23] для стехиомегрической смеси (WОз+2А1) и сделан вывод, что температура горения не должна превышать температуру кипения Аl2Оз, т. е. должна быть равной примерно 3000° С.
Необходимо еще раз отметить, что если температура горения превышает 2000—2500° С, то данные, полученные расчетным путем, являются лишь ориентировочными, а потому могут быть полезными только при сравнении между собой составов, резко обличающихся по своему рецепту.
Для ракетных топлив требуется высокая точность расчета температуры горения и других характеристик процессов горения. В этом случае для вычисления температуры горения выполняются весьма трудоемкие расчеты, при которых учитываются процессы термической диссоциации и испарения продуктов грения. Исходные данные для таких расчетов имеются в справочнике [86].
ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ
Измерение температуры пламени таких составов проводится чаще всего при помощи оптических методов. Основанием для применения их служит предпосылка, что излучение пламени следует… В этом случае излучение должно подчиняться:Tипы оптических пирометров
К и н о ф о т спирометр — это обычный киноаппарат, снабженный красным светофильтром (А=0,б65 мкм) и набором ленточных ламп, устанавливаемых рядом с… В основу этого метода измерения температуры положен принцип фотографирования…СВЯЗЬ МЕЖДУ НАЗНАЧЕНИЕМ СОСТАВА И ТЕМПЕРАТУРОЙ ГОРЕНИЯ
На основании имеющегося экспериментального материала можно заключить, что существует определенная .связь между назначением составов и максимальной температурой их горения (в°С):
фотоосветительные ..... 2500—3600
осветительные и трассирующие . . 2000—2500
зажигательные (содержащие окислитель) . ....... 2000—3500
составы ночных сигнальных огней . 1200—2000
дымовые .............. 400-1200
ГЛАВА VII
ЧУВСТВИТЕЛЬНОСТЬ СОСТАВОВ
Чем это количество энергии будет меньше, тем чувствительнее к внешним воздействиям будет состав. Возбудить быструю реакцию ,в пиротехническом составе можно, применяя различные… Для получения нормального эффекта при действии пиротехнических составов в большинстве случаев пользуются тепловым…ОПРЕДЕЛЕНИЕ ЧУВСТВИТЕЛЬНОСТИ К ТЕПЛОВЫМ ВОЗДЕЙСТВИЯМ
Температурой самовоспламенения называется та наименьшая температура, до которой должен быть нагрет состав, для того чтобы произошло его… Температура самовоспламенения для одного и того же состава не является вполне… Ряд испытаний, проводимых при различных температурах, каждый раз с новыми навесками состава, дает возможность…Таблица 7.2
Температура самовоспламенения пиротехнических смесей [117; 96]
| Смесь | Соотношение компонентов в вес. % | »С |
| Zr- Fe2O3- Si02 | 65-25-10 25—75 ----- 50—20—30 12—88 20—80 20—80 ----- 15—10—75 14—86 32—68 18-82 W—27—63 Zr/Ni 26—54 Мп 33—44 10—90 5—95 или 30% Zr; | |
| B—KNO3 | ||
| Mg -(C2F4)n | ||
| Si -Pb02- CuO | ||
| Mg—BaO2 | ||
| Mg -PbO2 | ||
| Mg - PbCr04 | ||
| Дымный порох | ||
| Идитол - Mg- КNНОз | ||
| Идитол - NaNO3 | ||
| Mg-Ba(N03)2 | ||
| Se—BaO2 | ||
| W- BaCr04- КС1СO4 | ||
| Zr/Ni-BaCr04-КС104 | ||
| Мп— BaCr04— PbCr04 | ||
| В—BaCr04 .............. . . | ||
| В—BaCr04 ................ | ||
| Примечание. Zr/Ni-сплавы содержат 70, 50 или 30% Zr, онипассивируются раствором Na2Cr2O7. |
Определение чувствительности к лучу огня
Чувствительность к лучу огня характеризует возможность воспламенения составов при случайном попадании на них искры. Иногда при этом испытании используется бикфордов шнур, нижний срез которого касается поверхности пиросостава;
результат испытания фиксируют следующим образом: «+» — воспламенение или «—» — отказ.
Дополнительные испытания
В последние годы разработана методика испытания пиросостaвoв на чувствительность их к воздействию лучистой энергии. Источником излучения может… В некоторых случаях проводят дополнительное исследование поведения составов…ОПРЕДЕЛЕНИЕ ЧУВСТВИТЕЛЬНОСТИ К МЕХАНИЧЕСКИМ ВОЗДЕЙСТВИЯМ
В артиллерийских снарядах в момент выстрела возникают значительные инерционные напряжения. Они могут повлечь за собой сдвиг пиротехяических зарядов,… В связи с этим изучение чувствительности составов к механическим воздействиям… Следует отметить, что, как правило, составы, более чувствительные к трению, обладают и большей чувствительностью к…Определение чувствительности к удару
Особо чувствительны к удару смеси КСlOз с роданистым калиeм (KCNS) и реальгаром (As2S2); для этих смесей работа удара равна соответственно 0,5 и 0,6… Ряд работ по выяснению механизма возникновения взрыва при ударе и уточнению… В известной мере выводы, сделанные в этих работах, могут быть перенесены и на пиротехнические составы.ФАКТОРЫ, ВЛИЯЮЩИЕ НА ЧУВСТВИТЕЛЬНОСТЬ СОСТАВОВ К НАЧАЛЬНОМУ ИМПУЛЬСУ
Влияние энергетики сказывается в способности реакции, начавшейся в малом объеме, к саморазвитию за счет выделяющейся энерпии. Чем эта склонность к… Внутреннее сопротивление системы определяется тем количеством энергии, которое… Абстрагируясь временно от влияния внешних физических факторов, можно сказать, что чувствительность химической системы…ГЛАВА VIII
ГОРЕНИЕ СОСТАВОВ
МЕХАНИЗМ ГОРЕНИЯ
инициирование (зажжение) воспламенение горение.ФАКТОРЫ, ВЛИЯЮЩИЕ НА СКОРОСТЬ ГОРЕНИЯ
Существует два способа для количественной характеристики скорости горения: линейной скорости и в мм/с и массовой скорости ит, выражаемой в… Как было уже указано, горение протекает равномерно лишь при достаточном… K=d/dmaxТаблица 8.2 Скорость горения стехиометрических двойных смесей в мм/с
| Горючее | Окислитель | |||
| КСlO3 | KNO3 | NaNO3 | Ва (N03)2 | |
| Сера ...... | 2,5 | Не горит | Не горит 0,5 | ---- 0,3 0,1 |
| Древесный уголь Сахар ..... | ||||
Примечание. К •=0,5 16 мм/0,6; смеси cжиuгались в картонных трубках диаметром 16 mm
Введение олифы или канифоли в многокомпонентные составы сильно замедляет процесс их горения.
Как видно из табл. 8.2, смеои хлората с серой горят довольно энергично; смеси же нитратов натрия или калия с серой зажигаются с большим трудом и горение их малоустойчиво. Это объясняется тем, что количество тепла, выделяющееся при горении серы, недостаточно для того, чтобы вызвать разложение нитрата и 0'беспечить прогревание соседних слоев состава.
Легче зажечь составы, содержащие избыток серы и малый процент нитрата натрия (17%); большая часть серы при этом сгорает за счет кислорода воздуха; такие составы нашли применение в народном хозяйстве (см. гл. XXI).
Каталитические добавки
Имеются работы по осуществлению горения при атмосферном давлении NH4C104 и NH4NO3 с каталитическими добавками: для первого оказались наиболее… Присадка к алюминию небольшого количества кобальта (~1%) вызывает, по… В пиротехнике для двойных смесей используются термины:Физические факторы
Большую роль в процессе горения играет газопроницаемость составов; определение газопроницаемости надлежало бы проводить и в условиях повышенной… Для составов, не содержащих в себе металлического горючего и имеющих более… Следует заметить, что существуют и такие малогазовые составы, увеличение плотности которых способствует передаче тепла…ГЛАВА IX
ВЗРЫВЧАТЫЕ СВОЙСТВА СОСТАВОВ
Изготовление составов, имеющих высокую чувствительность к удару и трению и вместе с тем обладающих значительной скоростью и силой взрыва, весьма… Способ изготовления изделий во многом определяется взрывчатыми свойствами… Кроме того, необходимо иметь ясное представление об условиях, при которых начавшийся процесс горения пиросоставов…Окислитель+алюминиевая пудра
Несколько легче возникает процесс взрывчатого разложения в нитратных осветительных составах, содержащих магний, но скорость взрывчатого разложения… Взрывчатое разложение неуплотнеяных двойных смесей нитратов с магнием или… Вследствие этого подобные смеси следует считать весьма опасными и обращаться с ними надо с большой осторожностьюРасширение в блоке Трауцля в см3 в зависимости от начального импульса; количество состава 20 г
Отдельные компоненты. Следует отметить, что в некоторых случаях опасность взрыва не исключена и при обращении с отдельными компонентами. Так, например, взрыв может последовать при наличии в воздухе больших… В монографии (61] для различных ортов порошков алюминия, магния и сплава Al—Mg приводятся следующие значения нижнего…ГЛАВА X
ФИЗИЧЕСКАЯ И ХИМИЧЕСКАЯ СТОЙКОСТЬ СОСТАВОВ
В результате исследований устанавливаются необходимые условия и допустимые сроки хранения отдельных видов пиротехнических изделий.ФИЗИЧЕСКИЕ ИЗМЕНЕНИЯ
Реже причиной деформации заряда (факела или звездки) являются механические воздействия или изменения температуры окружающей среды. Особо следует отметить изменения в составе, обусловливаемые возгонкой его… Гигроскопичность состава зависит в основном от гигроскопичности его компонентов, а также от плотности л состояния…ХИМИЧЕСКИЕ ИЗМЕНЕНИЯ
Они могут быть весьма разнообразными, что является следствием чрезвычайно большого ассортимента употребляемых для их производства компонентов. Но все же можно установить некоторые общие положения (.см. ниже).
Составы, содержащие порошки магния или алюминия и неорганические окислители
Mg+2H20=Mg(OH)2+'H2; А1+ЗН20=А1(ОН)з+1,5Н2. Рис. 10.1. Повышение температуры порошков магния (1) и алюминия (2) при добавлении к ним водыСоставы, не содержащие порошков металлов
Обменные реакции Примерами такой нежелательной комбинации солей могут служить составы желтого огня, в которые входят смеси нитрата бария с… Ва(NOз)2+Nа2СОз — ВаСОз+2NаNОз Образование гигроскопичной соли NаNОз обусловливает дальнейшее увлажнение состава и в образующемся растворе реакция…МЕТОДЫ ОПРЕДЕЛЕНИЯ ГИГРОСКОПИЧНОСТИ И ХИМИЧЕСКОЙ СТОЙКОСТИ
Дальнейшие испытания являются значительно более трудоемким, но дают уже количественную оценку стойкости пиросоставов. При обычных условиях хранения изделий, т. е. при влажности воздуха не более… Заметные химические изменения при хранении стойких составов в таких условиях происходят только по прошествии ряда лет.…ДОПУСТИМЫЕ СРОКИ ХРАНЕНИЯ
Для пиротехнических изделий устанавливаются максимально допустимые сроки хранения. Эти сроки, в зависимости от рецепта состава и степени… Нормальным сроком хранения изделий считается 10 лет и более. К наиболее стойким следует отнести составы сигнальных огней, не содержащие порошка металла. Из осветительных, а также…СПЕЦИАЛЬНЫЕ СВОЙСТВА ОТДЕЛЬНЫХ ВИДОВ ПИРОТЕХНИЧЕСКИХ СОСТАВОВ
ГЛАВА XI
ОСВЕТИТЕЛЬНЫЕ СОСТАВЫ
ОСВЕТИТЕЛЬНЫЕ СОСТАВЫ И СРЕДСТВА
Операции в ночных условиях широко практиковались всеми воюющими державами во второй мировой войне. Военно-воздушные силы США в агрессивной войне во… Для обеспечения боевых действий ночью используются средства сигнализации и… Основными средствами освещения поля боя являются прожекторы, осветительные артиллерийские снаряды и авиабомбы (САБ), а…Классификация осветительных средств и составов
В армиях капиталистических стран осветительные средства подразделяют следующим образом.
1. Средства артиллерия — снаряды (ОС) и мины (ОМ), реактивные осветительные снаряды (РОС);
2. Средства авиации — авиабомбы (САБ), посадочные осветительные авиабомбы и факелы.
3. Общевойсковые средства — осветительные патроны (ОП), выстреливаемые из пистолета-ракетницы (26 мм и др.), и реактивные; осветительные бомбы (бураки), выстреливаемые из специальной мортиры, и осветительные гранаты, выстреливаемые из винтовочной мортирки или специального гранатомета.
4. Инженерные осветительные мины.
В зависимости от конструкции эти средства бывают парашютные и беспарашютные. В беспарашютных средствах время свечения ограничивается временем свободного падения звездки или факела и обычно не превышает 20—25 с.
Осветительные элементы, снабженные парашютом, снижаются значительно медленнее, и потому их время горения может быть во много раз больше.
Осветительные составы делятся на быстро и медленногорящие. Первые, имеющие скорость горения 10 мм/с и больше, применяют обычно в относительно мелких изделиях (звездки для пистолетных патронов и винтовочных гранат). Эти составы имеют большую силу света с единицы горящей поверхности, чем мед-ленногорящие составы.
Для крупных изделий (факелы авиабомб, снарядов и мин), где время горения исчисляется минутами, пользуются обычно медленногорящими составами, имеющими скорость горения 1— 2 мм/с.
Осветительные составы могут быть также подразделены на твердые и пластичные или гелеобразные.
Практическое применение получили пока только твердые осветительные составы, получаемые либо прессованием порошкообразной смеси компонентов, либо самоотверждающиеся (при нормальной или повышенной температуре).
КРАТКИЕ СВЕДЕНИЯ ОБ УСТРОЙСТВЕ ОСВЕТИТЕЛЬНЫХ СРЕДСТВ
Средства артиллерии
Время горения элементов в зависимое от калибра снаряда (76—122 мм) составляет 15—25 с, сила света одного элемента 20—40 тыс. . Преимуществами… Основным недостатком беспарашютных снарядов является большая скорость падения… Большое распространение получили парашютные осветительные снаряды (ПОС) с выбрасыванием осветительного факела с…Средства авиации
Осветительные (светящиеся) авиабомбы (САБ) занимают важное место среди большого числа пиротехнических средств, используемых в авиации. Кроме целей освещения местности, они используются
Таблица 11.1 Светотехнические характеристики американских парашютных снарядов и мин
| Ско | Ско | ||||||
| Калибр снаряда или мины | Сила света тыс. ев | Время горе | рость снижения фа | Калибр снаряда или мины | Сила света, тыс. ев | Время горения | рость снижения |
| (кд) | ния, с | кела, | (кд) | с | факела, | ||
| м/с | м/с | ||||||
| 105-мм снаряд | -- | 60-мм мина | -- | ||||
| 155-мм снаряд | 1,5 | 81-мм мина | 3,7 | ||||
| 60-мм мина | 106,7-мм мина | -- |
также и для ослепления противовоздушной обороны противника;
САБы применяются и в качестве мишени при учебных стрельбах зенитной артиллерии.
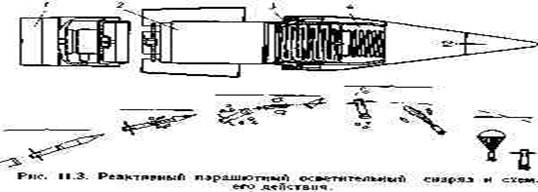
1-реактивный двигатель; 2—факел; 3—парашют; 4— пружина для выталкивания системы факел — парашют из корпуса снаряда
САБы могут быть сброшены с самолетов с замков бомбодержателей или из специальных кассет.
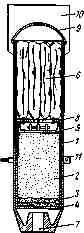
Рис. 11.4. Осветительная авиабомба САБ-.ЗМ [il7]:
/—стальной корпус; 2—осветительный состав; 3—восплайенятельный состав; 4—картонный кружок с замедлителем; 5—донная крышка факела; 6—парашют; 7—очко под дистанционный взрыватель; 8—войлочный обтюратор; 9— донная крышка; 70—стабилизатор; //—бугель
На рис. 11.4 показана схема САБ. Факел — это картонная или стальная цилиндрическая оболочка, в которую запрессованы основной и воспламенительный составы. После сбрасывания бомбы с самолета на заданной высоте срабатывает дистанционный взрыватель, который воспламеняет пороховую подмазку на торце факела и вышибной пороховой заряд. Образовавшиеся газы выталкивают через донную часть корпуса факел с парашютом и одновременно воспламеняют факел.
В некоторых конструкциях система факел—парашют извлекается из корпуса бомбы при помощи вытяжного троса, прикрепляемого одним концом к крышке факела САБ и к парашюту, а другим — к балке бомбодержателя. В других конструкциях воспламенение факела осуществляется при помощи терочного воспламенителя, срабатывающего в момент раскрытия парашюта.
В табл. 11.2 приведены некоторые данные американских осветительных авиабомб.
Таблица 11.2
Основные характеристики американских САБ (скорость снижения факелов 2,5—3,0 м/с)
| Индекс | Количество состава, кг | Размеры, мм | Сила света млн. ев (кд) | Время горения в минут. | ||
| длина | диаметр | |||||
| МК-6 | 13,6 10,4 8 ,2 -- 28,1 31,8 | >1,65 0,5 1,5 3,0 5,0 | б | |||
| МК-24 | ||||||
| МК-8 | ||||||
| М-138 | ||||||
| М-139 | ||||||
| МШ-44 | ||||||
Расход осветительных средств B современной войне огромен (в один из месяцев войны во Вьетнаме ВВС США израсходовали до 130 тыс. САБ). В связи с необходимостью непрерывно поддерживать освещение в течение довольно длительного временя в США разработаны автоматические кассеты, вмещающие до 400 осветительных бомб и выбрасывающие их с интервалом от 2 до 5 с.
В зарубежных армиях при учебных стрельбах ракетами «воздух — воздух» и «земля — воздух» с ИК-головками самонаведения используют буксируемые светящиеся мишени. Одна из таких мишеней [119] представляет собой факел весом 3,2 кг, диаметром 66 мм и длиной 470 мм, буксируемый самолетом на длинном тросе. Факел воспламеняется терочным устройством и горит 6 мин, имея силу света 65 тыс. см (кд).
Общевойсковые средства
На рис. 11.5 показано устройство 26-мм беспарашютного патрона. При ударе бойка воспламеняется капсюль, поджигающий вышибной заряд дымного пороха;… На рис. 11.6 показан парашютный патрон, отличающийся тем, что из пистолета…СВЕТОВЫЕ ХАРАКТЕРИСТИКИ ОСВЕТИТЕЛЬНЫХ СОСТАВОВ И СРЕДСТВ
2. Единицей светового потока является люмен (лм) — поток, излучаемый источником света силой в 1 св внутри телесного угла в 1 стерадиан. Источник, обладающий в любом направлении силой света в 1 св, излучает световой… 3. Единицей освещенности авляется люкс (лк) — освещенность, создаваемая световым потоком в 1 л,м, равномерно…ТЕПЛОВОЕ И ЛЮМИНЕСЦЕНТНОЕ ИЗЛУЧЕНИЕ
* Это вычисление является приближенным, так как пламя не имеет правильной геометрической формы и размеры его во время горения изменяются. личивается — появляется заметное на глаз световое излучение, т. е. тела… Наличие в пламени осветительного состава накаленных твердых и жидких частичек, безусловно, необходимо, так как горячие…СПЕЦИАЛЬНЫЕ ТРЕБОВАНИЯ К ОСВЕТИТЕЛНЫМ СОСТАВАМ; ДВОЙНЫЕ СМЕСИ
Достаточное количество лучистой энергии получается только при сгорании пламенных составов, выделяющих не менее 1,5 ккал/г (6,3 кДж/г). Эта цифра… Числовое значение светового к.п.д. определяется многими факторами:… Для получения наибольших значений светового к.п.д. следует путем подбора рецепта состава и конструкции изделия…Термохимические характеристики двойных смесей
Применение калиевых солей нежелательно ввиду невысоких световых показателей таких составов (см. табл. 11.7). Таблица 11.7Светотехнические характеристики двойных смесей нитрата бария с алюминиевой пудрой
МНОГОКОМПОНЕНТНЫЕ ОСВЕТИТЕЛЬНЫЕ СОСТАВЫ
Многокомпонентные составы обычно имеют меньшую скорость горения, чем соответствующие двойные смеси, но вместе с тем и меньшую силу света. Удельная светосумма составов с магниевым порошком снижается от введения… Составы с алюминием при употреблении грубо измельченного алюминия или при введении в них большого количества…Рецепты многокомпонентных осветительных составов в ч/о
В качестве добавочного окислителя в осветительных составах наряду с нитратами… Так, в норвежском патенте 99.194 (1961 г.) указывается следующий рецепт (в %):Самоотвёрждающиеся составы
Такие составы возникли в связи с созданием самоотверждаю-щихся ракетных смесевых твердых топлив. Составы такого типа изготовляются путем тщательного смешения порошкообразных… В качестве связующих предложены жидкие смеси эпоксидных и полигли-колевых смол, силиконовые смолы; сополимер…ФАКТОРЫ, ВЛИЯЮЩИЕ НА ЭФФЕКТИВНОСТЬ ОСВЕТИТЕЛЬНЫХ СОСТАВОВ И СРЕДСТВ
Светотехнические показатели изделия определяются прежде всего рецептом состава, измельчением его компонентов, степенью уплотнения состава. Известное… Наряду с этим большое значение имеют и условия, при которых происходит горение… Изменение силы света двойных смесей магниевого порошка с различными окислителями при увеличении содержания магния…Таблица 11.12 Влияние удельного давления прессования на характеристики состава на основе
(NaNO3+Mg)
| Удельное давление прессования, МН/м2 (кгс/см2) | Сида света, тыс. ев (кд) | Полная светосумма млн. св. с | Скорость горения | Удельная светосумма тыс. св. с/г | Плотность, г/см« | |
| линейная, мм/с | массовая, г/с | |||||
| 14 (140) | 7,2 | 2,60 | 6,54 | 42,6 | 1,54 | |
| 48 (490) | 7,1 | 2,35 | 6,75 | 38,7 | 1,74 | |
| 103 (1050) | 7,4 | 2,35 | 7,69 | 37,2 | 2,03 | |
| 148 (1400) | 7,6 | 2,38 | 7,55 | 38,6 | 1,95 |
от конструкции изделия и применяемого состава. Для многих горящих с одного торца осветительных факелов скорость горения
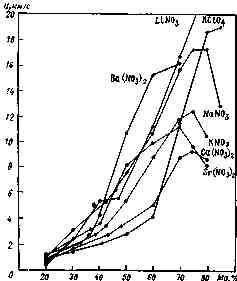
Рис. 11.10. Изменение скорости горения двойных смесей магния с различными окислителями, запрессованных под давлением 730 кгс/см2 (72 МН/м2), при изменении содержания магния
мало зависит от диаметра. Это было отмечено многократно, правда, в ограниченном интервале изменения диаметров. Сила света, конечно, увеличивается с увеличением диаметра, но в различной степени для различных составов и изделий. Материал оболочки факела также влияет на скорость горения и светоотдачу факелов. Стальные оболочки, имеющие большую теплопроводность по сравнению с картонными или пластмассовыми, способствуют более быстрому прогреву прилегающих слоев состава, что может привести к увеличению скорости горения.

Рис. 11.11. Зависимость линейной скорости горения состава (Mg+NaNO3 + поливинилхлорид+смола) от размера частиц магния
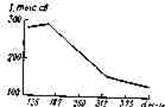
Рис. 11. 12. Зависимость силы света состава (Mg+NaN03+ 4-поливнилхлорид+смола) от размера частиц магния
При понижении давления окружающей среды скорость горения уменьшается и сила света факелов падает. Размеры пламени увеличиваются, но яркость его сильно уменьшается. При некотором достаточно малом давлении среды горение уже невозможно и факел затухает. Все эти эффекты B большей степени проявляются при горении составов, содержащих большой избыток металла. В этом случае решающую роль играет уменьшение содержания кислорода в разреженном воздухе. Для стехиометрических составов имеет значение главным образом понижение давления внешней среды.
При понижении начальной температуры изделия скорость горения и сила света составов уменьшаются.
В артиллерийских осветительных снарядах, которые не снабжены специальными устройствами для торможения вращения факела, горящий состав испытывает значительные центробежные ускорения, так как факел на воздухе некоторое время продолжает вращаться с большой угловой скоростью. Вращение приводит к значительному сокращению времени горения. В результате центрифугирования шлаки прижимаются в оболочке факела и не выносятся наружу. Это затрудняет отток газообразных продуктов и приводит к повышению давления внутри факела; в результате состав начинает гореть быстрее. Чем с большей скоростью вращается факел, тем интенсивнее протекает образование шлаков и тем больше ускоряется горение.
Все сказанное выше справедливо для факелов со стальной оболочкой, которая остается целой до конца горения. Если же оболочка сгорает одновременно с запрессовкой состава, то вращение может привести к сбрасыванию шлаков с поверхности горения состава и к его затуханию.
Так как форма пламени факелов и эвездок существенно отличается от сферической, пространственное светораспределение для н.их крайне неравномерно. В плоскости, проходящей через ось факела, сила света имеет наибольшие значения в направлении под углом 45—90° к оси пламени. В направлениях под углами О—45° она уменьшается до какой-то минимальной величины, наблюдаемой по оси пламени. Еще меньше сила света в направлениях 90—180° к оси пламени (см. рис. 11.13). В плоскости, перпендикулярной оси факела, кривая светораспределения представляет собой окружность вследствие симметричности объекта.
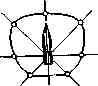
Рис. 11.13. Кривая светораспределения пламени осветительной звездочки в плоскости, проходящей через ось изделия
Отмеченная неравномерность оветораспределения учитывается в некоторых конструкциях осветительных изделий, в которых горящие факелы располагают горизонтально. При этом достигается наиболее высокая и равномерная освещенность местности.
КРАТКИЕ СВЕДЕНИЯ О ПИРОТЕХНИЧЕСКИХ ИК-ИЗЛУЧАТЕЛЯХ
Пиротехнические ИК-излучатели так же, как и осветительные средства, должны обеспечивать определенную интенсивность излучения в течение заданного… На рис. 11.14 представлена типичная конструкция пиротехнического ИК-излучателя… На рис. 11.15 представлен пиротехнический ИК-излучатель, моделирующий абсолютно черное тело. В нем для нагревания…Характеристики пиротехнических ИК-излучателей
Видимый человеческим глазом свет занимает лишь часть всего диапазона электромагнитных колебаний, как это показано на рис. 11.16. Инфракрасные лучи…Энергетические характеристики пиротехнических источников ИК-излучения
Если лучистая энергия видимого излучения обычно измеряется в описанных выше светотехнических единицах, то инфракрасное излучение, которое невидимо и интенсивность зрительного восприятия которого равна нулю, оценивается в энергетических единицах.
В табл. 1.1.14 приведены основные энергетические характеристики ИК-излучения.
Таблица 11.14
Энергетические величины и единицы
ФОТОМЕТРИРОВАНИЕ И РАДИОМЕТРИРОВАНИЕ ПЛАМЕН ПИРОТЕХНИЧЕСКИХ СОСТАВОВ
По освещенности или облученности рассчитывают силу света (излучения), пользуясь уравнением I=ER2 Рис. 11.18. Кривые спектральной чувствительности фотоэлементов:ГЛАВА XII
ФОТООСВЕТИТЕЛЬНЫЕ СОСТАВЫ
Основное назначение фотосоставов — использование в фото-авиабомбах и фотопатронах, которые применяются в качестве искусственных источников света при… Кроме этого, фотосоставы широко используются в тех случаях, когда требуется…НОЧНОЕ ВОЗДУШНОЕ ФОТОГРАФИРОВАНИЕ
Современные самолеты-разведчики летают на больших (до 30 км) или малых (менее 0,5 км) высотах co скоростью до 3 М, радиус действия их достигает 4000… Стратегический разведчик за 1 ч полета со скоростью, соответствующей М=2,5, на… В процессе воздушной разведки осуществляется автоматическое управление экспозицией, работой осветительных систем и…ФОТОМАТЕРИАЛЫ
Рис. 1.З. Характеристики аэрофотопленки панхром 10Н-10ОО (проявитель № I по ГОСТ):ФОТОАВИАБОМБЫ
Рис. 12.5. Схема взаимного расположения НАФА, вспышки фотобомбы и… и—угол отставания ФОТАБ; а—половина угла зрения объектива НАФА; h—высота взрыва ФОТАБ; Н—высота полета самолетаФОТО ПАТРОНЫ
Фотопатрон (рис. 12.9) содержит заряд фотосмеси и замедлительно-вос-пламенительные устройства (ЗВУ), помещенные в алюминиевую оболочку; Рис. 12.9. Устройство типичного фотопатрона:Основные характеристики фотоосветительных патронов
Рис. 12. 10. Схема съемки маршрута с использованием фотопатронов: /, 2, 3— снимаемые последовательно участки местности; 4— правление полета; С,—интервал между вспышками (или интервал…ФОТОСОСТАВЫ. ФАКТОРЫ, ВЛИЯЮЩИЕ НА СВЕТОТЕХНИЧЕСКИЕ ХАРАКТЕРИСТИКИ ВСПЫШЕК И СВОЙСТВА ФОТОСОСТАВОВ
Фотосмеси для получения большой силы света должны иметь высокую калорийность — более 2 ккал/г (8,4 кДж/г). Исходя из этого в качестве горючих в… В некоторых случаях к двойной смеси окислителя и горючего для получения… В табл. 12.3 приведены типичные составы фотосмесей, применяемых в ФОТАБ и фотопатронах, а также в зарядах-маркерах и…МЕТОДЫ ОПРЕДЕЛЕНИЯ ХАРАКТЕРИСТИК ФОТОВСПЫШЕК
Иногда при сопоставлении различных фотосмесей вычисляют также аветосумму L. Eдельную светосумму вспышки Lo=L/m, пде т—вес сжигаемого состава, а также Lэф,… Для полной качественной характеристики излучения необходимо наличие кривой спектрального распределения энергии, данных…СВЕТОВЫЕ ИМИТАТОРЫ, ФОТОЗАРЯДЫ-МАРКЕРЫ
В послевоенное время, в связи с разработкой ракетных снарядов среднего и большого радиуса действия, возникла необходимость точной записи траекторий… В дальнейшем были разработаны устройства, которые выдают серию вспышек с… Заряды-вспышки, называемые иногда световыми имитаторами или маркерами, применяются также для получения светового…ГЛАВА XIII
ТРАССИРУЮЩИЕ СОСТАВЫ
ТРАССИРУЮЩИЕ СРЕДСТВА
Поэтому еще в начале первой мировой войны были разработаны и применялись трассирующие боеприпасы. Особенно широкое применение они нашли во вторую… В послевоенный период трассеры стали применять также и в некоторых управляемых…Назначение трассеров и требования к ним
Трассер — это шашка из пиротехнического состава; состав запрессовывается непосредственно в корпус снаряда или в отдельную металлическую оболочку. … Трассирующие средства предназначаются для стрельбы по быстро движущимся целям.… Трассеры используются также для наведения на цель реактивных противотанковых снарядов (ПТУРС), ракет «воздух —…Классификация трассирующих средств
Различают трассеры к артиллерийским снарядам, к реактивным снарядам, к авиабомбам, к винтовочным пулям и к ружейному охотничьему выстрелу.
По пиротехническому эффекту трассеры подразделяют на огневые и дымовые. Дымовые трассеры, заполняемые желтым фосфором или составами цветных сигнальных дымов, оказались неэффективными и во вторую мировую войну применялись исключительно огневые. Большого размера дымовые трассеры иногда используются сейчас только для обозначения траекторий полета самолетов при различного рода показах и т. п.
По способу воспламенения трассеры .подразделяют на:
1) воспламеняемые при выстреле пороховыми газами — лучевое воспламенение;
2) воспламеняемые при помощи специального капсюльного устройства или дистанционного взрывателя — механическое воспламенение;
3) воспламеняемые электрозалалом от источника тока, имеющегося на борту реактивного снаряда,— электрическое воспламенение.
По конструкции трассеры могут быть вкладными и запрессованными IB корпус снаряда.
Вкладные трассеры — это либо безоболочные шашки, спрессованные из трассирующего состава (основного и воспламени-тельного) под большим давлением — от 300 до 900 МН/м2 (от 3 до 9 т/см2), либо металлическая оболочка, в которую запрессован под таким же давлением тот же состав. Вкладной трассер помещается в соответствующее гнездо в дне снаряда или закрепляется на хвостовике взрывателя.
В трассерах второй группы состав запрессовывается либо непосредственно в корпус снаряда, либо в гнездо, имеющееся в дне сн.аряда.
По цвету пламени различают трассеры красного, белого, желтого и зеленого огня.
Известны трассеры с постоянной силой света, трассеры с силой .овета, возрастающей по мере удаления от стреляющего, трассеры с периодически изменяющейся силой овета (мигающие, пульсирующие) и с меняющимся цветом трассы. В некоторых случаях, когда надо скрыть трассу от наблюдения противника или свести к минимуму ослепляющее действие трассы на стреляющего, используют так называемую «тлеющую» или «темную» («dim», «dark») трассу, которая не видима невооруженным глазом ни днем, аи ночью и предназначена для применения в комбинации с военными оптическими приборами ночного видения.
КРАТКИЕ СВЕДЕНИЯ ОБ УСТРОЙСТВЕ ТРАССЕРОВ
Трассирующие пули
Трассирующая пуля (рис. 13.1) — это плакированная оболочка, в которой помещается свинцовый сердечник и .стаканчик с запрессованным в нем… .Пуля БТ ,(ри,с. 13.2) имеет вместо свинцового стальной сердечник. Было замечено, что при попадании в .бензиновые баки трассирующие пули поджигают горючее. Поэтому первоначально…Артиллерийские снаряды
Одним из важных преимуществ трассеров механического воспламенения является то, что трасса начинается в 150—200 м от 183Снаряды с самоликвидацией через трассер
Самоликвидация осуществляется либо при помощи .специального устройства во взрывателе, либо путем подрыва шашки ВВ при помощи тепла, передаваемого к… На рис. 13.9 и 13.10 показаны два малокалиберных зенитных снаряда с… В снаряде, показанном на рис. 13. 10, имеется пороховой столбик, который, воспламенившись от раскаленного колпачка…Трассеры к управляемым реактивным снарядам (PC) и авиабомбам. Специальные виды трассеров
Кроме того, в связи с тем, что трассеры, используемые в ракетах и в управляемых авиабомбах, могут применяться на больших высотах в условиях… Требования в отношении силы света и времени горения ракетных трассеров… В патентах ФРГ 1.158.872, 1963 и 1.131.561, 1961 предлагается трассер с изменяющимся цветам трассы, так что наряду с…ТРАССИРУЮЩИЕ СОСТАВЫ
1) выделять при горении максимальное количество световой энергии; 2) гореть с определенной небольшой скоростью, порядка нескольких 'миллиметров… Кроме того, к трассирующим составам для артиллерийских снарядов предъявляются еще дополнительные требования. В момент…ВОСПЛАМЕНИТЕЛЬНЫЕ СОСТАВЫ ДЛЯ ТРАССЕРОВ
Указанный здесь состав, запрессованный под большим давлением, на воздухе от луча огня воспламеняется весьма трудно или не воспламеняется вовсе.… Навеска воспламенительного состава подбирается с таким расчетом, чтобы она… Различные воспламенительные составы для трассеров, применявшиеся во время второй мировой войны или предложенные после…ФАКТОРЫ, ВЛИЯЮЩИЕ НА ЭФФЕКТИВНОСТЬ ТРАССИРУЮЩИХ СОСТАВОВ И ТРАССЕРОВ
Следует помнить, что составы в артиллерийских трассерах лучевого воспламенения при выстреле непосредственно подвергаются действию больших давлений и… В момент выстрела весь снаряд в целом, а следовательно, и состав, находящийся… При недостаточном уплотнении состава может иметь место выброс части его или всей запрессовки из трассерной каморы…ВИДИМОСТЬ ТРАССЫ И РАСЧЕТ НЕОБХОДИМОЙ СИЛЫ СВЕТА ПЛАМЕНИ
Яркость фона может изменяться в весьма широких пределах: яркость ночного неба при новолунии составляет только 1 •10-8 cб, яркость белых… Для восприятия глазом светящейся точки необходимо, чтобы освещенность, создаваемая ею на поверхности зрачка, превышала…ИСПЫТАНИЯ ТРАССЕРОВ
При 'проведении испытаний учитывается специфика наблюдения и реальных условий работы трассеров. Так, силу света измеряют в направлении от трассера… Рис. 13.13. Расположение трассирующих изделий при фотометрированниГЛАВА XIV
СОСТАВЫ СИГНАЛЬНЫХ ОГНЕЙ
СИСТЕМЫ СИГНАЛИЗАЦИИ. ТРЕБОВАНИЯ, ПРЕДЪЯВЛЯЕМЫЕ К СОСТАВАМ
Наиболее употребительной системой сигнализации является трехцветная — с тгримеяенибм красного, желтого и зеленого огней. Желтый огонь в случае необходимости может быть заменен белым, получающимся при… Применение четырех или пятицветной сигнализации (последняя включает в себя красный, желтый, зеленый, синий и…ХАРАКТЕР ИЗЛУЧЕНИЯ ПЛАМЕНИ
Отношение интенсивности монохроматического излучения пламени Я/, к интенсивности всего видимого излучения Еобщ называется чистотой цвета пламени (р)… Так, например, чистота цвета пламени составов красного огня может быть… E=Ea * 100 / Eобщ = E (0,62/0,76 мкм) * 100 / E(0,40 / 0,76мкм)РАЗРАБОТКА РЕЦЕПТОВ СОСТАВОВ И ОСНОВНЫЕ ТРЕБОВАНИЯ К ИХ КОМПОНЕНТАМ
Достаточно мощное цветное излучение получается при сжигании составов, теплота горения которых не меньше 0,8 ккал/г (3,4кДж/г). 2. При использовании молекулярного излучения температура пламени не должна… Так, например, температура зеленых пламен не должна превышать 2000° С.СОСТАВЫ ЖЕЛТОГО ОГНЯ
Входящие в составы натриевые соли должны легко диссоци-ировать при высоких температурах, иметь возможно большее содержание натрия и по возможности… Интенсивность свечения линии натрия .в пламени пропорциональна введенному в… Кроме желтой D-линии натрия (0,589 мкм), при высоких температурах могут появляться и другие линии натрия, но…СОСТАВЫ КРАСНОГО ОГНЯ
Оксид стронция (SrO) дает широкую размытую полосу в оранжево-красной части спектра с максимумом излучения около 0,60 мкм. Идентичный спектр дает и… Пламя, получающееся при излучении оксида стронция, имеет лишь розовую окраску,… Хлористый стронций при высокой температуре диссоциирует, образуя монохлорид стронция и отщепляя свободный хлор:СОСТАВЫ ЗЕЛЕНОГО ОГНЯ
Атомарный барий дает ряд линий в различных частях спектра, и потому излучение его не может быть использовано. Оксид бария (ВаО) — высоколлавящееся и труднолетучее соединение — дает широкие… Идентичный спектр дает IB пламени и нитрат бария.СОСТАВЫ СИНЕГО И БЕЛОГО ОГНЯ
Синее пламя получают почти исключительно на основе излучения монохлорида меди CuCl. Наличие в пламени соединений меди сообщает ему зеленую или синюю окраску. Цвет… В составах синего огня обязательно должны присутствовать хлорсодержащие соединения. Приведем рецепт одного из составов…МЕТОДЫ ИСПЫТАНИЯ
Сила света определяется при помощи фотоэлектрических люксметров по той же методике, как и для осветительных составов. Определение цветности пламени сводится к установлению цветового тона и чистоты… Если говорят, что цветовой тон пламени равняется a =0,620 мкм и чистота цвета пламени р=40°/о, то это следует понимать…ГЛАВА XV
ЗАЖИГАТЕЛЬНЫЕ СОСТАВЫ
ЗАЖИГАТЕЛЬНЫЕ СРЕДСТВА И ЗАЖИГАТЕЛЬНЫЕ СОСТАВЫ. ОСНОВНЫЕ ТРЕБОВАНИЯ К СОСТАВАМ
Зажигательные средства используются всеми видами вооруженных сил и являются 'важным средством поражения противника. Они применяются для поражения самолетов и вертолетов, танков, кораблей,… Зажигательные средства широко используются для уничтожения или нанесения ущерба промышленным предприятиям, военным…КЛАССИФИКАЦИЯ ЗАЖИГАТЕЛЬНЫХ СРЕДСТВ И СОСТАВОВ
Зажигательные средства
2. Средства артиллерии: пушечные и реактивные снаряды сосредоточенного и рассеивающего действия, зажигательные мины сосредоточенного и рассеивающего… 3. Средства пехоты: винтовочные и ручные гранаты, зажигательные бутылки,… 4. Средства танковых войск: огнеметные танки и самоходные огнеметы, ампулометы, зажигательные патроны, БЗ и БЗТ…Зажигательные составы
В зависимости от вида используемых для их изготовления веществ зажигательные составы можно разделить на следующие четыре типа: 1) составы на основе высококалорийных металлов (Mg, A1, Zr); 2) составы (смеси) на основе жидких горючих;СОСТАВЫ С ПОРОШКАМИ МЕТАЛЛОВ И ОКИСЛИТЕЛЯМИ — СОЛЯМИ И ПРИМЕНЕНИЕ ИХ В МАЛОКАЛИБЕРНЫХ СНАРЯДАХ
Малокалиберные зажигательные снаряды и пули попользуются главным образом для поджигания жидкого горючего в самолетах и вертолетах. Поэтому рассмотрим условия, необходимые для надежного поджигания горючего.
Воспламенение и горение жидких топлив
Температура самовоспламенения — это та температура, до которой нужно нагреть вещество, чтобы оно загорелось. Большинство горючих жидкостей имеет… Авиационные топлива США марок JP-1 и JP-3 имеют температуру самовоспламенения… Температурой вспышки называют ту наименьшую температуру жидкости, при которой пары ее образуют с воздухом смесь,…ТЕРМИТНО-ЗАЖИГАТЕЛЬНЫЕ СОСТАВЫ
ЗFе304+8А1=4А12O3+9Fе+831 ккал (3478 кДж) .....................................76% ...24%.... 45% ....55% Таблица 15.1 Составы длямалокалиберных зажигательных снарядов и пуль Индекс или № патента Компоненты,…СПЛАВ «ЭЛЕКТРОН» И ЕГО ПРИМЕНЕНИЕ
Сплав «электрон» имеетплотность 1,80—1,83 г/см3 и обладает хорошими прочностными характеристиками. Он вполне стоек по отношению к щелочным…СМЕСИ НА ОСНОВЕ НЕФТЕПРОДУКТОВ НАПАЛМ
1) жидкие (незагущенные) нефтепродукты; 2) отвержденные горючие; 3) жидко-вязкие (загущенные) зажигательные смеси;ФОСФОР И ЕГО СОЕДИНЕНИЯ
Преимущество белого фосфора перед другими зажигательными веществами состоит в том, что он в мелкораздробленном состоянии загорается на воздухе при… 4Р+502=2Р205. При сгорании образуется желтовато-белое пламя и выделяется много белого дыма — Р20з.ГАЛОИДНЫЕ СОЕДИНЕНИЯ ФТОРА
Многие галогенфториды, обладая достаточно большой химической активностью, являются либо жидкостями, либо сравнительно легко сжижаемыми газами. В табл. 15.7 приведены физические свойства галогенфторидов.ПРОЧИЕ ЗАЖИГАТЕЛЬНЫЕ ВЕЩЕСТВА И СМЕСИ
Преимущество металлического натрия перед другими зажигательными веществами заключается в том, что он 'бурно реагирует с водой: 2Na+H20=2NaOH+H2+135 икал (56й кДж) При известных условиях водород может образовать с воздухом гремучую смесь, при взрыве которой частицы горящего…МЕТОДЫ ИСПЫТАНИЯ ЗАЖИГАТЕЛЬНЫХ СОСТАВОВ
1) от средней разности между температурой шлаков и пламени зажигательного состава и температурой зажигаемого предмета АГ п; 2) от 'поверхности соприкосновения шлаков и пламени с зажигаемым предметом… 3) от времени их соприкосновения t;ГЛАВА XVI
СОСТАВЫ МАСКИРУЮЩИХ ДЫМОВ
Дымовые завесы ставятся на суше, на воде и в воздухе. В настоящее время дымовыми средствами снабжены все рода войск. В число их входят: дымовые шашки и гранаты, дымовые снаряды и мины, дымовые… Образующаяся при действии указанных средств дымовая завеса должна обладать хорошей кроющей способностью, быть…ОБЩИЕ СВЕДЕНИЯ ОБ АЭРОЗОЛЯХ
Если дисперсная фаза в воздухе представляет собой мельчайшие капли жидкости, то такая система называется туманом, если же она состоит из частиц… В военной технике дымы и туманы находят применение для создания нейтральных…СПОСОБЫ ПОЛУЧЕНИЯ АЭРОЗОЛЕЙ.
Почти всегда методом диспергирования получаются аэрозоли с более крупными частицами, чем методом конденсации. Вследствие этого на практике для… — охлаждением горячего пара; — получением из газообразных продуктов твердого или жидкого вещества, пересыщающего своими парами пространство.СОСТАВЫ МАСКИРУЮЩИХ ДЫМОВ И ПРЕДЪЯВЛЯЕМЫЕ К НИМ ТРЕБОВАНИЯ
1) полученный три горении пиросоставов дым должен иметь высокую кроющую способность и быть достаточно устойчивым в воздухе; 2) при сгорании в дымовых шашках составы не должны давать пламени; 3) образующийся шлак должен быть рыхлым (пористым, чтобы он не препятствовал прохождению через него дыма.ГЛАВА XVII
СОСТАВЫ ЦВЕТНЫХ ДЫМОВ
Эти составы используются в военном деле для сигнализации в дневных условиях; они применяются также для пристрелки и целей Казани я при бомбометании и артиллерийской стрельбе. На транспорте они используются для подачи сигналов бедствия (аварийные сигналы) в наземных условиях и, особенно, на море.
ЦВЕТНЫЕ ОБЛАКА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ
Имеются указания о возможности применения для сигнализации и черного дыма, причем он дается или в качестве пятого сигнала или им заменяется один из… Основной недостаток дымовой сигнализации — зависимость четкости наблюдения… Качество наблюдения дымовых сигналов зависит от формы и размеров облака; яркости и цвета фона, на котором…КРАСИТЕЛИ
1) они должны быстро возгоняться при 400—500° С; 2) возгонка их должна сопровождаться минимальным разложением красителя; 3) образовавшийся при конденсации их ларов дым должен иметь специфичную окраску (красную, желтую) и быть достаточно…СОСТАВЫ ЦВЕТНЫХ ДЫМОВ
Термическая смесь должна выделять тепло в количестве, необходимом для перехода красителя в парообразное состояние, но не должна развивать при… Термическая смесь должна также выделять при горении значительное количество… Чаще всего в качестве горючих в составах сигнальных дымов употребляют углеводы; они образуют при своем сгорании…ГЛАВА XVIII
ТВЕРДЫЕ ПИРОТЕХНИЧЕСКИЕ ТОПЛИВА
КЛАССИФИКАЦИЯ И ЭНЕРГЕТИЧЕСКИЕ ХАРАКТЕРИСТИКИ
Некоторые виды известных в настоящее время твердых толлив для реактивных двигателей по своему составу и свойствам близки к пиротехническим составам.
По назначению их можно разделить на четыре характерных типа:
1) топлива для воздушно-прямоточных реактивных двигателей (ПВРДТ) или ракетно-прямоточных двигателей (РПДТ);
2) топлива для гидрореактивных двигателей (ГРД);
3) топлива для комбинированных двигателей (К.РД);
4) к твердым пиротехническим топливам близки также сме-севые топлива для ракетных двигателей (РДТТ).
Из указанных здесь типов топлива к пиротехническим в наибольшей степени относятся первые три, а именно те из них, которые содержат большое количество металлического горючего, а в качестве окислителя — соли неорганических кислот.
Горение топлива в камере сгорания происходит при повышенном давлении. При истечении продуктов сгорания из сопла происходит расширение газов, сопровождающееся падением давления и температуры. При этом движение газов ускоряется, т. е. происходит преобразование энергии топлива в кинетическую энергию струи.
,В предельном случае, без учета тепловых и других потерь, величина кинетической энергии 1 кг продуктов сгорания равна изменению теплосодержания:
A (v2 / 2g) = I
где v — скорость истечения газов на выходе из сопла в м/с;
I— изменение теплосодержания продуктов сгорания в кДж/кг;
А — тепловой эквивалент работы в кДж/кгм.
Основной энергетической характеристикой топлива принято считать удельный импульс, т. е. величину тяги, развиваемую.
Таким образом, расчет теоретической величины удельного импульса для заданного топлива сводится к определению теплосодержания продуктов сгорания в камере двигателя и на срезе сопла.
С этой целью проводят специальные термодинамические расчеты. B основе которых лежит равенство полного теплосодержания топлива полному теплосодержанию продуктов реакции при данном давлении, а также принцип полного термодинамического равновесия в продуктах сгорания при данной температуре и давлении [3; 7; 77]. При этом принимается во внимание теплота образования компонентов топлива, изменение термодинамических характеристик продуктов сгорания с изменением температуры;
учитывается диссоциация продуктов сгорания при высокой температуре [86].
В результате таких расчетов определяют температуру продуктов сгорания топлива при различных давлениях, состав и характеристики продуктов сгорания, удельный импульс при заданном давлении в камере.
Полученные результаты являются исходными для последующих расчетов двигателя и различных процессов, протекающих в двигателе при горении топлива, а именно, расчета сопла, геометрии заряда твердого топлива, условий течения продуктов сгорания по камере двигателя или по каналу заряда, расчетов теплоизоляции двигателя и тепловых потерь.
Превращение энергии у различных реактивных двигателей происходит по-разному.
1. Прямоточный воздушно-реактивный двигатель на твердом топливе развивает тягу в полете за счет изменения количества движения струи воздуха, протекающей сквозь двигатель. Схема этого двигателя представлена на рис. 18.1.
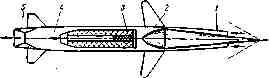
Рис. 18.1. Схема прямоточного воздушно-реактивного двигателя на твердом топливе:
/—сверхзвукоьая часть диффузора; 2—дозвуковая часть диффузора; 3— заряд твердого топлива; 4—камера сгорания; 5—выходное сопло
Увеличение количества движения происходит за счет тепла, выделяющегося при сгорании топлива.
Воздух, поступающий в двигатель через специальный воздухозаборник (диффузор), является в данном случае и окислителем и рабочим телом.
Повышенное давление в камере сгорания, необходимое для работы двигателя, получается за счет торможения воздуха, поступающего в воздухозаборник со скоростью полета. Чем выше скорость полета, тем выше давление в камере и эффективность двигателя. Напротив, при низких скоростях полета снаряда ПВРД не эффективен. Поэтому ооычно требуется предварительный разгон за счет стартового двигателя до сверхзвуковой скорости полета, после чего включается ПВРД в качестве маршевого двигателя. Эффективность ПВРД характеризуется удельной тягой и коэффициентом тяги. Удельный импульс / определяет экономичность двигателя, а коэффициент тяги Сд — максимальную величину тяги, которая может быть получена на данном топливе в определенном двигателе.
Из теории ПВРД известно, что величина удельного импульса / и коэффициента тяги Сд зависит от скорости и высоты полета
Относительный подогрев 9 при работе двигателя на твердом топливе зависит от теплотворной способности топлива Ни и соотношения между расходом воздуха и расходом тотива aLo:
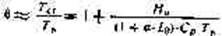
T ег— гемтература торможения продуктов сгорания в К;
Тв— температура торможения набегающего потока воздуха а К;
Ср — теплоемкость продуктов сгорания в кДж/кг-град. Поэтому наибольшую экономичность ПВРД или наибольшую удельную тягу можно получить, применяя топлива, которые имеют наибольшую теплотворную способность при сжигании их в воздухе.
Пример 1. Вычислить удельный импульс / ПВРД при ^=500 м/с на высоте НО км. Расход воздуха через двигатель G„=¦20 кг/с, От =2 кг/с Тоти-во — магний.
При заданных скоростях и высоте полета Г„=335 К теплоемкость продуктов сгорания можно принять равной Ср=1,26 кДж/кг.град. Теплотворная
способность магния 24700———. Комплекс аЬц = —в- = 20/2 = Ю.
Как видно из приведенных примеров, величина удельного импульса у ПВРД значительно выше, чем у обычных пороховых или жидкостных двигателей. Это объясняется тем, что основная масса рабочего тела (воздух), хотя и участвует в создании тяги двигателя, но не содержится в ракете, а забирается из атмосферы.
Имеются сообщения об экспериментально достигнутой величине удельного импульса: 500—700 кг-с/кг.
Для получения большого коэффициента тяги , который требуется в случае полета со сверхзвуковой скоростью, необходимо топливо с .высокой теплопроизводительностью W:
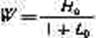
Теплопроизводительностью называется количество тепла, приходящегося на 1 .кг продуктов сгорания при стехиометрическом соотношении между топливом с воздухом. Поэтому твердые топлива для ПВРД наряду с высокой теплотворной способностью должны иметь как можно более низкое значение стехиометриче-окой постоянной LQ.
В частности, углеводороды, имеющие высокую теплотворную способность (37600—41 900 кДж/кг), не удовлетворяют последнему требованию, так как имеют вместе с тем стехиометрическую постоянную Z,o=13—15.
Такие металлы, как бериллий, бор, алюминий и магний, обладая достаточно высокой теплотворной способностью, имеют в то же время сравнительно низкие стехиометрические постоянные. Поэтому применение их в качестве компонентов твердых топлив для ПВРД и особенно для РПДТ считается перспективным.
Наилучшие теоретические характеристики имеет бериллий, однако обычно указывают на высокую стоимость и неполноту сгорания этого металла. Использование металлов в топливахдля ПВРД особенно необходимо при высоких скоростях полета (когда в камере сгорания развивается очень высокая температура), так как продукты сгорания металлов обладают высокой термической стойкостью. Обычно твердые топлива для ПВРД состоят из металлического горючего, органического горючего — связки и специальных добавок. Некоторые топлива содержат также окислитель. В частности, предлагалось использовать быстрогорящее топливо для ПВРД, состоящее из сплава магния с алюминием, небольшого количества связки и окислителя.
Заряды из такого топлива готовят методом прессования при высоком удельном давлении. Медленно горящие топлива наряду с металлом и окислителем содержат до 50% горючего-связки.
Заряды из такого топлива готовят методом литья в изложницу, где оно затвердевает при полимеризации связки.
Твердые топлива для ракетно-прямоточного двигателя, представляющего собой органическое сочетание в единой конструкции ракетного и прямоточного двигателя, наряду с высокой теплотворной способностью должны иметь также достаточно высокую собственную тягу. С этой щелью необходимо обеспечить высокую температуру продуктов сгорания топлива за счет собственного окислителя и достаточное количество газообразных продуктов сгорания. Поэтому топлива для РПДТ содержат в своем составе значительное количество окислителя.
Характерным для состава такого топлива является содержание 30—50% перхлората аммония, 40—60% металла, обычно алюминия или его сплавов, и 10—15% связующего.
Фирма Lockheed Missiles and Space исследует топливо, содержащее 48% перхлората аммония, 40% бора, 10,5% — овязкиполибутадиенакриловой кислоты и 1,5% полимеризующей добавки — эпоксидной смолы.
Одной из наиболее важных проблем использования металлов в топливах для ПВРД является обеспечение .полного сгорания в смеси с воздухом при минимальной длине камеры дожигания.
Получение высокой полноты сгорания требует решения таких важных вопросов, как смешение продуктов сгорания топлива и воздуха, воспламенение и дожигание в условиях камеры сгорания конденсированных частиц.
Горение металлов, у которых температура кипения окисла существенно превышает температуру кипения металла, происходит преимущественно в паровой фазе. Поэтому частицы таких металлов, как магний и алюминий, горят в диффузионном режиме, и если обеспечено воспламенение частиц и смешение с воздухом, то время, необходимое для полного выгорания частиц, пропорционально квадрату их диаметра.
Очевидно, при соответствующем подборе длины камеры дожигания и дисперсности частиц металлов можно добиться удовлетворительной полноты сгорания таких металлов, как алюминий, магний и их сплавы. Значительно труднее получить высокую полноту сгорания топлив, содержащих бор. Так как бор имеет высокую температуру кипения, горение частиц носит преимущественно поверхностный характер, т. е. во-первых, происходит значительно медленнее, чем горение в паровой фазе, а во-вторых, существенно зависит не только от смешения с воздухом, но и от температуры.
Большое значение в процессах горения металлов имеют свойства образующихся окислов и условия воспламенения частиц в камере дожигания.
В целом полнота сгорания топлива в двигателе характеризуется коэффициентом полноты сгорания (per, представляющим собой отношение прироста теплосодержания продуктов сгорания, реализованного в двигателе, к соответствующей теоретической величине.
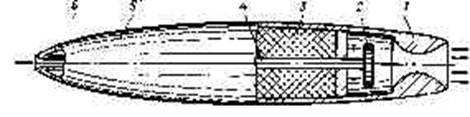 2. Гидр ©реактивные двигатели (ГРД) используют в качестве окислителя и рабочего тела забортную морскую воду. Схема такого двигателя дана на рис. 18.2.
2. Гидр ©реактивные двигатели (ГРД) используют в качестве окислителя и рабочего тела забортную морскую воду. Схема такого двигателя дана на рис. 18.2.
Рис. 18.2. Схема гидрореактивного двигателя на твердом топливе:
1— выходное сопло: 2— коллектор и головка с форсунками для распыла воды- 3—заряд твердого топлива; 4—канал для ввода воды; 5—корпус двигателя; б—водозаборник
Гидрореактивные двигатели применяют в торпедах; при движении торпеды морская вода поступает через специальные водозаборники в двигатель. В камере сгорания тепловая энергия, выделившаяся при сгорании топлива в парах воды, затрачивается на испарение воды. Смесь паров воды и продуктов сгорания топлива при истечении из сопла обеспечивает получение необходимой тяги. Для подводных двигателей определяющей является удельная объемная тяга, т. е. тяга, развиваемая двигателем при сгорании 1 л топлива в секунду. Поэтому важнейшей характеристикой гидрореагирующего топлива является количество тепла, выделяющегося при сгорании топлива при взаимодействии с водой, и количество воды Lo (кг), необходимое для сгорания 1 кг топлива.
Вещества, применяемые в качестве топлива, должны энергично реагировать с водой. Такие металлы, как Be, В, Al, Mg, Zr, Li, теоретически обладают весьма высокими энергетическими характеристиками.
Однако при практическом использовании металлов встречаются серьезные затруднения. Одним из путей решения этой задачи является разработка специальных гидрореагирующих топлив и зарядов из них путем запрессовки смеси порошков металлов и окислителя. Такое топливо должно иметь отрицательный кислородный баланс; в качестве окислителей могут быть использованы перхлораты. Иногда с целью повышения скорости горения топлива в их состав вводят добавки тонкоизмельченных порошков соединений кобальта, меди или феррованадия.
Величина удельного импульса гидрореагирующих топлив зависит от отношения секундного расхода воды Ов к секундному расходу топлива Ст:
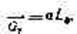
где а — коэффициент избытка воды.
Энергетические возможности гидрореагирующих топлив показаны на рис. 18.3.
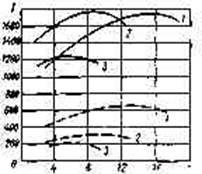
Рис. 18.3. Зависимость удельного импульса (/) ГРД от избытка воды в молях (п):
Давление в камере двигателя 23,2 кгс/см' (2,27 МН/м2), на срезе 1,14 кгс/см" (0,11 МН/м2)
3. Комбинированные ракетные двигатели (КРД) отличаются от других видов ракетных двигателей тем, что и топливо, и окислитель находятся в ракете, но конструктивно они разделены.
Одним из возможных вариантов комбинированного двигателя является такой, в котором используется жидкий окислитель в сочетании с зарядом твердого топлива (рис. 18.4).
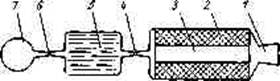
Рис. 18.4. Схема комбинированного ракетного двигателя:
/—выходное сопло; 2—заряд твердого топлива; 3— канал; 4—отсечный клапан и головка с форсунками для рас-пыла жидкого окислителя; 5—бак с жидким окислителем; 6—форсунка; 7—бак со сжатым газом
Преимуществам КРД является более высокий удельный импульс, чем у РДТТ, возможность регулирования тяги и многократного запуска посредством отсечки и 'повторной подачи жидкого окислителя.
В таких двигателях .возможно применение энергетически выгодных компонентов топлива, несовместимых химически при контакте друг с другом или находящихся в различном агрегатном состоянии.
В качестве жидких окислителей в КРД применяют азотную кислоту, окислы азота (N204), фтористый перхлорил (FC104), перекись водорода или треххлористый фтор (С1Fз).
Наиболее высокие энергетические характеристики могут быть получены на гидриде бериллия ВеН2. Однако необходимость придания заряду нужных механических характеристик и организации процесса горения требуют введения в состав топлива органических горючих-связующих и окислителя.
Практически ,все существующие и перспективные топлива для КРД содержат значительное 'количество металла — Al, Mg, Be или их гидриды — в виде мелкодисперсного порошка и органические горючие-связки.
Для 0'беспечения самовоспламенения топлива с жидким окислителем в состав твердых топлив вводят амины, например, пара-толундин, парафенилендиа,мин, 1,6-диаминонафталин и др.
Введение в твердую фазу до 20% перхлората аммония приводит к снижению .времени задержки воспламенения и образованию более чистой свободной поверхности горения, что улучшает характеристики горения.
Схема процесса горения заряда твердого топлива в потоке жидкого окислителя представлена на рис. 18.5.
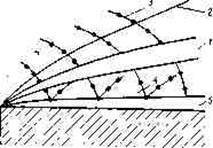
Рис. 18.5. Схема процесса горения в камере комбинированного двигателя:
/-—диффузионное пламя: 2—граница пограничного слоя; 3—траектории капель; 4—зона гетерогенного горения; 5—зона реакции между каплей окислителя и твердым горючим
Капли жидкого окислителя испаряются по мере приближения к поверхности горения. Пары окислителя образуют с парами продуктов разложения топлива диффузионное пламя. Капли окислителя, пролетевшие сквозь зону диффузионного пламени, «сгорают» в среде, переобогащенной газообразным горючим, а также вступают в непосредственное взаимодействие с повеохностью горящего заряда топлива при контакте с ней.
Скорость горения топлива в КРД зависит не только от давления и природы компонентов, но и от массового потока вдоль поверхности заряда, геометрии заряда, способа подачи жидкого окислителя и его количества на единицу поверхности заряда. Эти особенности позволяют осуществлять регулирование тяги двигателя количеством подаваемого в камеру жидкого окислителя.
В экспериментальных исследованиях подобных двигателей получена величина удельного импульса 255—265 кг-с/кг. Коэффициент полноты сгорания при этом достигал 0,90-0,95 [З].
4. Ракетные двигатели на твердом топливе (РДТТ) получили наибольшее распространение благодаря простоте конструкции и разработке высокоэнергетических смесе-вых топлив. Типичная схема РДТТ показана на рис. 18.6. Основные преимущества РДТТ — простота конструкции, постоянная готовность к запуску, удобство и относительная безопасность эксплуатации, высокая надежность действия.
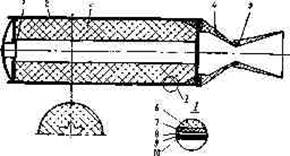
Рис. 18.6. Схема ракетного двигателя на твердом топливе: 1-воспламенитель; 2-корпус двигателя: 3-заряд твердого топлива; 4-сопло; 5-графитовый вкладыш; 6-топливо; 7-бронировка;8-зазор; 9-теплоизоляция двигателя; 10-стенка корпуса
Основной энергетической характеристикой топлива является удельный импульс:
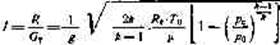
где k — показатель адиабаты;
и — средний молекулярный вес газообразных продуктов сгорания;
ir— универсальная газовая постоянная в кДж/моль-град;
То ро — температура и давление в камере;
рс — давление на срезе сопла в кгс/см2.
Пример. Рассчитать удельный импульс смесевого топлива при ро== =40 кгс/см2; температура горения топлива Го=2790 К, ц=25;5, fe=l,22.
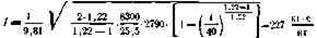
Методы расчета и измерения удельного импульса изложены достаточно полно в работах [3; 7; 69].
Наибольшую величину удельной тяги .будут иметь топлива, продукты сгорания которых имеют наименьший молекулярный вес и высокую температуру сгорания. Из всех видов твердых топлив для ракетных двигателей наиболее полно удовлетворяют этим требованиям смесевые ракетные топлива.
Эти топлива обычно состоят из тщательно перемешанных органических горючих-связующих и твердых кристаллических окислителей. Для повышения удельного импульса таких топлив в их состав обычно вводят 10—20% легких металлов или их сплавов — Mg, Al, Li, Be [7; 69].
Обладая высокой теплотой реакции и образуя при сгорании термически стабильные продукты, эти металлы позволяют повысить температуру продуктов сгорания топлива, а следовательно, и удельную тягу топлива. Однако продукты реакции этих металлов с кислородом и хлором, являясь высококипящими веществами, даже при температуре сгорания в значительной степени находятся в конденсированном виде. Поэтому введение в состав ракетных топлив значительного количества металла нецелесообразно. Наибольшее повышение удельного импульса получается при введении в состав топлива двойных сплавов или смесей легких металлов. При этом количество металла (например, Al), соединяющегося с кислородом, и количество металла (например, Li), соединяющегося с галогеном, должны соответствовать содержанию кислорода и галогена в используемом окислителе. Оптимальная величина удельного импульса получается у топлив, имеющих отрицательный кислородный баланс вследствие пониженного значения среднего молекулярного веса продуктов сгорания и меньших потерь энергии на диссоциацию, чем у стехиометрических топлив.
Используемые на практике топлива содержат обычно 80— 85% окислителя. При этом могут быть обеспечены удовлетворительные технологические свойства топлива и в некоторых случаях устранена склонность перхлоратного топлива к детонации.
Смесевые топлива могут иметь самый различный состав и обладать различными механическими свойствами. Подробный разбор с указанием как смесей, так и свойств отдельных компонентов дан в [149; 77].
В табл. 18.1 приведены некоторые типичные смесевые топлива для РДТТ.
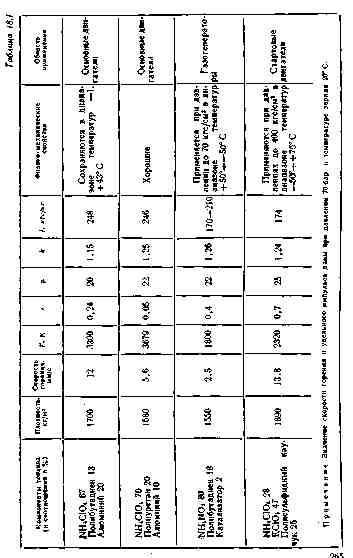
Таким образом, рассмотренные четыре типа твердых топлив для различных реактивных двигателей принципиально представляют собой гетерогенные системы, являющиеся смесями неорганического окислителя, органического горючего и металлического горючего. Неорганический окислитель и металлическое горючее вводятся в состав топлива в виде тонкоизмельченных порошков. Состав топлива, технология изготовления и характеристики определяются главным образом типом реактивных двигателей. В табл. 18.2 приведены составы различных типов твердых пиротехнических топлив и даны их характеристики [96; 3; 149].
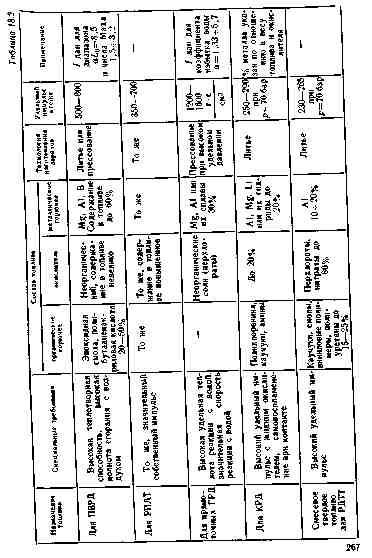
ЭКСПЛУАТАЦИОННЫЕ ТРЕБОВАНИЯ
Обычно для заданных габаритов, закона изменения тяги во времени, скорости горения топлива возможно подобрать геометрическую форму заряда,… На рис. 18.7 представлены наиболее распространенные формы зарядов твердого…ОКИСЛИТЕЛИ
ОРГАНИЧЕСКИЕ И МЕТАЛЛИЧЕСКИЕ ГОРЮЧИЕ
Кроме свойств связующего, технологичность топлива, изготовляемого литьем, зависит от объемного соотношения твердой и жидкой фазы, а также удельной… При отношении объемов твердой фазы к жидкой в пределах 3,5—2,5 топлива… Полимеризация горючего-связующего (с добавкой катализатора) осуществляется после заливки топливной массы в изложницу…ГЛАВА XIX
БЕЗГАЗОВЫЕ СОСТАВЫ
Пиротехнические замедлители рассчитаны обычно на небольшое время горения, не более нескольких минут. Конструкция некоторых из них дана в работе… 1) максимальная точность в соблюдении времени горения; 2) минимальная зависимость времени горения от температуры и давления окружающей среды;ВОСПЛАМЕНИТЕЛЬНЫЕ СОСТАВЫ. ГАЗОГЕНЕРАТОРНЫЕ СОСТАВЫ. ПРОЧИЕ ВИДЫ СОСТАВОВ
ВОСПЛАМЕНИТЕЛЬНЫЕ СОСТАВЫ И ПРЕДЪЯВЛЯЕМЫЕ К НИМ ТРЕБОВАНИЯ
Чем выше температура воспламенения основного состава, тем более «сильный» воспламенительный состав требуется для возбуждения в нем процесса… Составы, температура вспышки которых более 1000° С, воспламеняются с большим… К воспламенительным составам предъявляются следующие требования:ВОСПЛАМЕНИТЕЛЬНЫЕ СОСТАВЫ ДЛЯ РАКЕТНЫХ ДВИГАТЕЛЕЙ
Факел пламени пиротехнического воспламенителя имеет высокую температуру и достаточно большие размеры (большую площадь воспламенения). В литературе… На первой стадии отработки в пиротехнических воспламенителях была использована… Позднее в смесь А1С10 стали .вводить этилцеллюлозную связку. Для воспламенения смесевых топлив с высоким содержанием…ГАЗОГЕНЕРАТОРНЫЕ СОСТАВЫ
Амер. патент 2.988.876,11961. 2 Miss a Rockets, 'IBTO, 6, No 13(0; то же, .1959, 5, No 41. Газогенераторные составы должны иметь низкую температуру и малую скорость… Таблица 20.1 Свойства Аммония нитрат NH4NO, Гуанидиннитрат CNH(NH2)2*HNO, Нитрогуанидин…Высокоазотные газогенераторные составы по данным [117] в процентах
ряют полностью требованиям, предъявляемым к газогенераторным составам. В частности указывается, что смеси, содержащие NH4N03, гигроскопичны и трудно… В начале 60-х годов в США были разработаны газогенераторные составы на основе… C2H404N2—>2H2O + 2СО + N2ПРОЧИЕ ВИДЫ СОСТАВОВ
Чаще других для специальных целей применяют имитационные и свистящие составы. Имитационными составами снаряжают различные учебные пиротехнические изделия.… Некоторые имитационные изделия должны давать при своем действии сильный звук, сходный со звуком разрыва фугасного…ПРИМЕНЕНИЕ ПИРОТЕХНИЧЕСКИХ СОСТАВОВ В НАРОДНОМ ХОЗЯЙСТВЕ
Пиротехнические составы, используемые для мирных целей, можно разделить на две категории: 1) составы, назначением которых является получение в… 2) составы, а которых используется выделяющаяся при их горении энергия —…СОСТАВЫ ДЛЯ ПОЛУЧЕНИЯ ХИМИКАТОВ
В том случае, когда получение металла при помощи алюми-нотермической реакции затруднительно, используются следующие варианты для ее осуществления: … 1. Добавляют более активные окислители к низшему окислу, например, хроматы к… 2. Добавляют сильные окислители, увеличивающие тепловой эффект реакции и облегчающие протекание процесса, например…ИСПОЛЬЗОВАНИЕ ЭНЕРГИИ ПИРОТЕХНИЧЕСКИХ СОСТАВОВ
Термитные составы как источник энергии. Применение термитных составов для сварки рельс общеизвестно. В настоящее время разработаны пиропатроны для… щи специальных клещей, после чего поджигают надетый на место стыка проводов… Медный термит, состоящий из 64% CuO, 16% ферромарганца (80% Mn) и 20% сплава CuAl (46% Al), применяется для приварки к…СПИЧЕЧНЫЕ СОСТАВЫ
Мировое производство спичек — 30 миллиардов коробок в год; на одну коробку расходуется около 1 г спичечной массы. Следовательно, расход сличенной… * В США уже несколько лет проводятся испытания лазерной винтовки, с помощью… Процесс воспламенения современных спичек таков: при трении спичечной головкой о намазку на коробке происходит…ФЕЙЕРВЕРОЧНЫЕ СОСТАВЫ
Основными видами фейерверочных составов являются: составы цветных огней, искристые составы и составы звуковые, однако возможна и комбинация этих… Советскими специалистами разработаны фейерверочные составы с окислителем —…ОСНОВЫ ТЕХНОЛОГИИ И ОБОРУДОВАНИЕ ПИРОТЕХНИЧЕСКОГО ПРОИЗВОДСТВА
Пополнение аппаратурного и машинного парка посредством заимствования оборудования из родственных отраслей промышленности, а также разработка новых… За последние годы значительно расширилась номенклатура пиротехнических… Вес пиротехнического состава в изделиях колеблется от нескольких граммов до нескольких сот килограммов.ПОДГОТОВКА КОМПОНЕНТОВ
Снятие крышек с банок производится ломиками из цветного металла во избежание искрообразования. За последние годы было разработано и внедрено в… Наиболее простым по устройству является аппарат, в котором извлечение крышки… Контрольный просев осуществляют на ситах-трясунах или на виброситах. Опрокидывание банки с порошкам производится с…Техническая характеристика шкафа
Поверхность нагрева в м2 ....... 6,27 Остаточное давление в кг/м2 ...... 2,63 (20 мм рт.ст.) Размеры плиты в мм ........ 730х610ПРИГОТОВЛЕНИЕ СОСТАВОВ
Трудность состоит в том, что содержание некоторых компонентов в составах не превышает 2%. Часть компонентов вводится в составы в виде лаков… Все это вместе взятое сделало необходимым поиск новь/х конструктивных решений… При конструировании смесителей необходимо было принимать во внимание также ограничения по загрузке пиротехническим…УПЛОТНЕНИЕ СОСТАВОВ
В фотобомбах степень уплотнения состава должна быть незначительной. Это достигается путем виброуплотнения фотосмеси непосредственно в корпусе… При снаряжении шнекованием рабочим инструментом является архимедов винт,… Уплотнение составов достигается путем приложения извне к снаряжаемым изделиям (со стороны, противоположной той, откуда…СНАРЯЖЕНИЕ И СБОРКА ИЗДЕЛИЙ
а) подготовка деталей и узлов к снаряжению; б) сборка деталей и узлов; в) окончательная отделка изделий (окраска, лакировка, маркировка);СПИСОК ЛИТЕРАТУРЫ
1. Аксенов М. Я., Вернидуб И. И. и др. Получение льдообразующего аэрозоля с помощью пиросоставов. Труды Центральной Аэрологической обсерватории, 196Й, вып. 44, с. 63.
2. А к у н о в В. И. Струйные мельницы. М., Машгиз, 1962.
3. А л е м а с о в Б. Е., Д р е г а л и н А. Ф., Т и ш и н А. П. Теория ракетных двигателей. М., «Машиностроение», 1969.
4. Андреев К. К. Термическое разложение и горение ВВ. М., «Наука», 1966, 2-е изд.
б. А н д р е е в К. К., Б е л я е в А. Ф. Теория взрывчатых веществ. М., Оборонгиз, I960.
6. Андреев К. К. Об основных причинах различия между инициирующими и вторичными 'ВВ. ДАН СССР, .1992, Т. .Ж, вып. 2, с. 410.
7. Б а р р е р М., Жоммот А. и др. Ракетные двигатели. М., Оборонгиз, 1962.
8. Б а х м а н Н. Н., Б е л я е в А. Ф. Горение гетерогенных конденсированных систем. М., «Наука», 1967..
9. Б е л я е в А. Ф., Ц ы г а н о в С. А. Горение конденсированных смесей с нелетучими и неразлагающимися горючими. ДАН ССОР, 1962, Т. 146, вып. 2, стр. 363. »
10. Б е л я е в А. Ф. и др. Особенности горения порошкообразного алю-мания. — «Физика горения и взрыва», 1969, Т. 5, вып. 2, с. 20(7.
11. Беляев А. Ф. Горение, детонация и работа взрыва конденсированных систем. М., «Наука», 1968. ч мгг
12. Блюменталь У. Д. Химия циркония. Перев. с англ. М., ИЛ, 1963
13. Бондарю к М.М., ИльяшенкоС.М. Прямоточные воздушно-реактивные двигатели. М., Оборонгиз, 1958. V .
14. Б р а у э р. Пиротехнические устройства для космических аппаратов— «Вопросы ракетной техники», 1,969, вып. .10, с. 47.
15 Б рейтер А. Л., К а ш п о р о в Л. Я. и др. Горение одиночных частиц алюминиево-магниевых сплавов. —«Физика горения и взрыва», ¦1У/1, 1. /,
вып. 2, с. 222. „ ^, 1
16. Бубнов П. Ф., Сухов И. П. Средства инициирования. М., Обо-рон
17. Б у д н и к о в М. А., Б ы с т р о в И. В. и др. Взрывчатые вещества и пороха. М., Оборонгиз, 1955.
18. Ван-Везер Д. Р. Фосфор н его соединения. М., ИЛ, 1962.
19 Васильев А. В., Г о р б у н о в В. В. и др. О горении смесей сульфатов металлов с магнием или алюминием.—«Физика горения и взрыва», 197l, Т. 7, вып. ,1, стр. 150.
20. В е и ц е р Ю. М., Л у ч и н с к и и Г. П. Маскирующие дымы. М., Химиздат, 1947.
21 Вернидуб И. И., Ж и х а р е в А. С., С у л а к в е л и д зе Г. К. и др. Исследование льдообразующих свойств йодистого свинца.—«Известия АН СССР. Серия геофизическая». 1962, № 9, стр. Г286.
22. Володина Н. А. и др. - Исследование горения смесей хлората калия с идитолом и каталитическими добавками. ЖПХ, ¦1996, Т. 39, вып. 4,
23. Вспомогательные системы ракетно-космической техники. Перев. с англ. Под ред. И. В. Тишунина. М., «Мир», 1970. " ~"
24. Гайворонский И. И., Серегин Ю. А. О введении реагентов в облака при воздействии на градовые процессы — «Труды Центрально!! Аэрологической обсерватории», 1966, вып. 65, с. 48.
25 Гаррисон П. Сжигание титана и циркония. — В кн. Вопросы горения. Материалы VI и VII симпозиумов по горению. М., Металлургиздат, 1963.
26. Гетерогенное горение. Сб. статей. Перев. с англ. Под ред. В. А. Ильинского и И. Н. Садовского. М., «Мир», 1967.
27 Г о д ж е л л о М Г. Взрывы промышленных пылеи и их предупреждение. М., Пзд-во МКХ РСФСР, 1952.
28. Гольбиндер А. И. Лабораторные работы по теории ВВ. М„ Госвузиздат, 1963.
29. Г'о р б у н о в В. В., Васильев А. В., Ш и д л о в_с к н и А. А. О горении смесей порошков высококалорийных металлов с водой.— «Известия вузов. Химия и химическая технология», 1969, Т. 1'2, вып. 9, стр. ,1)171; 1970, Т. 13, вып. 3, с. 31118.
30. Горбунов В. В. и др. Способность к горению смесей порошков высококалорийных металлов с органическими веществами формулы СхНуОг.— «Физика горения и взрыва», -1968, Т. 4, вып. 2, с. 11Й2.
31. Гороховский Ю. Н., Баранова В. П. Свойства черно-белых фотографических пленок. М., «Наука», 1970.
32.ГорьковВ.А., КурбангалинаР.Х. Детонационная способность перхлората аммония. — «Физика горения и взрыва», L966, Т. ,2„ вып. 2, тр. 21. п v
33. Грин X., Лейн В., Аэрозоли — пыли, дымы и туманы. Л., «Химия», 1969.
34 Д е м и д о в П. Г. Горение и свойства горючих веществ. М., Изд-во МКХ РСФСР, 1961.
35. Джонс В. Д. Основы порошковой металлургии. М„ «Мир», 1964.
36. Дубровин А. С. и др. Влияние плотности алюминотермических составов на их горение. — «Физика горения и взрыва», 1970, Т. 6, яып. 1, с. 84.
37. Е в д о к и м о в В. В., Б а х м а н Н. Н. Влияние сажи и окиси железа на богатый предел горения конденсированных смесей.— «Физика горения и взрыва», I960, Т. б, вып. 4, с. 585.
38. Зайцев Г. С., Кузнецов А. Я. Дымовые средства и дымообразующие вещества. М., Воениздат, 1961.
39. Исследование внутрикамерных процессов в РПДТТ.—«Вопросы ракетной техники», 1969, вып. 5, с. 37—57.
40. Исследование ракетных двигателей на твердом топливе. Сборник статей. Под ред. М. Саммерфилда. М., ИЛ, 1988.
41. К а м и н с к и и А. А. и др. Квазинепрерывные ОКГ с пиротехническим возбуждением. — «Журнал технической физики», .1989, Т. 39, вып. 3, с. 535.
42. К а р а п е т ь я н ц М. X., Ка р а п е т ь я н ц М. Л. Основные термодинамические константы неорганических и органических веществ. М., «Химия», 1968.
43. Касаткин А. Г. Основные процессы и аппараты химической технологии. М., «Химия», 1971.
44. К и н д ж е р и В. Д. Измерения при высоких температурах. М., Ме-таллургиздат, 1963.
45. Киселев В. С., Абашкина А. Ф. Производство лаков, олиф и красок. М., «Химия». 1964, изд. 3-е.
46. Козлов В. М., Туровский В. Д. Бериллий — токсикология, клиника поражений, гигиена труда. М., Атомиздат, 1962.
47. К о з у л и н Н. А., Г о р л о в с к и и И. А. Оборудование заводов лакокрасочной промышленности. Л., «Химия», 1968.
48. Кубашевский О., Гопкинс Б. Окисление металлов и сплавов. М., Металлургиздат, 1965.
49. К у к и н А. И. Новые виды термитной сварки. М., Трансжелдориз-дат, 1955.
50. Лазарев Л. П. Инфракрасные приборы самонаведения летательных аппаратов. М„ «Машиностроение», 1970.
51. Лаример, Р е и к о. Сайде. Смесители для производства твердых ракетных топлив.— «Вопросы ракетной техники», 1969, № 7, с. 3.
52. Липатов Ю. С. и др. Структура и свойства полиуретанов. Киев, «Наукова думка»,1970.
53 Лихачев В. А. -Пиротехника в кино. М., «Искусство», 1963, изд. 2-е.
54. Лосев Б. И. и др. Твердый бензин. М., Гостоптехиздат, 1959.
55. Л у ч и н с к и и Г. П. Химия титана, М., «Химия», 1971.
56. М а р к ш т е и н Г. X. Гетерогенное горение металлов.— «Вопросы ракетной техники», 1968, вып. 4, с. 30.
57. Масленников П. Е., Москвин И. И. и др. Вооруженные силы капиталистических государств. М., Воениздат, 1971.
58. Мезон Дж. Ф. Разведывательный самолет «Могавк».—«Электроника», 1967, вып. 10, с.59.
59. Михайлов В. Н. Аэрофотография и общие основы фотографии. М., Геодезиздат, 1959.
60. М у с л и н Е. С. Новые химические изобретения. М., «Знание», 1967.
61. Не дин В. В. и др. Взрывоопасность металлических порошков. Киев, «Наукова думка», 1971.
62. Никифоров В. С., Б а х м а н Н. Н. Влияние добавки окиси железа на горение конденсированных смесей. — «Физика горения и взрыва», 1869, Т. б, вып. 2, с. 270.
63. Николаев А. Ф. Синтетические полимеры. М.—Л., «Химия», 1966.
64. Николаев Н. С. и др. Химия галоидных соединений фтора. М., «Наука», 1968.
65. П л а н о в с к и и А. Н., Р а м м В. М., К о г а н С. В. Процессы и аппараты химической технологии. М., «Химия», 1968.
66. П л и н е р Ю. А., И г н а т е н к о Г. Ф. Восстановление окислов металлов алюминием. М., Металлургиздат, 1967.
67. По зин М, Е. Технология минеральных солей, Т. 1—Е, М., «Химия», 1970.
68. П о х и л П. Ф., МальцевВ. М., Зайцев В. М. Методы исследования процессов горения и взрыва. М., «Наука», 1969.
69. Процессы горения. Сборник статей. Под ред. Б. Льюис и др. Перев. с англ. М., i961, Физматгиз.
70. Реактивные двигатели. Сборник статей. Под ред. О. Ланкастера, Перев. с англ. М., Воениздат, 1962.
71. Романов В. В., Коррозия магния. Изд-во АН СССР, 1961.
72. Ро мод а но в а Л. Д., По хил П. Ф. О горении состава Ее20з+ +А1+А120з.—«Физика горения и взрыва», 1969, Т. 5, вып. 2, стр. ;277.
73. Ромоданова Л. Д., По пеки н В. И., Апин А. Я. и др. О связи скорости горения смесевого состава с химическим строением горючего. —«Физика горения и взрыва», 1970, Т. 6, вып. 4, с. 419.
74. Р о м о д а н о в а Л. Д., П о х и л П. Ф. Влияние активности порошков алюминия и магния на горение составов.—«Физика горения и взрыва», 1970, Т. 6, вып. ill, с. ,12&
75. Самсонов Г. В. и др. Физико-химические свойства элементов, справочник. Киев, «Наукова думка», 1965.
76. С а м с о н о в Г. В., Ч и с т я к о в Ю. Д. Металлотермическне методы в химии и металлургии.—«Успехи химии», 1956, т. 25, вып. 10. с. 1223— 1248.
77. Сарнер С. Химия ракетных топлив. Перев. с англ. -Под ред. В. А. Ильинского. М., «Мир», 1967.
78. Саттон и др. Твердые топлива для газогенераторов.—«Вопросы ракетной техники», 1968, вып. 4, с. 48.
79. С а у д е р с Дж. X., Ф р и ш К. К. Химия полиуретанов. М., «Химия», 1968.
80. Сафронов Л. Т. Ночное воздушное фотографирование. М., Воениздат, 1947.
81. Сиденко П. М. Измельчение в химической промышленности. М.» «Химия», 1968.
82. Современные проблемы порошковой металлургии. Сборник статей. Киев, «Наукова думка», 1970.
83. Солодовников В. М. Пиротехника (производство и сжигание фейерверков). М., Оборонгиз, 1938.
84. Теория взрывчатых веществ. Сборник статей. Под ред. К. К. Андреева и др. М., Оборонгиз, 1963.
85. Теория взрывчатых веществ. Сборник статей. Под ред. К. К. Андреева. М., «Высшая школа», 1967.
86. Термодинамические свойства индивидуальных веществ. Справочник. Под ред. В. П. Глушко. М., Изд-во АН СССР, 1962, Изд. 2-е.
87. Т о м а ш о в Н. Д., Ч е р н о в а Г. П. Пассивность и защита металлов от коррозии. М., «Наука», 1965.
88. Фатьянов А. И. Судовые пиротехнические средства. М., «Транспорт», 1968.
89. Федорченко И. М., Андриевский Р: М. Основы порошковой металлургии. Киев, «Наукова думка», 1961.
90. Ф о г е л ь з а н г А. Е. и др. Влияние природы окислителя, содержащегося во взрывчатом соединении, на скорость его горения. ДАН СССР, 1971, Т. 199, вып. 6, с. ilG96.
91. Химия и технология редких и рассеянных элементов, Т. .1—Q. Под ред. К. А. Большакова. М., «Высшая школа», 1968—1969.
92. Цытович П. С. Опыт рациональной пиротехники. СПБ, 1894.
93. Ш а р о н о в В. В. Свет и цвет. М., Физматгиз, 1961.
94. Ш е в ч у к М. К. Зажигательные средства и защита от них. М., Воениздат, 19Q1.
95. Шершень А. И. Аэрофотосъемка. М., Геодезиздат, 1956.
96. Шидловский А. А. Основы пиротехники. М., «Машиностроение», 1964, 3-е изд.
97. Ш и д л о в с к и и А. А., С и д о р о в А. И., А н т о н о в В. М. Искусство управления огнем. М., «Наука и жизнь», 1971, вып.; 6, с. 82.
98. Шидловский А. А. Термическое разложение аммиачной селитры с различными добавками.— «Известия вузов СССР.. Химия и химическая тех-иология», 19(57. Т. !!, вып. 3, с. 105, 'I960. Т. 3, вып. и, стр. 405.
99. Шидловский А. А., Шмагин Л. Ф. Термическое разложение и горение перхлората аммония.—«Известия вузов СССР. Химия и химическая технология», 11862. Т. 15, вып. 4, с. 529.
100. Шиллинг Н. А. Взрывчатые вещества и снаряжение боеприпасов. М., Оборонгиз, 1946.
101. Шумахер И. Перхлораты, их свойства, производство и применение. М., Химиздат, 1963.
102. Э в а н с Ю. Р. Коррозия и окисление металлов. М., Машгиз, 1962.
103. Эверест Д. Химия бериллия. М., «Химия», 1968.
104. Юрьев П. Г. Зажигательные вещества и средства их применения.— «Журнал Всероссийского химического общества им. Д. И. Менделеева», 1968, Т. 13, вып. 6, с. 648.
105. Akhagen R. Grundlagende Pyroteknik. Forsvarets. Forskning,Sians-talt. Eskilstuna, 1966.
106. Backer C.R. Infantry, 1969, vol. 59, No. 8—9, p. 39.
107. Becher. «Pyrotechnik» in Ullman's Encyklopadie der technischen Chemie. Munchen — В., 1963, 3 Auflage, Bd. 14, S. 490.
108. В 1 ackman A. W., Kuehl D. H. ARS — Journal, 1961, vol 31, No. 9, p. 1265.
109. В 1 а у N. J., D u n s t a n I. Chemical Problems connected with stability of Explosives, 2, 1970 Sweden (2-nd Symposium on chem. Problems).
110. Bombs a. Bomb Components. Techn. Man. 9—1325—200, Washington, 1966.
111. Bond В. D., Jacobs P. W. M. Combustion a. Flame. 1966, vol. 10, p. 349.
112. Brownlow С. Av. Week a. Space Techn. 1965, vol. 82, No. 20, p. 52.
113. С avel 1 W. W. Perkins W. E., Caven J. J. Ordnance, 1967, vol. 52, No. 283, p. 66.
114. dark F. P. Special Effects in Motion Pictures. N.—Y. 1966.
115. Douda В. J. Optical Soc. of America, 1970, vol. 60, No. 8, 9, pp. 1116, 1257.
116. D u G a r d i n. Mem. poudres, 1958, vol. 40, p. 367.
117. Ellern H. Military a. Civilian Pyrotechnics. N.—Y. 1968.
118. E 11 e r n H. Modern Pyrotechnics. N.—Y., 1961.
119. Engineering Design Handbook. Military Pyrotechnics Series. Part One. AMC Pamphlet, 706—185, 1967.
120. Engineering Design Handbook. Explosives .Series. AMC — Pamphlet, 706—179, 1965, pp. 80—89.
121. F i e s e r L. F. The Scientific Method. N.—Y., 1964.
122. F i e s e r L. F., H а г r i s G. C. Napalm. Ind. Eng. Chem. 1946, vol. 38, No. 8, p. 768.
123. Freem a n E. S., H о g a n V. D., A n d e г s о n D. A. Comb. a. Flame, 1965, vol. 9, No. 1, p. 19:.
124. Gordon S., Campbell C. Analytical Chemistry, 1955, vol. 27, No. 5, p. 1102.
125. Harris R. C. «Compatibility problems» in «Chemical Problems connected with the stability of Explosives» 2, 1970, Sweden.
126. Harrison G. S. J. South African chem. Inst, 1964, vol. 17, No. 1, pp. 14—28.
127.Hartig H. Zflndwaren. Leipzig, 1971.
128. Held M. Explosivstoffe, 1969, Bd. 17, Nr. 8, s. 169—176.
129. Hoizmann R. T. Chemical Rockets a. Flame a. Explosives Technology, N.—Y., 1969.
130. Hossjer К. Foredrage vid Pyrotechnikdagen 1969. Stockholm, 1969.
131. Ide К H„ Koch H. W. Explosivestoffe. 1970, Bd. 18, Nr. 3, s, 56—66.
132. Installation a. Maintenance of Aerial Photographic Equipment. Air Force Manuel, No. 95—3, Washington, 1964.
133 Jacobs P. W. M., Whitehead H. M. Chem. Reviews, 1969, vol. 69, pp. 551—590.
134. J a r v i s A. Comb. a Flame, 1970, vol. 14, No. 3, p. 313.
135. Johansson S. in «Foredrage vid Pyrotechnikdagen». 1969, Stockholm, 1969.
136. Koenen H., IdeK.H., S w а г t K. H. Explosivstoffe. 1961, Bd. 9, Nr. 2, S. 30—42.
137. Lancaster R., Shimizu T. a. oth. Fireworks. Principles and Practice. N.—Y., 1972.
138. 0 h a r t T. C. Elements of Ammunition. N.—Y., 1952.
139. PartelG. Rivista di Ingegneria, 1962, No. 11, p. 1199.
140. Plattner В М. Av. Week a. Space Techn. 1967, vol. 86, No. 7, p. 89.
141. Poppi H. a. oth. Planetry a. Space Science. 1967, vol. 15, No. 2, p. 357.
142. R о s s i n i F. D. a. oth. Selected Values of chem. thermod. Properties. Circular 500. Washington, 1961.
143. R u m p f H. Der Hochrote Hahn. Darmstadt, 1952.
144. Tomlinson W., A u d r i e t h L. J. chem. Educ. 1950, vol. 27, No. 11, p. 606.
145. Utilisation des Elements Pyrotechnique et Explosifs dans les Systemes Spatiaux. Paris, 1969.
146. W a g m a n D. D. a. oth. Technical Note. 270. NBS. Washington. 1965— 1972, No. .1—7.
147. Watkins T. F., С а с k e t J. С., Н а 11 R. С. Chemical Warfare. Pyrotechnics a. Fireworks Industry. London, 1968.
148. W e i n g a r t G. Pyrotechnics. N.—Y., 1968.
149. Zaehringer A. L. Solid Rocket Technology. N.—Y., 1967.
150. Av. -Week a. Space Techn. 1967, vol. 86, No. 7, p. 79:
151. Explosjvstoffe, 1969, Bd. 17, Nr. 1, S. 22.
152. Ordnance, voL 55, No. 296, p. 128.
153. Baldwin К., В i 1 a n z W. Trans. Nucl. Sci. 1964, vol. 11, No. 2, p. 51.
154. Douda В. J. Opt. Soc. of America, 1965, vol. 55, No. 7, p. 787.
155. T e 11 e r E. J. chem. Phys., 1962, vol. 36, No. 4, p. 901.
156. Air Force a Space Digest, 1966, vol. 49, No. 1.
157. La Chaoelle R. Scientific American, 1966, No. 214, p. 99.
158. По хил П. Ф. и др. Горение порошкообразных металлов в активных средах. М., «Наука», 1072.
159. Современная химия ракетного топлива. Под ред. И. И. Моисеева. Перев. с англ. М., Атомиздат, 1972.
160. Мержанов А. Г., Б о р о в и н с к а я И. П. ДАН СССР, 1972, т. 204, вып. 2, с. 366.
ОГЛАВЛЕНИЕ
Предисловие...................................................................................................................... 1
Часть первая
ОБЩИЕ СВОЙСТВА ПИРОТЕХНИЧЕСКИХ СОСТАВОВ И ИХ КОМПОНЕНТОВ
ГлаваI.Общее понятие о пиротехнических средствах и составах ………....…... 1
§ 1. Классификация...............................................................................................…......... 2
§ 2. Горение составов........................................................................................................ 4
§ 3. Требования, предъявляемые к пиротехническим средствам и составам.............. 5
§ 4. Назначение компонентов.......................................................................................... 6
§ 5. Возможные высокоэкзотермические реакции ....................................................... 7
§ 6. Способность к горению различных веществ и смесей.......................................... 9
Глава II.Окислители ..................................................................................................... 10
§ 1. Выбор окислителей................................................................................................... 11
§ 2. Свойства окислителей.............................................................................................. 13
§ 3. Гигроскопичность..................................................................................................... 19
§ 4. Технические требования.......................................................................................... 22
Глава III.Горючие........................................................................................................... 22
§ 1. Выбор и классификация........................................................................................... 22
§ 2. Высококалорийные горючие................................................................................... 25
§ 3. Технические требования к порошкам металлов..................................................... 32
§ 4. Производство порошков металлов.......................................................................... 33
§ 5. Неорганические горючие средней калорийности.................................................. 34
§ 6. Органические горючие.............................................................................................. 36
Глава IV.Связующие — органические полимеры ................................................. 39
§ 1. Роль связующих. Испытание прочности звездок................................................... 39
§ 2. Факторы, влияющие на прочность ........................................................................ 39
§ 3. Классификация связующих. Их свойства ............................................................. 41
Глава V. Принципы расчета пиротехнических составов ..................................... 45
§ 1. Двойные смеси......................................................................................................... 45
§ 2. Тройные и многокомпонентные смеси ................................................................. 48
§ 3. Составы с отрицательным кислородным балансом ................................................. 49
§ 4. Металлохлоридные составы ...................................................................................... 51
§ 5. Составы с фторным балансом ................................................................................... 53
Глава VI. Теплота горения, газообразные продукты и температура горения составов….......................................................................................................................... 54
§ 1. Вычисление теплоты горения ................................................................................... 54
§ 2. Экспериментальное определение.............................................................................. 58
§ 3. Связь между назначением составов и теплотой их горения.................................... 59
§ 4. Газообразные продукты горения................................................................................ 59
§ 5. Определение температуры горения........................................................................... 63
§ 6. Экспериментальное определение ............................................................................. 67
§ 7. Связь между назначением состава и температурой горения.................................. 72
Глава VII. Чувствительность составов........................................................................ 72
§ 1. Определение чувствительности к тепловым воздействиям................................... 73
§ 2. Определение чувствительности к механическим воздействиям .......................... 75
§ 3. Факторы, влияющие на чувствительность составов к начальному импульсу..... 78
Глава VIII. Горение составов....................................................................................... 84
§ 1. Механизм горения..................................................................................................... 84
§ 2. Факторы, влияющие на скорость горения ............................................................. 87
Глава IX. Взрывчатые свойства составов................................................................ 97
Глава X. Физическая и химическая стойкость составов....................................... 105
§ 1. Физические изменения............................................................................................ 105
§ 2. Химические изменения........................................................................................... 106
§ 3. Методы определения гигроскопичности и химической стойкости.................... 111
§ 4. Допустимые сроки хранения .................................................................................. 113
Часть вторая
СПЕЦИАЛЬНЫЕ СВОЙСТВА ОТДЕЛЬНЫХ ВИДОВ ПИРОТЕХНИЧЕСКИХ СОСТАВОВ
Глава XI. Осветительные составы.............................................................................. 114
§ 1. Осветительные составы и средства ........................................................................ 114
§ 2. Краткие сведения об устройстве осветительных средств .................................... 115
§ 3. Световые характеристики осветительных составов и средств.............................. 121
§ 4. Тепловое и люминесцентное излучение ................................................................. 124
§ 5. Специальные требования к осветительным составам; двойные смеси ............... 126
§ 6. Многокомпонентные осветительные составы ....................................................... 131
§ 7. Факторы, влияющие на эффективность осветительных составов и средств....... 136
§ 8. Краткие сведения о пиротехнических ИК-излучателях ........................................ 140
§ 9. Фотометрирование и радиометрирование пламен пиротехнических составов... 144
Глава XII. Фотоосветительные составы .................................................................... 148
§ 1. Ночное воздушное фотографирование.................................................................... 148
§ 2. Фотоматериалы ........................................................................................................ 150
§ 3. Фотоавиабомбы ....................................................................................................... 152
§ 4. Фотопатроны ........................................................................................................... 155
§ 6. Фотосоставы. Факторы, влияющие на светотехнические характеристики вспышек и свойства фотосоставов .................................................................................................... 156
§ 6. Методы определения характеристик фотовспышек .............................................. 162
§ 7. Световые имитаторы, фотозаряды-маркеры .......................................................... 163
Глава XIII. Трассирующие составы ........................................................................... 164
§ 1. Трассирующие средства............................................................................................ 164
§ 2. Краткие сведения об устройстве трассеров…......................................................... 165
§ 3. Трассирующие составы.…........................................................................................ 171
§ 4. Воспламенительные составы для трассеров …...................................................... 174
§ 5. Факторы, влияющие на эффективность трассирующих составов и трассеров... 174
§ 6. Видимость трассы и расчет необходимой силы света пламени........................... 175
§ 7. Испытания трассеров................................................................................................ 177
Глава XIV. Составы сигнальных огней..................................................................... 178
§ 1. Системы сигнализации. Требования, предъявляемые к составам....................... 178
§ 2. Характер излучения пламени.................................................................................. 179
§ 3. Разработка рецептов составов и основные требования к их компонентам ....... 180
§ 4. Составы желтого огня.............................................................................................. 181
§ 5. Составы красного огня ............................................................................................ 183
§ 6. Составы зеленого огня ............................................................................................ 186
§ 7. Составы синего и белого огня ................................................................................. 187
§ 8. Методы испытания.................................................................................................... 188
Глава XV. Зажигательные составы............................................................................. 191
§ 1. Зажигательные средства и зажигательные составы. Основные требования к составам............................................................................................................................. 191
§ 2. Классификация зажигательных средств и составов ............................................. 192
§ 3. Составы с порошками металлов и окислителями - солями и применение их в малокалиберных снарядах ................………………………….……………………… 194
§ 4. Термитно-зажигательные составы......................................................................... 199
§ 5. Сплав "электрон" и его применение...................................................................... 203
§ 6. Смеси на основе нефтепродуктов. Напалм…....................................................... 203
§ 7. Фосфор и его соединения ...................................................................................... 210
§ 8. Галоидные соединения фтора …........................................................................... 211
§ 9. Прочие зажигательные вещества и смеси ……................................................... 213
§ 10. Методы испытания зажигательных составов ................................................... 214
Глава XVI. Составы маскирующих дымов…….................................................... 216
§ 1. Общие сведения об аэрозолях…........................................................................... 216
§ 2. Способы получения аэрозолей…......................................................................... 219
§ 3. Составы маскирующих дымов и предъявляемые к ним требования................ 221
Глава XVII Составы цветных дымов..................................................................... 225
§1. Цветные облака и способы их получения............................................................. 225
§ 2. Красители................................................................................................................ 227
§3. Составы цветных дымов…..................................................................................... 228
Глава XVIII Твердые пиротехнические топлива.................................................. 232
§ 1. Классификация и энергетические характеристики ............................................ 232
§ 2. Эксплуатационные требования............................................................................. 242
§ 3. Окислители............................................................................................................. 243
§ 4. Органические и металлические горючие............................................................ 246
Глава XIX Безгазовые составы ...................................................................... 247
Глава XX Воспламенительные составы. Газогенераторные составы. Прочие виды составов.……………………………………………………………………………... 249
§ 1. Воспламенительные составы и предъявляемые к ним требования................. 249
§ 2. Воспламенительные составы для ракетных двигателей................................... 251
§ 3. Газогенераторные составы.................................................................................. 252
§ 4. Прочие виды составов......................................................................................... 254
Глава XXI Применение пиротехнических составов в народном хозяйстве... 255
§1. Составы для получения химикатов..................................................................... 255
§ 2. Использование энергии пиротехнических составов........................................ 257
§ 3. Спичечные составы …........................................................................................ 260
§ 4. Фейерверочные составы......................................................................…........... 261
Глава XXII Основные технологии и оборудование пиротехнического производства...............……………………………………………………….…..... 263
§ 1. Подготовка компанентов................................................................................... 265
§ 2. Приготовление составов…................................................................................ 269
§ 3. Уплотненеие составов........................................................................................ 272
§ 4. Снаряжение и сборка изделий........................................................................... 275
ПРИЛОЖЕНИЯ....................................................................................................... 276
СПИСОК ЛИТЕРАТУРЫ……….......................................................................... 278
– Конец работы –
Используемые теги: Шидловский, развитие, химии, физики, горения0.074
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: А. А. Шидловский: Развитие химии и физики горения
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов