рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Образование
- /
- ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ
Реферат Курсовая Конспект
ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ
ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ - раздел Образование, Высшее Профессиональное Образование ...
ВЫСШЕЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАНИЕ
Ю. Д.СЕМЧИКОВ
ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ
Допущено
Министерством образования Российской Федерации
в качестве учебника для студентов высших учебных заведений,
обучающихся по специальности 011000 «Химия»
и направлению 510500 «Химия»
2-е издание, стереотипное

УДК 541. 64 ББК 24. 7я73 С30
Рецензенты:
доктор хим. наук, профессор, засл. деятель науки РФ В.П. Шибаев;
доктор хим. наук, профессор, засл. деятель науки РФ В.П. Зубов;
академик РАН Г. А. Абакумов
Семчиков Ю. Д.
С30
Высокомолекулярные соединения: Учеб. для вузов / Юрий Денисович Семчиков. - 2-е изд., стер. - М.: Издательский центр «Академия», 2005. - 368 с.
ISBN 5-7695-1928-2
В учебнике рассмотрены современные представления о строении, свойствах, синтезе и химических превращениях полимеров, приведены сведения о важнейших природных и синтетических полимерах. Книга содержит все основные разделы физики и химии полимеров, включая сведения о последних достижениях в этих областях. Широкий охват материала, наряду с фундаментальностью, доступностью и иллюстративностью изложения, позволит читателю и, прежде всего, студенту, сформировать полную и ясную картину о физической природе и особенностях полимерного состояния вещества, не прибегая к разрозненным сведениям из отдельных учебных пособий.
Для студентов химических факультетов университетов. Может быть использован студентами и аспирантами химических специальностей других вузов, научными сотрудниками и инженерами, работающими в области высокомолекулярных соединений.
УДК 541. 64
ББК 24. 7я73
©Семчиков Ю.Д., 2003
©Издательский центр «Академия», 2005
ISBN 5-7695-1928-2
ОТ АВТОРА
Данный учебник предназначен для обучения студентов химических факультетов университетов по специальности 011000 «Химия» в рамках преобладающей в… Учебник в целом соответствует новой программе «Высокомолекулярные соединения»,… Основной мотив, побудивший меня написать эту книгу, связан с отсутствием до настоящего времени современного учебника…ГЛАВА 1. ОБЩИЕ СВЕДЕНИЯ О ВЫСОКОМОЛЕКУЛЯРНЫХ
СОЕДИНЕНИЯХ
Особенности полимерного состояния вещества
Полимеры и наука о полимерах
В зависимости от величины относительной молекулярной массы, далее называемой просто молекулярной массой, химические соединения подразделяют на три… Процесс образования макромолекул из мономеров называется полимеризацией. В… Рассмотрим на примере виниловых мономеров CH2=CHZ, где Z - алкил, арил или любой другой заместитель, общую формулу…Различия в свойствах высоко- и низкомолекулярных соединений
Макромолекулы полимеров, в отличие от молекул низкомолекулярных веществ, являются нелетучими, для них характерны меньшие скорости диффузии, а для… L=nl, (1.1)Образование, получение и распространение полимеров
В соответствии с распространенностью в окружающем нас мире полимеры располагаются в ряд: природные неорганические полимеры >> природные… Синтетические полимеры. Искусственные полимерные материалы (Формулы полимеров,… Практически сразу же промышленное производство полимеров развивалось в двух направлениях - путем переработки природных…Таблица 1. 1 Содержание различных веществ в теле человека
| Тип вещества | Массовый, % |
| Вода | 60-80 |
| Сухой остаток: | 20-40 |
| белки | 15-20 |
| жиры | 3-20 |
| полисахариды | 1-15 |
| низкомолекулярные соединения | <2 |
| нуклеиновые кислоты | <0,1 |
Полисахариды образуются из низкомолекулярных соединений общей формулы СnН2nOn, называемых сахарами или углеводами. Для Сахаров характерно наличие альдегидной или кетонной групп, в соответствии с этим первые называются альдозами, вторые - кетозами. Среди Сахаров с n = 6, называемых гексозами, имеется 16 изомерных альдогексоз и 16 кетогексоз. Однако только четыре из них (a-галактоза, d-манноза, d-глюкоза, d-фруктоза) встречаются в живой клетке. Биологическая роль Сахаров определяется тем, что они являются источником энергии, необходимой организму, которая выделяется при их окислении, и исходным материалом для синтеза макромолекул.
В последнем случае большое значение имеет способность Сахаров образовывать циклические структуры, что иллюстрируется ниже на примере глюкозы и фруктозы:
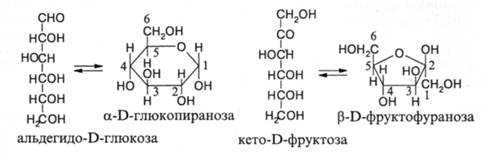
В водном растворе глюкоза содержит 99, 976% циклического изомера. У кетогексоз циклические изомеры пятичленные. Циклические молекулы моносахаридов могут связываться между собой с образованием так называемых гликозидных связей путем конденсации гидроксильных групп.
Наиболее распространены полисахариды, повторяющиеся звенья которых являются остатками a-D-глюкопиранозы или ее производных. Наиболее известна и широко применяема целлюлоза. В этом полисахариде кислородный мостик связывает 1- и 4-й атомы углерода в соседних звеньях, такая связь называется а-1, 4-гликозидной:
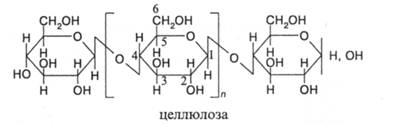
Химический состав, аналогичный целлюлозе, имеют крахмал, состоящий из амилозы и аминопектина, гликоген и декстран. Отличие первых от целлюлозы состоит в разветвленности макромолекул, причем амилопектин и гликоген могут быть отнесены к сверхразветвленным природным полимерам, т.е. дендримерам нерегулярного строения. Точкой ветвления обычно является шестой атом углерода a-D-глюкопиранозного кольца, который связан гликозидной связью с боковой цепью. Отличие декстрана от целлюлозы состоит в природе гликозидных связей - наряду с а-1,4-, декстран содержит также а-1,3- и а-1,6-гликозидные связи, причем последние являются доминирующими.
Химический состав, отличный от целлюлозы, имеют хитин и хитозан, но они близки к ней по структуре. Отличие заключается в том, что при втором атоме углерода a-D-глюкопиранозных звеньев, связанных а-1,4-гликозидными связями, ОН-группа заменена группами -NНСН3СОО в хитине и группой -NH2 в хитозане.
Целлюлоза содержится в коре и древесине деревьев, стеблях растений: хлопок содержит более 90 % целлюлозы, деревья хвойных пород - свыше 60 %, лиственных - около 40%. Прочность волокон целлюлозы обусловлена тем, что они образованы монокристаллами, в которых макромолекулы упакованы параллельно одна другой. Целлюлоза составляет структурную основу представителей не только растительного мира, но и некоторых бактерий.
В животном мире в качестве опорных, структурообразующих полимеров полисахариды «используются» лишь насекомыми и членистоногими. Наиболее часто для этих целей применяется хитин, который служит для построения так называемого внешнего скелета у крабов, раков, креветок. Из хитина деацетилированием получается хитозан, который, в отличие от нерастворимого хитина, растворим в водных растворах муравьиной, уксусной и соляной кислот. В связи с этим, а также благодаря комплексу ценных свойств, сочетающихся с биосовместимостью, хитозан имеет большие перспективы широкого практического применения в ближайшем будущем.
Крахмал относится к числу полисахаридов, выполняющих роль резервного пищевого вещества в растениях. Клубни, плоды, семена содержат до 70% крахмала. Запасаемым полисахаридом животных является гликоген, который содержится преимущественно в печени и мышцах.
Функцию запасаемого питательного продукта выполняет инулин, который содержится в спарже и артишоках, что придает им специфический вкус. Его мономерные звенья пятичленны, поскольку фруктоза относится к кетоам, в целом же этот полимер построен так же, как полимеры глюкозы.
Прочность стволов и стеблей растений, помимо скелета из целлюлозных волокон, определяется соединительной растительной тканью. Значительную ее часть в деревьях составляет лигнин - до 30 %. Его строение точно не установлено. Известно, что это относительно низкомолекулярный (М ~ 104) сверхразветвленный полимер, образованный в основном из остатков фенолов, замещенных в орто-положении группами -ОСН3, в пара-положении группами -СН=СН-СН2ОН. В настоящее время накоплено громадное количество лигнинов как отходов целлюлозно-гидролизной промышленности, но проблема их утилизации не решена. К опорным элементам растительной ткани относятся пектиновые вещества и, в частности пектин, находящийся в основном в стенках клеток. Его содержание в кожуре яблок и белой части кожуры цитрусовых доходит до 30%. Пектин относится к гетерополисахаридам, т.е. сополимерам. Его макромолекулы в основном построены из остатков D-галактуроновой кислоты и ее метилового эфира, связанных a-1,4-гликозидными связями:
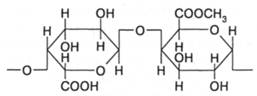
Из пентоз значение имеют полимеры арабинозы и ксилозы, которые образуют полисахариды, называемые арабинами и ксиланами. Они, наряду с целлюлозой, определяют типичные свойства древесины.
Упомянутый выше пектин относится к гетерополисахаридам. Помимо него, известны гетерополисахариды, входящие в состав животного организма. Гиалуроновая кислота входит в состав стекловидного тела глаза, а также жидкости, обеспечивающей скольжение в суставах (она находится в суставных сумках). Другой важный полисахарид животных - хондроитинсульфат - содержится в ткани и хрящах. Оба полисахарида часто образуют в организме животных сложные комплексы с белками и липидами.
Белки. В животном мире в качестве опорного, структурообразующего полимера обычно выступают белки. Эти полимеры построены из 20 типов так называемых а-аминокислот общей формулы:
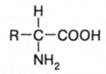
В табл. 1.2 представлены важнейшие аминокислоты, образующие белки. Остатки аминокислот связаны в макромолекулы белка пептидными связями, возникающими в результате реакции карбоксильных и аминогрупп. Ниже эта реакция приведена для двух аминокислот - глицина и аланина:
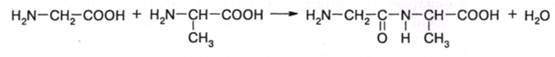
Из табл. 1.2 видно, что большинство аминокислот, из остатков которых построен белок, имеют достаточно простое строение и алифатический радикал. Реже встречаются аминокислоты, содержащие ароматические и насыщенные циклы. Практически все аминокислоты содержат атомы С, Н, О, N, и только цистеин содержит, наряду с ними, атом серы. Образование сульфидных мостиков играет важную роль в процессах структурообразования в белках. В результате соответствующей реакции, протекающей за счет сульфогидрильных групп цистеина, образуются меж- и внутримолекулярные «сшивки» макромолекул белка. Помимо карбоксильной и аминогрупп, аминокислоты белка могут содержать также гидроксильные группы, как, например в серине и треонине.
Таблица 1.2
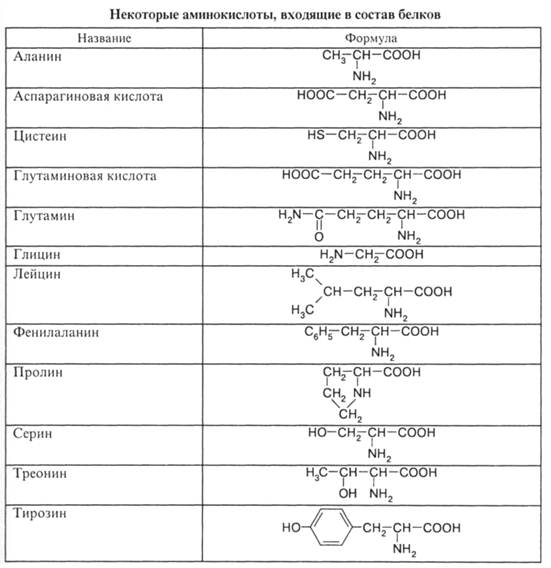
Значение белков в живой природе трудно переоценить. Это строительный материал живых организмов, биокатализаторы - ферменты, обеспечивающие протекание реакций в клетках, и энзимы, стимулирующие определенные биохимические реакции, т.е. обеспечивающие избирательность биокатализа. Наши мышцы, волосы, кожа состоят из волокнистых белков. Белок крови, входящий в состав гемоглобина, способствует усвоению кислорода воздуха, другой белок - инсулин - ответственен за расщепление сахара в организме и, следовательно, за его обеспечение энергией. Молекулярная масса белков колеблется в широких пределах. Так, инсулин - первый из белков, строение которого удалось установить Ф.Сэнгеру в 1953 г., содержит около 60 аминокислотных звеньев, а его молекулярная масса составляет лишь 12000. К настоящему времени идентифицировано несколько тысяч молекул белков, молекулярная масса некоторых из них достигает 106 и более.
Следует подчеркнуть, что многообразие форм жизни обусловлено невероятно большим числом изомерных макромолекул, которые могут быть получены из аминокислот 20 типов. Согласно расчету биохимика Р.Синджа, белок, содержащий 288 аминокислотных остатков, может содержать 10300 изомеров. Каждая из жизненно важных функций, например катализ биохимических реакций, выполняется белком определенного строения и только им. Классическим примером является белок гемоглобина. Изменение порядка чередования около 300 аминокислотных остатков, входящих в его макромолекулу, путем перестановки местами хотя бы пары из них, приводит к тяжелому заболеванию животных - серповидной анемии.
Нуклеиновые кислоты. В 1868 г. швейцарский ученый Фридрих Мишер выделил из ядер клеток фосфорсодержащее вещество, которое он назвал нуклеином. Позднее это и подобные ему вещества получили название нуклеиновых кислот. Их молекулярная масса может достигать 109, но чаще колеблется в пределах 105-106. Исходными веществами, из которых построены нуклеотиды - звенья макромолекул нуклеиновых кислот, являются: сахар, фосфорная кислота, пуриновые и пиримидиновые основания. В одной группе кислот в качестве сахара выступает рибоза, в другой - дезоксирибоза:
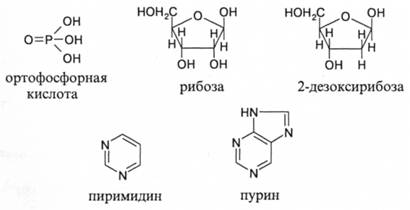
В соответствии с природой сахара, входящего в их состав, нуклеиновые кислоты называются рибонуклеиновой и дезоксирибонуклеиновой кислотами. Общеупотребительными сокращениями являются РНК и ДНК. Нуклеиновые кислоты встречаются во всех живых организмах. Последние делятся на две группы:
прокариоты, к которым относятся одноклеточные, т.е. древние и существующие ныне бактерии, их единственная клетка не имеет ядра и содержит одну двухнитевую спираль ДНК;
эукариоты, которые включают животных, растения, грибы и простейшие, их клетки содержат ядра, в которых сконцентрирована ДНК, тогда как РНК находится как внутри, так и вне ядра.
Как уже упоминалось выше, звенья нуклеиновых кислот, называемые нуклеотидами, содержат остатки фосфорной кислоты, сахара и оснований. Образование цепи из нуклеотидов происходит в результате катализируемой ферментами конденсации групп -ОН остатков сахара и фосфорной кислоты. В результате макромолекулы всех нуклеиновых кислот имеют цепи с регулярным чередованием остатков сахара и фосфорной кислоты, что схематически может быть представлено следующим образом:

Сахара относятся к группе пентоз (см. полисахариды в этом же разделе), основания - к рядам пиримидина и пурина. Упомянутые соединения представлены на схеме. Каждая из нуклеиновых кислот построена из четырех типов нуклеотидов, которые отличаются химической природой основания. ДНК содержит два основания пуринового ряда - аденин и гуанин и два основания пиримидинового ряда - цитозин и тимин. В РНК пуриновые основания те же, пиримидиновые основания несколько отличаются, это цитозин и урацил. Все эти основания присутствуют на приведенных далее схемах, на первой из них изображен фрагмент макромолекулы РНК:
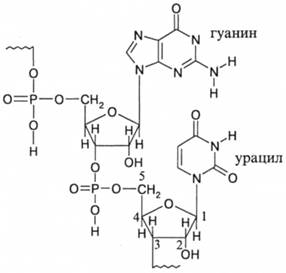
Из этого примера видно, что основная цепь нуклеиновых кислот образуется в результате конденсации гидроксильных групп, связанных с 3'- и 5'-атомами углерода сахара рибозы в РНК (представлено на схеме) и дезоксирибозы в ДНК - с группами ОН фосфорной кислоты. Основание во всех случаях присоединено к 1'-атому сахара. Одна из групп ОН фосфорной кислоты не участвует в реакции поликонденсации. Для дважды этерифицированной фосфорной группы найдено pK = 1,5, следовательно, нуклеиновые кислоты, содержащие несвязанные P-OH-группы, могут быть отнесены к достаточно сильным кислотам.
В 1953 г. Уотсон и Крик установили, что ДНК образует вторичную структуру в виде двойной спирали. Такая спираль образуется при скручивании двух макромолекул ДНК вокруг общей оси и фиксируется водородными связями между основаниями, связанными с разными цепями. Всегда попарно связываются пуриновые и пиримидиновые основания, поскольку только при этом условии сечение двойной спирали остается неизменным по длине. Исходя из принципа достижения максимальной энергии водородных связей, всегда оказываются попарно связанными тимин с аденином и цитозин с гуанином. Из схемы видно, что только в этой комбинации образуется максимальное количество водородных связей из числа возможных, и их энергия близка к максимальной, поскольку три атома, связанные водородной связью, во всех случаях лежат на линии, близкой к прямой:
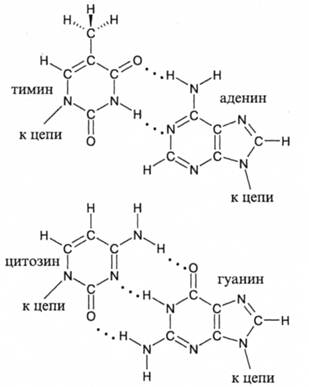
Нуклеиновые кислоты играют наиболее ответственную роль в процессах жизнедеятельности. С их помощью решаются две важнейшие задачи: хранения и передачи наследственной информации и матричный синтез макромолекул ДНК, РНК и белка. Наследственная информация зашифрована в макромолекулах ДНК в виде последовательности расположения четырех типов нуклеотидов, содержащих четыре разных основания. Такие последовательности называются генами. Они расположены в виде «отдельных островов» вдоль всей цепи ДНК, их суммарная длина составляет 3-5 % от общей длины макромолекулы.
К важнейшим процессам матричного синтеза относятся:
репликация, в ходе которой двойная спираль «расплетается» (сразу во многих местах) и на каждой материнской ДНК синтезируется дочерняя, комплементарная первой, таким образом, из исходной спиралиобразуются две идентичные ей; одна из них переносит в новую клетку, образующуюся при делении материнской, наследственную информацию;
транскрипция или синтез на молекулах ДНК так называемой информационной м-РНК, при котором генетическая информация, заложенная в ДНК, «сбрасывается» на м-РНК и кодируется там в виде последовательности расположения нуклеотидов;
трансляция или синтез белка на молекулах м-РНК, в данном случае используется трехбуквенный код, т.е. последовательность из трех нуклеотидов матричной м-РНК определяет тип очередной аминокислоты из 20 возможных, которая должна присоединиться к растущей полипептидной цепи белка.
Все перечисленные реакции катализируются ферментами - белками, а инициирование многих процессов осуществляется с помощью РНК.
Природные неорганические полимеры. Природные неорганические полимеры составляют основу земной коры, толщина которой достигает 15 км (литосфера). Литосфера образовалась и образуется при выходе на поверхность Земли расплавленной магмы, в которой химические реакции протекают при высокой температуре и давлении. Основной горной породой являются базальты. В табл. 1.3 приведены данные по составу базальтовых горных пород, полученных из проб, взятых со дна океанов Земли и лунных морей. Видно, что состав базальтовых пород Земли и ее спутника весьма близок, он состоит в основном из оксида кремния и в значительно меньшей степени из оксидов железа и алюминия. Оксид кремния является типичным полимерным кристаллическим телом, т.е. трехмерным полимером. Наряду с этим, для него известны двухмерные (подобные графиту) и цепные полимеры (рис. 1.1).
Основной структурной единицей всех полисиликатов является тетраэдр SiO4, в вершинах которого расположены атомы кислорода, в центре - атом кремния. Структура полимерного кристаллического тела с регулярной трехмерной структурой из SiO2 аналогична структуре алмаза - трехмерного полимера углерода. В обоих случаях регулярная трехмерная структура может быть получена при совмещении граней структурных единиц - тетраэдров. Подобный полимер встречается в природе в виде прозрачного минерала кварца, известного также как горный хрусталь. Полимерное тело с регулярной трехмерной структурой под названием корунд образует также одна из модификаций Al2O3. Окрашенные формы (за счет примесей) кварца и корунда встречаются в природе в виде драгоценных камней. К наиболее известным из них относятся аметист, топаз, опал (кварц), рубин, сапфир (корунд).
Таблица 1.3 Содержание различных оксидов в базальтовых породах, мас. %
| Оксид | Лунный грунт | Земная кора |
| SiO2 Al2O3 FeO TiO2 MgO CaO | 41-46 7-14 18-22 1-12 7-16 8-12 | 44-53 13-19 7-14 0,9-3,3 4-10 8-12 |
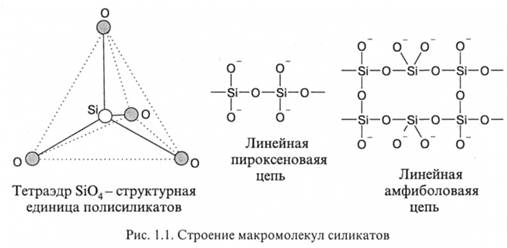
На рис. 1.1 представлены также фрагменты макромолекул линейных и двухмерно сшитых линейных двухтяжевых полисиликатов. Такие структуры могут быть получены при сочетании тетраэдров SiO2 вершинами, при этом, ионам кислорода должны соответствовать свободные вершины. Слоистые структуры SiO4 образуются при сочетании тетраэдров ребрами, при этом один атом кислорода должен оставаться свободным. Линейные макромолекулы SiO2 входят в состав минералов пироксен, энстатит, диопсид, сподумен, амфиболит, тремолит и др. Последние составляют основу природного волокнистого неорганического материала, известного как асбест. В состав многих минералов входят слоистые полимерные структуры SiO2, например в состав талька и каолинита (белой глины), где они чередуются со слоями полимерных гидроксида магния - в первом случае и гидроксида алюминия - во втором.
Помимо полисиликатов в природе широко распространены полимеры алюмосиликатов - линейные, двухмерно и трехмерно сшитые. Среди последних наиболее известны цеолиты с общей формулой MO.Al2O3.xSiO2.yH2O, где М - металл I или II групп. Цеолиты являются прекрасными сорбентами, их удельная поверхность выше, чем угля. Благодаря этому цеолиты широко используются на практике в качестве так называемых молекулярных сит.
Классификация и номенклатура полимеров
Принципы классификации полимеров
Наиболее развита классификация, основанная на химическом строении полимера (Коршак В. В., Платэ Н.А., Ренард Т.Л. и др. Общая классификация полимеров и ее применение для поиска информации о полимерах // ЖВХО им. Д. И. Менделеева. 1977. Т. 22. № 4. С. 393-397.). Последовательность деления полимеров на классы, подклассы, группы, подгруппы и виды основана на следующих классификационных признаках, соответствующих пяти ступеням детализации:
| I | Класс | наличие одинаковых или разных атомов в основной цепи |
| II | Подкласс | природа элементов основной цепи |
| III | Группа | тип связей и структур основной цепи |
| IV | Подгруппа | природа заместителей в основной цепи |
| V | Вид | строение повторяющегося звена |
В соответствии с этой классификацией полимеры «разделяют» на два больших класса - гомоцепные и гетероцепные полимеры. Первый из них делится на несколько подклассов - карбоцепные, кремнийцепные (полисила-ны), полимеры серы, олова и некоторые другие. Во всех случаях основная цепь построена из одинаковых молекул. Класс гетероцепных полимеров разделяется на значительно большее число подклассов - оксикарбоцепные, азоткарбоцепные, оксиалюминийцепные, оксикарбоазотцепные и др. В соответствии с природой связей и структур основной цепи подклассы делятся на группы, содержащие в основной цепи одинарные (полианы), двойные (полиены) и тройные (полиины) связи, ароматические (поликарбарилены) и гетероциклы и т.д. По природе заместителя группы делятся на подгруппы, например, полиолефины, галоидсодержащие полианы и т.п. Строение повторяющегося звена подгруппы является пятой конечной ступенью данной классификации, которая приводит к конкретному полимеру. Ниже приведены все ступени классификации карбоцепных полимеров вплоть до конкретных полимеров - полиолефинов:
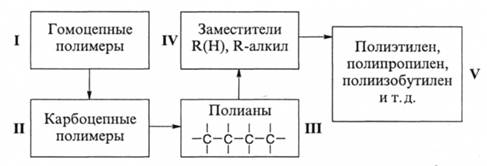
Данная система позволяет систематизировать накопленную информацию по полимерам и проводить их автоматизированный поиск.
Помимо рассмотренной классификации существуют и другие - менее детализированные. Так, по происхождению полимеры делятся на синтетические и природные, последние, в свою очередь, делятся на неорганические и органические, называемые также биополимерами. В соответствии с химической природой полимеры делятся на органические, неорганические и элементорганические.
Органические полимеры содержат атомы углерода, водорода, азота, кислорода, галогенов. Примером карбоцепных органических полимеров являются полиолефины и полимеры виниловых мономеров общей формулы [-СН2-СНХ(Н)-]n, где X - арил, галоген, эфирная, нитрильная или другая функциональная группа.
Неорганические полимеры не содержат связей С-Н. К гомоцепным неорганическим полимерам относятся линейные модификации серы и селена, к гетероцепным - полифосфонитрилхлорид [-PCl2=N-]n.
Элементорганические полимеры содержат как органические, так и неорганические группы. Примером гетероцепного элементорганического полимера является полидиметилсилоксан [-Si(CH3)2O-]n. К элементорганическим полимерам можно также отнести полиорганофосфазены [-PR2=N-]n, которые получаются при замене атомов хлора в полифосфонитрилхлориде на органические группы.
Помимо классификации, основанной на химической природе полимера, весьма распространена классификация, рассматривающая строение макромолекулы в целом. Для макромолекул цепных полимеров характерна большая или меньшая гибкость, поэтому пространственные формы макромолекул определяются как порядком расположения атомов, так и гибкостью макромолекулярной цепи. В связи с этим различают такие понятия, как конфигурация и конформация цепи.
Конфигурация цепи отражает химическую структуру макромолекулы. Под конфигурацией понимается взаимное расположение атомов вытянутой цепи, определяемое фиксированными значениями длин связей и валентных углов. Конфигурация цепи может быть изменена лишь путем разрыва химических связей, т.е. путем химической реакции. Вращение вокруг связей основной цепи не может ее изменить. Вследствие теплового движения отрезков гибкой цепи макромолекулы принимают различные, постоянно меняющиеся формы или конформации.
Под конформацией понимается пространственное расположение атомов макромолекулы в данный момент времени, определяемое фиксированными значениями длин связей, валентных углов и углов вращения вокруг связей основной цепи. Одна конформация переходит в другую путем простого вращения вокруг связей основной цепи, поэтому макромолекула может реализовать последовательно множество конформаций.
Строение макромолекулы цепного полимера определяет конфигурация основной цепи, т.е. хребта или скелета макромолекулы. Основные группы приведены на рис. 1.2, здесь же приведено условное изображение конфигурации дендримера - сверхразветвленного полимера с регулярным ветвлением.
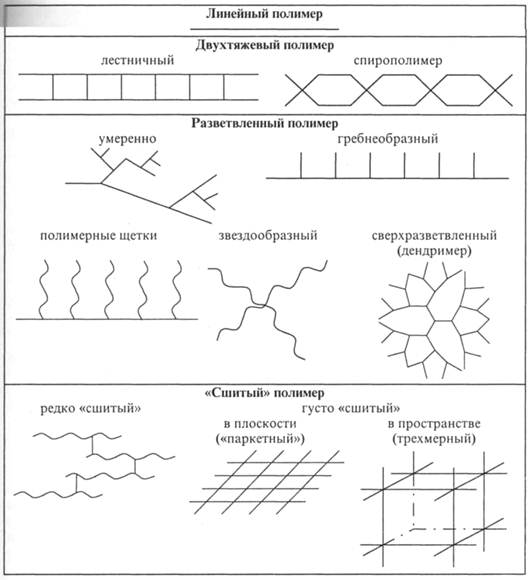
Рис. 1.2. Схематическое изображение различных структур полимерных молекул
Промышленное производство полимеров практически полностью базируется на цепных полимерах, среди которых наиболее распространены линейные, а среди последних - карбоцепные линейные полимеры. К ним относятся наиболее крупнотоннажные полимеры - полиолефины [-CH2-CH2(R)-]n, поливинилхлорид [-СН2-СНСl-]n, полистирол [-CH2-CHC6H5-]n.
Лестничные и спирополимеры имеют общее в строении. Формально их можно рассматривать как полимеры циклов, соединенных в одном случае через атом, в другом - через два атома. К лестничным полимерам относятся циклизованные полидиены, например циклизованный полибутадиен:
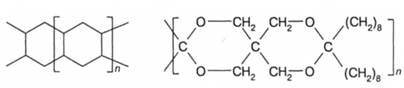
Примером спирополимера является полиспирокеталь, приведенный на схеме. Наиболее ценным свойством лестничных и, в меньшей степени, спирополимеров является высокая термостабильность.
Распространенными представителями гребнеобразных полимеров являются полимеры акриловых и метакриловых эфиров, имеющих в качестве заместителя в эфирной группе производные длинноцепочных спиртов, например цетилового:
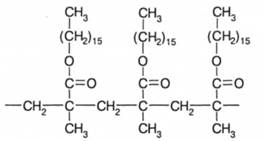
У гребнеобразных полимеров указанного типа боковые группы способны к кристаллизации, что приводит к жидкокристаллическому состоянию полимера в целом. Макромолекулы гребнеобразных полимеров содержат относительно короткие ответвления. Если этими ответвлениями являются макромолекулярные цепи, то соответствующая структура называется щеткой. Последняя может быть сформирована на сферической или плоской поверхности. Особенностью этой структуры являются вытянутые цепи щетки, тогда как линейные гибкоцепные макромолекулы самопроизвольно свертываются в клубки.
Наиболее известным примером статистически разветвленного полимера является полиэтилен, полученный методом высокого давления. При синтезе этого полимера вследствие протекания реакции передачи цепи на полимер через каждые 4-5 мономерных звеньев образуется ответвление от основной цепи, от последнего вновь образуются ответвления и т.д. Разница в свойствах полиэтилена с линейными и разветвленными макромолекулами весьма заметна. Первый имеет большие плотность, прочность и меньшую прозрачность, что связано с повышенной степенью кристалличности по сравнению с полиэтиленом высокого давления. Макромолекулы сверхразветвленных полимеров, в отличие от разветвленных, не имеют явно выраженной основной цепи. Редко сшитые полимеры относятся к цепным, они, как правило, обладают большой прочностью и твердостью по сравнению с линейными, в чем можно убедиться, сравнивая так называемый «сырой» каучук и резину. «Сшивка» в плоскости приводит к образованию так называемых «паркетных» полимеров. Вещества, находящиеся в данном полимерном состоянии, проявляют тенденцию к расслаиванию, что характерно для таких материалов, как графит и слюда. В графите гибридизация атомов углерода - sp2 ,он имеет плоскосшитую или паркетную конфигурацию макромолекулы. Повторяющейся геометрической фигурой этой конфигурации является правильный шестигранник, макромолекулы расположены в плоскости, так как такое расположение обеспечивает сопряжение и делокализацию p-электронов углерода. Благодаря последнему обстоятельству, графит является очень хорошим проводником электрического тока. В алмазе атомы углерода имеют sp3-гибридизацию, каждый атом углерода связан σ-связью с четырьмя другими атомами, следовательно, алмаз является пространственно «сшитым» полимером углерода с предельной плотностью «сшивки». Алмаз является самым твердым из известных материалов, графит - один из наиболее мягких.
Приведенная выше классификация рассматривает лишь «скелет» макромолекулы. Если же учитывать пространственное расположение заместителей основной цепи, то линейные полимеры разделяются на стереорегулярные, в макромолекулах которых существует строгий порядок в расположении заместителей относительно плоскости зигзага основной цепи, и стерео-нерегулярные. Первые, как правило, являются кристаллическими полимерами, вторые - за редким исключением аморфны. Например, поливинилхлорид является стереонерегулярным полимером, однако, содержит некоторое количество кристаллической фракции.
В соответствии со свойствами, определяющими область применения, полимеры делятся на волокнообразующие, пластомеры и эластомеры.
Одним из важнейших свойств, определяющих область применения полимеров, является обратимая деформация. В соответствии с величиной обратимой деформации растяжения полимеры указанных классов располагаются вряд:
эластомеры >> пластомеры > волокна,
которому отвечает относительная деформация порядка 103, 1, 10-3 %.
Волокна производятся из весьма ограниченного круга полимеров. К ним относятся целлюлоза и белки из природных полимеров, полиамиды, полиэфиры, полипропилен и полиакрилонитрил - из синтетических.
Пластомеры используются в виде полимерных материалов, называемых пластмассами или пластиками, которые подразделяются на пластики общего назначения и инженерные, или конструкционные, пластики. К пластомерам относится весьма широкий круг полимеров. Наиболее крупнотоннажными являются полимеры и сополимеры на основе олефинов, винилхлорида, стирола, акрилатов (производных акриловой и метакриловой кислот), винилацетата, а также полиамиды, фенопласты (полимеры фенола и формальдегида), аминопласты (полимеры мочевины или меламина и формальдегида).
Эластомеры образуют материалы, называемые каучуками и резиной («сшитый» каучук). Круг полимеров, относимых к эластомерам, достаточно узок. К крупнотоннажным относятся полимеры диеновых мономеров (изопрен, бутадиен), полисилоксаны. В меньшем количестве производятся акриловые (сополимер бутилакрилата с акрилонитрилом) и полисульфидные каучуки, содержащие атомы серы в основной цепи. Типичными эластомерами являются такие неорганические полимеры, как линейная сера [-S-]n и полифосфонитрилхлорид [-PCl2=N-]n.
В соответствии со способом переработки в изделия или полуфабрикаты полимеры подразделяются на термопласты и реактопласты. К термопластам относятся полимеры, перерабатываемые путем расплава, такие полимеры имеют относительно небольшую молекулярную массу (порядка 105). Один и тот же полимер может быть переработан через расплав несколько раз, что имеет значение с точки зрения утилизации отходов полимеров. К реактопластам относятся полимеры, изделия из которых получаются в результате химического формования, т.е. при нагревании в форме низкомолекулярного полимера с реакционноспособными группами (преполимер). Образующийся при этом «сшитый» полимер не может быть переработан вторично, что затрудняет его утилизацию.
Тривиальная, рациональная и систематическая номенклатура полимеров
Номенклатура, т.е. принципы и правила образования названий полимеров и сами названия, должна выполнять две основные задачи: позволять воспроизвести… Номенклатура, включающая торговые названия полимеров. Тривиальная номенклатура… Рациональная номенклатура. Рациональная номенклатура широко применяется в настоящее время по отношению к полимерам,…Классификация и номенклатура сополимеров
В 1985 г. Комиссия ИЮПАК (Ring W., Mita I., Jenkins A.D., and Bikales N.M. II Pure Appl. Chem., 57, 1427 (1985). Тальрозе Р.В. Номенклатура сополимеров, базирующаяся на их происхождении // Высокомолек. соед. А. 1986. Т. 28. № 5. С. 1096.) предложила номенклатуру сополимеров, основанную на их происхождении, т.е. исходных мономерах.
По определению, сополимеры являются полимерами, полученными из мономеров более чем одного типа. Классификация сополимеров основана на расположении мономерных звеньев в молекулах. Для обозначения мономерных звеньев в соответствии с тривиальной, рациональной или систематической номенклатурой ниже приведены классы сополимеров и предлагаемые современной номенклатурой названия, два типа мономеров условно обозначены как А и В:
| Тип | Пример |
| неустановленный (т.е. неизвестный) | поли(А-со-В), |
| статистический | поли(А-стат-В), |
| случайный | поли(А-сл-В), |
| чередующийся | поли(А-чер-В), |
| периодический | поли(А-период-В-период-С), |
| блочный | поли А-блок-поли В, |
| привитой | поли А-прив-поли В. |
Статистическими сополимерами называются сополимеры, в которых последовательность расположения мономерных звеньев в цепях подчиняется законам статистики, например, статистике цепей Маркова нулевого (статистика Бернулли), первого и второго порядков.
Случайный сополимер(Более детально статистические и случайные сополимеры охарактеризованы в разделе 6.1.1.) представляет особый случай статистического сополимера. Распределение звеньев в цепи случайного сополимера описывается статистикой Бернулли. Это означает, что присоединение того или другого мономера к цепи сополимера определяется лишь законом случая и не зависит от каких-либо параметров их реакционной способности.
Чередующиеся сополимеры имеют регулярное строение, так как в цепи за А всегда следует В и наоборот. Поэтому их можно также назвать в соответствии с номенклатурой однотяжевых линейных полимеров.
В периодических сополимерах звенья цепи также располагаются регулярным образом, например:
-ABCABCABC- или (ABC)n,
-ABBABBABB- или (ABB)n,
-AABAAABAAABA- или (AABA)n,
-ABACABACABAC- или (ABAC)n.
Для блок- и привитых сополимеров характерно блочное расположение мономерных звеньев в макромолекуле. Под блоком понимается участок макромолекулы, содержащий один тип мономерных звеньев. Ниже показано расположение блоков в привитых и блок-сополимерах:
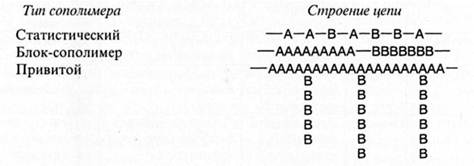
Когда блоки соединены фрагментом (атомом) X, не являющимся частью блоков, название соединительного звена помещается в соответствующем месте, а соединительное слово блок- может быть опущено, например поли А-блок-Х-блок-поли С или поли А-Х-поли С.
При названии привитых сополимеров первое название (А) соответствует звеньям, образующим основную цепь, второе (В) - образующим боковые цепи: поли А-прив-поли В. Если привитые цепи содержат разные мономерные звенья, они разделяются в названии точкой с запятой: поли А-прив-(поли В; поли С).
Параллельно широко используется альтернативная номенклатура, основные положения которой следующие:
1. Сополимер обозначается приставкой «сополи-», за которой следуют названия мономеров (номенклатура, базирующаяся на происхождении). Пример: сополи(стирол/бутадиен).
2. Уточнение типа сополимера (сокращения «блок», «чер» и т.д.) производится с помощью префикса, предшествующего приставке «сополи-» выделенного курсивом. Пример: блок-сополи(стирол/бутадиен).
3. В основную часть названия сополимера включаются только названия мономеров; концевые звенья уточняются до основного названия (с помощью префиксов а или о), а звенья, соединяющие блоки, упоминают после основного названия, используя символ м. Например: блок-сополи(стирол/бутадиен)-μ-диметилсилилен; α-бутил-ω-карбокси-блок-сополи(стирол/бутадиен).
4. Массовую долю, мольную долю, молекулярную массу или степень полимеризации мономерных звеньев в сополимерах обозначают отдельно: вскобках после названия.
Таблица 1.6 Названия основных типов сополимеров
| Тип (класс) сополимера | Соединительное слово | Исходные мономеры | Названия по номенклатуре | |
| систематической | альтернативной | |||
| Неустановленный (т.е. неизвестный) | -со- | Стирол, метилметакрилат | Поли(стирол-со-метилметакрилат) | сополи(стирол/метилметакрилат) |
| Статистический | -стат- | Стирол, бутадиен стирол, бутадиен, акрилонитрил | Поли(стирол-стат-бутадиен) поли(стирол-стат-бутадиен-стат-акрилонитрил) | стат-сополи(стирол/бутадиен) стат-сополи(стирол/бутадиен/акрилонитрил) |
| Случайный | -сл- | Этилен, винилацетат | Поли(этилен-сл-винилацетат) | сл-сополи(этилен/винилацетат) |
| Чередующийся | -чер- | Стирол, малеиновый ангидрид | Поли(стирол-чер-малеиновый ангидрид) | чер-сополи(стирол/малеиновый ангидрид) |
| Периодический | -период- | Этиленфенил фосфонит, метилакрилат, двуокись углерода | Поли(этиленфенил фосфонит-период-метилакрилат-период-диоксид углерода) | период-сополи(этиленфенилфосфонит/метилакрилат/диоксид углерода) |
| Блок-сополимер | -блок- | Стирол, бутадиен, метилметакрилат | Поли(стирол-блок-бутадиен-блок-метилметакрилат) | блок-сополи(стирол/бутадиен/метилметакрилат) |
| Привитой сополимер | -прив- | Бутадиен, стирол | Полибутадиен-прив-полистирол | прив-сополи(бутадиен/стирол) |
В табл. 1.6 приведены названия сополимеров разного типа, образованные в соответствии с той и другой номенклатурой.
Молекулярно-массовые характеристики полимеров
Распределение макромолекул по молекулярным массам
Согласно ИЮПАК рекомендуется применять два основных термина (Manual of Symbols and Terminology for Physicochemical Quantities and Units // Pure… относительная молекулярная масса или молекулярный вес (Мr) - отношение средней… Молярная масса выражается в г/моль или кг/моль. Первое предпочтительней, поскольку при этом численные значения…Моменты распределения и средние молекулярные массы
Определение понятия средней ММ полимера при непрерывном распределении базируется на теории случайных величин, каковыми и являются значения ММ… (1.8)Параметр полидисперсности
(1.15) Путем преобразования (1.15) получаем:Стереохимия полимеров
При одном и том же химическим составе мономерных звеньев или повторяющихся групп из нескольких звеньев конфигурация, т.е. пространственное расположение атомов соответствующего отрезка цепи, может существенно различаться, что отражается на свойствах полимера. Причина этого явления связана с химической, геометрической (цис-транс) и энантиоморфной изомерией.
Химическая изомерия звеньев
Этот вид изомерии может быть обусловлен изомеризацией мономерных звеньев в процессе полимеризации, что особенно характерно для олефинов, а также… -СН2-СНХ-СН2-СНХ- «голова» к «хвосту»,Стереоизомерия
Рассмотрим возможное пространственное положение звеньев в полимерах, полученных из монозамещенных этиленов, т.е. в полимерах виниловых мономеров.…Таблица 1.7 Температуры кристаллизации и плавления полидиенов
| Полимер | Изомер | Тк, 0C | Тпл, 0C |
| 1,4-полибутадиен 1,4-полиизопрен | цис- транс- цис- транс- | -95 -83 -73 -58 |
Это объясняется, как правило, большей степенью кристалличности транс-по сравнению с цис-изомерами. 1,4-цис-полиизопрен используется в качестве каучука, по свойствам близкого к натуральному, 1,4-транс-полиизопрен аналогичен балате и гуттаперче, выделяемым из латекса некоторых растений. Эти природные полимеры по свойствам напоминают кожу. Аналогично в качестве каучука используется 1,4-цис-полибутадиен, тогда как 1,4-транс, 1,2-изотактический и 1,2-синдиотактический полибутадиены являются жесткими кристаллизующимися пластиками.
ГЛАВА 2. ФИЗИКА ПОЛИМЕРОВ
Физика макромолекул
Идеальный клубок
Многие свойства цепных макромолекул и полимеров в целом, а также форма и размер первых могут быть предсказаны теоретически на основе анализа модели… Свободно сочлененная цепь. Построить такую цепь, т.е. зафиксировать одну из ее… Положение в пространстве свободно сочлененной цепи определяется набором координат X1, Х2 ... Хn, а вероятность…Реальные цепи. Эффект исключенного объема
Реальные цепи отличаются от идеальных взаимодействием звеньев между собой и с молекулами растворителя. Эти взаимодействия могут быть как… Второе обстоятельство, определяющее влияние объемных взаимодействий на размер… Особую группу представляют системы, в которых растворитель сольватирует цепи. Сольватные оболочки препятствуют…Гибкость цепи
Различают два вида гибкости цепи: термодинамическую (статистическую) и кинетическую (динамическую). Первая является равновесной, она определяется… Поворотно-изомерный механизм гибкости цепи. К гибкоцепным полимерам относятся…Таблица 2.4 Высоты барьеров для типичных потенциалов внутреннего вращения
| Соединение и связь | Высота барьера, кДж/моль | Соединение и связь | Высота барьера, кДж/моль |
| CH3-CH3 | 11,7 | CH3-SH | 4,45 |
| CH3-CH(CH3)2 | 16,4 | CH3-NH2 | 8,0 |
| CH3-C(CH3)3 | 18,5 | CH3-SH3 | 7,1 |
| CH3-CH=CH2 | 8,2 | CF3-CF3 | 18,3 |
| CH3CH2-CH2CH3 | 14,6 | CH3-CH=O | 4,9 |
| CH3-CF3 | 15,5 | CH3-OCH3 | 11,4 |
| CH3-OH | 4,5 | CH3-PH2 | 8,2 |
Если ΔE ≈ kТ, то переход между двумя локальными конформациями или транс-гош-изомеризация может происходить за время 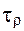 порядка 10-11 с, что отвечает кинетической гибкости цепи. В общем случае:
порядка 10-11 с, что отвечает кинетической гибкости цепи. В общем случае:

где 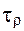 - время, необходимое для изменения локальной конформации;
- время, необходимое для изменения локальной конформации; 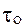 - величина, близкая 10-14 с.
- величина, близкая 10-14 с.
Макромолекулы могут обладать значительной термодинамической и малой кинетической гибкостью, например макромолекулы с гибкой основной цепью и объемными или полярными заместителями. В этом случае клубок «заторможен» в одном из конформационных состояний. Кинетическая гибкость, т.е. скорость изменения конформации может быть увеличена в результате воздействия на макромолекулу внешних сил.
Помимо химического состава и строения основной цепи и заместителей, кинетическая гибкость зависит от следующих факторов:
а) межцепного физического взаимодействия - в полимерных телах кинетическая гибкость всегда меньше по сравнению с растворами;
б) сшивки макромолекул - с увеличением плотности сшивки кинетическая гибкость падает;
в) молекулярной массы полимера - макромолекулы большей длины имеют более высокую гибкость по сравнению с менее длинными.
Кинетическая гибкость может проявляться как в растворе, так и в конденсированных полимерных телах. В первом случае она проявляется наиболее ярко в гидродинамическом поле. При действии больших напряжений сдвига макромолекулы разворачиваются. Кинетическая гибкость макромолекул в растворе характеризуется величиной кинетического сегмента, т.е. минимальным отрезком цепи, который может изменять форму под действием внешней силы. Длина кинетического сегмента зависит от скорости воздействия, с ее уменьшением длина кинетического сегмента уменьшается и стремится к длине термодинамического сегмента.
В конденсированном состоянии полимеров кинетическая гибкость цепи начинает проявляться при температурах, превышающих температуру стеклования. Кинетическую гибкость макромолекул в полимерных телах характеризуют длиной механического сегмента, равной длине цепи, при которой исчезает зависимость температуры стеклования полимера от молекулярной массы.
Гибкость цепи оказывает большое влияние на свойства полимеров и определяет области их использования. Например, кинетическая гибкость приводит к возникновению у полимеров такого уникального и технически важного свойства, как высокоэластичность, кроме того, она обусловливает способность макромолекул к ориентации, что имеет огромное значение при формировании волокон. Термодинамическая гибкость проявляется в процессах кристаллизации, плавления и растворения полимеров.
Природа упругости полимеров
Свойство, проявляющееся в обратимости деформации, называется упругостью. Для кристаллических тел обратимые деформации не превышают 1 %. Для…Термодинамические составляющие упругой силы
Природа упругой силы, вызывающей обратимость деформаций, может быть выявлена при анализе термодинамики обратимого растяжения упругого тела. В этом…Упругость идеального газа
Рассмотрим один моль идеального газа, находящегося в цилиндре с поршнем (рис. 2.22), при двух состояниях: р1, V1 и р2, V2, причем р1 > р2 и V1…Упругость идеального клубка
Первая теория эластичности каучука, так называемая кинетическая теория, была предложена в 1932 г. швейцарским ученым Мейером, далее она получила… Как термодинамическая система, изолированный макромолекулярный клубок…Упругость полимерной сетки
Чрезвычайно важное в практическом отношении свойство эластичности материально реализуется в резинах, т. е. сшитых каучуках, которые мы далее будем… Для количественного описания упругости полимерной сетки представим ее…Вязкоупругость полимерных систем
Характерной особенностью полимерного состояния вещества является то, что все полимерные материалы, а также расплавы и концентрированные растворы полимеров обладают свойствами как упругого тела, так и жидкости. Это общее явление определяется как вязкоупругость, оно ответственно за особый комплекс свойств, присущих полимерным материалам.
Модель Максвелла. Релаксация напряжения
Идеально упругое тело. Поведение идеально упругого тела описывается законом Гука (2.39), а универсальной характеристикой упругости является модуль… Ньютоновская жидкость. Основным законом, описывающим течение «идеальной», так…Теория рептаций
Из уравнения (2.63) следует, что свойства упруговязкой жидкости определяются временем релаксации . Для того, чтобы теоретически рассчитать…Модель Кельвина. Ползучесть
В модели Кельвина упругий и вязкий элементы соединены параллельно (см. рис. 2.28, б). Сила, прилагаемая к модели, эквивалентна напряжениям,… пружина не может мгновенно растягиваться и сжиматься, поскольку поршень… после снятия нагрузки цилиндр в поршне возвращается пружиной к исходному положению, т. е. деформация носит обратимый…Динамическая вязкоупругость
При постоянной нагрузке или определенной деформации моделей или материалов вязкоупругость называется статической, при переменных нагрузках и… Упругий гистерезис. Упругий гистерезис проявляется при периодическом…Релаксационные свойства полимеров. Принцип суперпозиции
В общем случае под релаксационными явлениями в полимерах понимают изменение их свойств во времени, обусловленное достижением равновесного состояния.… В основе механических релаксационных явлений в полимерах, которые проявляются… релаксация напряжения и ползучесть при статическом характере нагружения;ГЛАВА 3. РАСТВОРЫ ПОЛИМЕРОВ
Длительное время растворы высокомолекулярных соединений относили к лиофильным коллоидным. Считалось, что дисперсная фаза таких растворов состоит из мицелл-агрегатов макромолекул. Еще в 30-е гг. XX в. немецкий химик Г. Штаудингер одним из первых указывал, что полимеры в растворах диспергированы до макромолекул.
Решающее влияние на изменение взглядов на природу растворов высокомолекулярных соединений оказало построение первых фазовых диаграмм состояния растворитель - полимер и применение к ним правила фаз в работах Каргина, Папкова, Роговина. Из их опытов с очевидностью вытекало, что растворы высокомолекулярных соединений являются термодинамически обратимыми и, следовательно, истинными.
Для растворов высокомолекулярных соединений, так же как для коллоидных, характерны существенно меньшие величины скоростей диффузии, осмотического давления, изменения температур замерзания и кипения по сравнению с растворами низкомолекулярных соединений. Напротив, интенсивность светорассеяния растворов высокомолекулярных соединений и коллоидных на несколько порядков больше по сравнению с растворами низкомолекулярных веществ.
Вместе с тем растворы высокомолекулярных соединений имеют специфические, присущие только им свойства, наиболее важными из которых являются большая вязкость и наличие стадии набухания растворяемого вещества, предшествующего растворению.
Концентрацию растворов высокомолекулярных соединений обычно выражают в массовых, объемных долях или процентах растворенного вещества, а также числом граммов полимера в 100 мл раствора.
Термодинамика растворов полимеров
Используемые термодинамические понятия и величины
Принципы расчета энтальпии и энтропии смешения
Принципы расчета энтальпии и энтропии смешения были развиты в работах Гильдебранда, Ван-Лаара, Лоренца и др. в 20-30 гг. XX в. применительно к… Энтальпия смешения. При растворении происходит разрыв слабых межмолекулярных…Таблица 3.1 Значения параметров растворимости некоторых растворителей, полимеров и мономеров
| Растворители | δ·10-3, (Дж/м3)0,5 | Полимеры | δ·10-3, (Дж/м3)0,5 | Мономеры | δ·10-3, (Дж/м3)0,5 |
| н-Гексан | 14,6 | Политетра- фторэтилен | 12,5 | Изопрен | 14,8 |
| Диэтиловый эфир | 14,8 | Полидиметил- силоксан | 14,6 | Бутилмет- акрилат | 17,0 |
| н-Октан | 15,1 | Полиизо- бутилен | 15,8 | Винил- хлорид | 17,8 |
| Этилацетат | 18,2 | Полиэтилен | 15,9 | Метил- акрилат | 18,2 |
| Бензол | 18,3 | Полиизопрен | 16,3 | Стирол | 18,3 |
| Хлороформ | 18,6 | Полибутил- метакрилат | 17,6 | Метилмет- акрилат | 18,4 |
| Дихлорэтан | 19,6 | Полистирол | 18,2 | Винилацетат | 18,4 |
| Тетрагидро- фуран | 19,8 | Полиметил- метаакрилат | 18,6 | Акрило- нитрил | 21,4 |
| Нитробензол | 20,0 | Поливинил- ацетат | 18,8 | N-Винил- пирролидон | 21,422,2 |
| Ацетон | 20,2 | Поливинил- хлорид | 19,1 | ||
| Диметилформ- амид | 24,2 | Полиэтилен- терефталат | 20,2 | ||
| Этанол | 25,4 | Эпоксидная смола | 21,8 | ||
| Метанол | 29,0 | Полиокси- метилен | 22,0 | ||
| Вода | 46,4 | Полиакрило- нитрил | 30,8 |
Параметры растворимости оказались полезными при подборе растворителей полимеров, особенно в лакокрасочной промышленности, пластификаторов, приготовлении смесей полимеров. Существуют способы расчета параметров растворимости низкомолекулярных соединений и полимеров, исходя из вкладов функциональных групп. В случае смесей растворителей параметр растворимости рассчитывается по аддитивной схеме. Однако, как следует из рис. 3.1, параметры растворимости некоторых смесей далеки от аддитивности.
Со временем представления о природе параметра растворимости расширились. Согласно Хансону, величина параметра растворимости определяется всеми составляющими сил межмолекулярного взаимодействия:
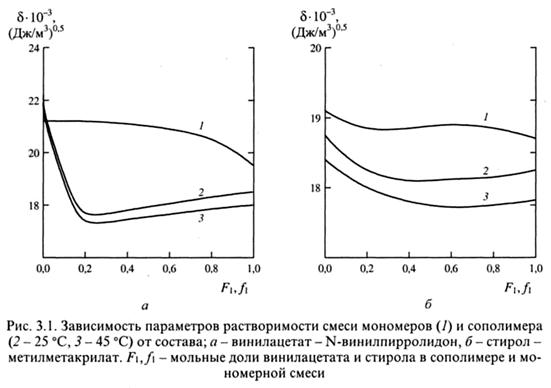

где δd, δh, δi - вклады, определяемые дисперсионными силами, водородными связями и индукционным эффектом.
В общем случае энергия взаимообмена ΔЕ определяет изменение внутренней энергии системы при смешении компонентов. И лишь в том случае, когда объем не меняется, тепловой эффект растворения практически равен энергии взаимообмена, т. е.

Энтропия смешения. Рассмотрим изменение энтропии при смешении двух компонентов с одинаковым размером молекул и одинаковой энергией взаимодействия всех молекул (ΔЕ = 0). В этом случае можно ожидать, что останутся неизменными составляющие энтропии, обусловленные вращательным, поступательным и колебательным движениями молекул, и, кроме того, в смеси появится новая составляющая энтропии, связанная с возможностью перестановок молекул относительно друг друга. Это специфическое приращение энтропии при образовании смеси носит название конфигурационной энтропии Sk. Исходя из сказанного выше, можно полагать, что для идеальных смесей именно этот вклад практически полностью обусловливает энтропию смешения, т. е.

Для расчета Sk представим, что каждая из молекул смеси расположена в ячейке плоской решетки. Если мы имеем N1 молекул компонента 1 и N2 молекул компонента 2, то число возможных перестановок в N1 + N2 ячейках решетки равно:

Рассматривая число перестановок как число микросостояний и, следовательно, как термодинамическую вероятность системы, мы можем применить формулу Больцмана:

где k - постоянная Больцмана. Преобразовав (3.25) при помощи формулы Стирлинга (y! = y/ey) и используя полученный результат в правой части (3.26), окончательно получаем:
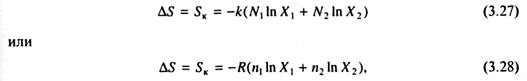
где N1, N2 - число молекул; n1, n2 - число молей; Х1 Х2 - мольные доли компонентов 1 и 2; R - универсальная газовая постоянная, связанная с постоянной Больцмана k через число Авогадро k = R/NA.
Теория Флори-Хаггинса
Первая термодинамическая теория растворов полимеров была разработана независимо Флори и Хаггинсом в 40-50 гг. XX в. Эта теория сыграла большую роль… В теории Флори-Хаггинса предполагается, что раствор является регулярным… Расчет энтропии и энтальпии смешения в теории Флори-Хаггинса проводится на основе модели квазикристаллической решетки,…Коллигативные свойства растворов полимеров. Осмотическое давление
К коллигативным свойствам относятся: снижение давления пара растворителя в растворе по сравнению с чистым… понижение температуры замерзания раствора по сравнению с температурой замерзания растворителя;Уравнение состояния. Термодинамическая характеристика раствора
Применительно к разбавленному реальному раствору указанный подход приводит к следующему выражению для химического потенциала растворителя:Исключенный объем и термодинамические свойства раствора
Вернемся вновь к проблеме исключенного объема (2.1.2) с тем, чтобы выявить влияние на него параметров, характеризующих термодинамическое качество… Исключенный объем макромолекулы (3iV/ определяется исключенным объемом…Ограниченная растворимость. Фракционирование
Для растворов высокомолекулярных соединений, как и для смесей низкомолекулярных веществ, характерно явление ограниченной растворимости. При…Свойства растворов полимеров
Набухание. Гели
Как уже отмечалось, растворению полимера предшествует его набухание, т.е. увеличение объема и массы высокомолекулярного соединения, находящегося в… Количественно набухание характеризуется степенью набухания:Вязкость разбавленных растворов полимеров
Существуют две модели движения макромолекулярного клубка в жидкости. Согласно модели Рауза, звенья (сегменты) цепи испытывают при движении трение,… Макромолекулярные клубки гибкоцепных полимеров с заключенным в них…Концентрированные растворы полимеров
При 1 < [ŋ]с < 10 раствор является полуразбавленным, т.е. умеренно концентрированным, для такого раствора характерно взаимодействие и… При [ŋ]с > 10 раствор является высококонцентрированным. Макромолекулы… Течение, вызываемое напряжением сдвига, наиболее наглядно можно представить при рассмотрении сосуда, в котором…Полиэлектролиты
Влияние зарядов на конформации макромолекул
Полиэлектролитами называют высокомолекулярные соединения, макромолекулы которых содержат ионогенные группы, способные к диссоциации на ионы. В…Взаимодействие заряженных цепей с противоионами. Коллапс сеток
Из теории двойного электрического слоя известно, что часть ионов адсорбируется на границе раздела, образуя так называемый слой Гельмгольца. В случае… Коллапс полимерных сеток. В разд. 3.1 было показано, что с уменьшением…Свойства растворов полиэлектролитов
Наиболее ярко влияние зарядов проявляется при изучении вязкостных свойств полиэлектролитов. Рассмотрим зависимость вязкости раствора желатины… При изменении pH (по сравнению с pH изоэлектрической точки), вызванном…Жидкокристаллическое состояние полимеров
Природа жидкокристаллического состояния вещества
Структура веществ в жидкокристаллическом состоянии является промежуточной между структурой жидкости и кристалла. Это промежуточное состояние… жидкие кристаллы, которые могут быть названы позиционно неупорядоченными… пластические кристаллы, образуемые молекулами с малой анизотропией формы, полимерными глобулами, для них характерно…Влияние температуры и полей на жидкокристаллические системы
Шаг холестерической спирали l имеет порядок длины волны видимого света и зависит от температуры. Кроме того, соответствующие мезофазы способны… Поведение гребнеобразных полимеров во внешних полях напоминает реакцию на них…Вязкость растворов жидкокристаллических полимеров
Жидкокристаллическое упорядочение в растворах приводит к появлению максимума на зависимости вязкости от концентрации. На рис. 3.19 приведена…Высокопрочные и высокомодульные волокна из жидкокристаллических полимеров
Впервые высокопрочные и высокомодульные волокна из растворов жидкокристаллических полимеров поли-n-бензамида и поли-n-фенилентерефталата были… Ароматические полиамиды в процессе синтеза растворяются в амидных… Для того, чтобы усилить ориентационный эффект, обусловленный жидкокристаллическим упорядочением прядильного раствора,…Таблица 3.5 Механические свойства основных типов волокон технического назначения
| Показатели | Кевлар-49 | Терлон | Нейлон 6,6 | Полиэфирное | Вискозное |
| Разрывная прочность, сН/текс | 250-260 | ||||
| Разрывное удлинение, % | 2,4-4,0 | 2-4 | 21,0-25,0 | 14,5 | 11,0 |
| Начальный модуль упругости, ГПа | 130,0 | 135-145 | 5,0-5,5 | 13,4 | 16,5 |
| Прочность в узле | 30-50 | 60-80 | 55.0 |
Преимущества формования высокопрочных волокон из растворов жидкокристаллических полимеров обусловлены тем, что достигается высокая степень ориентации макромолекулярных цепей и, следовательно, высокие прочностные показатели, благодаря жидкокристаллическому упорядочению прядильных растворов и фильерному вытягиванию. Последующая тепловая обработка приводит к существенному повышению их модуля.
Вслед за арамидными были освоены в производстве высокомодульные волокна из жидкокристаллических растворов гетероциклических полиари-ленов общей формулы:
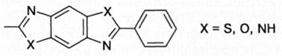
получение которых описано в разд. 5.6.8. При X = S получен полимер, превосходящий Кевлар по величине модуля (300 ГПа), что связано с большей жесткостью цепи. Персистентная длина его макромолекул составляет 64 нм против 15-20 нм у арамидов.
ГЛАВА 4. ПОЛИМЕРНЫЕ ТЕЛА
Кристаллические полимеры
Условия кристаллизации. Строение полимерного кристалла
Все полимеры делятся на аморфные и кристаллические. Необходимым условием кристаллизации полимеров является наличие дальнего порядка в расположении… Кристаллические полимеры, как правило, не являются однородными и содержат,… Принципиальным является то обстоятельство, что кристаллическую и аморфную фазы полимера никогда не удается разделить…Кинетика кристаллизации
Кристаллизация полимера из расплава возможна в достаточно широком температурном интервале между температурами плавления и стеклования. Из-за малой…Три физических состояния аморфных полимеров
Термомеханическая кривая
Для аморфных полимеров в зависимости от температуры характерны три различных состояния - стеклообразное, высокоэластическоеи вязкотекучее.Первые два… Температурные области существования различных физических состояний полимеров…Стеклообразное и высокоэластическое состояния полимеров
Стеклообразное состояние - это одна из форм твердого состояния аморфных полимеров, для которой характерны небольшие упругие деформации с высокими… Для высокоэластического состояния характерны большие обратимые деформации (до… Природа упругой силы, возникающей при деформировании полимеров, находящихся в стеклообразном и высокоэластическом…Вязкотекучее состояние полимеров
Это состояние полимеров относится к их расплавам, для него характерны преимущественно необратимые деформации, т.е. течение. Перемещение, т.е.…Пластификация полимеров
Под пластификацией понимается один из способов модификации полимеров, связанный с введением в них низкомолекулярных веществ, в результате чего… Существование представления о молекулярном механизме пластификации тесно…Механические свойства полимеров
Механические свойства полимера отражают реакцию полимера на действие внешних сил. Действие внешней силы на полимерное тело в зависимости от ее величины может привести к обратимой деформации, необратимой деформации и разрушению полимерного тела.
Деформационные свойства полимеров. Ориентация
При изучении механических свойств полимеров последние подвергаются различного вида деформациям, аналогичным тем, что имеют место при эксплуатации…Таблица 4.2 Механические свойства некоторых полимеров
| Полимер | Разрушающее напряжение при растяжении, МПа | Модуль упругости, МПа | Относительное удлинение при растяжении, % |
| Резина из натурального каучука | 650,0 | ||
| Полиэтилен низкой плотности | 300,0 | ||
| Полистирол | 1,5 | ||
| Полиметилметакрилат | 4,0 | ||
| Поликапролактам: пластик-капрон | 100,0 | ||
| волокно-капрон (корд) | 20.0 | ||
| капрон, наполненный стекловолокном (капролон) | — | ||
| Полиэтилентерефталат: пленка | |||
| волокно лавсан | 10-20 |
Как уже упоминалось, модуль Юнга является мерой жесткости материала. В табл. 4.2 приведены деформационно-прочностные характеристики некоторых крупнотоннажных полимерных материалов общего назначения. На примере капрона и полиэтилентерефталата видно, что ориентационное упрочнение, достигаемое при вытяжке волокна из полимера, приводит к увеличению как прочности, так и жесткости полимерного материала.
Ориентация.Односторонняя и двухсторонняя (вытяжка в двух направлениях) ориентации широко используются в промышленности для улучшения механических свойств аморфных и кристаллических полимеров, причем наиболее значительные эффекты достигаются в последнем случае. Существует несколько моделей ориентированных аморфных и кристаллических полимеров. К числу детально проработанных относится модель ориентированного кристаллического полимера Петерлина (рис. 4.13).
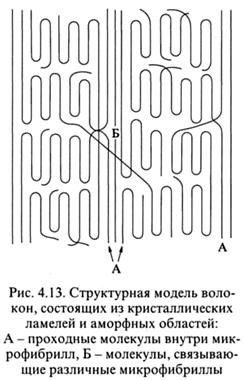
Согласно этой модели, кристаллические области - ламели или монокристаллы состоят из сложенных макромолекул, оси которых расположены параллельно оси вытяжки. Ламели следуют одна за другой вдоль этой оси, при этом большие грани ламели нормальны по отношению к ней. Между собой ламели соединены так называемыми проходными макромолекулами, входящими в два и более монокристалла.
Стопка ламелей образует микрофибриллу длиной 5-20 мкм и толщиной 10-20 нм. Микрофибриллы вытянуты вдоль оси вытяжки и разделены аморфными областями, вытянутыми в том же направлении. Последнее подтверждается тем, что при разрыве кристаллического ориентированного волокна область, прилегающая к разрыву, часто расщепляется наподобие щетки, причем трещины, разделяющие волоконца, ориентированы вдоль направления вытяжки. Очевидно, что эти трещины распространялись вдоль вытянутых аморфных областей. При разрушении полимера магистральные трещины распространяются нормально к направлению вытяжки. В случае ориентированного полимера им противостоит ансамбль выпрямленных макромолекул, что и является причиной ориентационного упрочнения.
Теоретические и реальные прочность и упругость кристаллических и аморфных полимеров
При растяжении кристаллических полимеров оси макромолекул ориентируются, т.е. располагаются в направлении действия растягивающей силы. В результате… На рис. 4.14 приведены в общем виде зависимости потенциальной энергии и сил…Таблица 4.3 Прочность и модуль Юнга различных материалов
| Материал | Прочность, МПа | Модуль упругости, ГПа | |
| продольный | поперечный* | ||
| Полиэтилен кристаллический** | |||
| Полиоксиметилен** | |||
| Полипропилен** | |||
| Сталь | |||
| Стекловолокно | |||
| Углеродное волокно | |||
| Волокно из ароматического полиамида «Кевлар» |
* Относительно направления вытяжки.
** Кристаллические ориентированные полимеры.
Несоответствие между теоретическими и экспериментальными величинами прочности является характерной особенностью полимерных материалов, в том числе и рассмотренных в таблице высокомодульных волокон, прочность которых не превышает 4·103 МПа. Это объясняется несовершенством кристаллической структуры полимеров, для которой характерно чередование кристаллических и аморфных областей. При разрыве волокон ориентированного полимера силы, приложенные в осевом направлении, передаются в основном на проходные макромолекулы, число которых составляет 10-30 % от числа макромолекул, расположенных в кристаллических областях. Уже из этих цифр ясно, что реальная прочность ориентированных кристаллических полимеров должна быть в несколько раз меньше теоретической. Показательно, что в случае металлов, кристаллическая структура которых более совершенна, удается вырастить нитевидные монокристаллы (усы), их экспериментально определяемая прочность близка к теоретической.
В отличие от кристаллических полимеров, для которых возникновение упругой силы связано с межатомным взаимодействием, механизм действия (возникновения) упругих сил при растяжении аморфных полимеров обусловлен изменением потенциальной энергии межмолекулярного взаимодействия, преимущественно потенциальной энергии вращения вокруг ковалентных связей. Из сказанного ясно, что в первом приближении модуль упругости аморфных стеклообразных полимеров можно оценить, измеряя модуль упругости кристаллических полимеров в направлении, поперечном вытяжке, т.к. в этом направлении макромолекулы кристаллического полимера связаны лишь физическими межмолекулярными связями. Из табл. 4.3 следует, что в поперечном направлении значение модуля упругости кристаллических полимеров составляет 3 - 4 ГПа. Однако модуль упругости стеклообразных полимеров существенно ниже. Одно из вероятных объяснений этого несоответствия состоит в том, что даже в «замороженных» конформациях под действием приложенного напряжения возникает определенная подвижность сегментов и, следовательно, напряжение релаксирует. Напомним, что аналогичным является механизм вынужденной эластичности, рассмотренный выше.
Оценка прочности неориентированных аморфных стеклообразных полимеров может быть сделана, исходя лишь из полуэмпирических расчетов. Прежде всего, уточним содержание понятия «прочность» в данном случае. Из рис. 4.9 следует, что при растяжении аморфного стеклообразного полимера при Т > Тхр можно получить две количественные характеристики прочности - предел текучести и напряжение, при котором образец физически разрушается. Обе характеристики с точки зрения поставленной задачи неприемлемы, ибо в первом случае образец не разрушается, а течет, во втором - мы имеем дело с ориентированными макромолекулами, что не соответствует исходному условию. Уже упоминалось, что вид деформационной кривой существенно зависит от скорости деформации. При ее увеличении кривые растяжения приобретают вид кривой 1, приведенной на рис. 4.9, а предельное значение напряжения называется пределом хрупкости σхр. Когда разрыву образца предшествует кривая растяжения типа 1, говорят о хрупком разрушении, когда кривая 2 - о пластическом разрушении. Исходя из сказанного, было введено понятие критической прочности σкр, равной напряжению, при котором меняется механизм разрушения (от хрупкого к пластичному или наоборот).
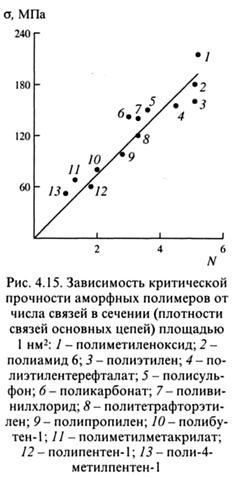
При разрыве аморфного стеклообразного полимера должны разделиться «замороженные» клубки макромолекул. Поскольку клубки являются взаимопроникающими, при их разделении необходимо затратить энергию как на преодоление межмолекулярного взаимодействия при «скольжении» цепей, так и на разрыв некоторого количества химических связей, образующих зацепления. Ясно, что и та, и другая составляющие тем больше, чем больше приходится число связей на единицу сечения. Площадь поперечного сечения макромолекул или поперечного сечения мономерного звена пропорциональна M0/ρl, где М0 - молекулярная масса мономерного звена, l - его длина, ρ - плотность полимера. Зная эту величину, легко рассчитать число звеньев, приходящихся на эту площадь. Из рис. 4.15 следует, что критическая прочность полимеров действительно пропорциональна числу связей основных цепей, приходящихся на единицу сечения.
Другой подход связан с учетом числа зацеплений макромолекул (см. рис. 2.30), приходящихся на единицу площади плоскости, перпендикулярной приложенному напряжению. Была проведена аналогия между зацеплениями и химическими сшивками, что позволило использовать известную зависимость между плотностью сшивки и прочностью каучуков. В результате для разрушающего напряжения ориентированных аморфных полимеров было получено:
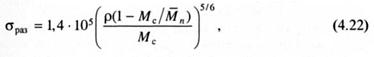
где ρ - плотность полимера; 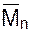 - среднечисловая молекулярная масса; Мс -средняя молекулярная масса отрезка между двумя зацеплениями.
- среднечисловая молекулярная масса; Мс -средняя молекулярная масса отрезка между двумя зацеплениями.
Механика и механизм разрушения полимеров
На вопрос, как и почему разрушаются твердые тела, впервые ответил Гриффит еще в конце XIX в. Его теория, которую можно отнести к механике… Согласно Гриффиту, разрушение твердого тела под действием механического…Ударная прочность полимеров
Разнообразные способы механического воздействия, приводящие к разрушению полимерного материала, можно отнести к трем типичным случаям: ударные воздействия, длительные воздействия при постоянной нагрузке,Таблица 4.4 Ударная вязкость (по Изоду) некоторых полимерных материалов
| Материал | Ударная вязкость, кДж/м2 |
| Полистирол | 13-21 |
| Ударопрочный полистирол | 26-210 |
| Сополимер акрилонитрила, бутадиена и стирола (АБС-пластик) | 53-200 |
| Поливинилхлорид | 20-50 |
| Поливинилхлорид, содержащий частицы бутадиенового каучука | 500-1600 |
| Полипропилен | 20-40 |
| Этилен-пропиленовый блок-сополимер | 100-800 |
Долговечность. Усталостная прочность полимеров
Представим, что некий груз поднят тросом из полимерного материала. Означает ли это, что груз может висеть в подвешенном состоянии к тросу сколь…Электрические свойства полимеров
По величине удельной электрической проводимости (Ом-1·см-1) или обратной ей… Объемная проводимость полимеров обычно имеет ионную природу, причем ионы, как правило, являются примесными. Поэтому…Релаксационные переходы
Если напряжение, приложенное к полимеру, изменяется по гармоническому закону, то по такому же закону, но со сдвигом фаз, меняется дипольная…Синтетические металлы
Полимеры с сопряженными связями (ПСС) в определенных условиях обладают проводимостью, равной или близкой проводимости металлов, поэтому данный класс… низкий потенциал ионизации, высокое сродство к электрону,Таблица 4.7 Синтетические металлы - полимеры с системой сопряжения
| Название полимера | Допирующий агент | Электропроводность, Ом-1·см-1 |
| Цис-полиацетилен | AsF5 | 3,5·103 |
| Транс-полиацетилен | AsF5 Na | 2,2·103 |
| Полидиацетилен | СlО4- | 1,8 |
| Полиин | СlO4- | 0,13 |
| Поли-n-фенилен | AsF5 К | 7,0 |
| Поли-n-фениленвинилен | AsF5 | 2,8·103 |
| Полихинолин | Na | |
| Полипиридин | - | 0,4 |
| Поли-n-фениленсульфид | AsF5 | |
| Полибензотиофенсульфид | AsF5 | |
| Полипиррол | CIO4- | ~103 |
| Политиенилен | CIO4- | ~100 |
| Полифуранилен | СlO4- | ~20 |
| Нитевидные кристаллы графита | AsF5 | 9,0·105 |
| Политиазил | Br2 |
Из табл. 4.7 видно, что все приведенные в ней допированные ПСС обладают металлической проводимостью, нижней границей которой считается значение, равное 0,1 Ом-1 см-1, а допированное графитовое волокно достигает проводимости меди. Считается, что синтетические металлы имеют большие перспективы практического использования в электротехнике, электронике и ряде смежных отраслей -при создании новых фотоизлучающих диодов, цветных дисплеев, источников тока большой мощности, ионных конденсаторов, солнечных батарей и многого другого, не говоря уже об их использовании как заменителей цветных металлов. Наиболее перспективным для практического использования в качестве синтетического металла считается полиацетилен. Однако у этого материла существует слабое место - быстрая окисляемость. От решения соответствующей проблемы зависит, как скоро полиацетилен появится в качестве товарного синтетического металла.
ГЛАВА 5. СИНТЕЗ ПОЛИМЕРОВ МЕТОДАМИ ЦЕПНОЙ И СТУПЕНЧАТОЙ ПОЛИМЕРИЗАЦИИ
Радикальная полимеризация
При цепной полимеризации макромолекулы полимера образуются в результате раскрытия кратных связей или циклов мономеров при действии на них активных… Радикальной полимеризации подвержены исключительно соединения, содержащие…Инициирование радикальной полимеризации
Первичные радикалы, необходимые для инициирования радикальной полимеризации, могут быть получены в результате химических реакций и при физическом… Вещественное инициирование.При химическом или вещественном инициировании… Среди пероксидов широкое применение нашли ацил-, алкил-, гидропероксиды и перэфиры. Круг азосоединений, практически…Таблица 5.1 Важнейшие инициаторы радикальной полимеризации
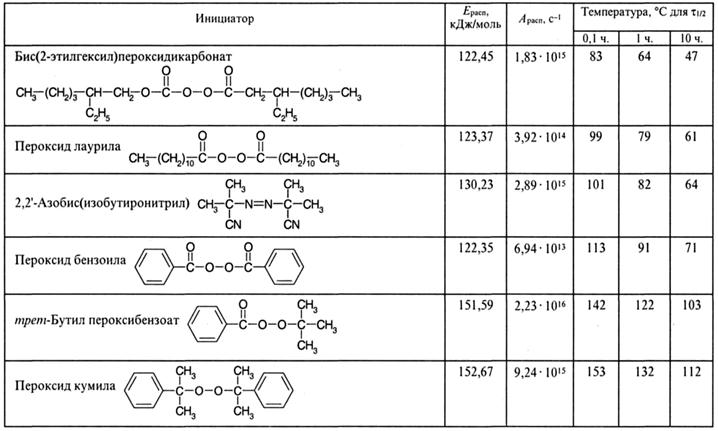
Окончание таблицы 5.1
Элементарные реакции и кинетика полимеризации
Неразветвленная цепная химическая реакция включает три последовательные стадии - инициирование, рост и обрыв кинетической цепи. Под последней…Инициирование.
Рост цепи.
Реакция роста протекает аналогично второй стадии реакции инициирования:
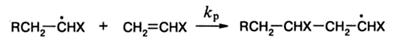
Так же как и в предыдущем случае, радикал, на этот раз радикал роста, атакует метиленовую группу двойной связи, т.е. «хвост» мономера. Такой порядок присоединения определяется как «голова» (радикал) к «хвосту» (мономер).
Обрыв цепи.
а) соединения (рекомбинации) радикаловМолекулярно-массовое распределение при радикальной полимеризации
Нахождение дифференциальной функции числового распределения при радикальной полимеризации сводится к нахождению вероятности образования макромолекул…Влияние температуры и давления на радикальную полимеризацию
Влияние температуры на скорость химической реакции выражается уравнением Аррениуса:Диффузионная модель обрыва цепи. Гель-эффект
Реакция обрыва является единственной элементарной реакцией, которая контролируется диффузией на всех стадиях процесса. Определяющее влияние диффузии…Каталитическая передача цепи
В 1980 г. было обнаружено, что кобальт порфирин (СоП), т.е. тетрапиррольный комплекс Со (II) катализирует реакцию передачи цепи на мономер при… Характерной особенностью каталитической реакции передачи цепи на мономеры…Псевдоживая радикальная полимеризация
При псевдоживой радикальной полимеризации растущие цепи часть времени (большую) являются неактивными, другую часть времени (значительно меньшую) -… В качестве инифертеров применяются главным образом серосодержащие соединения:…Таблица 5.8 Константы обратимого ингибирования псевдоживой полимеризации стирола в присутствии ТЕМПО
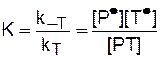 , моль/л , моль/л
| k-T, c-1 | kT, л·моль-1·c-1 | E*-T, кДж/моль |
| 2·10-11 | 6·10-4 | 3·107 | ~120 |
* Энергия активации распада высокомолекулярного аддукта полистирол-ТЕМПО.
из которого следует, что при t→∞, 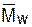 /
/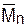 →1. Практически ММР при псевдоживой полимеризации становится узким к 15-20% конверсии, начиная с которой
→1. Практически ММР при псевдоживой полимеризации становится узким к 15-20% конверсии, начиная с которой 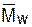 /
/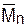 <1,15-1,20 (см. рис. 5.11). В целом «идеальная» псевдоживая полимеризация стирола реализуется при концентрации алкоксимов от 5·10-3 до 5·10-2 моль/л до 70% конверсии. В этих условиях образуется полистирол со строго контролируемой ММ - от 103 до (50-60)·103 и узким ММР.
<1,15-1,20 (см. рис. 5.11). В целом «идеальная» псевдоживая полимеризация стирола реализуется при концентрации алкоксимов от 5·10-3 до 5·10-2 моль/л до 70% конверсии. В этих условиях образуется полистирол со строго контролируемой ММ - от 103 до (50-60)·103 и узким ММР.
Способ реализации псевдоживой полимеризации при обратимом ингибировании ТЕМПО не влияет на механизм и константы основных элементарных реакций, которые приведены в табл. 5.8.
Исходя из этих данных и приведенных ранее кинетических закономерностей, был установлен «режим» идеальной псевдоживой полимеризации стирола. Оказалось, что при [PnT] ≈ [RT] = 4·10-2 моль/л «псевдоживая цепь» 40 мин «спит», затем ~ 10-3 - 10-4 с «бодрствует», т. е. растет на 10-12 звеньев, и этот цикл продолжается 60-70 раз до 70-80% исчерпания мономера примерно за двое суток. До больших конверсии проводить псевдоживую полимеризацию не имеет смысла из-за уменьшения скорости и увеличения полидисперсности полимера.
Псевдоживая полимеризация с переносом атома (галогена)принципиально отличается от рассмотренной выше полимеризации в присутствии ТЕМПО бимолекулярным окислительно-восстановительным актом реинициирования.
Типичным примером является псевдоживая радикальная полимеризация стирола при 110 °С в присутствии растворимых комплексов CuBr с лигандом L:
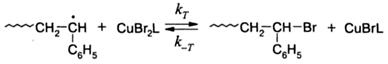
в которой растущие цепи обратимо реагируют с сильным ингибитором CuBr. В данном случае обратимая окислительно-восстановительная реакция ингибирования сопровождается переносом атома брома, константа равновесия этой реакции записывается в следующем виде:
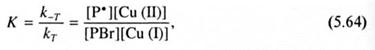
где kT, k-T определяются аналогично предыдущему случаю, [Р•], [PBr] -концентрации активных и «спящих» радикалов, [Cu (II)], [Cu (I)] - равновесные концентрации CuBr2 и CuBr. Для рассматриваемой реакции K = 10-8, стационарная концентрация Cu (II) составляет от 1 до 10 % по отношению к Cu (I). Наиболее важные характеристики рассмотренного Процесса отражены на рис. 5.11.
Эмульсионная полимеризация
В соответствии со способом проведения радикальная полимеризация подразделяется на полимеризацию в массе, растворе, суспензионную и эмульсионную.… Реакционная система в эмульсионной полимеризации представляет собой 30-60%-ную… Из рис. 5.12 видно, что в мицеллах ПАВ полярные группы обращены в воду, неполярные - внутрь мицеллы. Внутренняя…Катионная полимеризация
Элементарные реакции. Кинетика
Катионная полимеризация является цепной полимеризацией, при которой активным центром на конце растущей цепи является катион. К мономерам катионной… Инициаторами катионной полимеризации являются соединения, способные… 1. Инициирование протонными кислотами.К наиболее употребляемым для инициирования катионной полимеризации относятся…Таблица 5.9 Константы скорости роста в катионной полимеризации
| Мономер | Инициатор | Растворитель | T, °С | 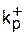 ·10-4, л/(моль·с) ·10-4, л/(моль·с)
|
| Изобутилен | ионизирующее излучение | в массе | ||
| Стирол | » | » | ||
| n-Метоксистирол | » (C6H5)3C+SbCl-6 | » CH2Cl2 | 36* | |
| N-Винилкарбазол | (C6H5)3C+SbF-6 | » | 60** | |
| Изопропилвиниловый эфир | (C6H5)C+SbCl-6 ионизирующее излучение | » » | 1,1 8,6 | |
| Изопрен | » | В массе | 0,2 |
* 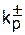 = 4,1·104 л/(моль·с).
= 4,1·104 л/(моль·с).
** 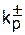 = 5,0·104 л/(моль·с).
= 5,0·104 л/(моль·с).
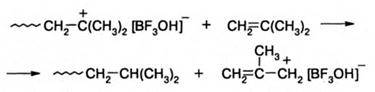
Движущей силой этой реакции в приведенном примере является образование аллильного катиона. Однако это не приводит к таким катастрофическим последствиям, к каким приводит образование аллильного радикала вследствие деградационного переноса цепи при радикальной полимеризации.
Реакция обрыва кинетической цепи.Приведенные выше реакции не вызывают обрыва кинетической цепи, поскольку сопровождаются регенерацией активных центров или инициатора. Гибель активных центров или обрыв кинетической цепи в катионной полимеризации происходит в результате присоединения противоиона или его фрагмента к карбкатиону. Ниже приведены примеры обеих реакций:
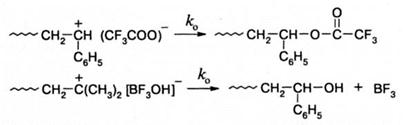
В качестве передатчиков или обрывателей кинетической цепи в катионной полимеризации могут выступать вещества примесного характера или специально введенные вещества, способные генерировать анионы при атаке карбкатиона, такие как спирты, кислоты, ангидриды.
Скорость полимеризации.Уравнение скорости катионной полимеризации может быть получено тем же путем, которым было получено уравнение скорости радикальной полимеризации - исходя из принципа стационарного состояния. Отличие состоит в том, что при катионной полимеризации реакция обрыва кинетической цепи является мономолекулярной. Уравнение имеет вид:

где К- константа равновесия реакции комплексообразования инициатора и соинициатора; [I], [IX] - концентрации инициатора и соинициатора; kин, kp, ko - константы скоростей инициирования, роста и обрыва цепи.
Степень полимеризации.Выражение для степени полимеризации при катионной полимеризации получается, исходя из тех же соображений, что и в случае радикальной полимеризации - путем деления скорости роста на сумму скоростей обрыва материальной цепи. При необходимости учета реакций передачи цепи более удобно использовать обратную степень полимеризации, что приводит к выражению, весьма напоминающему основное уравнение кинетики радикальной полимеризации:
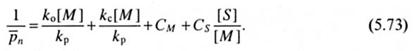
Здесь CM = kM/kp, CS = kS/kp - относительные константы передачи цепи на мономер и растворитель; kс - абсолютная константа скорости спонтанной передачи цепи на противоион.
Молекулярно-массовое распределение.Молекулярно-массовое распределение в катионной полимеризации аналогично тому, что имеет место на начальной стадии радикальной полимеризации в присутствии передатчика цепи и (или) при обрыве кинетической цепи в результате реакции диспропорционирования макрорадикалов. Эта аналогия обусловлена тем, что в обоих случаях при обрыве одна кинетическая цепь образует одну макромолекулу. Отсюда следует, что на начальной стадии катионной полимеризации 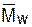 /
/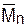 = 2, однако с увеличением конверсии индекс полидисперсности существенно возрастает.
= 2, однако с увеличением конверсии индекс полидисперсности существенно возрастает.
Псевдокатионная и псевдоживая катионная полимеризации
В некоторых случаях рост цепи при катионной полимеризации происходит путем присоединения мономера к «скрытой» ионной паре, компоненты которой…Влияние растворителя и температуры
Роль растворителя в катионной полимеризации заключается, прежде всего, в его влиянии на степень разделенности ионных пар на концах растущих цепей.…Анионная полимеризация
Анионной называется цепная полимеризация, при которой активными центрами на концах растущих цепей являются анионы. Акт роста цепи заключается в нуклеофильной атаке аниона на β-углеродный атом мономера, в результате чего возникает новая σ-связь, а пара электронов π-связи смещается на конечный α-атом углерода:
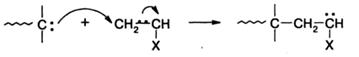
Основные реакции инициирования
Анионная полимеризация инициируется металлами I и II групп, их алкилами, арилами, амидами, алкоксидами, слабыми основаниями - гидроксидами, аминами… Алкилы и арилы металлов.Наиболее часто, особенно в промышленности, в качестве…Кинетика анионной полимеризации с обрывом цепи
Классическим примером анионной полимеризации с ярко выраженными реакциями передачи и обрыва цепи является полимеризация стирола в жидком аммиаке,… 1. Инициирование:Живая полимеризация. Блок-сополимеры
Впервые живую анионную полимеризацию наблюдали Абкин и Медведев в 1930-х гг., однако систематически исследовал этот процесс Шварц в 50-х гг. XX в.,… Карбанионы являются относительно более устойчивыми и, следовательно, менее…Полимеризация с переносом группы
Живая полимеризация таких полярных мономеров, как акриловые и метакриловые эфиры, может быть проведена при существенно более высокой температуре по… Наиболее распространенным и изученным инициатором этой реакции является…Влияние температуры, растворителя и противоиона
Влияние противоиона иллюстрируется данными анионной полимеризации стирола. Изменение природы противоиона в порядке Li+Na+K+Rb+Cs+ приводит к… Влияние температуры на скорость анионной полимеризации связано сдвумя…Ионно-координационная полимеризация
Среди разных видов цепной полимеризации ионно-координационная имеет особое значение, поскольку она позволяет получать стереорегулярные полимеры,… Разница энергий активации присоединения мономера в цис- или синдио-положение…Катализаторы Циглера-Натта. Исторический аспект
В 1932 г. Штаудингер впервые указал на то, что полимеры виниловых мономеров, подобные полистиролу, содержат в основной цепи макромолекул… Первый синтез стереорегулярного полимера - поливинилизобутилового эфира… Значение катализаторов Циглера-Натта состоит в следующем. Они являются наиболее универсальными инициаторами…Полимеризация на гетерогенных катализаторах Циглера-Натта
Формально в большинстве случаев полимеризация на катализаторах Циглера-Натта может быть отнесена к анионно-координационной. Это относится, прежде… Катализатор Циглера-Натта образуется в результате сложных процессов,…Анионно-координационная полимеризация диенов
Механизм полимеризации диенов-1,3, инициируемой литийорганическими соединениями, определяется природой растворителя. В зависимости от условий…Таблица 5.12 Влияние растворителя на анионную полимеризацию 1,3-диенов, инициируемую н-бутиллитием
| Растворитель | Структура полимера, % | |||
| цис-1,4 | транс-1,4 | 3,4 | 1,2 | |
| 1,3-бутадиен,0°С | ||||
| н-Пентан Тетрагидрофуран | ||||
| Изопрен, 25°С | ||||
| н-Гексан Тетрагидрофуран |
Из табл. 5.12 видно, что рассмотренный выше механизм наиболее ярко проявляется для полиизопрена. Промышленное производство стереорегулярного цис-1,4-полиизопрена на литиевых катализаторах было организовано в СССР в 50-х годах. При стереорегулярной полимеризации диенов, инициируемой катализаторами Циглера-Натта, достигается более высокая стереоспецифичность по сравнению с полимеризацией на литиевых катализаторах. Так, при полимеризации изопрена на катализаторе TiCl4+AlR3 образуется цис-1,4-полиизопрен, на VCI3+AIR3 - транс-1,4-полиизопрен с выходом, близким к 100 % в обоих случаях.
Синтез гетероцепных полимеров ионной полимеризацией
В отличие от карбоцепных полимеров, которые могут быть получены как радикальной, так и ионной полимеризацией, гетероцепные полимеры получаются лишь…Карбонилсодержащие соединения
В результате полимеризации карбонилсодержащих соединений образуются полиацетали:Полимеризация эфиров и эпоксидов с раскрытием цикла
Реакция роста при катионной полимеризации циклических эфиров, например тетрагидрофурана, протекает через оксониевые активные центры:Полимеризация лактамов и лактонов
Катионная полимеризация циклических амидов инициируется широким кругом протонных и апротонных кислот. Первые протонируют мономер, который затем…Другие гетероциклы
Очень важной с практической точки зрения является ионная полимеризация циклосилоксанов, осуществляемая в широких масштабах в промышленности.… Анионная полимеризация циклосилоксанов инициируется алкилами, гидроксидами,…Ступенчатая полимеризация
Как уже упоминалось в главе 1, при ступенчатой полимеризации, называемой также поликонденсацией, макромолекулы образуются в результате молекулярных… Согласно принципу Флори, реакционная способность функциональных групп в…Равновесная и неравновесная поликонденсация
Все реакции поликонденсации обратимы, однако, константа равновесия этой реакции может изменяться в широких пределах. Например, из наиболее…Кинетика поликонденсации
1. Протонирование кислоты-реагента кислотой-катализатором (НА):Молекулярно-массовое распределение полимера при поликонденсации
Рассмотрим молекулярно-массовое распределение полимера, полученного поликонденсацией мономера ARB или эквимолярной смеси ARA и BR1B. Используем… Макромолекула, содержащая p звеньев мономера ARB, образуется в том случае,…Разветвленные и сшитые полимеры
Рассмотренные выше линейные полимеры получаются в результате конденсации мономеров с функциональностью ƒ = 2. Под последней понимается число функциональных реакционноспособных групп, приходящихся на одну молекулу…Фенопласты, аминопласты
Фенолформальдегидные смолы. Фенопласты. Фенолформальдегидная смола была первым полимером, освоенным промышленным производством еще в 1909 г. Патент… Реакция между фенолом и формальдегидом катализируется как основаниями, так и…Полиуретаны. Полисилоксаны
Полиуретаны. Полиуретаны образуются в результате конденсации изоцианатных -N=C=O и гидроксильных групп. Линейные полиуретаны образуются при…Жесткоцепные ароматические полимеры
Полимеры с существенно большей температурой эксплуатации и прочностью, содержащие, как правило, в цепи ароматические структуры и поэтому являющиеся… Ароматические полиэфиры, полиэфиркетоны, полиэфирсульфоны. Ароматические…Сверхразветвленные полимеры
Возможность образования сверхразветвленных полимеров из полифункциональных мономеров типа ARB2, где А и В реагируют лишь друг с другом, но не с…Общие вопросы синтеза полимеров
Термодинамика синтеза
Полимеризация мономера возможна при условии:Сопоставление ионной и радикальной полимеризации
В целом радикальная полимеризация изучена более полно и глубоко по сравнению с ионной из-за значительных трудностей, встречающихся при… Наиболее существенные отличия в кинетике полимеризации связаны с порядками…Об общности процессов псевдоживой полимеризации
Почти полвека известна идеальная живая анионная полимеризация, включающая две элементарные реакции - инициирования и роста цепи. Радикальная… 1. В псевдоживой радикальной полимеризации, детально рассмотренной в разд.… 2. В карбкатионной полимеризации превращение растущих цепей в нерастущие, и наоборот, чаще всего происходит в…ГЛАВА 6. ЦЕПНАЯ СОПОЛИМЕРИЗАЦИЯ
Под сополимеризацией подразумевается совместная полимеризация двух или более мономеров. Сополимеризация является наиболее доступным и эффективным способом модификации свойств и, тем самым, расширения номенклатуры полимерных материалов. Из более чем 100 млн. т синтетических полимеров, выпускаемых ежегодно в мире, около 1/3 составляют сополимеры. Существуют три механизма влияния сомономерных звеньев на свойства сополимера:
1. Подавление кристаллизации полимера. В этом случае используются небольшие количества сомономера - до 10%. Такой прием часто применяется при получении полимерных материалов из олефинов.
2. Увеличение энергии когезии цепей, т.е. межмакромолекулярного взаимодействия за счет введения полярного сомономера. При этом одновременно уменьшается гибкость цепей.
3. Внутримолекулярная пластификация, т.е. уменьшение межмакромолекулярного взаимодействия за счет введения неполярного объемного сомономера, «раздвигающего» цепи.
Первый и третий увеличивают пластичность полимерного материала, улучшают его перерабатываемость. Второй приводит к увеличению температуры размягчения полимера (теплостойкость) и возрастанию прочности. Очень часто путем сополимеризации можно кардинально изменить растворимость полимера. Так, известно, что резиновый клей является раствором каучука в бензине или другом углеводороде. В то же время резиновые шланги используют в автомобилях для подачи бензина без видимых последствий для них. В последнем случае применяется не просто каучук - полимер диена, а его сополимер с акрилонитрилом - одним из наиболее полярных мономеров. В результате каучук, содержащий 15-20% полярных звеньев в цепи, перестает растворяться и набухать в бензине, сохраняя при этом свое наиболее ценное свойство - эластичность.
Количественная теория сополимеризации
Кривые состава сополимера и относительные активности мономеров
Около 90 % сополимеров, получаемых в промышленности, являются двухкомпонентными. Соответствующая сополимеризация называется двухкомпонентной или… Количественные соотношения, описывающие состав и строение сополимера, являются…Состав и микроструктура сополимера. Статистический подход
Уравнения состава сополимера могут быть получены более строгим -статистическим методом без каких-либо исходных допущений, как это было сделано выше,…Многокомпонентная сополимеризация
Как уже упоминалось, в практическом отношении весьма важна терполимеризация, которая используется для придания сополимеру специфических свойств -…Таблица 6.2 Предсказанные и определенные экспериментально составы сополимеров, полученных радикальной тер- и тетраполимеризацией
| Состав исходной смеси мономеров | Состав терполнмера, мол.% | ||||
| система | Мономер | Содержание, мол.% | Определено экспериментально | Вычислено по уравнению | |
| (6.64) | (6.66) | ||||
| Стирол Метилметакрилат Винилиденхлорид | 31,24 31,12 37,64 | 43,4 39,4 17,2 | 44,3 41,2 14,5 | 44,3 42,7 13,0 | |
| Метилметакрилат Акрилонитрил Винилиденхлорид | 35,10 28,24 36,66 | 50,8 28,3 20,9 | 54,3 29,7 16,0 | 56,6 23,5 19,9 | |
| Стирол Акрилонитрил Винилиденхлорид | 34,03 34,49 31,48 | 52,8 36,7 10,5 | 52,4 40,5 7,1 | 53,8 36,6 9,6 | |
| Стирол Метилметакрилат Акрилонитрил | 35,92 36,03 28,05 | 44,7 26,1 29,2 | 43,6 29,2 26,2 | 45,2 33,8 21,0 | |
| Стирол Акрилонитрил Винилиденхлорид | 20,00 20,00 60,00 | 55,2 40,3 4,5 | 55,8 41,3 2,9 | 55,8 41,4 2,8 | |
| Стирол Метилметакрилат Акрилонитрил Винилиденхлорид | 25,21 25,48 25,40 23,91 | 40,7 25,5 25,8 8,0 | 41,0 27,3 24,8 6,9 | 41,0 29,3 22,8 6,9 |
Уравнение (6.66) можно получить статистическим методом, используя «правило произведения вероятностей». Исходя из (6.65), можно записать:

что приводит к

Переходные вероятности в терполимеризации выражаются обычным образом - через отношение скорости роста рассматриваемой реакции к сумме скоростей роста всех возможных реакций роста с участием данного типа активных центров. Уравнение состава, получаемое статистическим методом, идентично уравнению (6.66). Оба уравнения состава терполимера приводят к одинаковым результатам, о чем можно судить по данным табл. 6.2.
Как кинетическим, так и статистическим методом могут быть получены уравнения состава сополимера для более сложных систем, включающих четыре и более мономеров. Константы сополимеризации в этих уравнениях также являются относительными активностями бинарной сополимеризации.
Сополимеризация до глубоких конверсии
В результате разной активности мономеров при сополимеризации текущий состав мономерной смеси и, следовательно, текущий состав сополимера постоянно… Интегрирование дифференциального уравнения Майо-Льюиса приводит к…Радикальная сополимеризация
Скорость сополимеризации
Изменение состава мономерной смеси, как правило, приводит к заметному, а иногда к драматическому изменению скорости и степени полимеризации. Это… Измерение скорости сополимеризации методом дилатометрии. Как правило, скорость…Природа эффекта предконцевого звена
Модель предконцевого звена была предложена Мерцем, Алфреем и Голдфингером в 1946 г., ими же впервые было получено уравнение (6.50). Долгое время эта… В настоящее время существует мнение, что границы применения предконцевой… В настоящее время природу явного и неявного эффектов предконцевого звена связывают с двумя составляющими - стерической…Влияние температуры и давления на радикальную сополимеризацию
Влияние температуры на скорость и степень сополимеризации аналогично го-мополимеризации (разд. 5.1.4). Исключения могут быть связаны с…Таблица 6.6 Значения относительных активностей мономеров при разных температурах и отношения частотных факторов
| Мономеры | r1, r2 | A11/A12, А22/А21 | |
| 60°С | 131°С | ||
| Стирол метилметакрилат | 0,520 0,460 | 0,590 0,536 | 1,06 1,10 |
| Стирол метилакрилат | 0,747 0,182 | 0,825 0,238 | 1,31 1,39 |
| Стирол диэтилмалеат | 6,52 ~0 | 5,48 ~0 | 2,55 |
| Стирол диэтилфумарат | 0,301 0,0697 | 0,400 0,0905 | 1,50 0,31 |
| Стирол n-хлорстирол | 0,742 1,032 | 0,816 1,042 | 1,27 1,22 |
| Стирол транс-стильбен | 5,17 (70°С) 0,33 | 7,23 (140°С) 0,22 | 34,34 0,003 |
откуда следует, что с увеличением температуры r1 → 1, r2 → 1 независимо от исходных значений относительных активностей. Другими словами, с увеличением температуры избирательность присоединения мономеров к радикалам уменьшается. Однако, этот эффект мал, поскольку мала разница в энергиях активации роста цепи (E11 – Е12) и (Е22 - Е21). В табл. 6.6 приведены значения относительных активностей мономеров при разных температурах, откуда видно, что теоретические представления для однотипных мономеров оправдываются.
Отклонения наблюдаются при сополимеризации мономеров с отличающейся структурой, например, при сополимеризации стирола с диэтилмалеатом (1,2-дизамещенный мономер) и транс-стильбеном (бифункциональный мономер СН2=СН-С6Н4-СН=СН2).
Влияние давления на скорость и степень сополимеризации качественно аналогично тому, что описано выше для гомополимеризации. Влияние давления на относительные активности может быть предсказано, исходя из уравнения (5.51). Применяя его к произведению относительных активностей, получаем:

при допущении, что 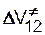 =
= 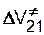 , где
, где 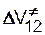 и
и 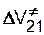 - изменение объема при образовании переходного комплекса из исходных мономера и радикала в реакциях перекрестного роста, т.е. активационные объемы этих реакций. Из разд. 5.1.4 следует, что
- изменение объема при образовании переходного комплекса из исходных мономера и радикала в реакциях перекрестного роста, т.е. активационные объемы этих реакций. Из разд. 5.1.4 следует, что 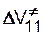 < 0,
< 0, 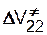 < 0, следовательно, с увеличением давления произведение r1·r2 должно возрастать. Из данных, приведенных в табл. 6.7, видно, что это предсказание оправдывается.
< 0, следовательно, с увеличением давления произведение r1·r2 должно возрастать. Из данных, приведенных в табл. 6.7, видно, что это предсказание оправдывается.
Увеличение давления всегда приводит к росту произведения r1·r2 в результате возрастания значений обеих констант сополимеризации r1 и r2.
Таблица 6.7 Влияние давления на сополимеризацию некоторых мономеров
| М1 | М2 | р·10-5, Па | r1 | r2 | r1·r2 |
| Стирол | Метилакрилат | 1,0 1013,2 2026,5 3039,8 | 0,704 0,710 0,714 0,718 | 0,159 0,163 0,167 0,171 | 0,112 0,116 0,119 0,123 |
| Стирол | Акрилонитрил | 1,0 1013,2 | 0,07 0,14 | 0,37 0,55 | 0,03 0,08 |
| Акрилонитрил | Метилметакрилат | 1,0 1013,2 | 1,34 2,01 | 0,12 0,45 | 0,16 0,91 |
| Стирол | Диэтилфумарат | 1,0 101,3 1013,2 | 0,26 0,29 0,32 | 0,06 0,09 0,15 | 0,02 0,03 0,05 |
| Стирол | Цис-1,2-дихлорэтилеи | 1,0 101,3 1013,2 | 0,00 0,00 0,01 | 0,00 0,00 2,20 |
Таким образом, давление приводит к уменьшению избирательности присоединения мономеров к радикалам. Необходимо обратить внимание на то, что значения констант сополимеризации стерически затрудненных мономеров, к которым относят 1,2-ди- и более замещенные этилена, равные или близкие к нулю при атмосферном давлении, при высоком становятся отличными от нуля и (или) увеличиваются (см. табл. 6.7).
Чередующаяся сополимеризация
При сополимеризации электроноакцепторных (А) и электронодонорных (D) мономеров довольно часто образуются сополимеры с регулярным или близким к… К электронодонорным относятся мономеры с развитой системой… 1. Этилен и мономеры с π-σ-сопряжением - α-олефины, циклоалкены, винилциклоалканы, аллиловые…Влияние реакционной среды
Вопреки существовавшему довольно долго после завершения количественной теории сополимеризации мнению, реакционная среда может оказывать существенное… 1. Посредством образования различного рода комплексов между мономерами и… 2. Через избирательную сольватацию растущих цепей мономерами - в том случае, когда последние обладают различным…Связь строения мономера и радикала с реакционной способностью. Схема Q-e
Параллельно с развитием количественной теории сополимеризации полвека назад была разработана количественная схема Алфрея-Прайса, связывающая константы сополимеризации с эмпирическими параметрами реакционной способности. Согласно этой схеме, константа скорости роста в радикальной полимеризации и сополимеризации выражается эмпирическим уравнением:

где Pi и Qj - параметры, учитывающие резонансный; еi и еj - полярный факторы реакционной способности. Исходя из (6.96), легко могут быть получены выражения для относительных активностей мономеров:
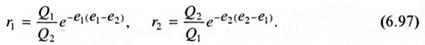
Далее, перемножив относительные активности мономеров в (6.97) и логарифмируя полученное произведение, получаем:

откуда следует, что тенденция к чередованию при сополимеризации определяется лишь разницей значений полярных параметров мономеров.
Схема Q-e широко используется в сополимеризации, так как она позволяет рассчитать относительные активности мономеров и, следовательно, состав и структуру сополимера, не проводя сополимеризации, по известным значениям Q и е мономеров. Эти значения, в свою очередь, были определены путем сополимеризации мономеров с известными и неизвестными значениями Q и е. В качестве исходного мономера был выбран стирол, которому приписаны e - -0,8, Q = 1. Значение схемы Q-e состоит также в том, что она позволила отнести мономеры к определенным группам, исходя из значений параметров Q и е: активным (Q > 0,5) и неактивным (Q < 0,1), электронодонорным (е < 0) и электроноакцепторным (е > 0) и, тем самым, предсказать тип полимеризационного процесса, в котором целесообразно использовать данный мономер. Квантово-химические расчеты показали, что параметры Q и е имеют ясное физическое содержание; это следует из корреляций, приведенных в следующем разделе.
Анализ систематических данных в области радикальной (со)полимеризации приводит к выводу о том, что реакционная способность мономеров и радикалов в реакции роста определяется резонансной стабилизацией (сопряжением), полярностью двойной связи, а также степенью ее экранирования заместителями.
Стерический фактор. Значение стерического фактора проявляется особенно ярко в реакциях радикального присоединения дизамещенных этилена. Известно, что 1,1-дизамещенные легко полимеризуются и сополимеризуются по радикальному механизму, тогда как 1,2-дизамещенные, например малеиновый ангидрид, практически не способны к гомополимеризации, а при сополимеризации их содержание в сополимере не превышает 50%. Причины столь различного поведения этих близких классов непредельных соединений могут быть поняты при рассмотрении стереохимии реакции роста цепи.
Пространственная структура органических соединений в значительной степени определяется типом гибридизации атомов углерода. Ненасыщенные атомы радикала роста и мономера имеют cp2-гибридизацию. Это означает, что оси p-орбиталей ненасыщенных атомов перпендикулярны плоскости, в которой расположены σ-связи. Атомы углерода основной цепи радикала образуют плоский зигзаг, все они, за исключением концевого ненасыщенного атома углерода, имеют cp3-гибридизацию. Из приведенной ниже схемы видно, что при сближении условного тетразамещенного мономера (АВ)С = = C(XY) со «своим» радикалом роста вероятно контактное взаимодействие, т.е. отталкивание заместителей А и В мономера и атома углерода радикала до совмещения осей р-орбиталей. В результате реакция роста не может осуществиться:
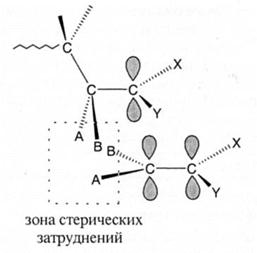
Аналогичная ситуация наблюдается при сближении три- и 1,2-диза-мещенных этилена со «своим» радикалом роста. Таким образом, полимеризация тетра-, три- и 1,2-замещенных этилена невозможна по чисто стерическим причинам. Исключением являются фторзамещенные этилена, при полимеризации которых, благодаря малому радиусу заместителя, стерические трудности не возникают. В отличие от полимеризации, сополимеризация тетра-, три- и 1,2-дизамещенных этиленов с моно- или 1,1-дизамещенными возможна. В этом случае в «опасной зоне» противостоят заместители и атомы водорода, что, как правило, не препятствует сближению мономера и радикала и протеканию реакции роста. Однако, поскольку элементарные акты гомополимеризации дизамещенного мономера невозможны, то содержание этого мономера в сополимере не превышает 50 %.
Таблица 6.1 Сополимеризация винилацетата (1) с хлорзамещенными этилена (2)
| Мономер | r1 | r2 |
| Тетрахлорэтилсн | 6,8 | |
| Трихлорэтилен | 0,66 | 0,01 |
| Цис-дихлорэтилен | 6,3 | 0,018 |
| Транс-дихлорэтилен | 0,99 | 0,086 |
| Винилиденхлорид | 3,6 | |
| Винилхлорид | 0,23 | 1,68 |
В табл. 6.8 приведены данные, иллюстрирующие влияние стерического фактора в сополимеризации. Винилхлорид и 1,2-дизамещенный мономер винилиденхлорид более активны по сравнению с винилацетатом (r1 > r2). Однако три- и тетразамещенные хлорэтилены менее активны, причем r1 =0, вследствие их неспособности к гомополимеризации. Транс-1,2-дизамещенные менее реакционноспособны по сравнению с цис-1,2-дизамещенными, что является общим правилом в сополимеризации.
Резонансный фактор. Значение резонансного фактора реакционной способности или влияние сопряжения на реакционную способность мономеров наиболее ярко проявляется в радикальной сополимеризации и полимеризации. В зависимости от наличия или отсутствия сопряжения двойной связи мономера с ненасыщенной группой заместителя все мономеры делятся на активные и неактивные. Типичные представители каждой группы представлены ниже:
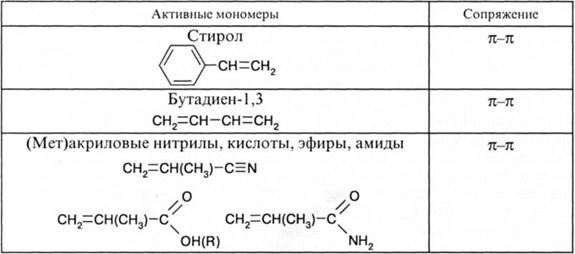
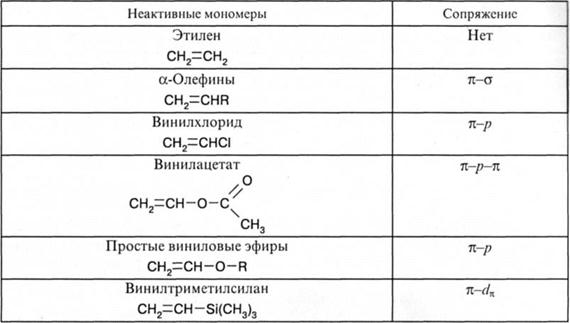
Из сравнения приведенных структур видно, что лишь прямое π-π-сопряжение в мономере делает его активным в сополимеризации, другие типы сопряжения неэффективны.
Как правило, сополимеризация целесообразна между мономерами одной группы, ибо только в этом случае удается избежать чрезмерного отличия состава сополимера от состава мономерной смеси. Так, на начальной стадии сополимеризации эквимолярных смесей неактивных мономеров винилхлорида и винилацетата и активных мономеров стирола и акрилонитрила образуются сополимеры, содержащие в первом случае 69 мол.% винилхлорида. во втором - 60 мол.% стирола. При сополимеризации же эквимолярных смесей неактивного мономера с активным - винилацетата со стиролом - образуется сополимер, содержащий 98 мол.% стирола, т. е. практически гомополимер.
Рассмотрим данные по константам скорости элементарных реакций роста цепи (л/(моль·с)) совместной и раздельной полимеризации винилацетата (1) и стирола (2) при 25°С:
| k11 | k22 | r1 | r2 | k12 | k11 |
| 0,04 | 0,73 |
Видно, что активный мономер стирол присоединяется к радикалу роста винилацетата со скоростью на четыре порядка большей по сравнению с неактивным мономером винилацетатом (k12 и k11). При сравнении резонансной способности радикалов ситуация изменяется на противоположную. Скорость присоединения радикала винилацетата к «своему» мономеру на три порядка больше по сравнению со скоростью присоединения радикала роста стирола к винилацетату (k11/k21 = 873). Аналогичная картина выявляется при сравнении скоростей присоединения радикалов роста стирола и винилацетата к мономеру стирола (k12/k22 =400). Таким образом, сопряжение или резонансный эффект противоположным образом влияет на реакционную способность мономеров и радикалов - увеличивает активность первых и уменьшает активность вторых. Из этого следует, что ряды реакционной способности мономеров и соответствующих им радикалов противоположны. Это положение известно как правило антибатности.
Таблица 6.9 Влияние резонансного фактора на величину константы скорости роста, 20-30°С
| Мономер | Q | kР, л/(моль·с) |
| Винилацетат | 0,026 | |
| Винилхлорид | 0,044 | |
| N-Винилпирролидон | 0,14 | |
| Метилметакрилат | 0,74 | |
| Стирол | ||
| Бутадиен-1,3 | 2,39 | 8,4 |
| Изопрен | 3,33 | 2,8 |
Влияние резонансного фактора реакционной способности весьма значительно также по отношению к скорости радикальной полимеризации и сополимеризации. Из табл. 6.9 видно, что константы скорости реакции роста ряда мономеров уменьшаются при увеличении резонансного параметра Q, т.е. с увеличением эффективности сопряжения двойной связи мономера с заместителем. В частности, константа скорости роста неактивного мономера винилацетата на два порядка больше по сравнению с активным мономером стиролом. На первый взгляд, этот результат кажется удивительным, поскольку, вследствие правила антибатности, высокая активность мономера компенсируется малой активностью соответствующего ему радикала, и наоборот. Дело заключается в том, что влияние сопряжения на реакционную способность мономеров и соответствующих им радикалов роста неодинакова по эффективности - активность мономера возрастает в меньшей степени по сравнению со стабилизацией, т. е. уменьшением реакционной способности радикала.
Третий важный эффект, обусловленный резонансным фактором реакционной способности, связан со строением полимерной цепи. Ранее рассматривалась возможность химической изомерии повторяющихся участков цепи, состоящих из нескольких звеньев, вследствие их различной ориентации вдоль цепи (разд. 1.1.5). Ниже представлена схема, на которой приведены два возможных направления реакции роста при сополимеризации стирола:
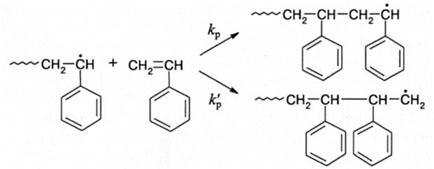
В первом случае реализуется сопряжение ароматического заместителя с образующимся радикалом и переходным комплексом, и поэтому мономер ведет себя как активный. Во втором случае сопряжение отсутствует, поскольку ненасыщенный атом углерода радикала разделен с ароматическим заместителем двумя σ-связями, и в этом случае мономер является неактивным. В результате первая реакция оказывается более предпочтительной (kр >> к'р) и присоединение радикала к мономеру происходит с вероятностью, большей 90 % по типу «голова» к «хвосту».
В основе механизма действия резонансного фактора реакционной способности лежит эффект стабилизации, уменьшения π-электронной энергии переходного состояния и радикала роста за счет сопряжения с заместителем. Количественно резонансный фактор стабилизации учитывается параметрами Р, Q схемы Q-e Алфрея-Прайса и рядом квантово-химических параметров, среди которых наиболее часто используется порядок связи Р и энергия локализации. Особое значение для характеристики реакционной способности ненасыщенных молекул имеет энергия локализации L, понятие о которой ввел впервые Уэланд. Применительно к реакции роста ее физический смысл заключается в следующем. Атом углерода мономера, атакуемый радикалом, изменяет гибридизацию sp2 на sp3 и, таким образом, выбывает из системы сопряжения. Энергия, необходимая для этого, и называется энергией локализации мономера Lβ. Аналогичное рассуждение можно провести и по отношению к сопряженному радикалу, однако энергия локализации радикала La не оказывает существенного влияния на относительные активности мономеров. Величину Lβ можно рассчитать как энергию перехода мономера в бирадикальное триплетное состояние:
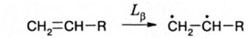
Обозначим энергию π-электронов мономера EM радикала  через Ер и радикала
через Ер и радикала 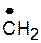 - α (кулоновский интеграл). Тогда энергия локализации мономера Lβ оказывается равной:
- α (кулоновский интеграл). Тогда энергия локализации мономера Lβ оказывается равной:

В табл. 6.10 приведены значения различных резонансных параметров мономеров, рассчитанные квантово-химическим методом. Все они коррелируют с lnQ и между собой. На рис. 6.10 приведена корреляция между Lβ - наиболее известным квантово-химическим параметром, характеризующим ре-зонансный фактор реакционной способности, и InQ.
Из данных рис. 6.10 и табл. 6.10 следует, что с увеличением параметра Q абсолютное значение энергии локализации мономера падает. Это означает, что с увеличением энергии сопряжения в мономере снижается энергия, необходимая для активации разрыва его двойной связи.
Таблица 6.10 Эмпирические и расчетные квантово-химические резонансные параметры строения мономеров и радикалов
| Мономер | InQ | Lβ | Р | Lα |
| CH2=C(CN)2 | 3,0 | 1,598 | 0,835 | 1,414 |
| CH2=CH-CH=CH2 | 0,871 | 1,644 | 0,894 | 0,828 |
| СН2=С(СН3)СНО | 0,372 | - | - | - |
| CH2=CH-CONH2 | 0,174 | - | - | |
| CH2=C(CH3)CN | 0,113 | 1,639 | - | 0,897 |
| СН2=СНС6Н5 | 0,00 | 1,704 | 0,911 | 0,721 |
| СН2=СНСНО | -0,163 | - | 0,910 | |
| СН2=С(СН3)СООСН3 | -0,301 | 1,737 | - | 0,691 |
| CH2=CH-CN | -0,511 | 1,696 | 0,913 | 0,839 |
| CH2=CH-COOCH3 | -0,868 | 1,783 | 0,914 | 0,645 |
| СН2=ССl2 | -1,514 | 1,832 | - | 0,867 |
| СН2=СНСН2ОН | -3,04 | - | - | - |
| СН2=СНСl | -3,12 | 1,877 | 0,989 | 0,474 |
| СН2=С(СН3)2 | -3,41 | - | - | - |
| CH2=CH-OC2H5 | -3,44 | 1,841 | 0,966 | 1,647 |
| CH2=CH-OCOCH3 | -3,65 | 1,885 | 0,965 | 0,445 |
| CH2=CHF | -3,69 | - | - | - |
| СН2=СН2 | -4,20 | 2,000 | 1,000 | 0,000 |
| СН2=СНСН3 | -6,21 | - | - | - |
Р - порядок связи в мономере, Lβ и Lα - энергии локализации мономера и радикала роста в единицах Р (резонансный интеграл).
Рассмотрим изменение потенциальной энергии сближающихся мономера и радикала с учетом энергии локализации мономера Lβ. Сближение неактивированных частиц должно приводить к возникновению сил отталкивания и, следовательно, возрастанию потенциальной энергии (рис. 6.11, кривая 2). Сближение радикала с активированным мономером, т.е. находящимся в бирадикальном состоянии, приводит к снижению потенциальной энергии (кривая 1), которая в данном случае изменяется в соответствии с функцией Морзе. Последняя описывает изменение потенциальной энергии при разъединении двух атомов, связанных химической связью. Из рис. 6.11 видно, что уменьшение энергии локализации приводит к снижению энергии активации реакции роста, т.к. положение кривой «отталкивания» (кривая 2) практически не зависит от строения мономера и величины Lβ.
Изложенный выше подход, развитый Эвансом и Шварцем, не учитывает роли полярного и стерического факторов. Реакционная способность мономеров и радикалов, определяемая лишь резонансным фактором, называется идеальной реакционной способностью.
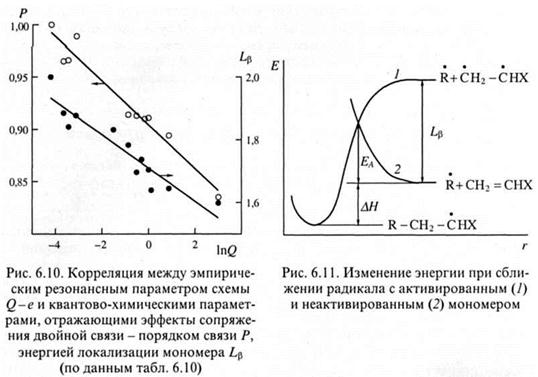
Полярный фактор. Двойная связь мономеров, подверженных радикальной сополимеризации, как правило, является поляризованной вследствие донорно-акцепторного действия заместителей, как и ненасыщенный атом углерода радикала роста:

Донорно-акцепторный эффект заместителей приводит к возникновению частичных зарядов на β-атоме углерода двойной связи и α-атоме углерода концевого звена радикала роста (ненасыщенном).
Влияние полярного фактора реакционной способности наиболее ярко проявляется в радикальной сополимеризации, где он ответственен за возникновение эффекта чередования мономерных звеньев. Впервые на значение полярного фактора в сополимеризации обратил внимание Прайс, который сделал заключение о том, что «легче всего сополимеризация протекает в таких бинарных системах, в которых один мономер имеет избыток, другой -недостаток электронов». Долгое время природа полярного эффекта объяснялась с позиции электростатических взаимодействий, что было признано впоследствии неудовлетворительным. Другая гипотеза, получившая широкое распространение к настоящему времени, объясняла склонность к чередованию звеньев при сополимеризации переносом электрона между компонентами переходного комплекса, т.е. является развитием гипотезы Уоллинга:
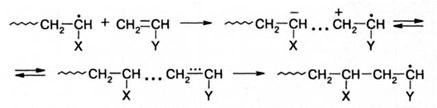
В приведенной схеме мономер СН2=СНХ, например метилметакрилат, и соответствующий ему радикал роста являются акцепторами электрона, а мономер CH2=CHY, например стирол, является донором электрона. Считается, что вклад ионной структуры в переходное состояние снижает энергию активации перекрестного роста, в результате при сополимеризации проявляется тенденция к чередованию мономерных звеньев, однако, образующийся сополимер остается статистическим. Изложенный механизм согласуется с данными квантово-химических расчетов, согласно которым с увеличением разности значений полярных параметров мономеров |e1 - e2| возрастает перенос заряда между компонентами переходного комплекса.
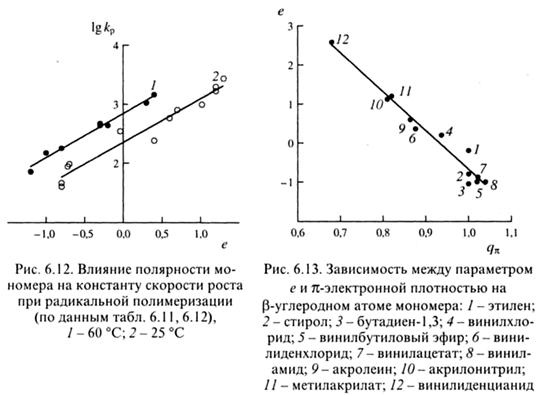
Таблица 6.11 Значения константы скорости реакции роста и параметра e пара-замещенных стирола, 60°С
| Заместитель | (СН3)2 | ОСН3 | Н | CI | Br | F | CN | O2R |
| kр, л/(моль·с) е | -1,2 | -1,0 | -0,8 | -0,3 | -0,2 | -0,3 | 0,3 | 0,4 |
Таблица 6.12 Значения константы скорости реакции роста и параметра е некоторых мономеров, 25-30°С
| Мономер | kp, л/(моль·с) | e | Q |
| 2-Метил-5-винилпиридин | 46, 25°С | -0,80 | 1,1 |
| Стирол | 40, 25°С | -0,80 | 1,0 |
| 4-Винилпиридин | 87, 25°С | -0,72 | 1,12 |
| 2-Винилпиридин | 96,5, 25°С | -0,70 | 1,35 |
| трет-Бутиловый эфир | 350, 25°С | -0,04 | 0,77 |
| метакриловой кислоты | |||
| Метилметакрилат | 240, 25°С | 0,40 | 0,74 |
| Метилакрилат | 580, 25°С | 0,60 | 0,42 |
| Бутилакрилат | 976, 25°С | 1,02 | 0,52 |
| Акрилонитрил | I960, 26°С | 1,20 | 0,60 |
| Этил-β-хлоракрилат | 1660, 30°С | 1,20 | 3,00 |
| Акриламид | 2700, диметилсульфоксид, 20 °С | 1,30 | 1,18 |
| Метакриламид | 800, 25°С | 0,70 | 0,70 |
Влияние полярного фактора существенно и в реакции гомополимеризации. Во-первых, мономеры с очень большим отрицательным значением параметра е, например винилалкиловые эфиры, не способны к гомополимеризации. Во-вторых, в ряду мономеров с соизмеримыми величинами параметра Q константа скорости роста закономерно возрастает с увеличением параметра е (рис. 6.12)- примерно на порядок при изменении е на единицу.
Таблица 6.13 Значения параметров реакционной способности мономеров схемы Q-e
| Мономер | Q | е |
| Впннлэтиловын эфир | 0,018 | -1,80 |
| Стирол | -0,80 | |
| Метилакрилат | 0,45 | 0,64 |
| Метакриловая кислота | 0,98 | 0,62 |
| Акриловая кислота | 0,83 | 0,83 |
| Бутадиен-1,3 | 1,70 | -0,50 |
| Изопрен | 1,99 | -0,55 |
| Винилацетат | 0,026 | -0,88 |
| Винилхлорид | 0,056 | 0,16 |
| Акрилонитрил | 0,48 | 1,23 |
| Метилметакрилат | 0,78 | 0,40 |
Таблица 6.14 Относительные активности при сополимеризации некоторых мономеров
| М1 | М2 | r1 | r2 |
| Активный с активным | |||
| Стирол | Метилметакрилат | 0,50 | 0,46 |
| Стирол | Метилакрилат | 0,75 | 0,18 |
| Стирол | Акрилонитрил | 0,38 | 0,04 |
| Метилметакрилат | Метилакрилат | 2,15 | 0,40 |
| Метилметакрилат | Акрилонитрил | 1,32 | 0,14 |
| Метилакрилат | Акрилонитрил | 0,85 | 1,42 |
| Бутадиен-1,3 | Акрилонитрил | 0,35 | 0,05 |
| Стирол | Бутадиен-1,3 | 0,78 | 1,39 |
| Активный с неактивным | |||
| Стирол | Винилацетат | 0,04 | |
| Метилметакрилат | Винилхлорид | 0,02 | |
| Неактивный с неактивным | |||
| Винилхлорид | Винилацетат | 1,68 | 0,23 |
Несмотря на то, что схема Q-e является полуэмпирической, имеется четкая физическая интерпретация полярного характера параметра е. Она следует из линейной корреляции между значениями параметра е и величиной π-электронного заряда на β-углеродном атоме мономера, рассчитанного квантово-химическими методами (рис. 6.13).
В табл. 6.13 и 6.14 приведены значения Q, е и r1, r2, относящиеся к наиболее распространенным мономерам.
Ионная сополимеризация
Ка i ионная сополимеризация
При катионной сополимеризации обычно r1 > 1, r2 < 1 (или наоборот), а произведение r1·r2 близко к единице, но часто превышает этот предел.… Активность мономеров в катионной сополимеризации определяется не только их…Таблица 6.15 Катионная сополимеризация некоторых мономеров
| М1 | М2 | r1 | r2 | Растворитель | Инициатор |
| Изобутилен | n-Хлорстирол | 1,0 | 1,0 | н-Гексан (ε=1,8) | АlBr3, -90°С |
| » | » | 14,7 | 0,15 | Нитробензол (ε=36) | » |
| » | » | 8,6 | 1,2 | » | AlCl3, 0°С |
| » | Стирол | 3,0 | 0.6 | CCl4 | 0°С SnCl4 |
| Тетрагидрофуран | β-Пропиолактон | 2,9 | 0,4 | - | 0oC, BF3·H2O |
| » | Окись этилена | 2,2 | 0,08 | - | BF3·(С2Н5)2О |
| » | Окись пропилена | 0,3 | 1,50 | - | » |
| Стирол | β-Пропиолактон | 0,04 | Метилхлорид | » | |
| » | Триоксан | 0,37 | Толуол | » |
При сополимеризации в неполярных растворителях избирательная сольватация ионной пары более полярным мономером может оказывать большое влияние на состав сополимера. Этот эффект иллюстрируется данными табл. 6.15.
Как следует из результатов сополимеризации изобутилена с n-хлорстиролом, первый является существенно более активным при сополимеризации в полярных растворителях вследствие наличия двух электронодонорных заместителей. При сополимеризации в неполярном растворителе более полярный из двух мономеров n-хлорстирол сольватирует ионную пару, что приводит к увеличению его содержания в сополимере и сближению величин относительных активностей мономеров. В данном случае реализуется идеальная сополимеризация, что не является редкостью при катионном процессе. Из табл. 6.15 также видно, что изобутилен более активен, чем стирол, в катионной сополимеризации. Это подчеркивает главенствующее значение полярного фактора реакционной способности по сравнению с резонансным в катионной полимеризации. Далее из табл. 6.15 следует, что простые циклические эфиры активнее сложных, т.е. лактонов, а виниловый мономер стирол и гетероциклы активнее того и другого.
Анионная сополимеризация
В анионной сополимеризации более активны мономеры с электроноак-цепторными заместителями: акрилонитрил > (мет)акриловые эфиры > стирол > изопрен, бутадиен-1.3Таблица 6.17 Влияние растворителя и противоиона на состав сополимера при сополимеризации стирола с изопреном
| Растворитель | Содержание стирола в сополимере, % | |
| Na+ | Li+ | |
| Без растворителя Бензол Триэтиламин Диэтиловый эфир Тетрагидрофуран |
При сополимеризации в полярном растворителе тетрагидрофуране при -78°С ионная пара сольватирована им, поэтому активность бутадиена-1,3 резко падает. При 25°С она становится не столь доминирующей, что допускает определенное присутствие бутадиена-1,3 в сольватной сфере ионной пары. В результате активность этого мономера несколько возрастает.
Аналогичен механизм влияния растворителя во втором примере (см. табл. 6.17). Растворитель - донор электронной пары приводит к уменьшению содержания изопрена в сополимере. Этот эффект ярче выражен для противоиона Li+, поскольку последний вследствие большей плотности заряда изначально образует более прочные ассоциаты с изопреном.
Анионная сополимеризация стирола (1) с метилметакрилатом (2) примечательна чрезвычайно большой разницей в активности мономеров r1 << 1, r2 >> 1.
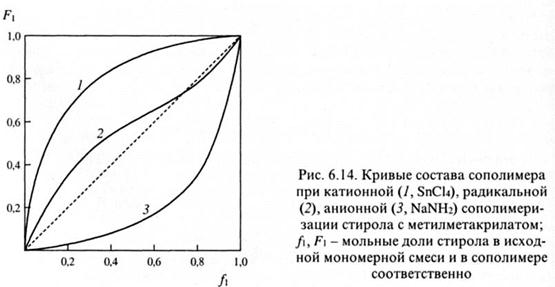
Радикал роста метилметакрилата практически не взаимодействует с мономером стирола (но не наоборот), что необходимо учитывать при получении блок-сополимеров этих мономеров методом живой полимеризации. Как следует из рис. 6.14, данная система может быть использована для установления механизма цепной сополимеризации и, следовательно, отнесения инициатора (обычно металлоорганического соединения) к одному из трех возможных типов - радикальной, катионной или анионной сополимеризации.
Сополимеризация на катализаторах Циглера-Натта
Сополимеризация с использованием катализаторов Циглера-Натта приводит к статистическим сополимерам. Обычно ряды активности мономеров в… этилен > пропилен > бутен-1.Таблица 6.18 Реакционная способность различных мономеров в сополимеризации Циглера-Натта
| М1 | М2 | Каталитическая система | r1 | r2 |
| Этилен | Пропилен | ТiСl3-Аl(С6Н13)3 ТiCl4-Аl(С6Н13)3 VCl3-Аl(С6Н13)3 | 15,7 33,4 5,61 | 0,110 0,032 0,145 |
| Этилен | Бутен-1 | VCl4-Аl(С6Н13)3 VCl3-Аl(С6Н13)3 | 29,6 67,0 | 0,019 0,043 |
| Пропилен | Бутен-1 | VCl4-Аl(С6Н13)3 VCl3-Аl(С6Н13)3 | 4,39 4,04 | 0,227 0,252 |
Завершая раздел ионной сополимеризации, следует еще раз остановиться на особенностях, отличающих ее от радикальной сополимеризации: повышенной чувствительности к полярности двойной связи; склонности к идеальной сополимеризации и отсутствию чередующейся; повышенной чувствительности к реакционной среде и температуре.
ГЛАВА 7. ХИМИЯ ПОЛИМЕРОВ
Характерные особенности макромолекул как реагентов
Влияние соседних звеньев
Согласно принципу Флори, реакционная способность функциональных групп макромолекул не должна отличаться от реакционной способности тех же групп в… Эффект соседа. Эффект соседа наиболее просто может быть интерпретирован в…Макромолекулярные и надмолекулярные эффекты
Гидрофобное взаимодействие. Если реакция проводится в водном растворе полимера, то на ее скорость может оказать влияние сродство между гидрофобными…Сшивание полимеров
Известно, что сшивка позволяет существенно улучшить свойства полимеров, повысить их термостабильность и устойчивость к действию растворителей. Поэтому реакции сшивки линейных полимеров имеют большое практическое значение.
Высыхание красок
Важное место среди полимеров, предназначенных для получения различного рода покрытий (красок), пленок и волокон, занимают полиэфиры. Сшивка…Вулканизация каучуков
До настоящего времени сшивка полимеров диенов-1,3 в промышленном масштабе осуществляется путем вулканизации серой. Впервые этот процесс был… Согласно первоначальной точке зрения, реакция серы с каучуком протекает по… В пользу ионного механизма вулканизации свидетельствуют многие факторы - ускоряющее действие кислот и оснований, а…Отверждение эпоксидных смол
Эпоксидные смолы образуются в результате реакции эпихлоргидрина с гидроксилсодержащими соединениями, например 2,2-дифенилолпропаном в щелочной…Деструкция полимеров
При эксплуатации или хранении полимеры стареют, что проявляется в неблагоприятном изменении комплекса их свойств. Старение полимеров может быть… Деструкция полимера может протекать в результате разрыва или распада… Различают физическую и химическую деструкцию. Физическая деструкция протекает под действием теплоты, света, излучений…Термическая деструкция. Циклизация
Термическая деструкция полимера протекает при высоких температурах в инертной атмосфере или в вакууме. Иногда этот процесс называют пиролизом. Из табл. 7.1 следует, что термический распад наименее стойких полимеров - поливинилхлорида и полиметилметакрилата - начинается при 150 и 220°С, а наиболее стойких - полидиметилсилоксана, политетрафторэтилена и полиимида - при 300, 400 и 450°С, соответственно.
Таблица 7.1 Температуры начала разложения и энергии активации термического распада некоторых полимеров
| Полимер | ЕA, кДж/моль | Температура начала разложения, °С |
| Полиэтилен | ||
| Полиметилакрилат | ||
| Полиметилметакрилат | ||
| Полистирол | ||
| Поливинилхлорид | 83-158 | |
| Поливинилацетат | 167-288 | |
| Полиакрилонитрил | ||
| Полиизопрен | ||
| Полиэтилентерефталат | ||
| Полидиметилсилоксан | - | |
| Политетрафторэтилен | ||
| Полиимид | - |
Деструкция по радикальному механизму. В большинстве случаев термический распад полимеров протекает как цепной радикальный процесс со стадиями инициирования, роста, передачи и обрыва цепи. Инициирование термического распада осуществляется за счет разрыва химических связей двух типов - слабых, например аллильных или пероксидных, и повторяющихся связей основной цепи. В соответствии с этим термический распад большинства полимеров протекает в две стадии - при разных температурах и с существенно различными энергиями активации (в табл. 7.1 приведены энергии активации второй стадии). Основная масса полимера, как правило, распадается на второй стадии термического распада.
Кинетическая цепь при термическом распаде полимеров развивается в результате трех элементарных реакций - деполимеризации, передачи цепи и β-распада радикалов. В результате термической деструкции полимер распадается на летучие продукты (часто нацело), состав которых определяется соотношением скоростей элементарных реакций роста цепи.
При распаде полиметилметакрилата (табл. 7.2), а также поли- α -метилстирола, полиформальдегида и некоторых других полимеров практически единственным продуктом является мономер. Это означает, что термический распад таких полимеров осуществляется посредством деполимеризации - реакции, обратной полимеризации.
Таблица 7.2 Продукты термического распада некоторых полимеров
| Полимер | T, °с | Глубина распада | Продукты распада, % | ||
| мономер | олигомер | углеводороды | |||
| Полиметилметакрилат | 60 % за 0,5 ч | ~100 | Следы | Следы | |
| Полистирол | 50 % за 2ч | Толуол - 3, другие - 1 | |||
| Полиэтилен | 3,4 % за 0,5 ч | 0,2 | Бутен - 1, бутан - 0,8 другие - 2 |
Деполимеризация карбоцепных полимеров протекает по радикальном) механизму, а для гетероцепных полимеров более характерен ионный механизм (например, для полиформальдегида). Термодинамическими условиями деполимеризации являются Т>Тп и [М]<[М]равн. Для большинства полимеров виниловых мономеров при T>200°С равновесные концентрации мономеров не превышают 10-3 - 10-5 моль/л. Однако при высокой температуре мономер, образующийся в результате деполимеризации, быстро улетучивается, поэтому условие [М]<[М]равн обычно выполняется.
Соблюдение термодинамических критериев является необходимым, но не достаточным условием деполимеризации. Для ее развития необходимо, чтобы макрорадикалы с активным центром на конце цепи были достаточно устойчивы, а полимер не содержал бы подвижных атомов водорода, обычно находящихся при третичных атомах углерода. Степень стабилизации активного центра на конце цепи можно качественно оценить по величине параметра Q. Данные табл. 7.3 находятся в полном соответствии с таким выводом. В случае полиметилметакрилата выполняются оба условия, способствующие деполимеризации. Поэтому при термическом распаде этого полимера выход мономера близок к количественному. Для полистирола и полиизобутилена выполняется одно из перечисленных выше условий. В продуктах термического распада этих полимеров доля мономера достаточно высока и, следовательно, реакция деполимеризации играет заметную роль среди других реакций продолжения кинетической цепи. В случае полиэтилена (и большинства других полиолефинов) не выполняется ни одно из условий, способствующих деполимеризации. Поэтому при термическом распаде таких полимеров этот процесс практически не протекает.
Таблица 7.3 Выход мономера при термическом распаде различных полимеров
| Полимер | Q | Содержание мономера в продуктах распада, % |
| Полиметилметакрилат Полистирол Полиизобутилен Полипропилен | 0,74 1,00 0,33 0,02 | ~100 Менее 1 |
Важную роль при термическом распаде полимеров играет реакция передачи цепи, о чем можно судить по следующим данным. Присутствие небольшого числа (10-15%) звеньев акриловых эфиров, стирола или акрилонитрила в сополимере с метилметакрилатом в несколько раз снижает скорость его термического распада по сравнению с гомополимером (полиметилметакрилатом). В продуктах термического распада полимеров акриловых эфиров практически отсутствует мономер. Указанные факты объясняются обрывом цепей деполимеризации в результате внутри- и межмолекулярной реакции передачи цепи на звенья акриловых эфиров, имеющие подвижные атомы водорода. Значение реакции передачи цепи определяется также тем, что эта реакция приводит к переносу свободной валентности. Как следует из табл. 7.2, при термическом распаде некоторых полимеров основным продуктом является олигомер. В специальных опытах было установлено, что олигомер, образующийся при термическом распаде полиэтилена, аналогичен ему по химическому составу. Средняя молекулярная масса олигомера равна 700; почти каждая из молекул олигомера содержит на конце двойную связь. Образование олигомера при термической деструкции полиэтилена, полистирола и других полимеров объясняется последовательным протеканием реакций внутримолекулярной передачи цепи и β-распада образующихся срединных радикалов:
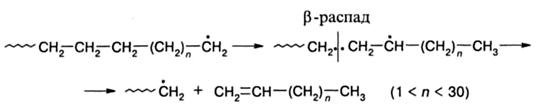
Реакция β-распада срединных радикалов, образующихся в результате межмолекулярной передачи цепи, наряду с реакцией разрыва углерод-углеродных связей основной цепи по закону случая приводит также к быстрому уменьшению молекулярной массы полиэтилена и других полимеров в процессе их термического распада (рис. 7.2).
Циклизация полиакрилонитрила.Этот полимер представляет большую практическую ценность как исходный материал для производства текстильных и высокомодульных армирующих волокон.
При нагревании полиакрилонитрила до 250 °С полимер окрашивается в светло-, затем - в темно-коричневый цвет, что связано с образованием сопряженных связей в результате полимеризации нитрильных групп по радикальному механизму:
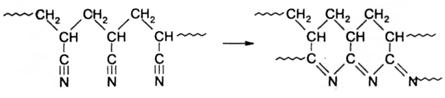
Этот процесс является высокоэкзотермичным. Параллельно выделяется аммиак - из концевых иминогрупп NH сопряженных структур и циановодород. Последний отщепляется от звеньев акрилонитрила, не участвовавших в процессе циклизации, которые расположены между короткими сопряженными нитрильными структурами. Экзотермическому процессу предшествует и сопровождает его заметное уменьшение молекулярной массы полимера и выделение в составе летучих продуктов олигомерной фракции, что связано с разрывом основной цепи. При дальнейшем нагревании выделяется водород (выше 300°С), образующийся в результате дегидрирования и ароматизации циклических структур и азот (850-900°С). После нагревания полимера до 1000°С в строгом соответствии со специальной программой (вначале он длительно прогревается при 200°С на воздухе), остается практически чистый графитный углерод, сохранивший форму исходного «текстильного» волокна. Другой пример циклизации, используемой при получении полиимидов, приведен в разд. 5.6.8.
Нерадикальные реакции деструкции. В качестве примера ниже рассмотрена термическая деструкция трех важных в практическом отношении полимеров.
Полисилоксаны. Наиболее распространенный из этого класса полимеров - полидиметилсилоксан - начинает распадаться при температурах, больших 300°С. Продуктами распада являются циклические олигомеры - от тримера до гептадекамера. Общепринятый механизм их образования предполагает возникновение циклических промежуточных структур с участием концевой группы, в которых и происходит согласованные разрыв и образование связей:
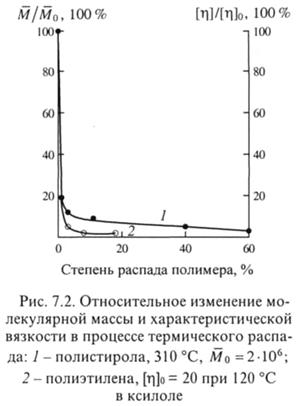
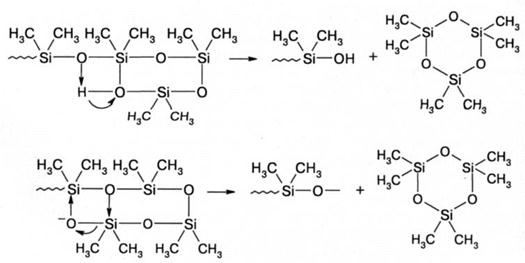
Первая схема относится к нестабилизированному полимеру с конечной ОН-группой, второй - к полимеру, стабилизированному путем замены конечной ОН-группы.
Полиуретаны. Термический распад полиуретанов протекает в две стадии. При T>220°С происходит исчезновение уретановых групп в полимере без выделения каких-либо летучих продуктов. Это происходит в результате деполимеризации, т.е. процесса, обратного уретанобразованию:
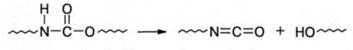
В отличие от цепной деполимеризации, рассмотренной ранее, разрыв уретановых групп полиуретанов протекает по закону случая. На второй стадии распада выделяются летучие в результате многочисленных превращений достаточно высокомолекулярных продуктов деполимеризации, находящихся в «горячей» зоне. Среди них СО, СО2, HCN, диимиды и др.* (* Грасси Н., Скотт Дж. Деструкция и стабилизация полимеров. М.: Мир, 1988. С. 47-48. 52-55.)
Полиэфиры. Первичной реакцией является распад эфирной группы, что приводит к разрыву основной цепи. Реакции предшествует образование циклического комплекса:
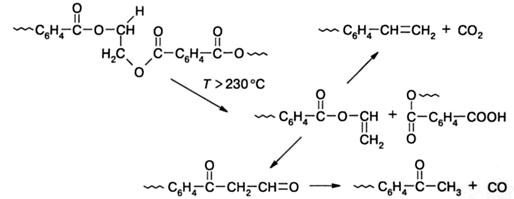
Основные летучие продукты распада образуются в результате дальнейших превращений конечной винилбензоатной группы - терефталевая кислота, ацетальдегид, оксид углерода. В меньшем количестве образуются бензойная и ацетилбензойная кислоты, ангидриды, ацетофенон, кетоны, этилен, ацетилен, метанол.
Поливинилхлорид. Данный полимер относится к числу полимеров, термическая деструкция которых изучена наиболее детально. Тем не менее, до настоящего времени существуют две точки зрения на механизм деструкции поливинилхлорида. Согласно одной из них, он является молекулярным, согласно другой - радикальным.
Поливинилхлорид - один из наименее термически стойких полимеров. Его распад с заметной скоростью начинается от 150°С. Продуктом термического распада поливинилхлорида является хлороводород, а также на глубоких стадиях следы бензола.
Для выяснения механизма распада поливинилхлорида была изучена кинетика дегидрохлорирования ряда модельных соединений. Из приведенных
ниже значений k(с-1) следует, что значение константы скорости мономолекулярной реакции дегидрохлорирования при 170°С значительно возрастает для тех соединений, в которых имеется сопряжение связи С-Сl с одной или двумя непредельными связями:
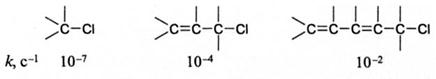
Эти данные хорошо объясняют образование полиеновых последовательностей на самой ранней стадии дегидрохлорирования. Двойные связи, образовавшиеся после случайного отщепления хлороводорода от основной цепи, активируют соседние связи С-Сl. При увеличении длины ненасыщенного участка эффект активации возрастает.
Полиеновые последовательности увеличиваются с возрастающей скоростью до тех пор, пока их рост не ограничивает одна из реакций, приводящих к потере сопряжения между ненасыщенной группировкой и связью С-Сl. Одна из них - реакция Дильса-Альдера - приводит к сшиванию цепей и потере растворимости полимера. К нарушению сопряжения полиеновой последовательности со связью C-CI приводит также реакция внутримолекулярной циклизации. Образующиеся циклодиенильные фрагменты при высокой температуре неустойчивы. При согласованном распаде двух связей С-С, сопряженных с диеновой последовательностью, отщепляется молекула бензола:
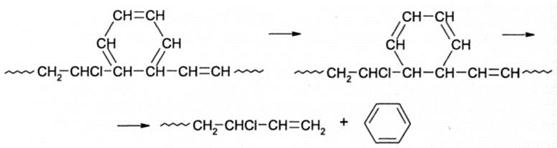
Расчеты показывают, что скорость дегидрохлорирования поливинилхлорида, инициируемого в результате случайного отщепления хлороводорода, существенно меньше наблюдаемой в опытах. Из этих результатов был сделан вывод о том, что первые акты отщепления хлороводорода, которые можно рассматривать как стадию инициирования, проходят с участием аномально подвижных атомов хлора. В промышленных образцах поливинилхлорида такие атомы хлора, часто называемые лабильными, могут находиться в непосредственной близости к случайным дефектам полимерной цепи - разветвлениям, контактам мономеров по типу «голова к голове», пероксидным или кислородсодержащим ненасыщенным группам.
Значительное каталитическое влияние на термической распад поливинилхлорида оказывает хлороводород, поэтому этот продукт термического распада следует связывать или удалять из системы. В противном случае кинетические кривые приобретают автокаталитический характер.
Термоокислительная деструкция. Горение
Наиболее губительной для полимеров по своим последствиям является термоокислительная деструкция. Считается, что механизм окисления полимеров не… Инициирование окисления «чистого» полимера теоретически возможно в результате…Таблица 7.4 Ограниченный кислородный показатель для некоторых полимеров
| Полимер | ОКП, мол.% | Полимер | ОКП, мол.% |
| Полиоксиметилсн | Нейлон | ||
| Полиметилметакрилат | Полифениленоксид | ||
| Полиэтилен | Поливинилхлорид | ||
| Полипропилен | Поливинилиденхлорид | ||
| Полистирол | Политетрафторэтилен | ||
| Поливиниловый спирт |
В воздухе содержится 21 мол.% кислорода, откуда следует, что, например полиметилметакрилат в воздухе гореть будет, а поливинилхлорид - нет.
Фотодеструкция. Фотоокисление
Фотохимические превращения происходят в полимере под действием ультрафиолетового (180<λ<400нм) и видимого света (400<λ<800нм),… Солнечный свет, достигший поверхности Земли, содержит ультрафиолетовый участок… Первичные процессы в полимерах проходящие под действием света, зависят от природы хромофорной группы. Как уже…Полимераналогичные превращения
Значительная часть полимерных материалов получается путем полимераналогичных, т.е. не приводящих к разрыву основной цепи, превращений базовых полимеров. В качестве примера рассмотрим наиболее важные в практическом отношении полимераналогичные превращения поливинилового спирта и целлюлозы.
Поливиниловый спирт
В промышленности поливиниловый спирт получают алкоголизом поливинила цетата:Химические превращения целлюлозы
Путем полимераналогичных превращений из целлюлозы получают три основных класса ценных полимерных материалов:Структурная модификация целлюлозы
Гидратцеллюлоза аналогична по составу исходной целлюлозе, отличается от нее расположением звеньев и большей степенью гидратации полярных групп.…ЛИТЕРАТУРА
1. Оудиан Дж. Основы химии полимеров. М.: Мир, 1974. 614 с.
2. Odian G. Principles of Polymerization. Wiley-Interscience: New York; 1991.
3. Киреев В. В. Высокомолекулярные соединения. М.: Высшая школа, 1992. 512 с.
4.Тенфорд Ч. Физическая химия полимеров. М.: Химия, 1965. 772 с.
5. Рафиков С. Р., Будтов В. П., Монаков Ю. Б. Введение в физико-химию растворов полимеров. М.: Наука, 1978. 328 с.
6. Нарисава И. Прочность полимерных материалов. М.: Химия, 1987. 400 с.
7. Грасси Н., Скотт Дж. Деструкция и стабилизация полимеров. М.: Мир, 1988. 446 с.
8. Гросберг А. Ю., Хохлов А. Р. Физика в мире полимеров. М.: Наука., 1989. 208 с. (Б-чка «Квант»; вып. 74).
9. Гросберг А. Ю., Хохлов А. Р. Статистическая физика макромолекул. М.: Наука, 1983.344 с.
10. Жидкокристаллические полимеры / Под ред. Н. А. Платэ. Л.: Химия, 1988. 500 с.
11. Платэ НА., Литманович А. Д., Ноа О. В. Макромолекулярные реакции. М.: Химия, 1977.256 с.
12. Энциклопедия полимеров. Т. 1, 2, 3. М.: Советская энциклопедия, 1977.
– Конец работы –
Используемые теги: Высокомолекулярные, соединения0.048
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов