рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Педагогика
- /
- ЛЕКЦИЯ 1. Предмет и метод термодинамики. Термодинамическая система
Реферат Курсовая Конспект
ЛЕКЦИЯ 1. Предмет и метод термодинамики. Термодинамическая система
ЛЕКЦИЯ 1. Предмет и метод термодинамики. Термодинамическая система - раздел Педагогика, Содержание ...
СОДЕРЖАНИЕ
| ВВЕДЕНИЕ........................................................................................................................... | |
| ЛЕКЦИЯ 1. Предмет и метод термодинамики..................................................................... | |
| Термодинамическая система............................................................................. | |
| Термодинамические параметры состояния..................................................... | |
| Уравнение состояния......................................................................................... | |
| Термодинамический процесс.......................................................................... | |
| Теплоемкость газов........................................................................................... | |
| ЛЕКЦИЯ 2. Смеси идеальных газов.................................................................................... | |
| Аналитическое выражение первого закона термодинамики............................ | |
| ЛЕКЦИЯ 3. Внутренняя энергия........................................................................................... | |
| Работа расширения.......................................................................................... | |
| Теплота................................................................................................................ | |
| Энтальпия.............................................................................................................. | |
| Энтропия.............................................................................................................. | |
| ЛЕКЦИЯ 4. Общая формулировка второго закона.............................................................. | |
| Прямой цикл Карно.............................................................................................. | |
| Обратный цикл Карно......................................................................................... | |
| Изменение энтропии в неравновесных процессах........................................... | |
| ЛЕКЦИЯ 5. Термодинамические процессы идеальных газов в закрытых системах......... | |
| Эксергия................................................................................................................ | |
| ЛЕКЦИЯ 6. Термодинамические процессы реальных газов................................................ | |
| Уравнение состояния реальных газов............................................................... | |
| ЛЕКЦИЯ 7. Уравнение первого закона термодинамики для потока................................... | |
| Истечение из суживающегося сопла.................................................................. | |
| Основные закономерности течения газа в соплах и диффузорах................... | |
| Расчет процесса истечения с помощью h-s диаграммы.................................... | |
| Дросселирование газов и паров.......................................................................... | |
| ЛЕКЦИЯ 8. Термодинамическая Эффективность циклов теплосиловых установок......... | |
| Циклы поршневых двигателей внутреннего сгорания.................................... | |
| Циклы газотурбинных установок....................................................................... | |
| Циклы паротурбинных установок.................................................................... | |
| Циклы Карно и Ренкина насыщенного пара. Регенерация теплоты............... | |
| Цикл Ренкина на перегретом паре...................................................................... | |
| Термический КПД цикла.................................................................................... | |
| Теплофикация....................................................................................................... | |
| ЛЕКЦИЯ 9. Основные понятия и определения.................................................................... | |
| Теория теплопроводности................................................................................... | |
| Задачи.................................................................................................................... | |
| ЛЕКЦИЯ 10. Теплопередача.................................................................................................... | |
| Плоская стенка.................................................................................................... | |
| Цилиндрическая стенка...................................................................................... | |
| Интенсификация теплопередачи....................................................................... | |
| Тепловая изоляция.............................................................................................. | |
| Задачи по теплопередаче.................................................................................... | |
| ЛЕКЦИЯ 11. Конвективный теплообмен. Основной закон конвективного теплообмена. | |
| Пограничный слой.............................................................................................. | |
| Числа подобия..................................................................................................... | |
| Массообмен.......................................................................................................... | |
| ЛЕКЦИЯ 12. Частные случаи конвективного теплообмена. Поперечное обтекание одиночной трубы и пучка труб.......................................................................... | |
| Течение теплоносителя внутри труб................................................................. | |
| Теплоотдача при естественной конвекции........................................................ | |
| Теплоотдача при конденсации............................................................................ | |
| Ориентировочные значения коэффициентов теплоотдачи.............................. | |
| ЛЕКЦИЯ 13. Описание процесса излучения. Основные определения............................... | |
| Теплообмен излучением системы тел в прозрачной среде.............................. | |
| Перенос лучистой энергии в поглощающей и излучающей среде................. | |
| ЛЕКЦИЯ 14. Теплообменные аппараты................................................................................ | |
| Типы теплообменных аппаратов....................................................................... | |
| Расчетные уравнения.......................................................................................... | |
| ЛЕКЦИЯ 15. Термодинамический анализ топливосжигающих устройств....................... | |
| Полезная тепловая нагрузка печи....................................................................... | |
| Расчет процесса горения топлива в печи............................................................ | |
| Тепловой баланс печи, коэффициент полезного действия, расход топлива... | |
| ЛЕКЦИЯ 16. Котельные установки. Общие сведения........................................................ | |
| Устройство парового котла.................................................................................. | |
| Тепловой баланс парового котла. Коэффициент полезного действия............. | |
| ЛЕКЦИЯ 17. Состав и основные характеристики жидкого топлива................................... | |
| Состав и основные характеристики газообразного топлива............................. | |
| Теплота сгорания топлива.................................................................................... | |
| Количество воздуха, необходимого для горения. Теплота «сгорания» воздуха................................................................................................................. | |
| Объемы и состав продуктов сгорания.................................................................. | |
| ЛЕКЦИЯ 18. Вторичные энергоресурсы. Классификация ВЭР.......................................... | |
| Методы использования тепловых ВЭР................................................................ | |
| Установки для внутреннего теплоиспользования............................................... | |
| Котлы-утилизаторы.............................................................................................. | |
| СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ.............................................................. |
ВВЕДЕНИЕ
В последние годы ученые всего мира со все большим беспокойством говорят о повышении концентрации СО2 в атмосфере. Если эти опасения подтвердятся, человечеству в не таком уж отдаленном будущем придется резко ограничить потребление углеродсодержащих топлив. Кроме выбросов СО2 топливосжигающие и теплоэнергетические установки производят тепловые загрязнения (выбросы нагретой воды и газов), химические (оксиды серы и азота), золу и сажу, которые с увеличением масштаба производства также создают серьезные проблемы.
Однако экономические факторы стимулируют резкое увеличение степени использования добываемого топлива. Вместе с тем пока еще энергетическая эффективность многих технологических процессов чрезвычайно низка, ибо технологи, разрабатывая соответствующие процессы, зачастую не ставили во главу угла вопросы экономии топлива.
Высокие цены на топливо (прежде всего нефть) на мировом рынке стимулируют разработку энергосберегающих технологий. Главная роль в разработке менее энергоемких технологий принадлежит технологам. Эту задачу невозможно решить без глубоких знаний основных законов теплотехники.
Сегодня выгоднее вкладывать средства не в увеличение добычи топлива, чтобы продолжать расходовать его с низкой эффективностью, а в разработку технологических процессов, обеспечивающих более экономное его использование. В целом более 90 % всей используемой человечеством энергии приходится на ископаемые органические топлива. Это определяет роль теплотехники – общеинженерной дисциплины, изучающей методы получения, преобразования, передачи, и использования теплоты и связанных с этим аппаратов и устройств.
ЛЕКЦИЯ 1
Термодинамика изучает законы превращения энергии в различных процессах, происходящих в макроскопических системах и сопровождающихся тепловыми… В зависимости от задач исследования рассматривают техническую или химическую… Рассматривая только макроскопические системы, термодинамика изучает закономерности тепловой формы движения материи,…Термодинамическая система
Выбор системы произволен и диктуется условиями решаемой задачи. Тела, не входящие в систему, называют окружающей средой. Систему отделяют от… Механическое и тепловое взаимодействия термодинамической системы… В самом общем случае система может обмениваться со средой и веществом (массообменное взаимодействие). Такая система…Термодинамические параметры состояния
Давление обусловлено взаимодействием молекул рабочего тела с поверхностью и численно равно силе, действующей на единицу площади поверхности тела… , (1.1) где n — число молекул в единице объема;Уравнение состояния
Для равновесной термодинамической системы существует функциональная связь между параметрами состояния, которая называется уравнением состояния. Опыт показывает, что удельный объем, температура и давление простейших систем, которыми являются газы, пары или жидкости, связаны термическим уравнением состояния вида 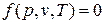 .
.
Уравнению состояния можно придать другую форму: 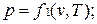
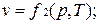
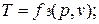
Эти уравнения показывают, что из трех основных параметров, определяющих состояние системы, независимыми являются два любых.
Для решения задач методами термодинамики совершенно необходимо знать уравнение состояния. Однако оно не может быть получено в рамках термодинамики и должно быть найдено либо экспериментально, либо методами статистической физики. Конкретный вид уравнения состояния зависит от индивидуальных свойств вещества.
Уравнение состояния идеальных газов
Из уравнений (1.1) и (1.2) следует, что 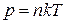 .
.
Рассмотрим 1 кг газа. Учитывая, что в нем содержится N молекул и, следовательно, 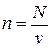 , получим:
, получим: 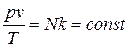 .
.
Постоянную величину Nk, отнесенную к 1 кг газа, обозначают буквой R и называют газовой постоянной. Поэтому
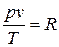 , или
, или 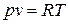 . (1.3)
. (1.3)
Полученное соотношение представляет собой уравнение Клапейрона.
Умножив (1.3) на М, получим уравнение состояния для произвольной массы газа М:
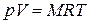 . (1.4)
. (1.4)
Уравнению Клапейрона можно придать универсальную форму, если отнести газовую постоянную к 1 кмолю газа, т. е. к количеству газа, масса которого в килограммах численно равна молекулярной массе μ. Положив в (1.4) М=μ и V=V μ, получим для одного моля уравнение Клапейрона — Менделеева:
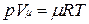 .
.
Здесь 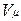 — объем киломоля газа, а
— объем киломоля газа, а 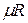 — универсальная газовая постоянная.
— универсальная газовая постоянная.
В соответствии с законом Авогадро (1811г.) объем 1 кмоля, одинаковый в одних и тех же условиях для всех идеальных газов, при нормальных физических условиях равен 22,4136 м3, поэтому
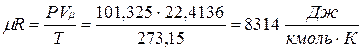
Газовая постоянная 1 кг газа составляет 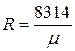 .
.
Уравнение состояния реальных газов
В реальных газах вотличие от идеальных существенны силы межмолекулярных взаимодействий (силы притяжения, когда молекулы находятся на значительном расстоянии, и силы отталкивания при достаточном сближении их друг с другом) и нельзя пренебречь собственным объемом молекул.
Наличие межмолекулярных сил отталкивания приводит к тому, что молекулы могут сближаться между собой только до некоторого минимального расстояния. Поэтому можно считать, что свободный для движения молекул объем будет равен  , где b — тот наименьший объем, до которого можно сжать газ. В соответствии с этим длина свободного пробега молекул уменьшается и число ударов о стенку в единицу времени, а следовательно, и давление увеличивается по сравнению с идеальным газом в отношении
, где b — тот наименьший объем, до которого можно сжать газ. В соответствии с этим длина свободного пробега молекул уменьшается и число ударов о стенку в единицу времени, а следовательно, и давление увеличивается по сравнению с идеальным газом в отношении 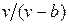 , т. е.
, т. е.
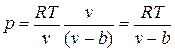 .
.
Силы притяжения действуют в том же направлении, что и внешнее давление, и приводят к возникновению молекулярного (или внутреннего) давления. Сила молекулярного притяжения каких-либо двух малых частей газа пропорциональна произведению числа молекул в каждой из этих частей, т. е. квадрату плотности, поэтому молекулярное давление обратно пропорционально квадрату удельного объема газа: рмол = а/v2, где а — коэффициент пропорциональности, зависящий от природы газа.
Отсюда получаем уравнение Ван-дер-Ваальса (1873 г.):
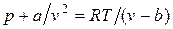 ,
,

 или
или
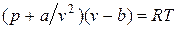 .
.
При больших удельных объемах и сравнительно невысоких давлениях реального газа уравнение Ван-дер-Ваальса практически вырождается в уравнение состояния идеального газа Клапейрона, ибо величина a/v2
(по сравнению с p) и b (по сравнению с v) становятся пренебрежимо малыми.
Уравнение Ван-дер-Ваальса с качественной стороны достаточно хорошо описывает свойства реального газа, но результаты численных расчетов не всегда согласуются с экспериментальными данными. В ряде случаев эти отклонения объясняются склонностью молекул реального газа к ассоциации в отдельные группы, состоящие из двух, трех и более молекул. Ассоциация происходит вследствие несимметричности внешнего электрического поля молекул. Образовавшиеся комплексы ведут себя как самостоятельные нестабильные частицы. При столкновениях они распадаются, затем вновь объединяются уже с другими молекулами и т. д. По мере повышения температуры концентрация комплексов с большим числом молекул быстро уменьшается, а доля одиночных молекул растет. Большую склонность к ассоциации проявляют полярные молекулы водяного пара.
Термодинамический процесс
Как уже отмечалось, система, выведенная из состояния равновесия, и предоставленная при постоянных параметрах окружающей среды самой себе, через… называется релаксацией, а промежуток времени, в течение которого система… Термодинамический процесс называется равновесным, если все параметры системы при его протекании меняются достаточно…Теплоемкость газов
. Обычно теплоемкость относят к единице количества вещества и в зависимости от… удельную массовую теплоемкость c , отнесенную к 1 кг газа,ЛЕКЦИЯ 2
Смеси идеальных газов
Закон Дальтона.В инженерной практике часто приходится иметь дело с газообразными веществами, близкими по свойствам к идеальным газам и… Основным законом, определяющим поведение газовой смеси, является закон…Работа расширения
Рассмотрим газ массой М и объемом V, заключенный в эластичную оболочку с поверхностью F.Теплота
Теплота может передаваться либо при непосредственном контакте между телами (теплопроводностью, конвекцией), либо на расстоянии (излучением), причем… Как будет показано ниже, элементарное количество теплоты , так же как и L, не… Внутренняя энергия — это свойство самой системы, она характеризует состояние системы. Теплота и работа — это…Энтальпия
В термодинамике важную роль играет сумма внутренней энергии системы U и произведения давления системы р на ее объем V, называемая энтальпией и обозначаемая Н:
.
Так как входящие в нее величины являются функциями состояния, то и сама энтальпия является функцией состояния. Так же как внутренняя энергия, работа и теплота, она измеряется в джоулях (Дж).
Энтальпия обладает свойством аддитивности. Величина
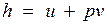 ,
,
называемая удельной энтальпией (h = H/M), представляет собой энтальпию системы, содержащей 1 кг вещества, и измеряется в Дж/кг.
Поскольку энтальпия есть функция состояния, то она может быть представлена в виде функции двух любых параметров состояния:
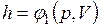 ;
; 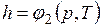 ;
; 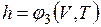 ,
,
а величина dh является полным дифференциалом.
Изменение энтальпии в любом процессе определяется только начальным и конечным состояниями тела и не зависит от характера процесса.
Физический смысл энтальпии выясним на следующем примере. Рассмотрим расширенную систему, включающую газ в цилиндре и поршень с грузом общим весом G .
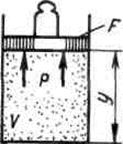 |
Энергия этой системы складывается из внутренней энергии газа и потенциальной энергии поршня с грузом в поле внешних сил: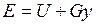 . В условиях равновесия (G = pF) эту функцию можно выразить через параметры газа:
. В условиях равновесия (G = pF) эту функцию можно выразить через параметры газа: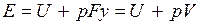 . Получаем, что
. Получаем, что 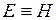 , т.е. энтальпию можно трактовать как энергию расширенной системы.
, т.е. энтальпию можно трактовать как энергию расширенной системы.
Уравнение 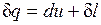 в случае, когда единственным видом работы является работа расширения, с учетом очевидного соотношения
в случае, когда единственным видом работы является работа расширения, с учетом очевидного соотношения  может быть записано в виде
может быть записано в виде 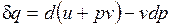 , или
, или
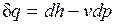 .
.
Из этого соотношения следует, что если давление системы сохраняется неизменным, т. е. осуществляется изобарный процесс (dp=0), то
 и
и 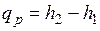 .
.
т. е. теплота, подведенная к системе при постоянном давлении, идет только на изменение энтальпии данной системы.
Это выражение очень часто используется в расчетах, так как огромное количество процессов подвода теплоты в теплоэнергетике (в паровых котлах, камерах сгорания газовых турбин и реактивных двигателей, теплообменных аппаратах), а также целый ряд процессов химической технологии и многих других осуществляется при постоянном давлении. Кстати, по этой причине в таблицах термодинамических свойств обычно приводятся значения энтальпии, а не внутренней энергии.
Для идеального газа с учетом получим
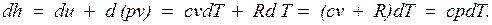
Так как между энтальпией и внутренней энергией существует связь 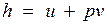 , выбор начала отсчета одной из них не произволен: в точке, принятой за начало отсчета внутренней энергии, h = pv.
, выбор начала отсчета одной из них не произволен: в точке, принятой за начало отсчета внутренней энергии, h = pv.
Например, для воды при t=0.01ºC и р =610,8 Па, u = 0, a
h = pv = 0,611 Дж/кг.
При расчетах практический интерес представляет изменение энтальпии в конечном процессе: 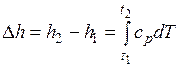 .
.
Энтропия
В математике доказывается, что дифференциальный двучлен всегда можно превратить в полный дифференциал путем умножения (или деления) на… Покажем это на примере изменения параметров идеального газа в равновесных… . (3.3)ЛЕКЦИЯ 4
Общая формулировка второго закона термодинамики
В 1755 г. французская Академия наук «раз и навсегда» объявила, что не будет больше принимать на рассмотрение какие-либо проекты вечных двигателей. … Рисунок 4.1 - Термодинамическая схема теплового двигателяПрямой цикл Карно
Итак, для превращения теплоты в работу в непрерывно действующей машине нужно иметь, по крайней мере, тело или систему тел, от которых можно было бы получить теплоту (горячий источник); рабочее тело, совершающее термодинамический процесс, и тело, или систему тел, способную охлаждать рабочее тело, т. е. забирать от него теплоту, не превращенную в работу (холодный источник).
Рассмотрим простейший случай, когда имеется один горячий с температурой T1 и один холодный с температурой T2 источники теплоты. Теплоемкость каждого из них столь велика, что отъем рабочим телом теплоты от одного источника и передача ее другому практически не меняет их температуры. Хорошей иллюстрацией могут служить земные недра в качестве горячего источника и атмосфера в качестве холодного.
Единственная возможность осуществления в этих условиях цикла, состоящего только из равновесных процессов, заключается в следующем. Теплоту от горячего источника к рабочему телу нужно подводить изотермически. В любом другом случае температура рабочего тела будет меньше температуры источника T1, т. е. теплообмен между ними будет неравновесным. Равновесно охладить рабочее тело от температуры горячего до температуры холодного источника T2, не отдавая теплоту другим телам (которых по условию нет), можно только путем адиабатного расширения с совершением работы. По тем же соображениям процесс теплоотдачи от рабочего тела к холодному источнику тоже должен быть изотермическим, а процесс повышения температуры рабочего тела от T1 до T2 — адиабатным сжатием с затратой работы. Такой цикл, состоящий из двух изотерм и двух адиабат, носит название цикла К а р н о, поскольку именно с его помощью С. Карно в 1824 г. установил основные законы превращения тепловой энергии в механическую.
Осуществление цикла Карно в тепловой машине можно представить следующим образом. Газ (рабочее тело) с начальными параметрами, характеризующимися точкой а, помещен в цилиндр под поршень, причем боковые стенки цилиндра и поршень абсолютно нетеплопроводны, так что теплота может передаваться только через основание цилиндра.
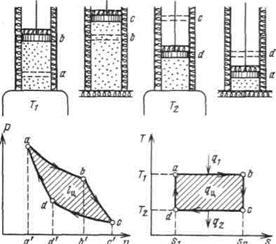
|
Рисунок 4.3 - Прямой цикл Карно
Вводим цилиндр в соприкосновение с горячим источником теплоты. Расширяясь изотермически при температуре от объема va до объема vb, газ забирает от горючего источника теплоту 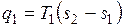 . В точке b подвод теплоты прекращаем и ставим цилиндр на теплоизолятор. Дальнейшее расширение рабочего тела происходит адиабатно. Работа расширения совершается при этом только за счет внутренней энергии, в результате чего температура газа падает до T2.
. В точке b подвод теплоты прекращаем и ставим цилиндр на теплоизолятор. Дальнейшее расширение рабочего тела происходит адиабатно. Работа расширения совершается при этом только за счет внутренней энергии, в результате чего температура газа падает до T2.
Теперь возвратим тело в начальное состояние. Для этого сначала поместим цилиндр на холодный источник с температурой T2 и будем сжимать рабочее тело по изотерме cd, совершая работу l2 и отводя при этом к нижнему источнику от рабочего тела теплоту  . Затем снова поставим цилиндр на теплоизолятор и дальнейшее сжатие проведем в адиабатных условиях. Работа, затраченная на сжатие по линии da, идет на увеличение внутренней энергии, в результате чего температура газа увеличивается до T1.
. Затем снова поставим цилиндр на теплоизолятор и дальнейшее сжатие проведем в адиабатных условиях. Работа, затраченная на сжатие по линии da, идет на увеличение внутренней энергии, в результате чего температура газа увеличивается до T1.
Таким образом, в результате цикла каждый килограмм газа получает от горячего источника теплоту q1, отдает холодному теплоту q2 и совершает работу lц.
Подставив в формулу 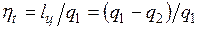 , справедливую для любого цикла, выражения для q1 и q2, получим, что термический КПД цикла Карно определяется формулой
, справедливую для любого цикла, выражения для q1 и q2, получим, что термический КПД цикла Карно определяется формулой
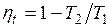 .
.
Из нее видно, что термический КПД цикла Карно зависит только от абсолютных температур горячего и холодного источников. Увеличить КПД цикла можно либо за счет увеличения температуры горячего источника, либо за счет уменьшения температуры холодного, причем влияние температур и на значение различно:
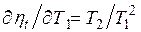 ,
,
 ,
,
а так как 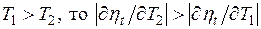 .
.
Таким образом, увеличение температуры горячего источника в меньшей степени повышает КПД цикла Карно, чем такое же (в Кельвинах) уменьшение температуры холодного.
Являясь следствием второго закона термодинамики, формула для КПД цикла Карно, естественно, отражает его содержание. Из нее видно, что теплоту горячего источника можно было бы полностью превратить в работу, т. е. получить КПД цикла, равный единице, лишь в случае, когда 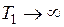 либо
либо 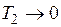 . Оба значения температур недостижимы. (Недостижимость абсолютного нуля температур следует из третьего начала термодинамики).
. Оба значения температур недостижимы. (Недостижимость абсолютного нуля температур следует из третьего начала термодинамики).
При T1=T2 термический КПД цикла равен нулю.
Это указывает на невозможность превращения теплоты в работу, если все тела системы имеют одинаковую температуру, т. е. находятся между собой в тепловом равновесии. Для ориентировки приводим значения термического КПД цикла Карно при различных температурах горячего источника и при температуре холодного источника, равной 10 °С.
| t,°С | ||||||||
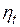
| 0,40 | 0,58 | 0,68 | 0,74 | 0,78 | 0,81 | 0,83 | 0,85 |
Приведенные цифры дают КПД идеального цикла. Коэффициент полезного действия реального теплового двигателя, конечно, ниже.
Обратный цикл Карно
Рисунок 4.4 - Обратный цикл Карно в р,v- и T, s-диаграммахИзменение энтропии в неравновесных процессах
Расширение будет равновесным только в случае, если температура газа Т равна температуре источника (Т=Т1), внешняя сила Р равна давлению газа на… Невыполнение хотя бы одного из указанных условий делает расширение газа…ЛЕКЦИЯ 5
Термодинамические процессы идеальных газов
В закрытых системах
Метод исследования процессов, не зависящий от их особенностей и являющийся общим, состоит в следующем: выводится уравнение процесса, устанавливающее связь между начальными и… вычисляется работа изменения объема газа;Эксергия
Рассмотрим изолированную систему, состоящую из горячего источника с температурой Ti, холодного источника (окружающей среды) с температурой То и… Работоспособностью (или эксергией) теплоты Q1, отбираемой от горячего… Из предыдущего ясно, что максимальная полезная работа L'макс теплоты Q1 представляет собой работу равновесного цикла…ЛЕКЦИЯ 6
Термодинамические процессы реальных газов
Процесс парообразования. Основные понятия и определения.Рассмотрим процесс получения пара. Для этого 1 кг воды при температуре 0 °С поместим в… Начальное состояние воды, находящейся под давлением р и имеющей температуру… При дальнейшем подводе теплоты начинается кипение воды с сильным увеличением объема. В цилиндре теперь находится…Уравнение состояния реальных газов
В реальных газах вотличие от идеальных существенны силы межмолекулярных взаимодействий (силы притяжения, когда молекулы находятся на значительном расстоянии, и силы отталкивания при достаточном сближении их друг с другом) и нельзя пренебречь собственным объемом молекул.
Наличие межмолекулярных сил отталкивания приводит к тому, что молекулы могут сближаться между собой только до некоторого минимального расстояния. Поэтому можно считать, что свободный для движения молекул объем будет равен  , где b — тот наименьший объем, до которого можно сжать газ. В соответствии с этим длина свободного пробега молекул уменьшается и число ударов о стенку в единицу времени, а следовательно, и давление увеличивается по сравнению с идеальным газом в отношении
, где b — тот наименьший объем, до которого можно сжать газ. В соответствии с этим длина свободного пробега молекул уменьшается и число ударов о стенку в единицу времени, а следовательно, и давление увеличивается по сравнению с идеальным газом в отношении 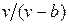 , т. е.
, т. е.
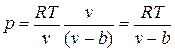 .
.
Силы притяжения действуют в том же направлении, что и внешнее давление, и приводят к возникновению молекулярного (или внутреннего) давления. Сила молекулярного притяжения каких-либо двух малых частей газа пропорциональна произведению числа молекул в каждой из этих частей, т. е. квадрату плотности, поэтому молекулярное давление обратно пропорционально квадрату удельного объема газа: рмол = а/v2, где а — коэффициент пропорциональности, зависящий от природы газа.
Отсюда получаем уравнение Ван-дер-Ваальса (1873 г.):
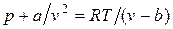 ,
,

 или
или
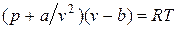 .
.
При больших удельных объемах и сравнительно невысоких давлениях реального газа уравнение Ван-дер-Ваальса практически вырождается в уравнение состояния идеального газа Клапейрона, ибо величина a/v2
(по сравнению с p) и b (по сравнению с v) становятся пренебрежимо малыми.
Уравнение Ван-дер-Ваальса с качественной стороны достаточно хорошо описывает свойства реального газа, но результаты численных расчетов не всегда согласуются с экспериментальными данными. В ряде случаев эти отклонения объясняются склонностью молекул реального газа к ассоциации в отдельные группы, состоящие из двух, трех и более молекул. Ассоциация происходит вследствие несимметричности внешнего электрического поля молекул. Образовавшиеся комплексы ведут себя как самостоятельные нестабильные частицы. При столкновениях они распадаются, затем вновь объединяются уже с другими молекулами и т. д. По мере повышения температуры концентрация комплексов с большим числом молекул быстро уменьшается, а доля одиночных молекул растет. Большую склонность к ассоциации проявляют полярные молекулы водяного пара.
ЛЕКЦИЯ 7
Уравнение первого закона термодинамики для потока
Под открытыми понимаются термодинамические системы, которые кроме обмена теплотой и работой с окружающей средой допускают также и обмен массой. В технике широко используются процессы преобразования энергии в потоке, когда рабочее тело перемещается из области с одними параметрами в область с другими. Это, например, расширение пара в турбинах, сжатие газов в компрессорах.
Будем рассматривать лишь одномерные стационарные потоки, в которых параметры зависят только от одной координаты, совпадающей с направлением вектора скорости, и не зависят от времени. Условие неразрывности течения в таких потоках заключается в одинаковости массового расхода m рабочего тела в любом сечении:
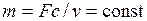 ,
,
где F — площадь поперечного сечения канала; с — скорость рабочего тела.
Рассмотрим термодинамическую систему, представленную схематически на рисунке 7.1.
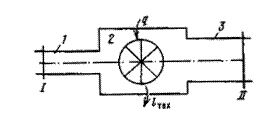
Рисунок 7.1 - Открытая термодинамическая система
По трубопроводу 1 рабочее тело с параметрами Т1 , p1, v1 подается со скоростью c1 в тепломеханический агрегат 2 (двигатель, паровой котел, компрессор и т. д.). Здесь каждый килограмм рабочего тела в общем случае может получать от внешнего источника теплоту q и совершать техническую работу lтех, например, приводя в движение ротор турбины, а затем удаляется через выхлопной патрубок со скоростью с2, имея параметры Т2 , p2, v2.
Если в потоке мысленно выделить замкнутый объем рабочего тела и наблюдать за изменением его параметров в процессе перемещения, то для описания его поведения будут пригодны все полученные выше термодинамические соотношения и, в частности, первый закон термодинамики в обычной записи:  .
.
Внутренняя энергия есть функция состояния рабочего тела, поэтому значение определяется параметрами рабочего тела при входе (сечение потока I), а значение — параметрами рабочего тела при выходе из агрегата (сечение II).
Работа расширения l совершается рабочим телом на поверхностях, ограничивающих выделенный движущийся объем, т. е. на стенках агрегата и границах, выделяющих этот объем в потоке. Часть стенок агрегата неподвижна, и работа расширения на них равна нулю. Другая часть стенок специально делается подвижной (рабочие лопатки в турбине и компрессоре, поршень в поршневой машине), и рабочее тело совершает на них техническую работу 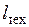
При входе рабочее тело вталкивается в агрегат. Для этого нужно преодолеть давление p1. Поскольку p1=const, то каждый килограмм рабочего тела может занять объем лишь при затрате работы, равной 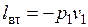 .
.
Для того чтобы выйти в трубопровод 3, рабочее тело должно вытолкнуть из него такое же количество рабочего тела, ранее находившегося в нем, преодолев давление р2, т. е. каждый килограмм, занимая объем v2 должен произвести определенную работу выталкивания 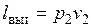 .
.
Сумма 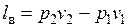 называется работой вытеснения.
называется работой вытеснения.
Если скорость на выходе больше, чем на входе, то часть работы расширения будет затрачена на увеличение кинетической энергии рабочего тела в потоке, равное 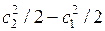 .
.
Наконец, в неравновесном процессе некоторая работа может быть затрачена на преодоление сил трения. Окончательно
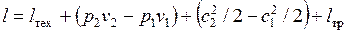 .
.
Теплота, сообщенная каждому килограмму рабочего тела во время прохождения его через агрегат, складывается из теплоты 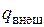 , подведенной снаружи, и теплоты
, подведенной снаружи, и теплоты 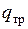 , в которую переходит работа трения внутри агрегата, т. е.
, в которую переходит работа трения внутри агрегата, т. е. 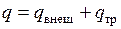 .
.
Подставив полученные значения q и l в уравнение первого закона термодинамики, получим
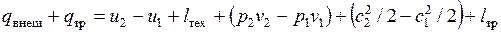 .
.
Поскольку теплота трения равна работе трения, окончательно запишем:
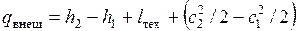 .
.
Это и есть выражение первого закона термодинамики для потока, который можно сформулировать так: теплота, подведенная к потоку рабочего тела извне, расходуется на увеличение энтальпии рабочего тела, производство технической работы и увеличение кинетической энергии потока.
В дифференциальной форме уравнение записывается в виде
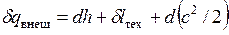 . (7.1)
. (7.1)
Оно справедливо как для равновесных процессов, так и для течений, сопровождающихся трением.
Выше было указано, что к замкнутому объему рабочего тела, выделенному в потоке, применимо выражение первого закона термодинамики для закрытой системы, т.е. 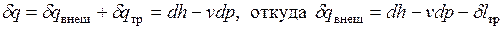 .
.
Сравнивая это выражение с уравнением *, получим:
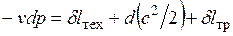 , или
, или
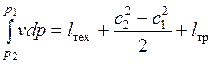 .
.
Величину 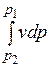 называют располагаемой работой. В p, v-диаграмме она изображается заштрихованной площадью.
называют располагаемой работой. В p, v-диаграмме она изображается заштрихованной площадью.
Применим первый закон термодинамики к различным типам тепломеханического оборудования.
Теплообменный аппарат(устройство, в котором теплота от жидкой или газообразной среды передается другой среде). Для него 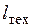 =0, a
=0, a  , поэтому
, поэтому
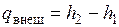 .
.
Следует подчеркнуть, что для теплообменника, установленного в потоке, это выражение справедливо не только в изобарном процессе, но и в процессе с трением, когда давление среды уменьшается из-за сопротивления.
Тепловой двигатель.Обычно 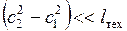 , поэтому рабочее тело производит техническую работу за счет уменьшения энтальпии:
, поэтому рабочее тело производит техническую работу за счет уменьшения энтальпии:
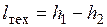 . (7.2)
. (7.2)
Величину 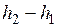 называют располагаемым теплоперепадом.
называют располагаемым теплоперепадом.
Интегрируя уравнение 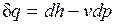 от p1 до p2 и от h1 до h2 для случая, когда
от p1 до p2 и от h1 до h2 для случая, когда 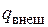 =0, получим
=0, получим
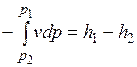 . (7.3)
. (7.3)
Сравнивая выражения (7.2) и (7.3), приходим к выводу, что
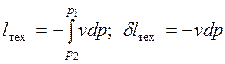 .
.
Таким образом, при  ,
, 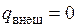 и отсутствии потерь на трение получаемая от двигателя техническая работа равна располагаемой, т. е. тоже изображается заштрихованной площадью на рисунке 7.2.
и отсутствии потерь на трение получаемая от двигателя техническая работа равна располагаемой, т. е. тоже изображается заштрихованной площадью на рисунке 7.2.
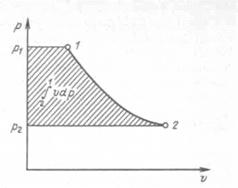
Рисунок 7.2 - Изображение располагаемой и технической работы в координатах p, v
Компрессор.Если процесс сжатия газа в компрессоре происходит без теплообмена с окружающей средой (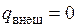 ) и c1=c2, что всегда можно обеспечить надлежащим выбором сечений всасывающего и нагнетательного воздухопроводов, то
) и c1=c2, что всегда можно обеспечить надлежащим выбором сечений всасывающего и нагнетательного воздухопроводов, то
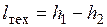
В отличие от предыдущего случая здесь h1<h2, т.е. техническая работа в адиабатном компрессоре затрачивается на увеличение энтальпии газа.
Сопла и диффузоры.Специально спрофилированные каналы для разгона рабочей среды и придания потоку определенного направления называются соплами. Каналы, предназначенные для торможения потока и повышения давления, называются диффузорами. Техническая работа в них не совершается, поэтому уравнение 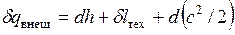 приводится к виду
приводится к виду
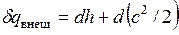 .
.
С другой стороны, для объема рабочего тела, движущегося в потоке без трения, применимо выражение первого закона термодинамики для закрытой системы 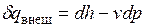 .
.
Приравняв правые части двух последних уравнений, получим
 . (7.4)
. (7.4)
 Видно, что dc и dp всегда имеют противоположные знаки. Следовательно, увеличение скорости течения в канале (dc>0) возможно лишь при уменьшении давления в нем (dp<0). Наоборот, торможение потока (dc<0) сопровождается увеличением давления (dp>0),
Видно, что dc и dp всегда имеют противоположные знаки. Следовательно, увеличение скорости течения в канале (dc>0) возможно лишь при уменьшении давления в нем (dp<0). Наоборот, торможение потока (dc<0) сопровождается увеличением давления (dp>0),
Так как длина сопла и диффузора невелика, а скорость течения среды в них достаточно высока, то теплообмен между стенками канала и средой при малом времени их контакта настолько незначителен, что в большинстве случаев им можно пренебречь и считать процесс истечения адиабатным (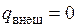 ). При этом уравнение
). При этом уравнение 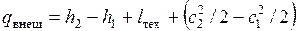 принимает вид
принимает вид
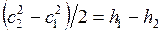 . (7.5)
. (7.5)
Следовательно, ускорение адиабатного потока происходит за счет уменьшения энтальпии, а торможение потока вызывает ее увеличение.
Проинтегрировав соотношение (7.4) и сравнив его с уравнением (7.5), получим, что для равновесного адиабатного потока
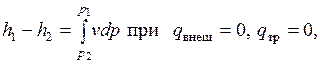
т. е. располагаемая работа при адиабатном расширении равна располагаемому теплоперепаду.
Истечение из суживающегося сопла
Расчет сопла сводится к определению скорости и расхода газа на выходе из него, нахождению площади поперечного сечения и правильному выбору его… Скорость истечения в соответствии с уравнением (7.5) .Основные закономерности течения газа в соплах и диффузорах
. (7.12) Секундный массовый расход т одинаков для всех сечений, поэтому изменение… Возьмем дифференциалы от левой и правой частей уравнения (7.11) при условии :Расчет процесса истечения с помощью h,s-диаграммы
Пусть пар с начальными параметрами вытекает в среду с давлением р2. Если потери энергии на трение при движении водяного пара по каналу и… Скорость истечения рассчитывается по формуле: ,Дросселирование газов и паров
Рисунок 7.6 - Дросселирование рабочего тела в пористой перегородкеТермодинамическая эффективность циклов теплосиловых установок
Эксергетический и термический коэффициенты полезного действия позволяют оценивать термодинамическое совершенство протекающих в тепловом аппарате… Эксергетический метод, наоборот, позволяет проанализировать качественную… Назначением теплосиловых установок является производство полезной работы за счет теплоты. Источником теплоты служит…Циклы поршневых двигателей внутреннего сгорания
Рисунок 8.2 - Циклы ДВС: а — в p,v-координатах; б — в T,s-координатах;Циклы газотурбинных установок
Рисунок 8.4 - Схема газотурбинной установкиЦиклы паротурбинных установок
Современная стационарная теплоэнергетика базируется в основном на паровых теплосиловых установках. Продукты сгорания топлива в этих установках являются лишь промежуточным теплоносителем (в отличие от ДВС и ГТУ), а рабочим телом служит чаще всего водяной пар.
Циклы Карно и Ренкина насыщенного пара. Регенерация теплоты.
Значительно удобнее и экономичнее в реальном цикле конденсировать пар до конца по линии 2-3, а затем насосом увеличивать давление воды от р2 до по…Цикл Ренкина на перегретом паре
Термический КПД цикла определяется, как обычно, по уравнению Теплота подводится при в процессах 4-5 (подогрев воды до температуры кипения), 5-6 (парообразование) и 6-1 (перегрев…Термический КПД цикла
Если не учитывать ничтожного повышения температуры при адиабатном сжатии воды в насосе, то и где — энтальпия кипящей воды при давлении р2.Общая характеристика холодильных установок
В зависимости от температуры, которая должна быть достигнута при охлаждении, различают холодильные установки умеренного холода (до – 70 ºС) и… Установки, в которых энергия для получения холода затрачивается в виде… Холодильные установки и тепловые насосы работают по обратным (против часовой стрелки) круговым процессам, или…Цикл паровой компрессионной холодильной установки
ЛЕКЦИЯ 9
Основы теории теплообмена
Сложный процесс переноса теплоты разбивают на ряд более простых. Такой прием упрощает его изучение. Кроме того, каждый простой процесс переноса… Явление теплопроводности состоит в переносе теплоты микрочастицами… Конвективный теплоперенос (конвекция) наблюдается лишь в жидкостях и газах. Конвекция - это перенос теплоты вместе с…Закон Фурье
, где - коэффициент теплопроводности, Вт/(м×К). Он характеризует… Знак «-» указывает на противоположное направление вектора теплового потока и вектора градиента температуры. Вектор…Многослойная плоская стенка
В этом случае плотность теплового потока определяется по формуле: Рисунок 9.4 - Распределение температур по толщине многослойной… где n - число слоев многослойной стенки;Однородная цилиндрическая стенка
В соответствии с законом Фурье, тепловой поток через однородную цилиндрическую стенку длиной l определяется по формуле: , d1 d2 … ,Многослойная цилиндрическая стенка
, где di и di+1 - соответственно внутренний и внешний диаметры iго слоя. Тогда линейная плотность теплового потока будет:Задачи
1. Определить тепловой поток через бетонную стену здания толщиной 200 мм, высотой 2,5 м и длиной 2 м, если температуры на ее поверхностях tc1=20°С, tc2= -10°С, а коэффициент теплопроводности 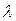 =1 Вт/(м×К).
=1 Вт/(м×К).
2. Определить коэффициент теплопроводности материала стенки толщиной 50 мм, если плотность теплового потока через нее 100 Вт/м2, а разность температур на поверхностях 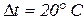 .
.
3. Плоскую поверхность необходимо изолировать так, чтобы потери теплоты с единицы поверхности в единицу времени не превышали 450 Вт/м2. Температура поверхности под изоляцией tc1=450°С, температура внешней поверхности изоляции tc2=50°С. определить толщину изоляции, выполненной из совелита, для которого 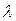 =0,09+0,0000874×t.
=0,09+0,0000874×t.
4. Распределение температуры по толщине плоской стенки с 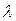 =2 Вт/(м×К) имеет вид tx=100+150×x , где температура t выражена в градусах Цельсия, а координата х - в метрах и измеряется от одной поверхности стенки. найти плотность теплового потока через стенку. Нарисовать распределение температур в стенке толщиной d=20см. В какую сторону направлен тепловой поток ?
=2 Вт/(м×К) имеет вид tx=100+150×x , где температура t выражена в градусах Цельсия, а координата х - в метрах и измеряется от одной поверхности стенки. найти плотность теплового потока через стенку. Нарисовать распределение температур в стенке толщиной d=20см. В какую сторону направлен тепловой поток ?
5. Плотность теплового потока через плоскую стенку толщиной 50 мм q=70 Вт/м2. Определить разность температур на поверхностях стенки и численное значение градиента температуры в стенке, если она выполнена: а) из латуни [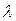 =70Вт/(м×К)]; из красного кирпича [
=70Вт/(м×К)]; из красного кирпича [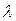 =0,7Вт/(м×К)]; из пробки [
=0,7Вт/(м×К)]; из пробки [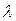 =0,07Вт/(м×К)].
=0,07Вт/(м×К)].
6. Плоская стенка бака площадью 5 м2 покрыта двухслойной тепловой изоляцией. Стенка бака стальная, толщиной d1=8мм с коэффициентом теплопроводности 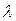 1=46,5Вт/(м×К). Первый слой изоляции выполнен из новоасбозурита толщиной d2=50мм (
1=46,5Вт/(м×К). Первый слой изоляции выполнен из новоасбозурита толщиной d2=50мм (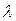 2=0,144+0,00014×t). второй слой изоляции толщиной d3=10мм представляет собой известковую штукатурку (
2=0,144+0,00014×t). второй слой изоляции толщиной d3=10мм представляет собой известковую штукатурку (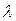 3=0,698 Вт/м×°С)). Температура внутренней поверхности стенки бака tc1=250°С и внешней поверхности изоляции tc4=50°С. Вычислить количество теплоты, передаваемой через стенку, температуры на границах слоев изоляции и построить график распределения температуры.
3=0,698 Вт/м×°С)). Температура внутренней поверхности стенки бака tc1=250°С и внешней поверхности изоляции tc4=50°С. Вычислить количество теплоты, передаваемой через стенку, температуры на границах слоев изоляции и построить график распределения температуры.
7. Стены сушильной камеры выполнены из слоя красного кирпича толщиной d1=250мм [l1=0,7 Вт/(м×К)] из слоя строительного войлока [l2=0,0465 Вт/(м×К)]. Вычислить температуру в плоскости соприкосновения слоев и толщину войлочного слоя при условии, что тепловые потери ровны 0.
8. Стенка неэкранированной топочной камеры парового котла выполнена из слоя пеношамота (l1=0,28+0,00023×t) толщиной d1=125мм и слоя красного кирпича (l2=0,7 Вт/(м×К)) толщиной d2=500мм. Слои плотно прилегают друг к другу. Температура на внутренней поверхности топочной камеры tc1=1100°С, а на наружной tc3=50°С. Вычислить плотность теплового потока и температуру в плоскости соприкосновения слоев.
9. Нефтепровод с наружным диаметром 1220мм и толщиной стенки dтр=10мм [lтр=55 Вт/(м×К)] имеет три слоя изоляции толщиной d1=8мм, d2=12мм, d3=25мм. Коэффициенты теплопроводности изоляции l1=0,0035Вт/(м×К), l2=0,06Вт/(м×К), l3=0,12 Вт/(м×К). температура на внутренней поверхности трубы tвн=60°С, а на наружной поверхности изоляции tнар= -5°С. Определить линейную плотность теплового потока.
10. Железебетонная дымовая труба [l2=1.1 Вт/(м×К)] внутренним диаметром d2=800мм и наружным диаметром d3=1300мм должна быть футерована внутри огнеупором [l1=0,5 Вт/(м×К)]. Определить толщину футеровки и температуру наружной поверхности трубы tс3 из условий, чтобы тепловые потери с 1м трубы не превышали 2000 Вт/м, а температура внутренней поверхности железобетонной стенки tс2 не превышала 200°С. Температура внутренней поверхности футеровки tс1=425°С.
11. В приборе для определения коэффициента теплопроводности жидкостей по методу «нагретой нити» в кольцевой зазор между платиновой нитью и кварцевой трубкой залито испытуемое трансформаторное масло. Диаметр и длина платиновой нити d1=0,12мм и l=90мм; внутренний и наружный диаметры кварцевой трубки d2=1мм, d3=3мм, коэффициент теплопроводности кварца lкв=1,4 Вт/(м×К). Вычислить коэффициент теплопроводности и среднюю температуру трансформаторного масла, если при расходе теплоты через кольцевой слой масла Q=1,8Вт, температура платиновой нити tс1=106,9°С и температура внешней поверхности кварцевой трубки tс3=30,6°С.
ЛЕКЦИя 10
Теплопередача
В технике часто приходится рассчитывать стационарный процесс переноса теплоты от одного теплоносителя другому через разделяющую стенку. Такой процесс называется теплопередачей.
Плоская стенка
1) В начале теплота передается от горячего теплоносителя tж1 к поверхности стенки путем конвективного теплообмена, который может сопровождаться… d1 d2 dn …Цилиндрическая стенка
аналогично теплопередаче через плоскую стенку, линейную плотность теплового потока через многослойную цилиндрическую стенку при стационарном режиме… 1. по закону Ньютона - Рихмана ,Интенсификация теплопередачи
, для интенсификации теплопередачи нужно либо увеличить числитель (tж1-tж2) либо… Термическое сопротивление теплопередачи Rk, можно уменьшить, воздействуя на любую из составляющих Ra1, Rl, Ra2.…Тепловая изоляция
Теплоизоляционные свойства материалов ухудшаются с увеличением плотности, температуры и влажности материала. Для плоской стенки увеличение толщины слоя изоляции увеличивает ее термическое… Для цилиндрической стенки увеличение толщины слоя изоляции так же увеличивает Rl, но одновременно уменьшает…Задачи по теплопередаче
2. Вычислить температуры на поверхностях стенки, если заданы следующие величины: температура дымовых газов tж1=1000°С, кипящей воды tж2=200°С;… 3. Вычислить плотность теплового потока q,Вт/м2, в пластинчатом… 4. Определить температуры на поверхностях кирпичной стены помещения толщиной в 2 кирпича (d=510мм) с коэффициентом…ЛЕКЦИЯ 11
Конвективный теплообмен (теплоотдача)
Основной закон конвективного теплообмена
Согласно закону Ньютона и Рихмана тепловой поток в процессе теплоотдачи пропорционален площади поверхности теплообмена F и разности температур… Q=aF½tc-tж½ В процессе теплоотдачи независимо от направления теплового потока Q (от стенки к жидкости или наоборот) значение его…Пограничный слой
Как уже отмечалось, частицы жидкости, непосредственно соприкасающиеся с поверхностью, адсорбируются («прилипают»). Соприкасаясь с неподвижным слоем,… Аналогичным образом осуществляется и тепловое взаимодействие потока с… С удалением от лобовой точки количество охлаждающейся у пластины жидкости увеличивается, и толщина теплового…Числа подобия
Каждое из безразмерных чисел имеет определенный физический смысл. Их принято обозначать первыми буквами фамилий ученых, внесших существенный вклад в… Число Нуссельта:Массообмен
Если в некоторой изолированной системе содержится смесь компонентов с первоначально неоднородным распределением концентраций, то в ней возникает… Перенос вещества в смеси, обусловленный тепловым хаотическим движением… При перемещении, т.е. конвекции, масса компонента переносится макроскопическим элементами смеси. Перенос массы за счет…Числа подобия конвективного массообмена
При конвективном массообмене вместо теплового числа подобия Прандтля Pr используют диффузионное число Прандтля в научной литературе его часто… При наличии фазового перехода используют число подобия . где r – теплота фазового перехода;ЛЕКЦИЯ 12
Частные случаи конвективного теплообмена
Поперечное обтекание одиночной трубы и пучка труб
значение коэффициента С и показателя степени n в зависимости от критерия Reж…ЛЕКЦИЯ 13
Описание процесса излучения. Основные определения
Тепловое излучение как процесс распространения электромагнитных волн характеризуется длиной волны l и частотой колебаний n=с/l, где с – скорость… Тепловой поток, излучаемый на всех длинах волн с единицы поверхности тела по… Часть энергии излучения Епад, падающего на тело, поглощается (Еа), часть отражается (ЕR) и частично проникает сквозь…Теплообмен излучением системы тел в прозрачной среде
Еэф=Е+REпад. Для непрозрачного тела (D=0 и R=1-A) выражение Еэф=Е+REпад запишется в виде… Каждое из рассматриваемых тел имеет эффективное (полное) излучение, соответственно Еэф1 и Еэф2. Для первого тела Еэф2…Перенос лучистой энергии в поглощающей и излучающей среде
С ростом температуры, когда максимум излучения смещается в область коротких волн, степень черноты уменьшается. Поскольку степень черноты газа er… Излучение газов носит объемный характер. Способность газа излучать энергию… er=eco2+eH2O.ЛЕКЦИЯ 14
Теплообменные аппараты
Типы теплообменных аппаратов
Чаще всего в теплообменных аппаратах (ТОА) осуществляется передача теплоты от одного теплоносителя к другому, т.е. нагревание одного теплоносителя… Теплообменники с двумя теплоносителями по принципу действия подразделяются на… 1) рекуперативные;Расчетные уравнения
Сущность расчета любого ТОА - совместное решение уравнений теплового баланса и теплопередачи.
1) Уравнения теплового баланса .
Тепловой поток Q1, отраженный в теплообменнике горячим теплоносителем при его охлаждении от температуры t1' до t1" равен:
Q1=m1×(Cp1'×t1'-Cp1"×t1"), кДж
где индекс 1 относится к горячему теплоносителю;
m - массовый расход теплоносителя , кг/с;
Cp' и Cp" - теплоемкости соответственно на входе и выходе ТОА , кДж(кг× град);
t' и t" - температура теплоносителя соответственно на входе и выходе ТОА , °C.
Из-за потерь ( до 10% ) второму теплоносителю передается не вся теплота Q1, а часть ее Q2=h×Q1 (h - КПД теплообменника)
Тогда уравнение теплового баланса будет иметь вид :
Q2=h×Q1 или

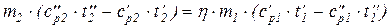 ,
,
2) Уравнение теплопередачи .
В простейших случаях , когда поверхность теплообмена можно считать плоской (тонкие стенки трубок рекуперативных ТОА практически всегда считают плоскими) , можно записать уравнение теплопередачи :
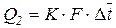 ,
,
где к - коэффициент теплопередачи через поверхность;
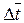 - среднее по поверхности значение температурного напора (t1-t2). Изменения температурного напора показаны на рисунке ниже.
- среднее по поверхности значение температурного напора (t1-t2). Изменения температурного напора показаны на рисунке ниже.
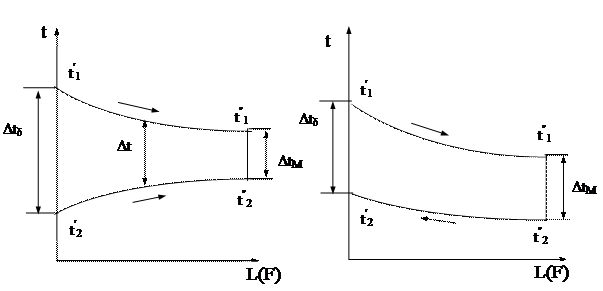 |
Рисунок 10.4 - Изменение температур горячего и холодного теплоносителей по длине рекуперативного ТОА
Пользоваться среднеарифметическим значением Dtcp=0,5×(Dtб+Dtм) можно только при Dtб/Dtм <=1,4, когда ошибка составляет не более 4% ; что допустимо для технических расчетов.
Во всех остальных случаях следует пользоваться среднелогарифмическим температурным напором :
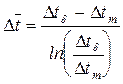 ,
,
Эта формула справедлива для любых схем движения теплоносителей.
Следует заметить, что среднелогарифмический напор всегда меньше среднеарифметического: Dt<Dtcp.
ЛЕКЦИЯ 15
Термодинамический анализ топливосжигающих устройств
Источником теплоты в пламенных печах служат различные виды жидкого и газообразного углеводородного топлива. Жидким топливом для промышленных печей является мазут, получающийся как… Флотские мазуты относятся к категорий средних топлив, M100 – к категории тяжелых мазутов.Полезная тепловая нагрузка печи
Если в печи помещены несколько самостоятельных змеевиков, то полезная тепловая нагрузка равна сумме теплот, полученных отдельными потоками. Полезную тепловую нагрузку рассчитывают по формуле, кВт, , где - расход продукта, кг/с;Расчет процесса горения топлива в печи
для жидкого топлива, кДж/кг топл., где – содержание углерода, водорода, серы, кислорода, влаги в топливе (элементарный состав), % массовый;Тепловой баланс печи. Коэффициент полезного действия. Расход топлива
где - располагаемая теплота, т.е. теплота, вносимая в трубчатую печь при… - полезно используемая теплота в печи;ЛЕКЦИЯ 16
Котельные установки. Общие сведения
Устройства, предназначенные для получения пара или горячей воды повышенного давления за счет теплоты, выделяемой при сжигании топлива или подводимой от посторонних источников (обычно с горючими газами), называют котлами. Они делятся соответственно на котлы паровые и котлы водогрейные. Котлы, использующие (т. е. утилизирующие) теплоту отходящих из печей газов или других основных и побочных продуктов различных технологических процессов, называют котлами-утилизаторами.
С целью обеспечения стабильной и безопасной работы котла его снабжают вспомогательным оборудованием, служащим для подготовки и подачи топлива, воздуха, очистки и подачи воды, отвода продуктов сгорания и их очистки от золы и токсичных примесей, удаления золошлаковых остатков.
Комплекс устройств, включающий в себя собственно котел и вспомогательное оборудование, называют котельной установкой.
Устройство парового котла
Топливо подается к горелкам 7 (рисунок 16.1). К горелкам подводится также воздух, предварительно нагретый уходящими из котла газами в…Тепловой баланс парового котла.
Коэффициент полезного действия
Здесь — низшая теплота сгорания единицы топлива в рабочем состоянии. Часть теплоты, затрачиваемая на подогрев, испарение воды и перегрев пара, составляет использованную теплоту ,…ЛЕКЦИЯ 17
Состав и основные характеристики жидкого топлива
Мазутная фракция может подвергаться дальнейшей переработке на светлые нефтепродукты путем крекинга, т. е. расщепления тяжелых молекул на более… Мазут, как и моторные топлива, представляет собой сложную смесь… Мазуты, получаемые из нефти ряда месторождений, могут содержать много серы (до 4,3%), что резко усложняет защиту…Состав и основные характеристики газообразного топлива
Теплота сгорания топлива
Продукты сгорания пробы топлива охлаждаются в калориметре до комнатной температуры. При этом вода, образующаяся при сгорании водорода и… В технических устройствах вода обычно выбрасывается вместе с продуктами… Поскольку 1 кг водорода дает при сгорании 9 кг воды, а конденсация 1 кг пара при 20 °С — около 2,5 МДж теплоты , то…Количество воздуха, необходимого для горения.
Теплота “сгорания” воздуха
В соответствии со стехиометрическим уравнением реакции горения водорода Н2 + 0,5О2 = Н2О на 2 кг, т. е. на 1 кмоль водорода, необходимо затратить 16 кг (0,5 кмоль) кислорода, при этом образуется 18 кг…Объемы и состав продуктов сгорания
При полном сгорании Здесь — избыточный кислород воздуха, «транзитом» проходящий в продукты сгорания; — азот воздуха, также проходящий…ЛЕКЦИЯ 18
Вторичные энергоресурсы
Классификация ВЭР
Под ВЭР подразумевают энергетический потенциал продукции, отходов, побочных и промежуточных продуктов, образующихся в технологических агрегатах, который не используется в самом агрегате, но может быть частично или полностью использован для энергоснабжения других агрегатов.
Все ВЭР разделяются на 3 основные группы:
1. Горючие (топливные) ВЭР — горючие газы плавильных печей, горючие отходы процессов химической и термохимической переработки углеродистого или углеводородного сырья (степень использования 90-95%).
2. Тепловые ВЭР — физическая теплота отходящих газов технологических агрегатов, физическая теплота основной и побочной продукции. Теплота рабочих тел системы принудительного охлаждения технологических агрегатов, теплота горячей воды и пара, отработавших в технологических и силовых установках.
3. ВЭР избыточного давления — потенциальная энергия газов и жидкостей, покидающих технологические агрегаты с избыточным давлением, которую необходимо снижать перед последующей ступенью использования этих газов и жидкостей или выбросом их в атмосферу.
Методы использования тепловых ВЭР
внутреннее регенеративное теплоиспользование, которое характеризуется возвратом теплоты отходящих потоков (их части) для проведения основного… внешнее теплоиспользование, при котором используется теплота отходящих… комбинированное теплоиспользование, когда теплоту отходящих потоков используют как для внутреннего регенеративного,…Установки для внутреннего теплоиспользования
Работа технологической печи улучшают повышением температуры горения при использовании подогретого воздуха, что, в свою очередь, повышает полноту… В некоторых случаях регенерацию теплоты целесообразно использовать и на… Во многих случаях возможности технологического (внутреннего) теплоиспользования ограничены. Поэтому, если в данном…Котлы-утилизаторы
Первичное охлаждение газов в свободном от змеевиков объеме необходимо для затвердевания уносимых из печи расплавленных частиц шлака или… Если отходящий из технологических установок газ не содержит горючие… При конструировании котлов-утилизаторов, использующих тепловые отходы, следует учитывать содержащиеся в греющих…СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
1. Латыпов Р.Ш., Шарафиев Р.Г. Техническая термодинамика и энерготехнология химических производств.-М.:Энергоатомиздат, 1998.-344 с. 2. Баскаков А.П. Теплотехника.-М.:Энергоатомиздат, 1991.-244 с. 3. Алабовский А.Н., Константинов С.М., Недужий А.Н. Теплотехника.-Киев: Выща Школа, Головное издательство, 1986.-255…– Конец работы –
Используемые теги: Лекция, Предмет, метод, Термодинамики, термодинамическая, система0.082
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: ЛЕКЦИЯ 1. Предмет и метод термодинамики. Термодинамическая система
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов