рефераты конспекты курсовые дипломные лекции шпоры
- Раздел Электроника
- /
- ТОКСИКОЛОГИЯ – ПРЕДМЕТ И ЗАДАЧИ
Реферат Курсовая Конспект
ТОКСИКОЛОГИЯ – ПРЕДМЕТ И ЗАДАЧИ
ТОКСИКОЛОГИЯ – ПРЕДМЕТ И ЗАДАЧИ - раздел Электроника, Токсикология – Предмет И Задачи, Особенности Химико-Токс Анализа...
ТОКСИКОЛОГИЯ – ПРЕДМЕТ И ЗАДАЧИ, ОСОБЕННОСТИ ХИМИКО-ТОКС АНАЛИЗА
Токсикология – наука, изучающая свойства ядовитых веществ, вызываемые ими патологические изменения в организме, и эффективные средства для лечения и профилактики отравлений.
Судебная токсикология – раздел судебной медицины, изучающий отравления, возникающие при применении ядов для убийства и самоубийства и интоксикации, являющиеся следствием несчастных случаев.
Токсическая химия – наука, изучающая методы выделения и ядовитых веществ из различных объектов и методы их обнаружения и количественного определения. Токсическая химия относится к фармацевтическим дисциплинам.
Вопросы ТХ:
1. Разработка и совершенствование методов изолирования токсических вещества из обиологического материала.
2. Изучение методов очистки токсических вещества, выделяемых из биологического материал.
3. Разработка методов анализа токсических веществ, определение пригодности и чувствительности химических реакций для идентификации веществ, применение фармхимических методов.
4. Изучение метаболизма токсических вещест.
5. Изучение сохраняемости ЯВ и СД в трупном материале.
6. Изучение экспресс-методов определения ЯВ и СД в трупном материале.
7. Разработка методов анализа вещественных доказательств, не являющихся биологическим материалом.
Разделы ТХ.
1) Судебная химия. Задачи решаются в рамках БСМЭ. Устанавливают причины отравления на основе анализа вещественных доказательств.
Вещественные доказательства – предметы, которые служили орудием совершения преступления, сохранили следы преступления, были объектом преступления и служат средством к раскрытию преступления.
а) биологического происхождения (внутренние органы, биологические жидкости, рвотные массы, промывные воды).
б) небиологического происхождения (остатки пищи, жидкости, посуда, таблетки, одежда).
2) Химико-токсикологический анализ – совокупность научно обоснованных методов применяемых на практике, применяемых для выделения, обнаружения и количественного определения токсических веществ. Выполняется в клиниках по лечению острых отравлений. Выполняется с биологическими жидкостями лиц, находящися в состоянии острой интоксикации (кровь, моча, рвотные массы, промывные воды). Цель – диагностика причины отравления, определение эффективности методов лечения; также профилактическое значение.
3) Промышленная и санитарная химия. Связана с испытанием бытовой химии, средств от насекомых и пр.
4) Ветеринарная экспертиза. Пестициды, гербициды.
5) Пищевая токсикология. Добавки, эссенции, консерваны, красители и их сочетания.
6) Военная токсикология. Химические БАВ (производство, хранение, утилизация).
7) Лекарственная токсикология.
ОСОБЕННОСТИ ХИМИКО-ТОКСИКОЛОГИЧЕСКОГО АНАЛИЗА
Особенности ХТА:
1) Работа с биологическим материалом (внутренние органы, волосы, ногти).
2) Огромное разнообразие объектов исследования.
3) Необходимость выделения яда из объекта, чрезвычайно малые количества яда.
4) Учет метаболизма ТВ в организме.
5) Необходимость интерпритации результатов анализа (можно ли вещество в данных количествах вызвать отравление).
Этапы ХТА: Методы ХТА:
1. Изолирование вещества из биологического материала. Настаивание; жидкость – жидкостаная экстрация; перегонка с водяным паром; минерализация.
2. Очистка полученой вытяжки от сопутствующих (соэкстрактивных вещств). Реэкстрация, диализ (электродиализ), форез (электрофорез), возгонка, различные методы осаждения и высаливания, хроматография (колончатая, гель-хроматограяия, ТСХ).
3. Идентификация (качественный анализ).
Физические методы: тпл, ткип, растворимость, плотность (для вещественных доказательств небиологического происхождения).
Физико-химические методы: хроматография, спектральные методы (СФМ, ИК-спектр, ФЭК, ЯМР, ПМР), рефрактометрия, поляриметрия, хроматометрия, масс.
Фармакологическая проба (на алкалоиды, сердечные гликозиды).
Биохимический метод (для определения карбоксигемоглабина, метгемоглабина, активности холинэстеразы). Иммуноферментный анализ.
4) Количественное определение: физико-химические методы.
| Метод | Абсолютная чувствительность в граммах |
| Полярография | 10-7-10-6 |
| СФМ | 10-7-10-6 |
| Колориметрия | 10-7-10-6 |
| ТСХ | 10-7-10-6 |
| Бумажная хроматография | 10-7-10-6 |
| ГЖХ с детектором ДИП | 10-9-10-8 |
| ГЖХ с детектором ДЭЗ | 10-10-10-9 |
| ВЖХ с УФ детектором | 10-7-10-6 |
| ВЖХ с флюоресцирующим детектором | 10-9-10-8 |
| Иммуноферментный анализ | 10-11-10-10 |
| Радиоизотопный метод | 10-12-10-11 |
| Цветные реакции | 10-6-10-5 |
ОРГАНИЗАЦИЯ СУДЕБНО – ХИМИЧЕСКОЙ ЭКСПЕРТИЗЫ
Организация судебно-медицинской службы.
БСМЭ находится в ведении МЗиСР. Существует должность «главный суд-мед эксперт РФ». При нем организуется… Российский центр СМЭ – находится в ведении МЗ, осуществляет организацонно-методическое руководство БСМО различных…Порядок оказания помощи при острых отравлениях
1. Реанимация 2. Токсикологический отдел. 3. Биохимическая лаборатория.ЯДЫ И ОТРАВЛЕНИЯ. ИХ ХАРАКТЕРИСТИКИ И КЛАССИФИКАЦИЯ
Классификация отравлений:
I. По клинической картине.
1. Острые - при однократном поступлении завышенной дозы ТВ, нарастание симптомов отравления, симптомы ярко выраженные.
Может заканчиваться смертью в течение нескольких минут, часов, суток.
2. Хронические – при длительном прерывистом поступлении небольших доз ТВ, способного к кумуляции. Характеризуется неярко выраженной картиной отравления и длительным течением.
II. По тяжести отравления.
1. Легкой степени.
2. Средней степени.
3. Тяжелой
4. Крайне тяжелой.
5. Смертельные.
Степени отравления зависят от выраженности клинических симптомов и в меньшей степени от величины принятой дозы. Развитие осложнений ухудшает прогноз течения отравлений.
III. По причине и месту отравления
1. Случайные
а) бытовые (происходят дома, в медицинских учреждениях: неправильный прием средств, неправильный путь ввода, неправильная доза)
б) производственные (возникают на производствах при нарушении ТБ, при авариях). Бывают острые и хронические.
2. преднамеренные.
а) Криминальные – умышленное отравление с целью убийства или приведения в бессознательное состояние.
б) Суицидальные.
IV. По источнику ТВ.
1. Биологический источник. При укусах змей, яд насекомых.
2. Пищевые.
а) Химические – при попадании в пищу ЯВ, растворителей.
б) инфекционные. При попадании в пищу бактерий или бактериальных токсинов.
V. По происхождению яда
1. Растительного.
2. Животного происхождения.
3. Синтетические вещества.
VI.
1. Экзогенные – поступление яда извне.
2. Эндогенные – при нарушении метаболизма (сахарный диабет).
VII По пути поступления яда
1. Ингаляционные
2. Пероральные
3. Перкутальные
4. Ректальные
5. Парэнтерельные
6. Внутриутробные.
Классификация ядов
I. Общая
1. По химической природе.
а) Неорганические (ТМ, HCN, соли).
б) Органические (ЛП, Алкалоиды)
в) Элементорганические (яды-химикаты).
2. По происхождению
а) Растительные
б) Животные
в) Синтетические
3. По применению яда
а) Ядохимикаты (P, Hg-органика)
б) Промышленные яды (растворители).
в) ЛВ
г) Бытовые яды (средства бытовой химии, моющие средства)
д) Боевые отравляющие вещества
4. Гигиеническая оценка (по степени опасности). Критерий – ПДК, смертельная доза.
а) Чрезвычайно токсичные – первый класс токсичности. ПДК<1 мг/м3 воздуха.
б) Высоко токсичные. ПДК<10 мг/м3 воздуха.
в) Умеренно токсичные. ПДК<100 мг/м3 воздуха.
г) Малотоксичные. ПДК>100 мг/м3 воздуха.
5. Токсикологическая. По характеру воздействия на организм.
а) Нервно-паралитические. Удушье, судороги, паралич. БОВ, фтор-органика, никотин, анабазин.
б) Кожно-резорбтивного действия. Некоторые изменений слизистой кожи на месте первичного контакта + общее отравление. Уксусная кислота, хлорсодержащие ядохимикаты, органические соединения мышьяка, ртути.
в) Яды слезоточивого действия. Они же ирританты. В незначительных концентрациях – избирательное раздражение слизистой глаза, ВДП. Пары крепких кислот, щелочей, хлорпикрин.
г) Яды общетоксического действия. Судороги, паралич, отек головного мозга. HCN, CO, этанол, суррогаты этанола.
д) Яды психического действия. Нарушение психической активности, сознания. Наркотики, БОВ.
II. Специальная.
1. По механизму токсического действия.
а) По патохимическому действию различают. Яды – структурные аналоги ферментов, гормонов, или яды, избирательно воздействующие с ними. Это фосфор-органика.
б) По патофизиологическому действию.
- Едкие яды (щелочи, кислоты, ртуть-органика)
- Резорбтивного действия. Действуют после всасывания.
- Яды крови – бензол, нитробензол, CO, HCN.
- Деструктивные яды – дистрофия и некроз внутренних органов.
- Функциональные яды – изменение функций органа без видимых морфологических изменений.
в) По избирательности токсичности.
- Избирательно на ЦНС
- Яды печени
- Яды почек
г) По методам изолирования.
Токсикокинетика – наука, изучающая процессы всасывания, распространения, биотрансформации и выделения ТВ в организме человека.
Перкутанный путь – через кожу, пот, кожное сало и т.п.
Пероральный путь – ЖКТ, печень, желчь, кишечник, кал.
Ингаляционный путь – легкие, выдыхаемый воздух.
Парентеральный путь – сразу в кровь (в кровь ТВ также попадает любым другим путем).
ПУТИ ПОСТУПЛЕНИЯ ЯДОВ В ОРГАНИЗМ, ТОКСИКОКИНЕТИЧЕСКИЕ КОНСТАНТЫ
Вещества в газообразном, парообразном или пылеобразном состоянии. Вещества быстро поступают в кровь, что связано с большим легочных альвеол (100-150… Крупные частицы (до 10 мкм) задерживаются в верхних дыхательных путях и… 2. Пероральный.Распределение яда.
Некоторые соединения, циркулируя в крови, взаимодействуют с эритроцитами (мышьяк, свинец). Неэлектролиты находятся в жидкофазной части крови и… Распределение яда в организме зависит от кровоснабжения органа и физико-химических свойств яда. Липофильные соединения…Токсикокинетические константы.
1. Одночасная (для сосудистого пути поступления яда). Введение – кровь – выведение. 2. Двучасная система (для внесосудистого поступления). Введение – ткань – кровь – выведение.ПАТОЛОГИЧЕСКИЕ СИМПТОМЫ ПРИ ОСТРЫХ ОТРАВЛЕНИЯХ, МЕТОДЫ ДЕТОКСИКАЦИИ
Диагностика острых отравлений: 1. Анамнез – сбор сведений, беседа с пострадавшим, результаты осмотра места… 2. Данные лабораторных исследований (химической, химико-токсикологической).Факторы, влияющие на развитие отравления
1. Физико-химические свойства яда. 2. Токсическая доза и концентрация в биологической среде. 3. Характер связи с субстратом.ГАЗОЖИДКОСТНАЯ ХРОМАТОГРАФИЯ.
Разделяют с помощью ГЖХ: вещества, испаряющиеся без разложения или вещества, которые разлагаются, но дают идентифицируемые газообразные продукты;… Схема:ПРЕДВАРИТЕЛЬНЫЕ ИСПЫТАНИЯ
Предварительные испытания проводят перед составлением плана хим-токс анализа. Результаты позволяют исключить ряд веществ и предположить какие вещества или группы веществ могут содержаться в объекте. Позволяют рационально расходовать биоматериал и экономические резервы и время анализа.
Определение рН среды
Универсальные индикаторн бумажки: - Красная лакмусовая бумажка (КЛБ) - Синяя лакмусовая бумажка (СЛБ)Особенности изолирования некоторых летучих ядов.
Реакции на фенол: с бромной водой и FeCl3. Мешают органические спирты и кислоты. К дистилляту добавляют NaHCO3, с которым кислоты образуют соли.… Высшие спирты. Качественные реакции: реакция окисления, образования алкилацетатов, Комаровского (с салициловым…Синильная кислота и ее соли, Метиловый спирт.
2. Действие на организм: LD50HCN – 1мг/кг, NaCN – 3мг/кг, амигдалин – 16 мг/кг. Отравление происходит быстро, потеря сознание, изгиб дугой, через 5… 3. Первая помощь: вдыхание амилнитрита, внутривенно раствор NaNO3. При этом… Внутрь – раствор Na2S2O3, при этом цианиды превращаются в роданиды.Метиловый спирт.
1. Токсикологическое значение: используют как растворитель, для получения формальдегида, муравьиной кислоты, пластмасс. 2. Действие на организм. Токсическая доза – 7-8 мл. Смертельно – 30-100 мл.… Стадии отравления:Этанол.
2. Действие на организм. Токсическая доза индивидуальна. Смертельная доза – 6-8 мл на килограмм. Этанол – наркотический яд, возбуждение переходит в… Этанол хорошо всасывается и распространяется, передается с грудным молоком.… Стадии резорбции: через 15-20 минут (на голодный желудок) и через 30-40 минут (на сытый желудок). Выводится через…Изоамиловый спирт, Этиленгликоль, Уксусная кислота
Большое его количество содержится в самогонке, в чаче. Высшие спирты очень медленно окисляются, выводятся с мочой в виде коньюгатов с… При вскрытии – особенностей нет. Из полости рта – запах изоамилового спирта.Этиленгликоль
Отравления: потеря сознания, судороги, отеки легких, падение артериального давления. На 2-3 сутки развивается почечная и печеночная недостаточность. Первая помощь: гемодиализ, перитониальный диализ, форсированный диурез, этанол внутрь (внутривенно), CaCl2…Ацетон, Фенол, Хлорированные углеводороды, дихлорэтана
Яд наркотического действия. Метаболизируют до CO2. Может быть обнаружен у людей, страдающих СД. На…Фенол
Токсикологическое значение: в медицинской практике – дезинфицирующее средство. В химическое промышленности – для получения красителей, фарм препаратов, производстве используется для защиты р-й.
В организм попадает через кожу (ожоги). Смертельная доза – 10,0. Отравление: рвота, боли в желудке, ожоги, моча оливкового цвета.
Выводится с мочой в виде коньюгатов с глюкуроновой и серной кислотами (см. лекцию метаболизм).
На анализ: моча, печень, почки, головной мозг.
Изолирование: макродистилляция.
Моча: макродистилляция, но предварительно проводится гидролиз ( + HNO3, HCl) для разрушения коньюгатов.
Анализ проводится после пробоподготовки. Добавляют NaHCO3.
Идентификация:
а) C бромной водой.
б) с FeCl3
Количественное определение:
1) Гравиметрия
2) Броматометрия.
Хлорированные углеводороды.
Токсикологическое значение: широко применяются в быту, в промышленности. Действуют на ЦНС, наблюдается почечная и печеночная недостаточность, рвота,… Первая помощь: срочная госпитализация, промывание желудка, гемодиализ, перитональный диализ (с фистулой),…Высшие спирты. Формальдегид.
К дистилляту + эфир, фильтруют ч/з безводный Na2SO4 в сухую выпарительную чашку. Испаряют эфир при комнатной температуре. С сухим остатком проводят… 1) Получение амилацетата – запах грушевой эссенции: C5H11OH + 2 CH3COONa + H2SO4 à CH3COOCH2CH2CH(CH3)2 + Na2SO4 + H2OФормальдегид.
Также как у хлороформа (“-“ СХЗ) 2) С аммиачным раствором AgNO3 – серый осадок или “серебрянное зеркало” HCOH + [Ag(NH3)2]NO3 à 2Ag↓ + HCOONH4 + 2 NH4NO3 + NH3ВЕЩЕСТВА, ИЗОЛИРУЕМЫЕ МЕТОДОМ МИНЕРАЛИЗАЦИИ
Яды, имеющие судебно-медицинское значение: Ba, Cr, Zn, Tl, Mn, Cu, Ag, Pb, Hg, Bi, Cd, As, Sb, Sn, Ni. Металлические яды попадают в организм главным образом per os, через кожу,… 2 группы металлических ядов:Обнаружение катионов в минерализате.
Систематический: последовательное выделение групп ионов, затем разделение на подгруппы, затем обнаружение их в подгруппах (сероводородный метод). … Недостатки: большая навеска биоматериала, длительность анализа, большое… Дробный метод по Крыловой.Анализ вещественных доказательств.
Р-ры д/инъекций или ампулы. Описание: внеш вид – V, герм-ть, надпись. Ампулу вскр-т и опр-т pH р-ра и пок-ль прел-я η на рефрактометре. Получ… Порошки. Предварит-е исп-я: описание- вн вид, цвет, запах, размер и форма… Жидкости. Опсание – внеш вид, цвет, запах. Опред-е рН: < 7 – опр-т анион SO4 – с HCl и BaCl2, Cl - с HNo3 и AgNO3,…Анализ ЛРС.
1. внешний вид сырья (макро- и микро-), 2. изолирование: ЛРС изм-т, зал-т водой, подк-т H2SO4 до рН=2-2,5. Наст-т 30… 3. Анализ:СХЕМА ДРОБНОГО АНАЛИЗА ПО А.Н. КРЫЛОВОЙ.
БАРИЙ, СВИНЕЦ, ТЕТРАЭТИЛСВИНЕЦ
Первый вариант: после минерализации мы имеем бесцветный или окрашенный раствор. Окраску дают Mn, Cr, Cu.
Второй вариант: прозрачный раствор с осадком. В осадок выпадают Ba, Pb (Ca, но он не имеет токсикологического значения) – BaSO4, PbSO4. На поверхности осадка десорбируются Cr, Mn. При наличии осадка к минерализату добавляют воду (чтобы фильтр не сгорел) и фильтруют. Фильтр промывают горячим раствором (NH4)CH3COO, Pb(CH3COO)2 переходит в раствор.
Ba.
Применяют как рентгеноконтрастное вещество, для изготовления керамики, для борьбы с грызунами.
заб. гол.м.
Паралич сердца.
Незначительная часть кумулируется в печени, почках, наибольшая – в почках. Выводится с мочой, через ЖКТ.
Первая помощь: промывание желудка, прием Na2SO4.
Идентификация: Минерализация смесью 2-х кислот.
1. Микрокристаллическая реакция. На предметное стекло помещают осадок, добавляют к.H2SO4 и нагревают в пламени горелки до выделения паров сернистого ангидрида. Охлаждают, получаются характерные кристаллы в виде «летящих птиц»
2. Микрокристаллическая реакция с KIO3. На платиновую петлю помещают осадок BaSO4 и вносят в пламя горелки. Содержимое петли помещают в каплю HCl, помещают на предметное стекло и добавляют кристалл KIO3 à образуются призматические кристаллы.
BaSO4  BaS + 2O2
BaS + 2O2
BaS + 2HCl à BaCl2 + H2S
BaCl2 + KIO3 à Ba(IO3)2 + 2KCl
Количественное определение:
Гравиметрия, обратная трилонометрия (растворяют в горячем насыщенном трилоне).
Pb
Используют в производстве аккумуляторов, при изготовлении свинцовых белил, для получения этилированного бензина.
Много свинца содержится в выхлопных газах и растительном сырье, произрастающем вдоль дорог.
Изменяется картина крови. Частично кумулируется в костях, печени, почках, выводится через ЖКТ.
Первая помощь: трилон Б.
Изолирование: смесью 2-х кислот.
Идентификация:
1. Реакция с дитизоном (основная):

(тион-тиольная таутомерия)
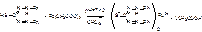
Хлороформный слой окрашивается в пурпурно-красный цвет. Его отделяют и добавляют раствор HNO3 (реэкстракция).

Хлороформный слой отбрасывают и с реэкстрактом проводят реакции:
2. С насыщенным раствором Na2S à черный осадок.
Pb(NO3)2 + Na2S à PbS↓ + 2NaNO3
3. Образование сульфата (белый осадок).
Pb(NO3)2 +H2SO4 à PbSO4↓ + 2HNO3
4. С раствором KI. Желтый осадок (золотой дождь).
Pb(NO3)2 + KI à PbI2↓ + 2KNO3
5. С K2Cr2O7. Желто-оранжевый осадок.
Pb(NO3)2 + K2Cr2O7 + H2O à 2PbCrO4↓+ 2KNO2 + 2H2O
При малых количествах Pb используют микрокристаллические реакции:
1. С хлоридом цезия. Желто-зеленые кристаллы.
CsCl + 3KI + Pb(NO3_2 à CsPbI3↓ + KCl + 2KNO3
2. С солями меди. Черные кристаллы в виде куба.
Pb(NO3)2 + Cu(CH3SOO)2 + 6KNO2 à K2CuPb(NO2)6↓ + 2CH3COOK + 2KNO3
Количественное определение:
ФЭК, СФМ в видимой области (по первой реакции), комплексонометрия, бихроматометрия, йодометрия.
Тетраэтилсвинец. Pb(C2H5)4
Изолирование: 1. Метод дистилляции. Биоматериал измельчают и проводят перегонку с водяным… 2. Смесью 2-х кислот.Mn
Стекольная промышленность, металлургия, медицинская практика.
Отравление с целью суицида.
Ожоги слизистой. Mn воздействует на ЦНС, кумулируется в печени, почках, выводится с мочой или через ЖКТ.
Изолирование:
1. При целенаправленном исследовании – сухое озоление (сжигание)
2. Смесью 2-х кислот.
Идентификация:
Основана на реакциях окисления.
1. 2MnSO4 + 5KIO4 + 3H2O  2HMnO4 + 5KIO3 + 2H2SO4
2HMnO4 + 5KIO3 + 2H2SO4
Розовое окрашивание.
Дигидрофосфат Na необходим для связывания Fe, Sb, которые мешают окраске.
Реакция носит отрицательное судебно-химическое значение, т.к. открывает эндо и экзогенный Mn.
2. 2MnSO4 + 8H2O + 5(NH4)S2O8  2HMnO4 + 5(NH4)SO4 + 7H2SO4
2HMnO4 + 5(NH4)SO4 + 7H2SO4
Розовое окрашивание. AgNO3 – катализатор. Реакция носит положительное суд-мед значение.
Количественное определение:
ФЭК или СФМ по первой реакции, йодометрия.
Cr
Токсикологическое значение: применяется в кожевенной промышленности, в гальванических цехаха, в сельском хозяйстве для протравливания семян.
Очень опасны соли Cr+6, они вызывают онкологические заболевания, ожоги слизистой. На анализ берут желудок, пищевод (окрашены в желтый цвет).
Кумулируется в печени, почках, выводится с мочой, через ЖКТ.
Антидот: унитиол и различные мази при экземах и ожогах.
Изолирование: смесью 2-х кислот.
Идентификация: чтобы проводит основную реакцию на Cr, необходимо перевести его из Cr3+ в Cr6+.
Cr(SO4)3 + 3(NH4)2S2O8 + 7H2O  H2Cr2O7 + 3(NH4)2SO4 + 6H2SO4
H2Cr2O7 + 3(NH4)2SO4 + 6H2SO4
1. Образование надхромовых кислот. Эфирный слой окрашивается в синий цвет.
H2Cr2O7 + 4H2O2 à 2H2CrO6 + 3H2O
2. С дифенилкарбазидом.
а)
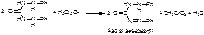
б)
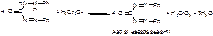
в)

Розовое окрашивание. При добавлении этилацетата окраска усиливается (до красно-фиолетовой).
Количественное определение:
ФЭК или СФМ по реакции с дифенилкарбазидом.
Ag
Токсикологическое значение: в производстве зеркал, в фотографии, в медицине, реактив в лабораториях.
При попадании на кожу, внутрь – прижигающее действие. Длительное применение – аргирия (кожа серо-зеленого цвета).
Выводится с мочой, через ЖКТ.
Первая помощь: трилон Б, NaCl.
Изолирование:
1. Целенаправленное обнаружение – сухое озоление.
2. Смесью двух кислот.
Идентификация:
1. С дитизоном. Хлороформный слой окрашивается в золотисто-желтый цвет.

Аналогичным образом реагирует ртуть. Для того, чтобы их отличить, хлороформный слой отделяют, добавляют раствор HCl. Если эффект сохраняется, то имеем дело с ртутью, если хлороформный слой становится зеленым, а в водном слое появляется белый осадок, то у нас серебро.
2. Т.к. Ag мешает определению других катионов, его выводят: добавляют NaCl насыщенный, нагревают, фильтруют. Теперь с минерализатом можно проводить дальнейшие исследования, а осадок растворяют в NH4OH, часть раствора помещают на предметное стекло, упаривают и добавляют KI. Появляются желтые кристаллы.
3. Микрокристаллическая реакция. К раствору прибавляют тиомочевину, пикрат калия – выпадают желтые призматические кристаллы.
Количественное определение:
Роданидом аммония
СФМ или ФЭК по реакции с дитизоном.
Серебро не мешает определению Mn, Cr, но мешает определению последующих катионов, поэтому его выводят из минерализата, добавляя насыщенный NaCl. Но открытию Mn, Cr будут мешать хлорид-ионы:
2HMnO4 + 14HCl à 2MnCl2 + 5Cl2 + 8H2O
В реакциях окисления Cr, Mn в качестве катализатора используют AgNO3, серебро выпадет в осадок AgCl. Поэтому в первую очередь открывают Cr, Mn.
МЕДЬ, ЦИНК, КАДМИЙ
Cu
В ювелирной промышленности, в медицинской промышленности, в стекольной промышленности, в сельском хозяйстве.
Картина отравления: рвота, измененная картина крови, кумулирует в печени, выводится через ЖКТ.
Первая помощь: трилон Б, ферроцианид калия, промывание желудка.
Отравления редки: суицид, в сочетании с ЛП.
Изолирование:
1. Целенаправленное исследование – сухое озоление, сплавление.
2. Смесью двух кислот.
Идентификация:
1. Основная реакция с диэтилдитиокарбоминатом свинца в хлороформе.

При исследовании меди пользуются правилом Таннанаера: каждый предыдущий металл в ряду Hg>Cu>Pb, находящийся в водном растворе, вытесняет его из комплексов с ДДТК.
(ДДТК)2Pb + CuSO4  (ДДТК)2Cu + PbSO4
(ДДТК)2Cu + PbSO4
Хлороформный слой окрашивается в коричневый цвет. Его отделяют и добавляют раствор HgCl2.
(ДДТК)2Cu + HgCl2 à (ДДТК)2Hg + CuCl2
Хлороформный слой отбрасывают, а с реэкстрактом проводят следующие реакции:
а) С пиридинродановым реактивом.
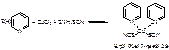
б) С тетрароданмеркураммонием. Розовато-малиновый осадок.
CuCl2 + 2(NH4)2Hg(SCN)4 + ZnSO4 à CuZn[Hg(SCN)4]2↓ + 2NH4Cl + (NH4)2SO4
в) С гексацианоферратом калия. Красно-бурый осадок.
CuCl2 + CdCl2 + K4[Fe(CN)6] à CuCd[Fe(CN)6]↓ + 4KCl
Количественное определение.
1. ФЭК, СФМ по первой реакции.
2. Комплексная йодометрия.
3. Комплексонометрия.
Zn
Применяют в медицине, в паяльном деле (паяльная кислота), для консервирования древесины, в сельском хозяйстве применяют фосфид Zn.
Отравления редки.
Расстройство желудка, судороги. Кумулируется в печени, поджелудочной железе. Выводится с мочой и через ЖКТ.
Первая помощь: промывание желудка, раствор трилона Б.
Изолирование:
1. Целенаправленное исследование: сухое озоление, сжигание.
2. Смесью двух кислот.
Идентификация.
1. Основная реакция – с дитизоном.
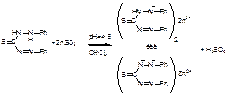
Хлороформный слой окрашивается в розово-красный цвет с фиолетовым оттенком.
Если эффект есть, к минерализату добавляют (ДДТК)Na для концентрирования Zn.
ZnSO4 + (ДДТК)Na 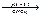 (ДДТК)2Zn + Na2SO4.
(ДДТК)2Zn + Na2SO4.
Хлороформный слой отделяют и добавляют раствор HCl
(ДДТК)2Zn + 2HCl à 2ДДТКH + ZnCl2
Хлороформный слой отбрасывают, с реэкстрактом проводят реакции:
а) ZnCl2 + Na2S à ZnS↓ + 2NaCl
Белый осадок.
б) С гексацианоферратом калия. Белый осадок.
3ZnCl2 + 2K4[Fe(CN)6] à Zn3K2[Fe(CN)6]2↓ + 6KCl
в) С тетрароданмеркураммонием. Кристаллы клиновидной формы.
ZnCl2 + (NH4)Hg(SCN)4 à ZnHg(SCN)4↓ + 2NH4Cl
г) С дитизоном. (смотри выше)
Количественное определение: ФЭК, СФМ по реакции с дитизоном, комплексонометрия.
Cd
Соединения очень токсичны. Отравления в основном у детей (краски на играх содержат CdSO4). Много в сточных водах.
Анализ аналогичен Zn, но не проводят реакции с дитизоном, а сразу прибавляют ДДТКNa, проводят реэкстракцию.
ДДТКNa + CdCl2 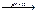 (ДДТК)2Cd + 2NaCl
(ДДТК)2Cd + 2NaCl
(ДДТК)2Cd + HCl à 2ДДТКН + CdCl2
Далее с реэкстрактом проводят реакции:
1. Образование CdS. Осадок желтого цвета.
CdCl2 + Na2S à CdS↓ + 2NaCl
2. Микрокристаллические реакции:
а) Каплю реэкстракта выпаривают на предметном стекле, добавляют раствор бруцина в растворе H2SO4 и каплю KBr. Наблюдаем призматические кристаллы, собранные в пучки.
б) Сухой остаток реэкстракта + капля пиридина + капля KBr à призматические кристаллы, собранные в пучки (аналогично предыдущей).
Количественное определение: комплексонометрия.
Изолирование: смесью двух кислот.
Первая помощь: трилон Б.
ВИСМУТ, СУРЬМА, ТЕЛЛУР, ЭТИЛМЕРКУРХЛОРИД
Bi
Применяют в стекольной промышленности, в медицине, для приготовления люминофоров. Отравления: прием внутрь, вдыхание пыли с Bi.
Кумулируется в головном мозге, печени, почках, селезенке. Выводится с мочой, потом, через ЖКТ.
Первая помощь: промывание желудка, раствор трилона Б.
Изолирование: смесью двух кислот.
Идентификация:
1. С тиомочевинной. n=3-9. Лимонно-желтое окрашивание.
Bi2(SO4)3 + nS=O(NH2)2 à Bi2(SO4)3 • nS=O(NH2)2
2. С 8-оксихинолином.
Bi2(SO4)3 + 8KI + 2HCl à 2HBiI4 + 2KCl + 3K2SO4
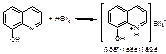
Если реакция дает положительный эффект, то проводят реэкстракцию.
Bi2(SO4)3 + 6ДДТКNa à 2(ДДТК)3Bi + 3Na2SO4
Хлороформный слой, содержащий (ДДТК)3Bi, отделяют, добавляют HNO3
(ДДТК)3Bi + HNO3 à Bi(NO3)3 + 3ДДТКН
С реэкстрактом проводят реакции:
а) С тиомочевинной (смотри выше).
б) Микрокристаллическая реакция.
- к сухому остатку добавляют бруцин и раствор KBr à желто-зеленые кристаллы, собранные в пучки.
- с CsCl. К сухому остатку прибавляют CsCl, KI. Эффект – оранжево-красные кристаллы в виде шестиугольников.
Bi(NO3)3 + CsCl + 4KI à CsBiI4 + 3KNO3 + KCl.
К минерализату добавляют Zn пыль à восстановление до Bi°, его отфильтровывают, добавляют HNO3, тиомочевину à ярко-желтое окрашивание.
Количественное определение: комплексонометрия.
Sb
Как реактив в стекольно-резиновой промышленности.
Очень токсична. Воздействует на ЦНС, нарушается обмен веществ, действует на сердечную мышцу.
Первая помощь: промывание желудка, прием «антидотум-металлурум» (Na2S + NaHCO3 + MgSO4), который связывает катион сурьмы.
Изолирование: смесью двух кислот.
Идентификация: образование ионных ассоциатов с малахитовым или бриллиантовым зеленым.
Чтобы провести реакцию, сурьму переводят из Sb3+ в Sb5+
Sb2(SO4)3 + 2NaNO2 + 16HCl à 2HSbCl6 + 4NH4Cl + 3H2SO4 + 4H2O + 4NO
2NaNO3 + 2HCl + O=C(NH2)2 à 2N2 + CO2 + 2NaCl + 2H2O
Добавляют толуол и бриллиантовый (малахитовый) зеленый.

Толуоловый слой окрашивается в синий цвет.
Такой же эффект дает таллий, поэтому чтобы их различить, проводят реакцию с тиосульфатом Na. Выпадает оранжево-желтый осадок.
Sb2(SO4)3 + 3Na2S2O3 + 3H2O à Sb2S3↓ + 2Na2SO4 + 3H2SO4
Количественное определение: ФЭК, СФМ по реакции образования ассоциата.
Tl
Используется для изготовления ламп, в оптической промышленности, в стекольной промышленности, в кожевенной промышленности, для обработки древесины.
Кумулируется в печени, почках, выводится с мочой, через ЖКТ.
Первая помощь: активированный уголь, тиосульфат натрия, «Антидотум-металлурум», промывание желудка.
Изолирование: смесью двух кислот.
Идентификация:
1. С бриллиантовым или малахитовым зеленым.

Толуольный слой окрашивается в голубой или синий цвет. Аналогичную реакцию дает сурьма.
2. С дитизоном. Сперва необходимо перевести Tl из Tl3+ и Tl1+
3Tl2(SO4)3 + 4NH2OH + 12NH4OH à 3Tl2SO4 + 4NO + 6(NH4)2SO4 + 12H2O

Хлороформный слой окрашивается в красный цвет.
Количественное определение:
1. ФЭК, СФМ по обеим цветным реакциям.
2. Комплексонометрия.
Этилмеркурхлорид C2H5HgCl
Изолирование: настаивание с концентрированной HCl недостаточно. Жидкость фильтруют и проводят экстракцию хлороформом. Идентификация: хлороформное извлечение наносят на пластинку ТСХ, погружают ее… Колончатая хроматография: извлечение пропускают через колонку, затем проводят реакцию с дитизоном.МЫШЬЯК, РТУТЬ
As
Широко применяется в металлургии, медицине.
Мышьяк сам по себе не токсичен, токсичны соединения As3+, As5+.
Кумулируется в ногтях, волосах, костях.
Воздействует на ЦНС, нарушает картину крови.
Антидоты: унитиол, «Антидотум-металлурум», промывание желудка.
Изолирование:
1. Целенаправленное исследование – сплавление.
2. Смесью двух кислот.
Идентификация:
1. Предварительные пробы
а) Изучение фарфоровидных крупинок (их находят в желудке)
б) Проба Рейнша (с мочой).
в) Проба Зангер-Блека.
Все они имеют отрицательное судебно-химическое значение.
При испытании пробы 3ангер-Блека определению мышьяка мешает сурьма. Если эффекта нет, то дальше исследование не проводим, если есть, то делаем основные исследования – проба Марша.
2. Метод Марша - проводят в специальном приборе.

Метод многодоказательный и позволяет отделить мышьяк от сурьмы.
а) Если было отравление мышьяком – ощущается чесночный запах арсина AsH3.
б) На выходе поджечь – горит синим пламенем.
в) К выходу подставить охлажденную фарфоровую чашку – будет буровато-серый с металлическим блеском налет мышьяка.
г) Трубку Маша в узком месте нагреть, а выше охладить – будет налет мышьяка. Для сурьмы – матово-черный налет.
д) Трубку Маша отсоединить от прибора и место налета нагреть, а выше охладить, образуется налет оксида мышьяка = кристаллы (октаэдры), сурьма дает аморфный осадок.
е) Конец трубки Марша поместить в раствор AgNO3 à выпадет осадок серебра.
AgNO3 + AsH3 à Ag3As + 3HNO3
Ag3As + 3AgNO3 à Ag3As•3AgNO3
Ag3As•3AgNO3 + 3H2O à 3HNO3 + 6Ag + H3AsO3
Используют при КО.
ж) Чтобы отличить мышьяк от сурьмы, налет из трубки Марша помещают на предметное стекло, растворяют в HNO3, добавляют CsCl + HCl. Для сурьмы будут кристаллы в виде многогранников, а для мышьяка ничего не будет. При дальнейшем добавлении кристалла I2 для обоих будут шестиугольные кристаллы. При добавлении 1 капли пиридина для сурьмы кристаллы обесцветятся, но сохранят форму, а для мышьяка кристаллы растворятся, по краю капли образуются зеленовато-желтые игольчатые кристаллы.
Количественное определение: визуальная калориметрия по методу 3-Б, аргентометрия (осадок серебра отфильтровывают и титруют NH4SCN); атомно-абсорбционная СФМ; ФЭК по реакции с диэтилдитиокарбоминатом серебра. Мешает сурьма (?).
Hg
В неорганических соединениях, в приборостроении, в электротехнике, для изготовления люминесцентных ламп, для изготовления термометров. Металлическая ртуть используется для выделения благородных металлов из руд.
Органические соединения ртути – ядохимикаты.
Токсичны соединения ртути, растворимые в воде, поражают ЦНС, печень, почки, слюнные железы, ЖКТ. При отравлении ощущается металлический привкус, выводится с мочой, через ЖКТ. При вскрытии обнаруживается нефронекроз, сулемовая почка (серая почка).
Первая помощь: промывание желудка, «Антидотум металлорум».
Предварительные испытания на ртуть с мочой (проба Рейшина). К моче добавляют медные спиральки, HCl, и нагревают на водяной бане. Если было отравление, спиральки покрываются налетом, их вынимают, промывают последовательно водой, спиртом, эфиром и помещают в тугоплавкую пробирку, добавляют кристаллы I2, нагревают в пламене горелки; выносят из пламени, охлаждают смоченным тампоном. Под микроск видны крист характерной формы.
Изолирование: деструктивный метод. На анализ: печень, почки по 20,0 и помещают в разные колбы. При естественном содержании ртути в почках больше, в печени меньше. При отравлении происходит перераспределение – в печени больше.
В каждую колбу добавляют 10 мл воды, 1 мл этанола (катализатор), 10 мл HNO3, 10 мл по каплям H2SO4, после окончания выделения пузырьков окислов азота, колбу нагревают в течение 10-15 минут на водяной бане, охлаждают, добавляют воду и фильтруют в раствор мочевины. Минерализуют смесью трех кислот и этанола (катализатор) в течение 5 минут. Далее как первый метод.
Идентификация:
1. С дитизоном.

Хлороформный слой окрашивается в золотисто-желтый цвет. Аналогично реагирует серебро, чтобы их отличить, хлороформ отделяют и добавляют HCl, комплекс ртути разлагается, а серебра – нет.
2. Основное доказательство – метод Рубцова-Полежаевой. Хлороформный слой с дитизоном (из предыдущей реакции) отделяют и добавляют раствор I2 в KI.
Hg(DzH)2 + I2/KI à K2HgI4
Хлороформный слой отбрасывают, к реэкстракту добавляют:
K2HgI4 + 2CuSO4 + 2KI + Na2SO3 + 2NaHCO3 à Cu2HgI4↓ + 2CO2 + 2K2SO4 + Na2SO4 + H2O + 2NaI
Выпадает розовый осадок.
2CuSO4 + 4KI à 2CuI2 + 2K2SO4
2CuI2 à I2 + 2CuI
2CuI + K2HgI4 à Cu2HgI4 + 2KI
I2 + H2O + Na2SO3 à 2HI + Na2SO4
2HI + 2NaHCO3 à 2NaI + 2CO2 + 2H2O
Сульфит натрия используется в реакции, чтобы убрать I2, который будет мешать окраске. Выделяющийся HI будет разлагать медный комплекс, поэтому добавляют NaHCO3.
Количественное определение: ФЭК по реакции Рубцова-Полежаевой; ФЭК, СФМ в видимой области по реакции с дитизоном.
ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА. Общие методы изолирования.
ЛВ (официально ЛП и наркотические средства) 1) Кислотного характера (производные барбитуровой кислоты, салициловой… 2) Вещества нейтрального или слабокислого характера (производные п-аминофенола, СГ).Общие методы изолирования.
Метод Стаса-Отто 50,0-100,0 биоматериала измельчают и заливают абсолютным этанолом, подкисляя… 1. Для подкисления используют органические кислоты для избежания гидролиза сложноэфирных, амидных и других связей.Бензодиазепины
(Диазепам, Седуксен, Валиум) 7-хлор-5-фенил-1-метил-1,2-дигидро-3Н-1,4-бенздиазепин-2-он. ЛФ - табл., растворыПроизводные пурина.
TheophyllinumПАПАВЕРИН. ДИМЕДРОЛ ХИНИН
Tox знч-е: спазмолитик, оказ-т сосудорасшир-е д-е. Исп при бронх-й астме и с др ЛП. Мет-м: ____________________________. Изол-е: част-й – Кромаренко, общ – Стас-Отто и Васильевой. Слаб-е основание – м.б как в кислом, так и в щелочном…ДИМЕДРОЛ
β-диметил-аминоэтилового эфира tox значение – п/гист-й преп-т д/леч-я крапивницы, разл-х форм аллергии, как… П/помощь: пром-е жел-ка, форсир диурез, гемосорбция, при возб-ии – аминазин в/м, судороги – диазепам в/м.ХИНИН
1. талейохинная проба – в лекциях

2. микрокрист-я р-я – (с роданидом аммония)
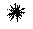
Папаверин
1. с р-вом Марки – вишнево-кр
2. с к.HNO3 – желт-оранж
3. H2SO4 – сине-фиол
4. микрокрист-я – см рисунки.
БАРБИТУРАТЫ. ПРОИЗВОДНЫЕ ПИРАЗОЛОНА. АЛКАЛОИДЫ ТРОПАНА
Антипирин, амидопирин, анальгин
2. с азотистой к-той: антипирин – зеленое окр-е, амидопирин – фиол-е.АЛКАЛОИДЫ ПРОИЗВОДНЫЕ ТРОПАНА
Токсическое значение: при язвенной болезни, бронх.астме, в глазной практике, скополамин как противорвотное и успокоительное. Отравление: возбуждение, галлюцинации, ↓АД, судороги. Первая помощь: промывание желудка марганцовкой, активированный уголь, форсированный диурез, гемосорбция, седуксен…ВЕЩЕСТВА, ИЗОЛИРУЕМЫЕ ИЗ ИССЛЕДУЕМЫХ ОБЪЕКТОВ НАСТАИВАНИЕМ С ВОДОЙ С ПОСЛЕДУЮЩИМ ДИАЛИЗОМ.
Соляная кислота, Серная кислота, Азотная кислота. Уксусная кислота, Щавелевая. Щелочи: едкие и карбонатныеСЕРНАЯ КИСЛОТА
Из вещ доков проводят прямую экстракцию этанолом. Т.к. tкип кислоты очень ↑ à для повышения её летучести переводят медными опилками в… 2H2SO4 + Cu à H2SO3 + CuSO4 + H2O H2SO3 à SO2↑ + H2OАЗОТНАЯ КИСЛОТА
2HNO3 + 3Cu à 2NO + 3CuO + H2O 6HNO3 + 3CuO à 3 Cu(NO3)2 + 3 H2O 2NO + O2 à 2 NO2 (оранжевые пары)ХЛОРИСТОВОДОРОДНАЯ КИСЛОТА
Является составной частью организма. Диализат перегоняют досуха.
Идентификация:
1) С нитратом серебра
2) 6HCl + KClO3 à 3 Cl2 + KCl + 3 H2O
Cl2 + KJ à J2 + 3 KCl
Посинение J-крахмальной бумажки.
ОБНАРУЖЕНИЕ ЩЕЛОЧЕЙ
КОН
1) Диализат нейтрализуют уксусной кислотой до слабо кислой среды, проводят реакцию с гидротартратом Na à белый крист ↓, растворимый в горячей воде.
2) С гексанитрокобальтитом
2KOH + Na3[Co(NO2)6] à K2Na[Co(NO2)6]↓ + 2 NaOH
NaOH
1) гидролизат нейтрализуют уксусной кислотой + гидроксистиьбиат К
KH2SbO4 + NaOH à NaH2SbO4↓ белые кристаллы, растворимые в горячей воде.
2) с цинкуранилацетатом в уксуснокислой среде(белый осадок):
NaOH + Zn[(UO2)3(CH3COO)8] +CH3COOH à NaZn[(UO2)3(CH3COOH)9]
NH4OH
Перед тем как исследовать на аммиак, проверяют свежесть б/м. Затем проводят реакцию с р-вом Несслера à оранж-коричн ↓.
ОПРЕДЕЛЕНИЕ НИТРАТОВ И НИТРИТОВ
Изолирование проводят диализом. Не перегоняют соли данных соединений.
Идентификация:
1) С помощью J-крахмальной бумажки: +1кап.HCl 1% + 3-4 кап.нейтраль.диализата à посинение бумажки.
2) С реак-вом Грисса (1% сульфоновая к-та в 30% укс. к-те, 0,1% α-нафтиламина в 30% УК).
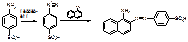
ОПРЕДЕЛЕНИЕ КАРБОКСИГЕМОГЛОБИНА В КРОВИ
Образуется при неполном сгорании древесины, м.б. обнаружен в выхлопных газах машин (13%), в табачном дыму (1%). CO является кровяным ядом, проникает через дыхательные пути и связывается с Hb… 3 стадии отравления:ФОСФОРОРГАНИЧЕСКИЕ ЯДОХИМИКАТЫ
Могут вызывать хронические отравления. Нарушения ф-ции печени, ССС.
Пути поступления: ингаляционный, пероральный, ч/з кожу.
Производные алкилфосфорной кислоты
ХЛОРОФОС

Производные фосфорной кислоты
ДИХЛОФОС

Производные тиофосфорной кислоты
МЕТАФОС

ТРИХЛОРМЕТАФОС
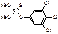
Производные дитиофосфорной кислоты
Токсическое действие на организм: Основные симптомы из-за нарушения действия АХЭ:Хлорофос и дихлофос.
Изолирование: б/м измельчают и заливают водой, подкисляют серной кислотой до…К.О.
1) ФЭК по р-ции с 2,4-ДНФГ
Метафос
Изолирование: Б/м измельчают + 50мл гексана в присутствии б/в Na2SO4. Настаивают 12ч. при перемешивании. Жидкость сливают,…Карбофос
Угнетает АХЭ, но возможно активность проявляют продукты метаболизма. Метаболизируются до кислородных производных: малооксонК.О.
После минерализации по H3PO4.
ПЕСТИЦИДЫ
Ядохимикаты (пестициды) – химические вещества различной природы, применяемые в народном хозяйстве для защиты растений и животных от вредителей и болезней
Классификация
По хим природе:
1) соединения неорг природы (серы, соли меди, As, Hg, Se, производные фтористых и кремнефтористых кислот)
2) Соединения органической природы (хлорорганика, ФОС, пр.карбаминовой кислоты (севин), пр.фенола, орг.соединения.ртути).
По назначению:
1) Акалициды (борьба с клещами)
2) Альгициды (водоросли, вод.растения)
3) Антисептики (обработка древесины)
4) Арборициды (учитожение нежелат.древесн. и кустар. растений)
5) Инсектициды (насекомые)
6) Гербициды (сорные травянистые растения)
7) Фунгициды (грибковые организмы)
По пути поступления ядов в организм насекомых:
1) контактного действия
2) кишечного действия
3) системного действия
4) фумиганты
По действию на организм растения:
1) Гербициды контактного действия
2) Системного действия
3) Через корневую систему или проросшие семена.
По токсичности:
1) Высокотоксичные
2) Среднетоксичные
3) Малотоксичные
По персистентности:
1) Высокоперсистентные
2) Среднеперсистентные
3) Низкоперсистентные
Персистентность – способность ядохимикатов сохраняться в окружающей среде.
ЗАДАЧКИ
Прим-ся в кач-ве ср-ва дератизации в виде паст, tab, а также пищевые продукты с ним. Это темно-серый порошок, н/р в воде и спирте, слабо р-м в щелочах и маслах,… картина отравления типична для отр-я PH3. для анализа берем жел-к и киш-к.Подозрение на отравление ртутью.
Предварит исп-е – проба Рейнша. Антидот-я терапия – пром-е жел-ка, Antidotum metallorum. Далее – см выше.
Отравление парами ртури.
Берут печень и почки. См выше.
5. Тушеная картошка с мясом, в-во вызывает парез, выпадение волос– Tl.
Изол-е: мокрое озоление: смесью к-т: HNO3, H2SO4, HClO4, H2O и EtOH или H2SO4, HNO3 или KClO3, HCl или NH4NO3, H2SO4.
Идент-я: 1. с малахитовым зеленым – голуб окр-е толуольного слоя ______________________ 2. с дитизоном pH=12, CHCl3 слой окр-ся в красн цв ____________________
К.О. по 1 или 2 р-ии.
Парень, нюхавший момент.
7. фенолформальдегидные смолы.
8. Mn и Cu.
Металлические яды.
Минерализация.
Дробный м-д обн-я по Крыловой:______________________
СОHb
спектроскопия, спектрофотометрия, фотоколориметрия, ГЖХ,
28. маковая соломка и таблетки «Седальгин»
кодеина фосфат, фенобарбитал, кофеин, фенацетин, ацетилсалициловая к-та
29. «Валокордин» и «Сибазон»
фенобарбитал, этиловый эфир бромизовалериановой к-ты
30. «Белоид»
эрготоксин, Alk красавки, 5,5-бутилэтилбарбитуровая к-та
43. «Дуплекс» -тводный р-р стрихнина нитрата и натрия арсената
– Конец работы –
Используемые теги: Токсикология, Предмет, задачи0.061
Если Вам нужно дополнительный материал на эту тему, или Вы не нашли то, что искали, рекомендуем воспользоваться поиском по нашей базе работ: ТОКСИКОЛОГИЯ – ПРЕДМЕТ И ЗАДАЧИ
Что будем делать с полученным материалом:
Если этот материал оказался полезным для Вас, Вы можете сохранить его на свою страничку в социальных сетях:
| Твитнуть |
Хотите получать на электронную почту самые свежие новости?







Новости и инфо для студентов